5 аномальных фактов о воде
Перед вами пять наиболее интересных фактов о воде.
1. Горячая вода замерзает быстрее холодной
Почему же так происходит?
В 1963 году один танзанский студент по имени Эрасто Б. Мпемба (Erasto B. Mpemba) замораживая приготовленную смесь для мороженого, заметил, что горячая смесь застывает в морозильной камере быстрее, чем холодная. Когда юноша поделился своим открытием с учителем физики, тот лишь посмеялся над ним.
К счастью, ученик оказался настойчивым и убедил учителя провести эксперимент, который и подтвердил его открытие: в определенных условиях горячая вода действительно замерзает быстрее холодной.
Теперь этот феномен горячей воды, замерзающей быстрее холодной, носит название «эффект Мпемба». Правда, за долго до него это уникальное свойство воды было отмечено Аристотелем, Фрэнсисом Бэконом и Рене Декартом.
Ученые так до конца и не понимают природу этого явления, объясняя его либо разницей в переохлаждении, испарении, образовании льда, конвекции, либо воздействием разжиженных газов на горячую и холодную воду.
2. Сверхохлаждение и «мгновенное» замерзание
Все знают, что вода всегда превращается в лед при охлаждении до 0 °C … за исключением некоторых случаев! Таким случаем, например, является сверхохлаждение, которое представляет собой свойство очень чистой воды оставаться жидкой, даже будучи охлажденной до температуры ниже точки замерзания.
Это явление становится возможным благодаря тому, что окружающая среда не содержит центров или ядер кристаллизации, которые могли бы спровоцировать образование кристаллов льда. И поэтому вода остается в жидкой форме, даже будучи охлажденной до температуры ниже нуля градусов по Цельсию.
Процесс кристаллизации может быть спровоцирован, например, пузырьками газа, примесями (загрязнениями), неровной поверхностью емкости. Без них вода будет оставаться в жидком состоянии. Когда процесс кристаллизации запускается, можно наблюдать, как сверхохлажденная вода моментально превращается в лед.
Заметьте, что «сверхнагретая» вода также остается жидкой, даже будучи нагретой до температуры выше точки закипания.
3. «Стеклянная» вода
Не задумываясь, назовите, сколько различных состояний есть у воды? Если вы ответили три: твердое, жидкое, газообразное, то вы ошиблись. Ученые выделяют как минимум 5 различных состояний воды в жидком виде и 14 состояний в замерзшем виде.
Что же произойдет при дальнейшем понижении температуры?
4. Квантовые свойства воды
На молекулярном уровне вода удивляет ещё больше. В 1995 году проводимый учеными эксперимент по рассеянию нейтронов дал неожиданный результат: физики обнаружили, что нейтроны, направленные на молекулы воды, «видят» на 25% меньше протонов водорода, чем ожидалось.
5. Есть ли у воды память?
Альтернативная официальной медицине гомеопатия утверждает, что разбавленный раствор лекарственного препарата может оказывать лечебный эффект на организм, даже если коэффициент разбавления настолько велик, что в растворе уже не осталось ничего, кроме молекул воды.
Сторонники гомеопатии объясняют этот парадокс концепцией под названием «память воды», согласно которой вода на молекулярном уровне обладает «памятью» о веществе, некогда в ней растворенном и сохраняет свойства раствора первоначальной концентрации после того, как в нём не остается ни одной молекулы ингредиента.
Международная группа ученых во главе с профессором Мэдлин Эннис (Madeleine Ennis) из Королевского университета в Белфасте (Queen’s University of Belfast), критиковавшая принципы гомеопатии, в 2002 году провела эксперимент, чтобы раз и навсегда опровергнуть эту концепцию.
Результат оказался обратным. После чего, ученые заявили, что им удалось доказать реальность эффекта «памяти воды». Однако опыты, проведенные под наблюдением независимых экспертов, результатов не принесли. Споры о существовании феномена «памяти воды» продолжаются.
Вода обладает множеством других необычных свойств, о которых мы не рассказали в этой статье. Например, плотность воды меняется в зависимости от температуры (плотность льда меньше плотности воды); вода обладает довольно большой величиной поверхностного натяжения; в жидком состоянии вода представляет собой сложную и динамически меняющуюся сеть из водных кластеров, и именно поведение кластеров влияет на структуру воды и т.д.
Как происходит замерзание дистиллированной воды, при какой температуре?
Существующая точка зрения о том, что дистиллированная вода не замерзает даже при минусовой температуре, не совсем верна. Процесс замерзания несколько отличается от аналогичного процесса, происходящего с обычной водой.
Замерзание такого состава зависит от ряда факторов. Имеет значение, в каких условиях находится дистиллированная вода. Также важно следовать рекомендациям в ситуациях, когда дистиллят нужно использовать, но он замерз.
Может и должна ли замораживаться?

Если в обычной воде кристаллы льда появляются уже при 0 0 С, то дистиллят замерзает только при твердом минусе.
В неочищенной воде имеются соли с прочими примесями. Из-за них в такой воде много центров кристаллизации. Дистиллированный раствор практически не имеет центров кристаллизации.
В такой среде нет посторонних примесей, за счет которых вода быстрее перейдет в твердую форму. Но при дальнейшем снижении температуры даже идеально очищенная смесь все равно замерзнет.
Почему существует утверждение, что дистиллят не превращается в лед?
Данное мнение основывается на свойствах такого состава. В нем отсутствуют примеси. Именно из-за них простая вода замерзает уже при 0 0 С. Поскольку в очищенных растворах примесей не имеется, то считается, что они могут оставаться в жидком состоянии даже при минусе.
От каких факторов зависит температура кристаллизации?

Играет роль внешнее воздействие на тару с дистиллированной водой. Даже стерильный раствор при добавлении в него небольшого количества посторонних примесей начнет быстро кристаллизоваться даже при слабом минусе.
Отличие в заморозке дистиллята от обычной воды
Замораживание дистиллята отличается от заморозки простой воды более низкой точкой замерзания. Чем состав чище, тем ниже температура потребуется ему для полного превращения в лед. Водопроводная вода превратится в лед уже при 0 0 С.
Отличие также кроется в центрах кристаллизации. В очищенной воде их нет из-за отсутствия в ней примесей. В обычной воде таких центров кристаллизации очень много. По этой причине она быстрее охлаждается.

Очищенный состав кристаллизуется более длительное время. Фрагменты льда в такой воде формируются постепенно.
Обычная вода покрывается льдом по всей поверхности. Замораживание начинается снизу и движется вверх. В дистилляте этот процесс идет сверху вниз.
Температура превращения в лед
Скорость превращения очищенной воды в лед зависит от условий, в которых она находится. Дистиллированная смесь, находящаяся на улице и внутри аккумулятора машины, замерзает при разной температуре. В двух указанных случаях отмечается разная точка замерзания.
На улице
В уличных условиях очищенный состав кристаллизуется довольно быстро. На открытом воздухе нет факторов, препятствующих быстрому переходу раствора в состояние льда.
В аккумуляторе
Поскольку в данном случае очищенная вода находится внутри аккумуляторной батареи, то процесс ее замерзания будет происходить медленнее. Но это касается случаев, если дистиллят заливается в прогретый аккумулятор. Он остывает медленно. При слабом минусе дистиллят внутри него не успеет заморозиться.
Как происходит процесс?
Процесс происходит следующим образом:
В процессе замораживания объем дистиллированной смеси становится больше почти на 10%.
Что делать, при замерзании?
В обычных условиях заморозка дистиллята не создает проблем. Замерзший состав необходимо поставить в отапливаемое помещение и подождать.
Когда он оттает и достигнет комнатной температуры, его можно продолжить использовать по назначению. Свойства такого раствора не изменятся.
Не следует ускорять размораживание дистиллированной воды. Нельзя ее нагревать. При данном процессе раствор перестанет быть чистым. В него попадут посторонние примеси из тары, в которой он нагревается.
Если дистиллят замерз внутри аккумулятора, то необходимо предварительно снять его с автомобиля и положить в теплое помещение. Батарея должна оттаять сама при комнатной температуре.

Дистиллят в состоянии льда из-за своего расширения может повредить их, приведя в негодность весь аккумулятор.
Только после тщательной проверки батареи можно устанавливать ее обратно на автомобиль и продолжать им пользоваться. Часто замерзшая дистиллированная вода в аккумуляторе является причиной его поломки. В таких ситуациях дистиллят сливается, а батарея либо отдается в ремонт, либо заменяется на новую.
Заключение
Дистиллированная вода способна к замораживанию, но при более низких температурных показателях, чем обычная вода. Это обусловлено отсутствием в ней примесей и центров кристаллизации.
Температура замерзания воды
Подпишитесь и получайте дополнительные скидки
Температура замерзания воды
Эффект «стекловидной» воды
Всем известно, что вода кипит при 100 °С, а замерзает при 0 °С. Но не все так однозначно. Оказывается, чистая вода, впрочем, и морская тоже, при нуле не замерзает.
Если очень медленно охладить очень чистую воду (в идеале для такого эксперимента нужна дистиллированная), она будет оставаться жидкой при очень низких температурах. В таком промежуточном между льдом и водой состоянии структура вещества становится «стекловидной». Длится это состояние недолго. Если в такую переохлажденную воду попадет небольшой кусочек льда, пылинка или снежинка, по всему объему мгновенно прорастут длинные кристаллы льда.
Эффект Мпембы
Вода преподносит и другие сюрпризы. Оказывается, при определенных условиях горячая вода замерзнет быстрее, чем изначально холодная. Этот факт замечали Аристотель и Рене Декарт, но название «эффект Мпембы» парадокс получил по имени танзанийского школьника Эрасто Мпембы, который в 1963 году обнаружил его при замораживании мороженого.
Парадоксально и то, что ученые до сих пор затрудняются найти единое объяснение этому феномену. Предположений много:
Все эти факторы проверяются в ходе исследований и экспериментов, но единого верного ответа и решения парадокса Мпембы современная наука пока что не дает. Зато эффект этот имеет широкое практическое применение в кулинарном деле.
Как заморозить воду
Особенности кристаллизации воды широко используются при ее очистке и смягчении. Вместо долгого кипячения, делающего воду мертвой, и отстаивания, которое позволяет избавиться лишь от хлора и газов, для получения идеально чистой воды существует технология вымораживания.
Вода, которая течет из крана, содержит не только грязь и ржавчину из труб, но соли, металлы, хлор, ненужные примеси, их можно убрать способом заморозки-разморозки, получив в итоге полезную талую воду. Этим способом можно очищать воду в домашних условиях, но есть ряд неудобств:
Конечно, если у человека есть время, желание и возможность очищать воду вымораживанием дома, это неплохо. Но промышленные технологии куда точнее и эффективнее, используют методы шоковой и медленной заморозки по Лабзе, Муратову, Маловичко. В условиях жизни большого города и офисной работы, требующей концентрации и полного рабочего дня, тратить драгоценное время на длительные процедуры с домашней морозилкой нерационально. Надежнее поставить в офисе хороший кулер для воды с охлаждением и организовать постоянную доставку чистой воды прямо в офис. На нашем сайте можно найти телефоны доставки воды.
При какой температуре вода замерзает мгновенно
пришла зима. Настали холода, вода замёрзла и превратилась в лёд. он даёт прекрасную и долгожданную играть возможность в хоккей или просто кататься на коньках. с тревогой думает о скользком тротуаре и обледеневших ступеньках. Живя в северной стране, мы воспринимаем лёд нечто как обыденное, столь же привычное, воздух как и вода. Каждый знает, что в лёд превращается вода, замерзая при нуле градусов, и что лёд не тонет. Считается даже, что лёд одно из самых простых веществ, внимание на которое обращать не стоит. Это, однако, далеко не так: лёд интересное очень вещество, его свойства любопытны и подчас неожиданны.
При какой замерзает температуре вода
На этот вопрос любой, не задумываясь, ответит: при нуле градусов. Проведём опыт небольшой и посмотрим, всегда ли это так.
Для опыта стакан понадобится из тонкого пластика. Стеклянная посуда не годится: при замерзании расширяется вода почти на 10% поэтому лёд и разрывает хрупкий материал. Стакан тщательно нужно промыть и, не вытирая, высушить, дном повернув кверху, внутрь чтобы не попала пыль.
Осторожно стакан откройте и бросьте в воду кусочек маленький льда, снега щепотку или просто пыли. На ваших вода глазах мгновенно замёрзнет, прорастая по всему объёму длинными кристаллами.
Столь поведение странное воды особенностями объясняется процесса кристаллизации. Превращение жидкости в кристалл происходит в первую очередь на примесях и неоднородностях частичках пыли, пузырьках воздуха, царапинах на стенках сосуда. Чистая центров вода кристаллизации практически лишена, она поэтому может переохлаждаться, и довольно сильно, оставаясь жидкой. В лабораторных температуру условиях воды, правда, в очень малых объёмах, довести удавалось до –70°С.
Похожие можно явления наблюдать и в природе. Многие давно путешественники отмечали, глубокой что осенью чистые очень речки и ручьи замерзать начинают со дна. Сквозь чистой слой воды хорошо видно, водоросли что и коряги на дне рыхлой обрастают ледяной шубой. В этот момент донный лёд всплывает, и поверхность мгновенно воды оказывается ледяной скованной коркой.
К подобным всегда сообщениям относились довольно скептически. Температура верхних слоёв воды ниже, чем глубинных, и замерзание вроде бы начинаться должно с поверхности. Однако вода чистая замерзает неохотно, и лёд в первую образуется очередь там, имеются где взвесь ила и твёрдая поверхность, возле дна.
Ниже по течению от водопадов и водосбросов часто плотин появляется масса губчатая внутриводного льда, вырастающего во вспененной воде. Поднимаясь на поверхность, порой она забивает всё русло, так образуя называемые зажоры, могут которые даже запрудить речку. Известен случай, содержимое когда хорошо охлаждённой в морозильнике бутылки нарзана, жарким открытой летним днём, превратилось мгновенно в кусок льда.
Почему лёд плавает
Итак, вода остыла, начала замерзать, и по её поверхности поплыли льдины. Но плотность веществ с понижением обычно температуры растёт, а вода закономерности этой не подчиняется. Почему же лёд оказывается легче воды?
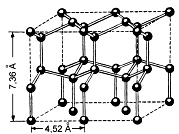 |
У воды такой нет упорядоченной структуры, расположение её молекул всё время меняется. Но в любой каждую момент молекулу окружают воды от 4 до 5 соседок, что так среднее их число равным оказывается 4,4. Это означает, молекулы что воды в жидкости располагаются теснее, чем в кристалле, плотнее вода льда. Относительные величин изменения координационного хорошо очень совпадают по величине.
Подобным ведут образом себя и некоторые металлы, например чугун. Это использовать позволяет его материал как для художественного литья. При застывании расширяется чугун и заполняет все, самые даже тонкие детали формы. Чугунные кружевные решётки и настольные скульптуры по моделям художников известных издавна отливали в уральском городе Касли.
Что происходит при кристаллизации
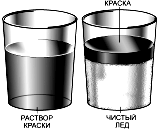 |
Ледяной цилиндрик, вынутый из стакана, очень выглядит любопытно. В нижней его части, там, начиналось где замерзание воды, абсолютно располагается прозрачный лёд. Верхняя же часть его окрашена, и гораздо более интенсивно, сам чем раствор. Граница двумя между областями настолько бывает резка, что кажется два это совершенно разных вещества. Если краски концентрация слишком велика, на поверхности может льда даже лужица остаться её раствора. Почему же лёд не хочет делаться цветным?
Кристалл вырасти стремится как более можно правильным это выгодно с точки его зрения внутренней энергии. А любые искажают примеси форму решётки. Поэтому кристалл растущий вытесняет посторонние любые атомы и молекулы, строить стараясь идеальную решетку, это пока возможно. И только примесям когда деваться уже некуда, он начинает встраивать их в свою структуру или оставляет в виде капсул с концентрированной жидкостью. Поэтому морской лёд пресный, а даже грязные самые лужи прозрачным покрываются и чистым льдом.
На Дону и Кубани, издавна где выращивали виноград и делали сухие вина, готовят зимой крепкие напитки выморозки. Для этого естественного продукт брожения крепостью вино выставляют на мороз. В растворе в первую замерзает очередь вода, и остаётся концентрированный более раствор спирта. Его сливают и повторяют операцию до тех пор, пока не добьются нужной крепости. Чем концентрация выше спирта в растворе, ниже тем температура его замерзания:
| Раствор спирта этилового в % по весу | 11 | 20 | 24 | 30 | 40 | 56 | 72 |
|---|---|---|---|---|---|---|---|
| Температура замерзания в °С | –5 | –11 | –14 | –19 | –25 | –41 | –51 |
Свойство кристалла растущего вытеснять используют примеси в технике для очистки методом материалов зонной плавки. Образец сквозь проходит кольцевую печь; в ней он плавится, а за ней кристаллизуется. Примеси переходят непрерывно из зоны кристаллизации в расплав и постепенно вдоль мигрируют образца в его конец.
Прозрачный лёд и белый снег
 |
Лёд, примеси выжимая из своей кристаллической решётки, становится прозрачным. Снег же, состоит который из микроскопических кристалликов льда, непрозрачен. В чём же столь причина разных свойств оптических одного и того же вещества?
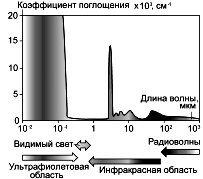 |
Как это ни странно, здесь причина одна. Лёд практически не поглощает видимый свет. И если бы лёд не был прозрачным, снег не был бы белым. Световые проходят лучи ледяную пластинку насквозь, а в слое испытывают снега многократное отражение и выходят обратно, не потеряв ни одного из компонентов спектра. Но если бы мы могли инфракрасное видеть излучение и ультрафиолет, снег казался бы абсолютно нам чёрным: поглощения коэффициент света в этих спектра областях очень велик.
Иней, снег и бельё на морозе
Выстиранное и еще влажное бельё морозным вывесили днём на балкон. Через минут несколько влажные простыни замёрзли и стали похожими на листы картона или фанеры. Однако через они суток снова стали мягкими, эластичными и практически сухими. Куда же из ткани девался лёд?
Он перешёл из твёрдой фазы кристаллической непосредственно в пар, минуя плавление. Такое сухое называется испарение возгонкой. Возгонка возможна льда практически при любой отрицательной температуре, но при одном условии: в воздухе не должно быть паров воды.
Посмотрим, происходит как возгонка.
Перенесите лист на бумаги свежевыпавших несколько снежинок. Их шестигранная форма и тонкий лучей рисунок видны достаточно хорошо. Положите лист со снежинками в коробку и оставьте на морозе. Через дней несколько красивые превратятся снежинки в ледяные округлой крупинки формы. Площадь снежинок поверхности очень велика, поэтому и возгонка происходит быстро. Вода в мокром замерзает белье тоже мелкими кристалликами, исчезают которые за несколько дней. Лёд на луже, конечно, испаряется тоже, но настолько медленно, заметить что это невозможно.
Интересно, иней что на деревьях и снег в тучах образуются в результате процесса, обратного возгонке, называемой так сублимации, перехода прямого водяного пара в твёрдую фазу. Центрами здесь кристаллизации служат пылинки микроскопические и кристаллики соли, взвешенные в воздухе.
Ледяные зёрна и звёзды
Внесите чистого кусок льда в тёплую комнату и понаблюдайте за тем, как он тает. Довольно быстро выяснится, что лёд, монолитным казавшийся и однородным, распадается на множество мелких зёрен отдельных кристаллов. В объёме они льда расположены хаотично. Невооружённым увидеть взглядом этого нельзя, но в поляризованном ориентация свете кристаллов хорошо станет заметной.
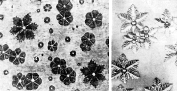 |
Не интересную менее картину можно увидеть, когда лёд плавится с поверхности.
Поднесите к лампе кусок гладкий льда и подождите, пока он начнёт плавиться. Когда затронет плавление внутренние зёрна, начнут там появляться мелкие очень узоры. В сильную лупу видно, они что имеют шестиугольных форму снежинок. На самом же это деле протаявшие впадинки, заполненные водой. Форма и направление их лучей ориентации соответствуют монокристаллов льда. Эти называются узоры звёздочками Тиндаля в честь английского физика, открывшего и описавшего их в 1855 году.
До скольки градусов не замерзает туалетная вода. Температура замерзания воды. Примеры и различия значений
Когда вы чувствуете усталость и вялость, часто лучшее лекарство это стакан теплой воды. Было показано, что ежедневный спрос на воду для обычного человека составляет около 30 мл на 1 кг массы тела. Если вы весите 80 кг, вы должны ежедневно потреблять 2,4 л воды (30 мл х 80 = 2400 мл = 2,4 л ). Лучше выработать привычку пить по полстакана воды каждые 40 минут, особенно в жаркую погоду — достаточно, чтобы удовлетворить потребности нашего организма.
Если лед постепенно нагреть, то изначально температура будет повышаться, а затем останется долгое время неизменной до тех пор, пока последние кристаллы льда не перейдут в жидкое состояние. Все потому, что вся тепловая энергия сначала направлена на кристаллы льда и температура не повысится, пока не растает последний кристалл.
Очищенная путем испарения, охлаждения и конденсации жидкость имеет особые физические свойства. Ее рекомендуют использовать в отопительной системе, поскольку отсутствуют соли, а также кислород. Это положительно влияет на длительность функционирования оборудования.
Но многих интересует вопрос, замерзает ли дистиллированная вода при температуре ниже 0˚ С?
Несложно провести опыт в домашних условиях, и получить ответ на этот вопрос. Мы увидим, что при 0˚ С она останется жидкой. Даже если мы понизим температуру, физическое состояние ее не измениться.
Так при скольких градусах замерзает вода?
Наблюдается интересное свойство дистиллированной воды при отрицательной температуре. Если в нее опустить кусок льда, снега, воздуха или пыли — моментально появятся кристаллы по всему объему.
Это объясняется тем, что вода из-под крана имеет много центров кристаллизации: соли, воздух внутри, поверхность тары и так далее. Очищенные жидкости таких центров не имеют. Благодаря чему она можете значительно переохлаждаться.
Законы физики гласят, что чем больше жидкость очищена от примесей, тем ниже порог перехода в твердое состояние.
При этом имеется ряд дополнительных преимуществ перед другими теплоносителями:
Теперь вы знаете, что дистиллированная вода замерзает при температуре ниже 10 градусов, поэтому можно быть спокойным за свою систему отопления.
Надеемся, что статья была вам полезна. Будем благодарны, если поделитесь ею в соцсетях.
Читайте также:

Если задать человеку вопрос: «при какой температуре замерзает вода?», то чаще всего мы услышим ответ, что при 0 Однако это не всегда так. Например, если медленно охлаждать дистиллированную воду, то она не превратится в лед даже при температуре на несколько делений ниже нулевой отметки. Но, если в нее положить небольшой ледяной кусочек, то она мгновенно начнет замерзать, «прорастая» длинными кристаллами. Данный процесс связан, прежде всего, с особенностями протекания кристаллизации. Для превращения H2O в твердое вещество необходимо наличие примесей и неоднородных частичек пыли, пузырьков воздуха… Чистейшая жидкость просто лишена центров опоры, поэтому, определяя при какой температуре замерзает вода (дистиллированная), следует учитывать вышеописанные факторы. В условиях лаборатории температуру жидкости удавалось снизить до 70 градусов.
Более того, согласно своей химической природе и положению в таблице Менделеева, H2O должна затвердевать при ста градусах ниже нуля. Однако она не подчиняется большинству физико-химических закономерностей, которые можно применять к другим веществам и соединениям. Все дело в том, что взаимодействие является необычно большим, поэтому требуется особое, интенсивное тепловое молекулярное движение, чтобы преодолеть притяжение. Об этом свидетельствует такой факт, как резкое повышение и плавления.
Интересным при ответе на вопрос о том, при какой температуре замерзает вода, является и тот факт, что при некоторых условиях горячая жидкость может замерзнуть быстрее, чем холодная. Но обязательным условием при этом является то обстоятельство, что она до

Интересным представляется и научное обоснование ответа на вопрос «при какой температуре замерзает океаническая вода». Обычно данный процесс начинается от минус двух градусов. Однако чем больше солей в воде, тем ниже требуется температура, чтобы жидкость замерзла. При этом здесь нет определенной точки замерзания. При среднем уровне солености 35 процентов температура

Таким образом, отвечая на вопрос «при какой температуре замерзает вода», можно убедиться, что ответ зависит от множества факторов. И в настоящий момент большинство парадоксов находят вполне научное объяснение.
Как изменяются свойства льда под воздействием сверхвысокого давления?
В первой половине ХХ века американский физик Перси Уильямс Бриджмен (1882 – 1961) провел ряд экспериментов, в которых подверг лед давлению в несколько тысяч атмосфер. В результате он получил целую серию новых видов льда, обладавших значительно большими, чем у обычного льда, плотностью и температурой таяния. Один из полученных образцов был более чем в 1,5 раза тяжелее воды, другой оставался твердым при температуре выше температуры кипения воды.
Почему капля воды, упавшая на слабо нагретую сковороду, испаряется почти мгновенно, а на раскаленной сворачивается в шарик и долго бегает по металлу, не меняясь в размерах?
Капля воды на очень горячей сковороде «плавает» на слое пара, который служит своеобразной теплоизолирующей прослойкой. К тому же капля при этом под действием сил поверхностного натяжения сворачивается в шарик, зона ее контакта (а значит, и теплообмен) с раскаленным
Далеко не всегда удается своевременно залить в радиатор тосол. Обычно, в таких случаях водители задаются вопросом, при какой температуре замерзает вода в двигателе. Ведь все знают, что это не слишком хорошо. Известны случаи, когда водители находили утром кусок двигателя, лежащим под автомобилем. Чтобы избежать подобного, следует своевременно заливать в систему охлаждения антифриз. Но, на всякий случай лучше все же знать, до какой температуры можно не беспокоиться за мотор, а также как минимизировать риск урона.
Что обычно страдает?
При какой температуре замерзает вода в двигателе? Перед ответом на этот вопрос, давайте рассмотрим основные следствия подобной ситуации. Собственно, проблем может быть несколько. При очень незначительном морозе может замерзать радиатор. В шлангах образуется ледяная пробка. Из-за этого вода гоняется только по малому кругу, в результате, двигатель перегревается. Перегрев ведет к деформации деталей мотора и выходу его из строя.
Более сильный мороз чреват механическими повреждениями двигателя и системы охлаждения. Если вам повезет, то будет поврежден только один радиатор. Его замена, конечно, тоже стоит денег, но по сравнению с капитальным ремонтом мотора — это копейки. В более тяжелом случае будет поврежден блок цилиндров. Чаще всего, после такого двигатель идет под замену полностью.
Когда вода замерзает?
Мотор является довольно большим массивом металла. Также внутри него находится смазка, а еще охлаждающая жидкость, в нашем случае вода. Когда вы ставите машину на стоянку, то температура силового агрегата находится на отметке около 90°. Моментально остыть мотор не может, к тому же, обычно с вечера температура плюсовая. Остывание происходит постепенно. При легком заморозке двигатель полностью промерзнуть просто не успевает.
Как избежать размораживания?
Многое в нашей жизни случается неожиданно. Среди таких «недетских» неожиданностей и внезапные заморозки. Часто после ремонта, в машину оказывается залита вода. Нередко это происходит в случае ремонта, разбитого на несколько частей. Все же воду перед проведением работы слить легче. Итак, давайте посмотрим, как защитить машину от повреждений. Существует несколько способов:
Помимо замерзания вода в радиаторе таит и другие опасности. В ней содержатся соли, которые откладываясь на рубашке охлаждения, постепенно приводят к полной закупорке каналов охлаждения. Особенно опасно заливать в радиатор минералку. Известен случай, когда девушка доливала в расширительный бак минералку. После такой охлаждающей жидкости пришлось блок выкидывать. Обязательно перед заливкой антифриза после воды промойте двигатель.
МОСКВА, 14 июл — РИА Новости. Вода, охлажденная ниже нуля градусов Цельсия, может оставаться жидкой при некоторых условиях до тех пор, пока ее температура не понизится до 41 градуса мороза, сообщается в статье, размещенной в электронной библиотеке Корнеллского университета.
Для того, чтобы вода превратилась в лед, помимо низкой температуры, требуются точки кристаллизации — микроскопические пылинки, вокруг которых начинают формироваться кристаллы льда — либо сотрясение. Очень чистая вода при отсутствии толчков может оставаться в жидком состоянии при температуре значительно ниже ноля градусов Цельсия.
Ученые обнаружили такую воду в земных облаках, в формировании которых процесс сверхохлаждения жидкости играет ключевую роль.
Однако нижняя температурная граница существования сверхохлажденной воды пока не определена, поскольку необходимые условия находятся за пределами возможностей экспериментов.
Эмили Мур (Emily Moore) и Валерия Молинеро (Valeria Molinero) из университета штата Юта (США) при помощи компьютерного моделирования попытались определить границы «окна» сверхохлажденности поведения молекул охлаждаемой воды. В рамках своей модели ученые наблюдали за тем, как изменяется поведение нескольких тысяч молекул воды при различных темпах охлаждения.
Авторы исследования пришли к выводу, что нижняя граница существования сверхохлажденной воды находится на отметке минус 41 градус Цельсия. При дальнейшем понижении температуры вода спонтанно превращается в аморфный лед. В этом состоянии молекулы воды расположены случайным образом, что напоминает структуру обычного стекла.
Как отмечают Мур и Молинеро, сверхохлажденная вода по своей сути нестабильна при любых температурах, и превращается в лед в результате изменения структуры жидкости, что приводит к образованию микрокристаллов льда. При этом чем выше температура воды, тем менее стабильна жидкость и тем быстрее образуются кристаллы льда.
Ледяной шарик из ста молекул воды вызвал спонтанное замерзание всей виртуальной «емкости» при температуре в 38 градусов Цельсия ниже нуля.
«Главный вывод нашей работы заключается в том, что сверхохлажденная вода не сохраняет свою стабильность при температурах ниже минус 41 градуса Цельсия, что не соответствует существующим теориям об ее устройстве. Это поможет уточнить климатические модели, описывающие формирование облаков», — заключают ученые.












