Негонококковые уретриты у мужчин
Уретрит представляет собой воспалительное заболевание мочеиспускательного канала, которое может иметь как инфекционный, так и неинфекционный характер.
Негонококковый уретрит (НГУ) считается полиэтиологичным заболеванием и может быть вызван различными возбудителями. Из года в год имеет место рост заболеваемости негонококковыми уретритами. С 1972 года этот показатель превосходит заболеваемость гонореей.
Наиболее часто выявляемым и потенциально опасным этиотропным агентом является хламидия (Chamydia trachomatis), являющаяся причиной негонококкового уретрита у 15-55 % больных. Немаловажным представляется и тот факт, что хламидии одновременно выявляются у 30-45 % больных гонореей. По современным эпидемиологическим данным, у молодых людей заболеваемость инфекциями, вызванными Chamydia trachomatis, каждый год увеличивается на 5 % [3].
Другими причинами негонококкового уретрита могут быть Ureaplasma urealyticum, Mycoplasma genitalium, Trichomonas vaginalis, вирус простого герпеса и аденовирус. Немаловажно, однако, что вызывать воспаление мочеиспускательного канала может и банальная флора, в частности, кишечная палочка (Esherichia coli). У 20-30 % больных причину негонококкового уретрита установить не удаётся. У большинства из них не представляется возможным убедительно доказать, что негонококковый уретрит был вызван микоплазмой, трихомонадами, вирусом простого герпеса, аденовирусом или другими микроорганизмами.
Инкубационный период при негонококковом уретрите составляет 1-5 недель с момента полового контакта, однако, зачастую имеет место и более продолжительный инкубационный период. Хламидийный уретрит может осложниться эпидидимитом, простатитом и синдромом Рейтера (сочетание уретрита с коньюнктивитом и артритом).
Воспаление мочеиспускательного канала у мужчин бывает бессимптомным, но все-таки чаще сопровождается характерными проявлениями: гнойными или слизисто-гнойными выделениями, резью или болью при мочеиспускании и повышенной чув ствительностью наружного отверстия мочеиспускательного канала.
Учитывая, что у больного негонококковым уретритом с большой долей вероятности причиной может являться микроорганизм, передающийся половым путем, важен сбор анамнеза интимной жизни за последние 2 месяца (количество половых партнерш, незащищённые барьерными методами оральные, генитальные и анальные контакты).
Лабораторным подтверждением диагноза «уретрит» является наличие при исследовании мазка по Граму > 5 полиморфноядерных лейкоцитов в п/зр (х 1000) и/или выявление более 10 лейкоцитов при исследовании осадка (х 400) первой порции мочи. Мазок из уретры с окраской по Граму позволяет не только документировать наличие воспалительного процесса, но и, при выявлении внутриклеточных грамотрицательных диплококков, с 99 % специфичностью и 95 % чувствительностью диагностировать уретрит гонококковой природы.
Основными способами профилактики НГУ являются: ограничение/прекращение беспорядочных половых связей, а также использование барьерных методов контрацепции (презервативов) при генитальных, оральных и прочих интимных контактах.
Принципы лечения больного негонококковым уретритом следующие:
1. Назначение больному антибиотика.
2. Одновременное лечение полового партнера/половых партнеров, с которыми был контакт за последние 2 месяца.
3. Воздержание от интимной близости в течение 7 дней терапии.
В соответствии с современными международными клиническими рекомендациями [1, 2] препаратами выбора для лечения НГУ являются:
Доксициклин по 100 мг 2 раза в сутки 7 дней или азитромицин 1 г однократно.
В качестве альтернативных представлены следующие схемы лечения:
При трихомонадном уретрите рекомендуется назначение внутрь:
Поскольку у ряда больных этиотропный агент НГУ установить не удаётся, признаки воспаления после первичной терапии могут выявляться у 20-40 % пациентов, что обычно требует проведения дополнительного лечения альтернативными антибактериальными препаратами.
Следует отметить, что современные клинические рекомендации по лечению больных НГУ не лишены недостатков. Основным из них является тот факт, что за исключением случаев трихомонадной инфекции, выбор препарата для эмпирической терапии НГУ не зависит от выявляемого возбудителя и, главным образом, основывается на его активности в отношении Chlamydia trachomatis.
Доксициклин и азитромицин стали препаратами первой линии, поскольку мета-анализ, опубликованный в 2002 году [4], показал сходную и достаточно высокую их эффективность при лечении больных с хламидийной инфекцией. Отметим, однако, что данный мета-анализ обобщает результаты применения рассматриваемых препаратов в лечении хламидиоза не только у мужчин с НГУ, но и у женщин с цервицитами. Данный факт делает не вполне корректной экстраполяцию его результатов на когорту мужчин с НГУ.
В связи с этим, для сравнительной оценки доксициклина и азитромицина в лечении исключительно хламидийных НГУ у мужчин, а также с целью обновления данных по клинической и микробиологической эффективности рекомендуемых режимов антибиотикотерапии, в 2008 году российскими исследователями был проведён ещё один мета-анализ [5]. Для включения в мета-анализ отбирали только проспективные рандомизированные контролируемые клинические исследования (РКИ), сравнивающие эффективность и безопасность доксициклина 100 мг, применяемого в течение 7 дней, и азитромицина, назначаемого однократно в дозе 1,0 г у мужчин с НГУ. Отбирали исследования, в которые включались только мужчины, или исследования, из которых можно вычленить данные, касающиеся мужчин.
Из 160 оригинальных печатных работ по рассматриваемой теме (статьи в журналах, абстракты конференций, записи библиографических баз данных) было найдено 17 публикаций, описывающих потенциально подходящие для включения в мета-анализ исследования. Однако только восемь из этих работ являлись проспективными рандомизированными исследованиями и полностью соответствовали критериям включения в мета-анализ.
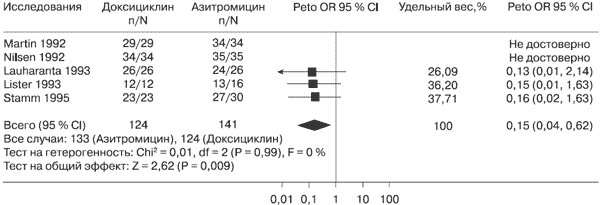
В результате мета-анализа было установлено, что у пациентов, получавших доксициклин, достоверно чаще отмечалась эрадикация C. trachomatis на 4-й неделе терапии по сравнению с пациентами, получающими азитромицин (100 и 92,5 % соответственно). Отношение шансов, рассчитанных по методу Peto для этого показателя, составило 0,15 (CI: 0,04, 0,69, p = 0,009) (рисунок).
Рисунок. Отношение шансов по показателю эрадикации C. trachomatis на 4-й неделе терапии
По другим параметрам эффективности и безопасности, таким как эрадикация возбудителя на 2-й неделе терапии, выздоровление (клиническая эффективность на 2-й неделе), стойкий клинический ответ (эффективность на 4-й неделе), количество нежелательных реакций, статистически достоверных различий выявлено не было.
Очевидно, что появление новых антибактериальных средств расширяет возможности врача при подборе оптимальной антимикробной терапии. Так произошло при появлении азитромицина в качестве средства для лечения хламидиоза. С другой стороны, как показало рассматриваемое исследование, доксициклин, относительно недорогой и достаточно давно используемый для лечения хламидийных НГУ препарат, имеет все основания считаться препаратом выбора, поскольку имеет преимущества перед азитромицином по показателю эрадикации C. trachomatis на 4-й неделе с начала терапии.
Весьма значимой и актуальной является проблема оптимальной антибиотикотерапии нехламидийных НГУ. Наиболее часто при нехламидийных НГУ выявляются Mycoplasma genitalium (у 23,8 % пациентов) и U. urealyticum (у 18,8 %). И если НГУ, вызванные U. urealyticum, очень хорошо поддаются терапии препаратами первой линии (доксициклином и азитромицином), то в случае инфицирования M. genitalium результаты лечения указанными препаратами являются далеко не такими однозначными. Так, к примеру, в одном из недавно (2006 г.) проведённых исследований неэффективность лечения при стандартном однодозном приёме азитромицина в дозировке 1 г достигала 28 % [8]. Эффективность терапии фторхинолонами уретритов, вызванных M. genitalium, низкая, а данные по тетрациклинам противоречивые.
Возможные пути повышения эффективности терапии заболеваний, обусловленных M. genitalium, представляются в использовании более длительных схем назначения азитромицина (5 дневный курс: 0,5-0,25-0,25-0,25-0,25), применении более активных в отношении данного микроорганизма макролидов (например, джозамицина) или использовании антибактериальных препаратов других групп (фторхинолоны IV поколения) [9].
Пока идёт накопление информации о роли и особенностях (чувствительность к антимикробным препаратам, методы культивирования и т. д.) разных микоплазм в развитии инфекций репродуктивных органов у мужчин, основным критерием выбора антимикробных препаратов должны быть результаты клинических исследований.
Представляется очевидным, что для выработки оптимальной антимикробной терапии уретритов, вызванных микоплазмами, потребуется дальнейшее накопление и анализ данных по клинической эффективности разных схем терапии. В настоящее время это направление исследований является весьма актуальным.
Заключение
Данные наиболее актуального на сегодняшний день мета-анализа свидетельствуют о том, что доксициклин является наиболее эффективным и безопасным препаратом для лечения НГУ у мужчин, вызванного Clamydia trachomatis. При этом важно отметить, что с точки зрения переностимости и удобства приёма предпочтение стоит отдавать доксициклину в виде соли моногидрата (Юнидокс Солютаб). Весьма актуальной представляется сегодня проблема определения оптимальных схем лечения НГу, вызванных Mycoplasma genitalium, поскольку традиционно применяющиеся противохламидийные режимы терапии, в частности однократный приём азитромицина в дозе 1 г, в отношении данного возбудителя оказываются недостаточно эффективными. Джозамицин имеет высокую активность in vitro в отношении различных видов микоплазм, а результаты современных клинических исследований свидетельствуют о высокой эффективности этого макролида при НГУ, вызванном Mycoplasma genitalium у мужчин. Представляется перспективным дальнейшее накопление клинических данных по возможностям терапии джозамицином в рамках более крупных сравнительных рандомизированных исследований, что позволит определить место этого препарата в терапии больных НГУ.
Негонококковые уретриты у мужчин: современные взгляды на этиологию и подходы к лечению
Проблема негонококковых уретритов (НГУ) у мужчин известна уже более 100 лет — так, первое сообщение в литературе о неспецифическом уретрите у мужчин датируется 1886 г.
Проблема негонококковых уретритов (НГУ) у мужчин известна уже более 100 лет — так, первое сообщение в литературе о неспецифическом уретрите у мужчин датируется 1886 г. [1]. Впервые термин «негонококковый уретрит» для обозначения случаев воспаления уретры, вызванных не гонококками, был предложен на симпозиуме, посвященном данной проблеме, который проводился Международным союзом по борьбе с венерическими заболеваниями и трепонематозами (The International Union against the Veneral Diseases and Treponematoses) в Монте-Карло (Монако) в сентябре 1954 г. [2]. Эксперты обратились к ВОЗ с просьбой рассмотреть возможность пересмотра международной медицинской терминологии и включить в нее термин «негонококковый уретрит». В настоящее время в МКБ10 присутствуют различные нозологические формы гонококковой (код А54) и хламидийной (код А55) инфекций, а также такие отдельные нозологические формы, как «неспецифический уретрит» (код 34.1) и «другие уретриты» (код 34.2).
Эпидемиология
Негонококковый уретрит является широко распространенным заболеванием как в мире, так и в России. В мире ежегодно регистрируют около 50 млн случаев НГУ [3], в США — 4–8 млн случаев [4]. В США и Великобритании заболеваемость НГУ значительно превысила заболеваемость гонококковым уретритом, что обусловлено не только действительным ростом числа уретритов, вызываемых микроорганизмами, отличными от Neisseria gonorrhoeae, но и повышением качества лабораторных методов идентификации различных инфекционных агентов [5, 6]. Так, в Великобритании за период 1998–2000 гг. у мужчин в общей практике частота гонореи составила 1,3 на 100 тыс., хламидийной инфекции — 5,0 на 100 тыс., а неспецифических уретритов и выделений из уретры — 210,3 на 100 тыс. [7]. При анализе распространенности этих заболеваний по данным клиник, занимающихся проблемами мочеполовой системы, оказалось, что гонорея у мужчин регистрировалась с частотой 42 на 100 тыс., хламидийная инфекция — 90,2 на 100 тыс., а неспецифические уретриты и выделения из уретры — 217,3 на 100 тыс. [7].
В России, по данным официальной статистики, выявляется около 350 тыс. случаев НГУ ежегодно, однако эти показатели явно занижены ввиду недостаточной регистрации инфекций во многих коммерческих клиниках, с одной стороны, и высокой распространенности самолечения, с другой [8, 9].
Этиология
Диагноз НГУ устанавливается в том случае, когда у пациента имеются клинические симптомы уретрита и при микроскопии мазка из уретры, окрашенного по Граму, выявляются признаки воспаления, но при этом не определяются внутриклеточно расположенные грамотрицательные диплококки и трихомонады [10]. Частой причиной НГУ (15–55% случаев) является Chlamydia trachomatis, при этом частота обнаружения данного патогена при НГУ уменьшается с возрастом [10]. Этиология некоторых случаев негонококкового нехламидийного уретрита остается неизвестной. В ряде исследований в качестве этиологически значимых патогенов при НГУ рассматриваются Ureaplasma urealyticum и Mycoplasma genitalium [11–14]. Кроме того, возбудителями НГУ могут быть вирус простого герпеса и аденовирусы [15, 16]. В данной статье мы не будем касаться проблемы хламидийного уретрита у мужчин, поскольку эта инфекция, передаваемая половым путем (ИППП), хорошо изучена и разработаны четкие рекомендации по ее лечению, в отличие от неспецифического уретрита (негонококкового нехламидийного уретрита).
Микоплазмы и уреаплазмы являются самыми мелкими свободно живущими прокариотами [17]. Они принадлежат к семейству Mycoplasmataceae, входящему в класс Mycoplasmatales, поэтому фактически оба микроорганизма являются микоплазмами. Семейство Mycoplasmataceae разделяется на два рода: Mycoplasma и Ureaplasma.
В настоящее время общепризнана этиологическая роль трех основных видов микоплазм в патогенезе инфекций мочеполовых путей у человека — M. genitalium, M. hominis и Ureaplasma urealyticum, причем последние два возбудителя также могут быть причиной проблем со стороны репродуктивного тракта и инфекций у новорожденных [17–20]. Роль ряда других микоплазм в инфекционной патологии человека является не столь определенной.
M. genitalium была впервые выделена у мужчины с клиникой негонококкового уретрита в 1980 г. [21]. Изучение роли M. genitalium в этиологии заболеваний урогенитального тракта человека было в значительной степени затруднено, поскольку процесс культурального исследования для выделения данного микроорганизма является крайне сложным. Появление полимеразной цепной реакции (ПЦР) значительно расширило диагностические возможности при НГУ — после широкого внедрения этого метода диагностики получены доказательства роли M. genitalium в этиологии НГУ у мужчин, а также цервицита и эндометрита у женщин. Кроме того, был подтвержден половой путь передачи M. genitalium у гетеросексуальных партнеров [22].
За последние 5 лет было опубликовано достаточно много работ, в которых изучалась роль M. genitalium в этиологии НГУ: один метаанализ, выполненный J. S. Jensen [23], семь исследований типа «случай-контроль» и пять исследований серии случаев НГУ.
По результатам метаанализа частота выделения M. genitalium у пациентов с нехламидийным негонококковым уретритом варьирует от 18,4% до 45,5% [24]. В табл. 1 приведены данные ряда исследований о частоте выделения M. genitalium у пациентов с клиникой уретрита. Как оказалось, бессимптомное носительство M. genitalium наблюдается редко.
U. urealyticum была впервые выделена в 1954 г. у пациента с НГУ [31], а название микроорганизма обусловлено его способностью гидролизовать мочевину с образованием аммиака, т. е. уреазной активностью. В ряде исследований (табл. 1) получены доказательства этиологической роли U. urealyticum в развитии острого НГУ — по различным данным уреаплазмы выявляются примерно в 10% случаев этого заболевания [32]. Необходимо отметить, что с момента идентификации двух различных биоваров U. urealyticum (биовар 1 U. parvum и биовар 2 U. urealyticum) обнаружено, что биовар 2 (U. urealyticum) достоверно чаще встречается при урогенитальных инфекциях с клиническими проявлениями, чем биовар 1 (вид U. parvum) [33].
В то же время, согласно результатам других исследований, микроорганизмы рода Ureaplasma spp. и M. hominis могут обнаруживаться в нижних отделах урогенитального тракта у 30–40% здоровых сексуально активных молодых людей [34].
При изучении влияния M. hominis на состояние сперматогенеза (подвижность сперматозоидов, плотность спермы, морфологию) у 234 пациентов установлено, что, несмотря на высокую частоту обнаружения этих микроорганизмов (13,3%), они не оказывают отрицательного влияния на характеристики спермы, а следовательно, и на фертильность мужчин [35].
В отношении НГУ имеется целый ряд невыясненных моментов. Отмечается значительное число ошибок при анализе и интерпретации результатов микроскопии мазков из уретры и подсчете количества полиморфно-ядерных лейкоцитов (ПМЯЛ) как при исследованиях разными лаборантами, так и при повторном анализе одним и тем же лаборантом. Особенно это касается случаев уретрита с незначительно выраженной воспалительной реакцией [36, 37]. У многих мужчин с уретритом не выявляется ни один из известных патогенов [24, 38–40]. Примерно у трети мужчин, инфицированных C. trachomatis или M. genitalium, не отмечается увеличения числа ПМЯЛ [39, 41–44, 45]. Чувствительность микроскопического исследования мазка из уретры (≥ 5 ПМЯЛ) значительно выше при наличии явных выделений из уретры; кроме того, различия в чувствительности исследования зависят от исследуемой популяции и техники взятия материала. При наличии явных выделений из уретры частота обнаружения C. trachomatis или M. genitalium достигает 50% [39, 42, 44]. При обследовании половых партнеров пациентов с неспецифическим уретритом неустановленной этиологии в 3–20% случаев выявляется бессимптомная инфекция C. trachomatis или M. genitalium [39, 46–49].
Чувствительность к антимикробным препаратам и проблемы антибиотикорезистентности генитальных микоплазм и уреаплазм
Патогенные для человека микоплазмы имеет существенные биологические отличия от «типичных» бактериальных возбудителей. Специфической характеристикой микоплазм и уреаплазм, определяющей их природную резистентность ко многим антимикробным препаратам (АМП), является отсутствие у них клеточной стенки, в результате чего эти микроорганизмы устойчивы ко всем бета-лактамным антибиотикам (пенициллинам, цефалоспоринам, карбапенемам) и гликопептидам (ванкомицину). Кроме того, микоплазмы устойчивы к полимиксину, рифампицину, сульфаниламидам, триметоприму и налидиксовой кислоте.
Данные об активности различных АМП in vitro против микоплазм и уреаплазм приведены в табл. 2 [50, 51].
Наиболее активными антибиотиками, подавляющими рост микоплазм, являются макролиды, тетрациклины и новые фторхинолоны [52–54]. Аминогликозиды обладают значительно меньшей активностью против микоплазм и не применяются в клинической практике для лечения микоплазменной инфекции, так как эти микроорганизмы часто находятся внутриклеточно.
Профили резистентности различных видов микоплазм и уреаплазм к разным макролидам, тетрациклинам и фторхинолонам существенно различаются (табл. 2). Тем не менее, проведено крайне мало исследований, направленных на изучение связи между показателями чувствительности in vitro и результатами клинической эффективности терапии.
Так, в исследовании Yasuda M. с соавт. (2005 г.) изучалась минимальная подавляющая концентрация (МПК) фторхинолонов в отношении M. genitalium и их бактериологическая эффективность в лечении пациентов с НГУ, вызванными M. genitalium. In vitro левофлоксацин оказался менее активным, чем гатифлоксацин, тосуфлоксацин и спарфлоксацин, а in vivo бактериологическая эффективность гатифлоксацина превосходила таковую левофлоксацина или тосуфлоксацина [55].
Определение чувствительности микоплазм и уреаплазм к антибиотикам in vitro имеет объективные трудности. В связи со сложностью культивирования и медленным ростом M. genitalium для выявления резистентности у данного микроорганизма обычно используют молекулярные методы. Для определения чувствительности более быстро растущих и легче культивируемых M. hominis и U. urealyticum используют методы разведения в агаре, микроразведений в бульоне и Е-тестов. В настоящее время компанией bioMerieux предложен коммерческий тест для определения чувствительности указанных микроорганизмов, основанный на принципе микроразведений в бульоне. Тем не менее, следует учитывать, что до сих пор нет единой стандартизированной и общепринятой методики определения чувствительности микоплазм к антибиотикам, что может приводить к значительным расхождениям при определении активности различных АМП в отношении микоплазм и уреаплазм. Более того, не установлена четкая корреляция между значениями МПК антибиотиков in vitro и показателями микробиологической эффективности терапии микоплазменных и уреаплазменных инфекций.
В настоящее время изучается новый метод для определения чувствительности M. genitalium к антибиотикам, основанный на ПЦР в режиме реального времени [54, 56].
Таким образом, на сегодняшний день существует крайне много «белых пятен» в наших представлениях о резистентности к антибиотикам микоплазм и уреаплазм и ее значении для клинической практики, что требует дальнейших экспериментальных и клинических исследований в данной области и разработки стандартизированного метода определения чувствительности данных микроорганизмов, приемлемого для рутинной практики.
Современные подходы к терапии НГУ у мужчин, вызванного микоплазмами или уреаплазмами
Проблема терапии урогенитальных инфекций, обусловленных микоплазмами или уреаплазмами, представляется достаточно сложной и неоднозначной.
В соответствии с существующими рекомендациями при урогенитальных инфекциях микоплазменной и уреаплазменной этиологии используются традиционные схемы терапии макролидами, тетрациклинами или фторхинолонами, принятые для лечения хламидийной инфекции (табл. 3) [10, 34]. Выбор варианта лечения НГУ определяется его доступностью — все перечисленные режимы обладают приемлемой эффективностью.
Аналогичные препараты и схемы лечения НГУ у мужчин рекомендуются и в руководстве «Урогенитальные инфекции», изданном Европейской урологической ассоциацией в 2010 г. [14]:
Современная антибактериальная терапия негонококковых уретритов: проблемы и решения
Представлен обзор современных подходов к антибактериальной терапии негонококковых уретритов. Актуальность данной проблемы связана с крайне высокой распространенностью заболевания в России и мире. Наиболее частыми возбудителями негонококковых уретритов являются Chlamydia trachomatis, Mycoplasma genitalium, Ureaplasma urealyticum. К основным препаратам для лечения инфекций, вызванных атипичными микроорганизмами, относятся макролиды, тетрациклины и новые фторхинолоны. Однако в последнее время большую актуальность приобретает проблема резистентности основных возбудителей негонококковых уретритов к отдельным антибиотикам, в частности фторхинолонам и макролидам.
Представлен обзор современных подходов к антибактериальной терапии негонококковых уретритов. Актуальность данной проблемы связана с крайне высокой распространенностью заболевания в России и мире. Наиболее частыми возбудителями негонококковых уретритов являются Chlamydia trachomatis, Mycoplasma genitalium, Ureaplasma urealyticum. К основным препаратам для лечения инфекций, вызванных атипичными микроорганизмами, относятся макролиды, тетрациклины и новые фторхинолоны. Однако в последнее время большую актуальность приобретает проблема резистентности основных возбудителей негонококковых уретритов к отдельным антибиотикам, в частности фторхинолонам и макролидам.
Уретрит, или воспаление мочеиспускательного канала, – широко распространенное инфекционное заболевание, в большинстве случаев передающееся половым путем. Заболевание протекает, как правило, с жалобами на патологические выделения из уретры, дизурию и/или дискомфорт в уретре, но может и клинически не проявляться. Диагноз уретрита подтверждается повышением уровня полиморфноядерных лейкоцитов в первой порции мочи или мазке из уретры.
Уретриты подразделяются на гонококковые, если при выполнении микроскопии мазка с окраской по Граму обнаружены Neisseria gonorrhoeae, и негонококковые (НГУ), если грамотрицательные диплококки в мазке не выявлены.
Термин «неспецифический уретрит» применяется для заболеваний негонококковой и нехламидийной природы. Уретрит хламидийной этиологии может сопровождаться артритом и конъюнктивитом [1, 2].
Существует ряд сложностей в постановке диагноза НГУ, что связано с ошибками в выполнении и интерпретации мазков из уретры, подсчетом числа лейкоцитов у пациентов со слабой степенью выраженности воспаления и затруднениями в типировании возбудителя заболевания [3].
В России, по данным официальной статистики, регистрируется около 350 тыс. случаев НГУ ежегодно, однако реальная распространенность этой патологии может быть значительно выше [4, 5].
Центр по контролю и профилактике заболеваний США не публикует данные по уретриту как синдрому, в то же время предоставляя сведения по заболеваемости инфекциями, передаваемыми половым путем. Чаще других регистрируется хламидиоз, причем наблюдается ежегодный рост этого показателя. В 2016 г. число новых случаев заболевания превысило 1,5 млн, увеличившись с 2015 г. на 4,7%. Женщины болеют хламидиозом в 2 раза чаще, чем мужчины, представители негроидной расы – в 5,6 раза чаще, чем представители белой расы, а самая высокая заболеваемость наблюдается среди подростков и молодых людей [6, 7].
Основные возбудители негонококковых уретритов
Самый распространенный возбудитель НГУ – Chlamydia trachomatis (11–50% случаев НГУ, по данным разных исследований), однако частота обнаружения этого патогена при НГУ уменьшается с возрастом.
Mycoplasma genitalium впервые была выделена из уретры в 1980 г. Появление метода полимеразной цепной реакции позволило чаще диагностировать этот микроорганизм (в 6–50% случаев НГУ).
В 5–15% случаев и Chlamydia trachomatis, и Mycoplasma genitalium выделяются одновременно. Согласно Европейским рекомендациям по ведению пациентов с НГУ 2016 г., обнаружение Chlamydia trachomatis и Mycoplasma genitalium наиболее характерно:
Кроме того, Mycoplasma genitalium чаще связана с баланопоститом, а Chlamydia trachomatis – баланитом.
В 30–80% случаев НГУ ни Chlamydia trachomatis, ни Mycoplasma genitalium не определяются [1].
Реже при НГУ выявляются уреаплазмы (11–26%), трихомонады (1–20%), аденовирусы (2–4%) и вирус простого герпеса (2–3%) [8, 9].
Выделение Trichomonas vaginalis зависит от локального уровня распространенности данного микроорганизма в популяции.
Существуют убедительные доказательства того, что Ureaplasma urealyticum может в некоторых случаях вызывать уретрит [10]. Обнаружение уреаплазмы даже с использованием теста амплификации нуклеиновых кислот не позволяет отличить бессимптомное носительство и возможную причину развития НГУ [11]. Более высокая нагрузка на организм (> 1000 копий/мл FVU) считается более сильным предиктором НГУ.
В ранних исследованиях не проводилось различия между Ureaplasma urealyticum и Ureaplasma parvum (последняя чаще выявляется у пациентов контрольной группы без НГУ), а потому последовательная связь уреаплазм с развитием НГУ не могла быть доказана.
Сейчас накапливается все больше подтверждений того, что бактерии, связанные с бактериальным вагинозом, могут вызывать НГУ [10, 11].
Аденовирусы и вирус простого герпеса ответственны за 2–4% симптомных случаев НГУ и могут сочетаться с конъюнктивитом.
Neisseria meningitidis, Haemophilus spp., Candida spp., стриктуры и инородные тела уретры, вероятно, составляют небольшую долю в этиологии НГУ, в то время как ранее обсуждаемая роль вируса Эпштейна – Барр в настоящее время сомнительна.
Причина НГУ при отрицательных микробиологических тестах (идиопатический уретрит) неясна, и в таком случае НГУ, вероятно, может носить и неинфекционный характер. Однако диагностические инструменты в настоящее время не могут гарантировать отсутствие инфекционного агента на 100%.
Бессимптомный уретрит без видимых выделений в отличие от симптоматического уретрита, вероятно, имеет другую этиологию, причем Chlamydia trachomatis и Mycoplasma genitalium обнаруживаются значительно реже в отсутствие клинических симптомов [1].
Таким образом, наиболее частыми возбудителями при НГУ являются внутриклеточные микроорганизмы, хламидии и микоплазмы. Ввиду того что данные патогены не имеют собственной клеточной стенки, они природно резистентны к большой группе антибактериальных препаратов, реализующих действие за счет нарушения синтеза и целостности клеточных стенок бактерий, – бета-лактамным антибиотикам, гликопептидам и др.
Обзор современных клинических рекомендаций по лечению негонококковых уретритов
К основным препаратам для лечения инфекций, вызванных атипичными микроорганизмами, относятся макролиды, тетрациклины и новые фторхинолоны (табл. 1) [12, 13].
Согласно Европейским рекомендациям по ведению пациентов с НГУ 2016 г., мужчинам с ярко выраженными проявлениями уретрита следует назначать антибиотикотерапию эмпирически до получения результатов лабораторных анализов. В качестве препарата первой линии рекомендован доксициклин, препаратов второй линии – азитромицин, тетрациклин и лимециклин (табл. 2) [1]. Считается, что лимециклин обладает большим профилем безопасности, чем доксициклин, однако в России он зарегистрирован только для лечения акне.
Для лечения хламидийной и микоплазменной инфекции как в Европе, так и в России существуют отдельные клинические рекомендации. Так, согласно Федеральным клиническим рекомендациям 2015 г. по ведению пациентов с хламидийной инфекцией нижнего отдела мочеполовой системы, к препаратам выбора также относятся доксициклин и азитромицин, а кроме того, 16-членный макролид джозамицин (табл. 3) [14]. В Европейских рекомендациях 2015 г. наряду с указанными выше препаратами присутствуют эритромицин и фторхинолоны (табл. 4) [15].
Для лечения урогенитальных инфекций, вызванных Mycoplasma genitalium, Федеральные клинические рекомендации 2015 г. предлагают использовать доксициклин, джозамицин и офлоксацин (табл. 5) [16]. В то время как в Европейских рекомендациях 2016 г. наряду с вышеперечисленными препаратами указаны азитромицин в качестве одного из вариантов терапии первой линии при отсутствии резистентности к макролидам, моксифлоксацин и пристинамицин (табл. 6) [17]. Последний препарат, представитель стрептограминов, в РФ не зарегистрирован.
В настоящее время лечение инфекции, вызванной Mycoplasma genitalium, вызывает затруднения ввиду стремительного распространения антибиотикорезистентных штаммов. Появление мультирезистентных штаммов Mycoplasma genitalium отмечено уже во многих странах. Например, в Австралии в 2013 г. резистентность Mycoplasma genitalium к фторхинолонам и макролидам составляла 9,8% [18], а в Японии в 2016 г. – 30,8% [19].
Определение чувствительности внутриклеточных возбудителей – трудоемкий и затратный процесс. В отечественной литературе имеются единичные публикации, посвященные изучению распространенности резистентных штаммов Mycoplasma genitalium. По данным E. Shipitsyna и соавт. (четыре города, 2013–2016 гг.), резистентность Mycoplasma genitalium к макролидам составила в среднем 4,6%, фторхинолонам – 6,2% и одновременно к макролидам и фторхинолонам – около 1% [20].
Как уже было сказано, в Европейских рекомендациях по ведению пациентов с НГУ 2016 г. в качестве препарата первой линии выбран представитель тетрациклинов – доксициклин [15]. Во-первых, этот препарат эффективен в отношении Chlamydia trachomatis – возбудителя, ответственного за 50% случаев НГУ. Во-вторых, при его применении снижена вероятность селекции штаммов Mycoplasma genitalium, резистентных к макролидам и фторхинолонам. Однако клиническая эффективность терапии доксициклином в отношении Mycoplasma genitalium составляет порядка 30–40% и также сопряжена с риском развития побочных реакций, в частности фотосенсибилизацией [21].
При инфекциях, вызванных Mycoplasma genitalium, описаны случаи клинической и/или микробиологической неэффективности и макролидов, и тетрациклинов, и фторхинолонов, что может приводить к хроническому или рецидивирующему течению урогенитальной инфекции [22]. Применяемые в настоящее время режимы терапии доксициклином, эффективные при уретрите хламидийной природы, не всегда обеспечивают эрадикацию микоплазм [23–25].
В рандомизированном исследовании L.A. Mena и соавт., проведенном с участием 398 мужчин с уретритом, терапия азитромицином в дозе 1 г однократно и доксициклином в дозе 100 мг в течение семи дней оказалась неэффективной у 16 и 64% пациентов, пришедших на контрольный осмотр, соответственно [24].
Качественной альтернативой доксициклину является другой представитель тетрациклинов – миноциклин. В исследовании S. Maeda и соавт. частота эрадикации Mycoplasma genitalium на фоне применения миноциклина у пациентов с микоплазменным НГУ составила 90,9% [26].
C. Foschi и соавт. изучали антибиотикорезистентность Mycoplasma hominis и Ureaplasma spp. у 4660 пациентов с урогенитальной инфекцией в Италии в 2015–2016 гг. (табл. 7) [27]. Наиболее часто (69,8%) определялись уреаплазмы, гораздо реже Mycoplasma hominis (11,4%) и смешанная инфекция (18,8%). Резистентность менее частых возбудителей НГУ к макролидам и фторхинолонам достигала высокого уровня в отличие от тетрациклинов, что позволяет рекомендовать их, в частности миноциклин, в качестве препаратов первой линии для эмпирической терапии НГУ.
Y.H. Zhou и соавт. с 2011 по 2016 г. изучали уровень антибиотикорезистентности Ureaplasma spp. и Mycoplasma hominis у 5016 мужчин, страдающих бесплодием (табл. 8) [28]. Уровень резистентности возбудителей к полусинтетическим тетрациклинам, включая миноциклин, за весь период не превышал 3%, при этом доля возбудителей, устойчивых к фторхинолонам, в 2016 г. составила 80,2%, а к азитромицину – 33,9%.
Миноциклин, представитель полусинтетических тетрациклинов, разрешен к использованию в РФ и показан для лечения НГУ, в соответствии с официальной инструкцией по медицинскому применению. Для лечения неосложненных урогенитальных инфекций рекомендуется назначать миноциклин по 100 мг 2 р/сут курсом семь – десять дней. По сравнению с доксициклином миноциклин обладает лучшим профилем безопасности и более выраженной клинической эффективностью, что, вероятно, связано с его дополнительной иммуномодулирующей и противовоспалительной активностью [29].
E.A. Eady и соавт., изучая антихламидийный эффект миноциклина в системах in vitro и in vivo, наглядно продемонстрировали, что Минолексин способен ингибировать рост в культуре клеток 11 изолятов хламидий, выделенных при НГУ, в минимальной концентрации 0,03–0,06 мкг/мл, что свидетельствует о высокой чувствительности возбудителей к данному препарату [30]. При пероральном использовании Минолексина в суточной дозе 100 мг в течение семи дней у всех наблюдаемых больных НГУ (n = 31) удалось добиться элиминации хламидий [30]. В аналогичном исследовании 192 женщины с хламидийной инфекцией, осложненной трихомониазом и гонореей, принимали миноциклин по 50 мг 2 раза в день [31]. Через 8–14 дней после завершения лечения Chlamydia trachomatis была выделена только у одной из 112 пациенток.
Е.С. Снарская и соавт. в России применяли Минолексин и доксициклин у 30 больных обоего пола с установленным диагнозом урогенитального хламидиоза, у семи из них выявлено сочетание Chlamydia trachomatis с уреаплазменной инфекцией, у трех – с гарднереллезной, у двух – с кандидозной инфекцией. Минолексин получали 20 пациентов (десять мужчин и десять женщин, средний возраст 26,78 ± 0,89 года, средняя продолжительность заболевания 58,02 ± 1,33 дня) по 100 мг перорально 2 р/сут, курс 14 дней. Доксициклин был назначен десяти пациентам (семи мужчинам и трем женщинам, средний возраст 26,3 ± 1,29 года, средняя продолжительность заболевания 57,42 ± 1,71 дня) по 100 мг перорально каждые 12 часов, курс 14 дней [32]. В процессе лечения у больных, принимавших Минолексин, чувство дискомфорта в области половых органов исчезало быстрее, чем у пациентов, получавших доксициклин (в среднем 52,2 ± 4,25 и 82,67 ± 5,78 часа соответственно, p