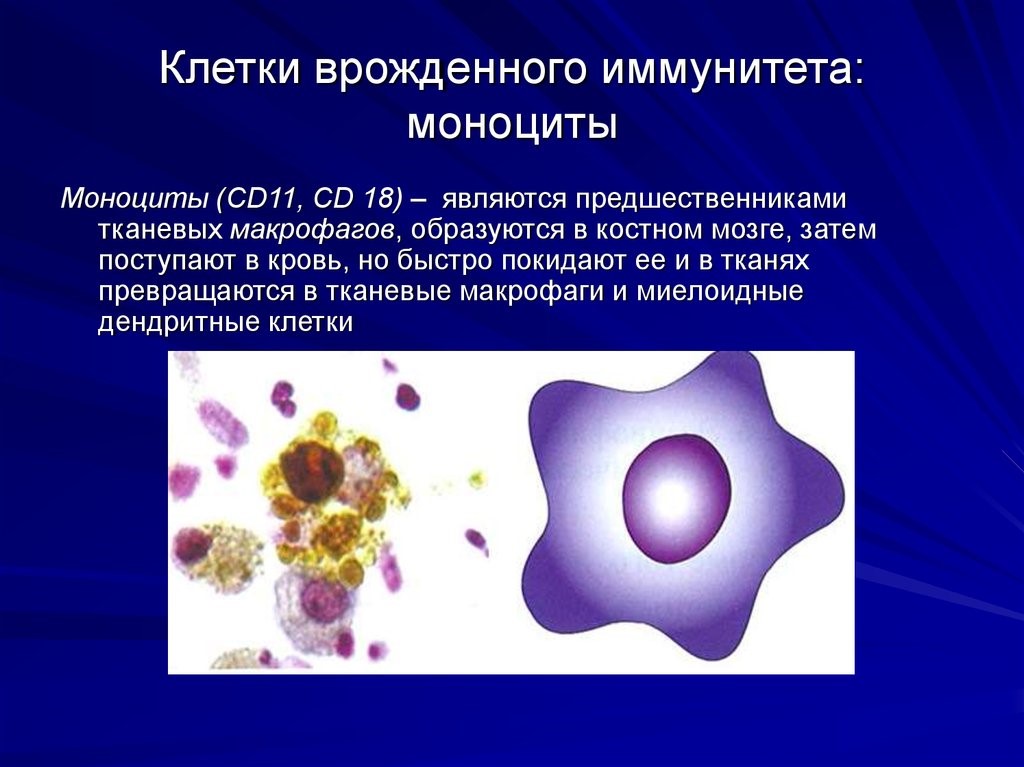
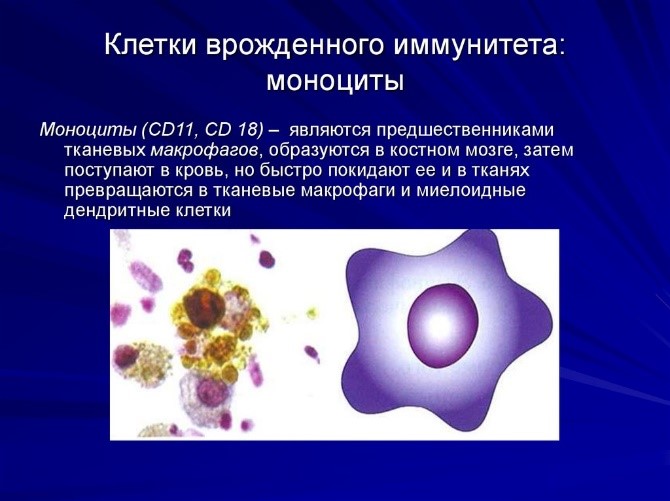
Cобственный интерферон —
лучший из возможных
Как организм вырабатывает интерферон. Эффективность естественных интерферонов для иммунитета. Бактериальные лизаты как естественный активатор иммунной системы и стимуляции собственного интерферона.
Человек борется с вирусами с незапамятных времен. За миллионы лет эволюции наш организм выработал универсальную стратегию борьбы с неприятелем. Одним из ключевых игроков этого противостояния являются интерфероны. Это вещества, помогающие организму в короткий срок справиться с вирусами. Сегодня существует большое количество препаратов, содержащих в своем составе те или иные интерфероны. Но так ли они эффективны как собственный интерферон, вырабатываемый организмом?
Что такое интерферон?
В настоящее время известно более 20 интерферонов, которые подразделяются на три типа 3,4 :
Как работают собственные интерфероны человека?
Противовирусные свойства интерферонов вызывали у исследователей большой интерес с точки зрения терапии ряда заболеваний. И со временем благодаря различным медицинским и технологическим возможностям удалось получить лекарственные препараты, которые содержат в своем составе интерферон.
Использование препаратов интерферона в медицине
Препараты интерферона активно используются в лечении широкого спектра вирусных заболеваний. В частности, речь идет о вирусе папилломы человека, вирусных гепатитах, герпетической инфекции, а также гриппа и простудных заболеваний. Важным фактором выбора препаратов, содержащих интерферон для лечения того или иного заболевания, будет являться концентрация интерферона в препарате, то, каким способом он получен и какой тип интерферона (α, β, γ или λ) содержит в своем составе. Несмотря на то, что существуют препараты интерферона, которые отпускаются без рецепта, все же с врачом лучше заранее проконсультироваться, поскольку в отношении этих препаратов есть ряд противопоказаний. По способу получения препараты интерферона можно поделить на 4 типа 6,7 :
Преимущества и недостатки привнесенных интерферонов
К преимуществам препаратов, содержащих в своем составе интерфероны, можно отнести их доступность. Немаловажное преимущество интерферонов – возможное их применение против широкого спектра вирусов.
Сравнительно высокий уровень безопасности препаратов интерферона позволяет их применять и детям, которые, как известно, часто болеют гриппом и другими ОРВИ.
Экстренная иммунозащита от вирусов
Наш организм в процессе эволюции приспособился к борьбе с вирусами, однако при необходимости мы можем ему помочь, не сильно вмешиваясь в его работу.
Семь мифов об иммунитете

Миф №1. Витамин C укрепляет иммунитет
Считается, что витамин C укрепляет иммунную систему, однако это не совсем так. Принимая аскорбинку ежедневно, нельзя избежать простуды, можно лишь незначительно ослабить некоторые симптомы заболевания.
Многие люди убеждены также в пользе цинка. На самом деле он не помогает при простуде и не укрепляет иммунитет так существенно, как считается.
По-настоящему эффективен витамин Д, который еще называют солнечным, поскольку он образуется в клетках кожи под влиянием ультрафиолетовых лучей. Под их воздействием защитные клетки организма активируются, что очень важно для иммунной системы. Возможно, именно поэтому мы особенно подвержены инфекциям в холодное время года, когда световые дни короткие, и недостаток солнечного света приводит к дефициту витамина Д, что ослабляет иммунитет. Много витамина Д содержится в рыбе, особенно в сардинах, лососе, семге и в рыбьем жире. В связи с этим для укрепления иммунитета рекомендуется есть рыбу, а после приема пищи обязательно совершать длительные пешие прогулки.
Миф №2. Прививки? Нет уж, ведь каждая болезнь создает свой иммунитет
Люди, которые выросли в больших семьях вместе с братьями и сестрами, заражавшими друг друга разными инфекциями, и те, кто провел детство в условиях сельской местности, впоследствии страдают от болезней значительно реже, чем единственные в семье дети, к тому же живущие в городских квартирах. Именно в раннем возрасте наша иммунная система нуждается в подобных вирусных тренировках, чтобы, становиться устойчивыми к опасным патогенным возбудителям.
Отказываться от прививок ни в коем случае нельзя. Их делают, прежде всего, от смертельно опасных и вызывающих серьезные осложнения болезней. Согласно статистике, при отсутствии иммунитета риск осложнений значительно выше.
Миф №3. Спорт укрепляет иммунитет
Известно, что те, кто занимается спортом несколько раз в неделю, болеют реже, а заболев, быстрее выздоравливают. Дело в том, что регулярные занятия физической культурой активизируют и мобилизуют защитные силы организма. В равных условиях больные раком, занимающиеся спортом, несмотря на болезнь, имеют больше шансов выжить, чем те, кто из-за заболевания практически не двигается.
Однако надо соблюдать чувство меры, поскольку чрезмерно интенсивные тренировки вредят здоровью. В таких случаях спорт становится для организма стрессовым фактором, особенно если сопровождается психологическим давлением в виде конкуренции. В подобном состоянии человек особенно подвержен болезням. Доказано, что профессиональные спортсмены болеют чаще, чем любители.
Золотое правило для всех и каждого – во время болезни прекратить тренировки до полного выздоровления. Иначе даже обычная простуда может привести к смертельно опасным осложнениям, например, миокардиту. Спорт полезен для здоровья в разумных пределах.
Миф №4. При хорошем иммунитете прививки необязательны
Это не так. Существуют группы риска. Люди, которые в них входят, особо уязвимы для болезней и чаще страдают от осложнений. Так, сезонный грипп опасен для пожилых и хронических больных. Для ребенка, который еще ни разу не был привит, смертельным может стать коклюш. А вирус, вызывающий краснуху, при попадании в организм будущей мамы, вредит не столько ей самой, сколько еще не родившемуся малышу. Особенно опасно заболевание в первом триместре беременности, когда у плода развиваются врожденные уродства.
Зачастую люди являются переносчиками опасных микроорганизмов, и при этом сами не болеют. Поэтому специалисты советуют делать прививки не только тем, кто входит в группу риска, но и работающим или живущим рядом с ними.
Миф №5. Чем сильнее простуда, тем слабее иммунитет
В этом специалисты были убеждены долгое время, однако данное утверждение верно лишь отчасти. Например, при попадании в организм вируса гриппа чем меньше иммунная система противостоит возбудителю, тем сильнее человек болеет. Этого можно избежать при подготовленном и укрепленном вакцинацией иммунитете. Он защищает и от осложнений, которые нередко возникают вследствие тяжелого течения заболевания.
Миф №6. Если организм справился с заболеванием, то в дальнейшем оно не грозит
Это утверждение верно лишь частично. При попадании микроба в организм, иммунная система человека побеждает его, вырабатывая специфическую защиту против чужеродных агентов – антитела. При повторном проникновении возбудителя в организм эти активные частицы обезвреживают микроб, и человек остается здоровыми. Именно поэтому детскими инфекционными болезнями люди болеют один раз в жизни, получая к ним стойкий иммунитет.
Но респираторные инфекции могут вызывать различные возбудители, число которых доходит до 200. Это значит, что иммунная система способна не распознать один из них, и человек снова заболеет. А вирус гриппа мутирует с высокой скоростью, поэтому в период новой вспышки сезонного заболевания иммунитет на него не реагирует, и в результате развивается эпидемия.
Миф №7. Если иммунитет сильный, то высокой температуры не будет
Повышение температуры тела указывает на то, что организм старается справиться с болезнью. Вступает в действие иммунная реакция – начинает вырабатываться такой защитный фактор, как интерферон. Происходит это при температуре тела 38 градусов, поэтому «сбивать» ее не рекомендуется. Исключение делается только для тех, кто плохо переносит гипертермию. Эксперты считают, что у людей, которые болеют без повышения температуры, ослаблен иммунитет.
Однако очень высокая температура ослабляет организм и может стать опасной. Поэтому надо ориентироваться не только на показания термометра, но, в первую очередь, на самочувствие больного.
Ольга Карулина,
врач Областного центра медицинской профилактики
Иммунолог рассказал, почему COVID-19 считается самым хитрым вирусом: обманывает организм
Как лечиться в первую неделю после заражения
Положим, вы все-таки подцепили коронавирус – или думаете, что подцепили. Можно ли в домашних условиях предпринять какие-то экстренные меры, чтоб переболеть легко – без осложнений, реанимации и ИВЛ? Подстегнуть иммунитет, наделать уколов, напихаться таблетками? Или все бессмысленно, спасения нет?
Мы попросили ответить на эти вопросы нашего соотечественника, который сейчас проживает в Лос-Анджелесе, США, доктора биологических наук Петра Игнатова, профессора, специалиста в области инфекционной иммунологии.
– Петр Евгеньевич, раньше считалось, если человек заболел ОРВИ, надо принимать препараты, повышающие иммунитет. Но в случае коронавируса это правило не работает. Ведь тяжелые осложнения, как объясняют медики, как раз и происходят из-за слишком сильного иммунного ответа организма на инфекцию. Выходит, в начале болезни иммунитет надо, наоборот, подавлять?
– Это не совсем так. Подавлять иммунитет, особенно в начале болезни, дело ненужное и даже очень опасное.
Существует два типа иммунного ответа: клеточный и гуморальный. Если отвечать на ваш вопрос очень упрощенно, то я считаю, что клеточный иммунный ответ при коронавирусной инфекции надо ослаблять, а гуморальный – наоборот, усиливать.
Но в начале инфекционного процесса все иммунные реакции запускают одни и те же клетки врожденного иммунитета. Поэтому на ранних стадиях болезни лучше ничего не подавлять, а активировать процессы, склоняющие иммунитет именно к гуморальному типу. Разделение и их взаимный антагонизм будут развиваться на более поздних этапах болезни.
– Чем отличается клеточный иммунный ответ от гуморального?
– При клеточным типе иммунного ответа с инфекцией воюют лимфоциты, способные обнаруживать и распознавать в организме клетки, пораженные вирусом. Это– киллеры. Они убивают наши зараженные клетки, ликвидируя таким образом, сразу всю «фабрику» по производству вирусов.
Это вроде бы хорошо. Но при ближайшем рассмотрении оказывается не очень нужным. При большинстве респираторных болезней с острым течением инфицированные клетки всё равно погибают при выходе из них вирионов. Все развивается очень быстро, и киллеры, часто, просто не успевают их обнаружить.
Гораздо успешнее при коронавирусной инфекции другая стратегия: заранее подавить способность вируса внедряться в здоровые клетки. Для этого нужно блокировать адгезивные свойства его поверхностного S-белка. Тогда вирус просто не сможет поражать здоровые клетки, и клеткам-киллерам уже не понадобится их убивать.
Наиболее эффективным блокирующим агентом здесь оказываются антитела. Они вырабатываются нашим организмом в процессе гуморального типа иммунного ответа. Это совершенно иной механизм, чем клеточный ответ.
Сейчас, кстати, предлагаются различные технологии по созданию искусственных антител и антителоподобных молекул-ловушек, блокирующих адгезию вируса на клетках. Некоторые лекарственные препараты тоже демонстрируют способность изменять адгезивные свойства вирусного S-белка — низкомолекулярные гепарины, например. Так, что эти направления противовирусной терапии имеют сейчас большую перспективу.
– Но почему надо оказывать предпочтение только одному типу иммунного ответа? Пусть война с вирусом идет в организме на двух фронтах.
Но SARS-CoV2 обманывает наш организм. Он вызывает выработку специальных белков, которые, словно компьютерный вирус, встраиваются и нарушают работу сигнальных путей в наших макрофагах. Это заставляет их усиленно продуцировать про-воспалительные цитокины. Если про-воспалительные цитокины вырабатываются в очень большом количестве, они буквально «сводят с ума» клетки иммунитета, и те начинают быстро разрушать собственный организм. Такой феномен называют «цитокиновым штормом».
Кроме того, что данные цитокины индуцируют массовые воспалительные реакции по всему организму, они активно включают запуск именно клеточного иммунного ответа, малоэффективного для организма в плане защиты. А, это в свою очередь, влечет за собой подавление гуморального иммунитета и снижение продукции антител, нейтрализующих коронавирус.
Коронавирус «научился» провоцировать такой тип ответа, который ему выгоден, поскольку при нем снижается выработка опасных для него противовирусных антител. Таким образом он избегает эффективной атаки со стороны иммунитета. Подобные уловки возбудителей совсем не редкость при инфекционных болезнях и носят название «иммунного отклонения».
– Можно ли помочь организму скорректировать иммунные реакции?
– Да. Как я уже сказал, надо активировать реакции гуморального иммунитета и, наоборот, при необходимости – подавить клеточный.
– У таких препаратов есть побочные явления? Можно принимать их самостоятельно, в домашних условиях, если человек только что заболел? Или это опасно?
– Самому этого делать не следует. Эти вещества небезопасны и имеют массу побочных эффектов. Подавление воспалительных реакций, индуцированных массивным «цитокиновым штормом», проводят обычно в условия стационара, на этапе развития серьезных патологий в легких и других органах.
– А какими препаратами можно активировать гуморальный иммунный ответ?
– Они тоже достаточно известны. Например, холекальциферол (или витамин Д3), который действует в организме наподобие гормона. Рецепторы к нему имеются на многих клетках и особенно на макрофагах. Включение этих рецепторов оказывает на них очень сильное воздействие, заставляя отменять выработку про- воспалительных цитокинов.
Вместо про-воспалительных цитокинов макрофаги начинают синтезировать цитокины анти-воспалительные, что естественным образом подавляет воспаление в организме. Они же запускают и процесс гуморального иммунного ответа. То есть, этот витамин способен выступать в роли некого переключателя, отменяющего «неправильный» и запускающего «правильный» механизм иммунного ответа для данной болезни.
В целях профилактики дефицита витамина Д3 в организме, его ежедневно можно принимать в небольших дозах (1-2 тыс. ед.), но при лечении эти дозы должны быть существенно выше. В течение кратковременного периода это не опасно, но в любом случае лучше проконсультироваться с врачом, поскольку имеются противопоказания.
– Если бы у вас поднялась сейчас температура и держалась сутки, какую дозу витамина Д3 вы бы приняли?
– При подозрении на коронавирусную инфекцию я бы начал принимать витамин Д3 в дозе 10-15 тыс.ед в день, а может и больше. Но принимал бы его в такой дозе только до уменьшения или прекращения симптомов болезни. Потом дозу необходимо снизить до профилактической. Витамин Д3 очень активный продукт и в больших дозах работает как сильное лекарство. Поэтому длительное его использование в очень больших дозах опасно и даже токсично для организма.
– Как еще можно помочь гуморальному иммунитету?
– Вообще-то стимуляторов гуморального иммунитета довольно много, как среди фармацевтических препаратов, так и среди продуктов природного происхождения. Препараты цинка, например, усиливают многие ферментативные процессы в клетках и активируют В-лимфоциты. Это известные стимуляторы гуморального иммунитета и выработки антител. Их применение в различных странах уже продемонстрировало хороший терапевтический эффект при COVID-19. Причем некоторые американские доктора рекомендуют очень большие дозы цинка, но не все люди их легко переносят. При повышенной кислотности цинк может раздражать желудок.
Препараты гаммаглобулинов или их фрагментов тоже хорошо работают. Показано, что введение продуктов такого рода значительно усиливает синтез антител в организме. Даже простое переливание плазмы крови способно стимулировать этот процесс.
– Вы имеете в виду плазму донора с антителами к короновирусу? Или просто обычное переливание плазмы, рутинную процедуру, которую делают, например, после операций, чтоб пациент быстрее восстановился?
– Да, я имею в виду обычное переливание плазмы. Процессы антителообразования могут стимулировать и препараты неспецифических человеческих гамма-глобулинов и даже их фрагментов. А уж гипериммунная плазма или сыворотка, с антителами к коронавирусу считается очень эффективным лекарством при данной болезни.
– Как ученый-микробиолог, что бы вы посоветовали человеку, который с большой вероятностью заразился коронавирусом? Стоит ли экстренно принять какие-то препараты? Вызвать врача? Поехать на КТ легких? Залечь в постель? Или, наоборот, больше двигаться, ходить по квартире? Делать дыхательную гимнастику?
– Я считаю, что двигаться следует как можно меньше. Нужно отлежаться! Вспомните сколько осложнений дает перенесенный «на ногах» грипп. Организм мобилизует все силы для борьбы с вирусом, а различные стрессы, переохлаждения, физические нагрузки и т. п. совершенно точно снижают активность защитных реакций при остром инфекционном процессе.
Если есть возможность, следует обязательно обратиться к врачу и выслушать его рекомендации. Кстати, не забывайте и о «втором мнении», то есть рекомендации других врачей. Любой доктор – это не господь Бог и может ошибаться.
Конечно, лечиться надо как можно раньше и интенсивно. Бездействие или недостаточно эффективное действие не способно нейтрализовать того вреда, какой наносит организму быстро размножающийся возбудитель инфекции. Я уже говорил, что в отсутствии врачебной помощи начал бы как можно раньше принимать витамин Д3 и препараты цинка.
Очень осторожно нужно относиться к приему иммуномодуляторов и интерфероногенов, поскольку большинство из них будут стимулировать нежелательные про-воспалительные реакции и в дальнейшем ухудшат ситуацию.
Доступное средство омепразол может повышать рН в эндосомах клеток и таким образом затруднять репликацию коронавируса. Он же усиливает эффект противовирусных препаратов, ингибиторов протеаз, в частности.
При першении в горле, я бы рекомендовал полоскания теплым раствором (не кипятком!) жженого сахара. В него можно добавлять соль и немного соды. Кстати, жженый сахар (без соли и соды, конечно) полезно просто рассасывать и съедать где-то по 15-20 гр. в день.
В последнее время появляется все больше работ о лечении COVID-19 с помощью ингаляций лекарственных препаратов. При такой доставке непосредственно в бронхи и легкие требуются дозы лекарств на порядок меньшие, чем обычно. Причем действуют они намного эффективнее и в основном только местно. Ингаляции можно делать с помощью обыкновенных нибулайзеров, которые продаются в любой аптеке.
На ранних этапах развития болезни ингаляции даже обыкновенного раствора соды могут быть полезны. А если встает вопрос об ингаляции каких-либо лекарств, то обязательно проконсультируйтесь с лечащим врачом.
Температуру до 38-38,5 градусов лучше вообще не сбивать. Защитные реакции врожденного иммунитета функционируют при таких температурах лучше. Если выше — можно применять парацетамол или ибупрофен. Парацетамол слабее, но считается более безопасным в плане подавления противовирусного ответа.
Можно использовать препараты интерферонов – альфа, бета, лямбда. Но гамма-интерфероны могут спровоцировать нежелательные реакции при коронавирусной инфекции.
Что касается антибиотиков, то их прием на ранних этапах болезни, (в том числе и с целью профилактики) – вопрос довольно дискутабельный. Обычно их начинают применять при затруднении дыхания, когда к патологическим процессам присоединяется вторичная микрофлора. Наиболее эффективным при COVID-19 все-таки признается азитромицин, который не только подавляет микрофлору, но и непосредственно ингибирует репликацию коронавируса. Он же усиливает действие некоторых противовирусных препаратов. Однако и другие антибиотики, применяемые для лечения респираторных инфекций, могут быть эффективны.
Поэтому антибиотик лучше иметь в запасе, но применять только в соответствии с рекомендациями врача, так как можно ошибиться с дозировкой, режимом приема и кроме того, здесь тоже имеются свои противопоказания.
А при серьезном затруднении дыхания не стоит медлить и необходимо срочно требовать госпитализацию.
Так что выбор не маленький, и незачем просто так ходить по квартире. Надо лежать и лечиться!
Иммунная система человека
к.м.н. Гольдинберг Б. М., Васюк Я.В.
Городской центр трансфузиологии учреждения здравоохранения «6-я городская клиническая больница», г. Минск,
учреждение здравоохранения «7-я городская детская поликлиника», г. Минск
ИММУНННАЯ СИСТЕМА ЧЕЛОВЕКА
Введение
Группа органов, имеющих общее происхождение, единый план строения и выполняющая общую функцию называется системой органов. Пять из всех десяти систем органов являются регулирующими (управляющими): нервная, кровеносная, эндокринная, лимфатическая и иммунная. Уточним, что лимфатические органы и лимфатических узлы, которых насчитывается около 600, функционально является частью иммунной системы, а к собственно лимфатической системе относится обширная сеть сосудов, которая проходит почти через все наши ткани, обеспечивая движение жидкости, называемой лимфой.
Слово «иммунитет» происходит от латинского «immunis» (на английском – immunity), что означает «чистый от чего-либо», невосприимчивый к чему-либо. Иммунная система появилась вместе с многоклеточными организмами и развивалась, как помощница их выживанию. Она объединяет органы и ткани, которые гарантируют защиту организма от генетически чужеродных клеток и веществ, поступающих из окружающей среды.
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным.
Органы иммунной системы человека
Иммунная система включает центральные и периферические органы.
Центральные органы иммунной системы представляют собой красный костный мозг и тимус.
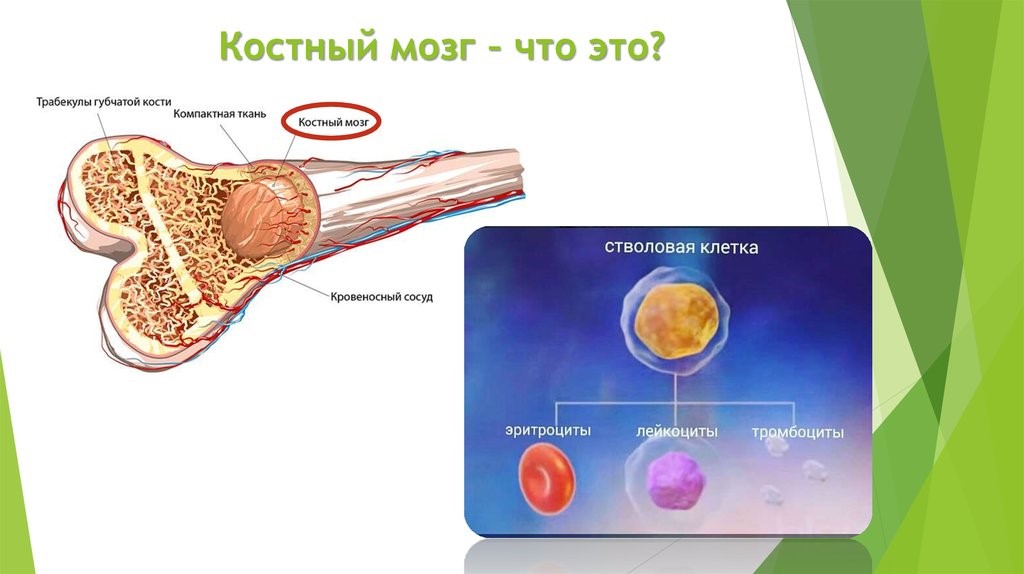
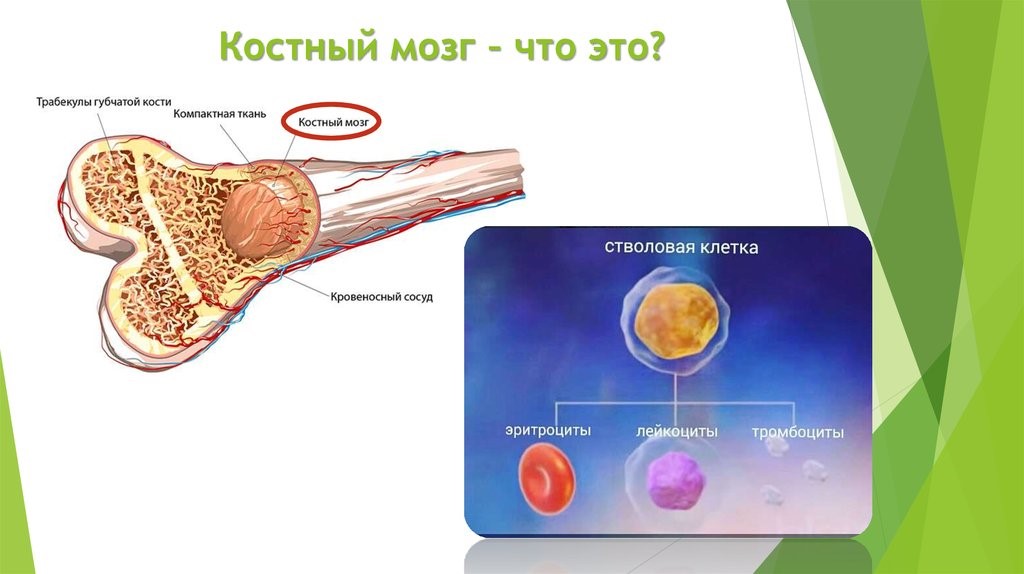
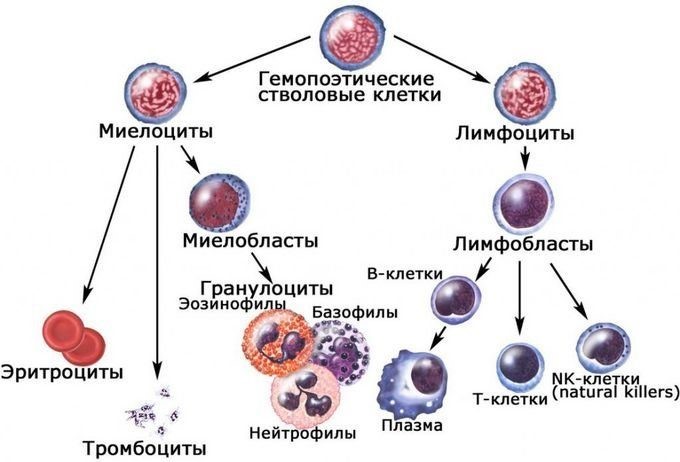
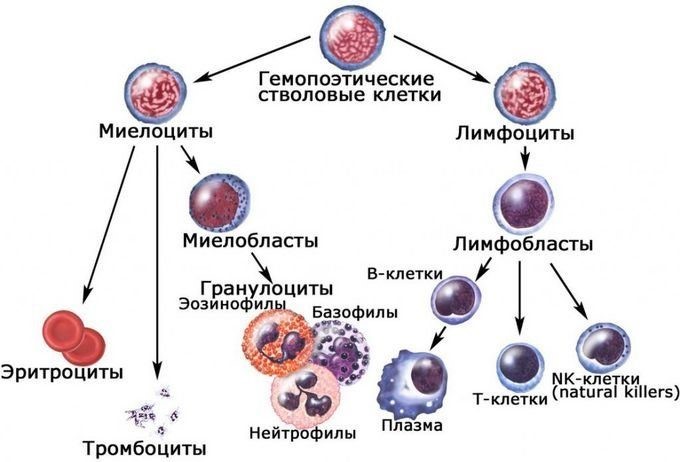
Костный мозг является хранилищем стволовых клеток, из которых образуются клетки крови (рис.1). В зависимости от ситуации, стволовые клетки трансформируются в иммунные В-лимфоциты. При необходимости, определенная часть B-лимфоцитов превращается в плазматические клетки, которые способны вырабатывать антитела.
Рис.1. Костный мозг содержит стволовые клетки
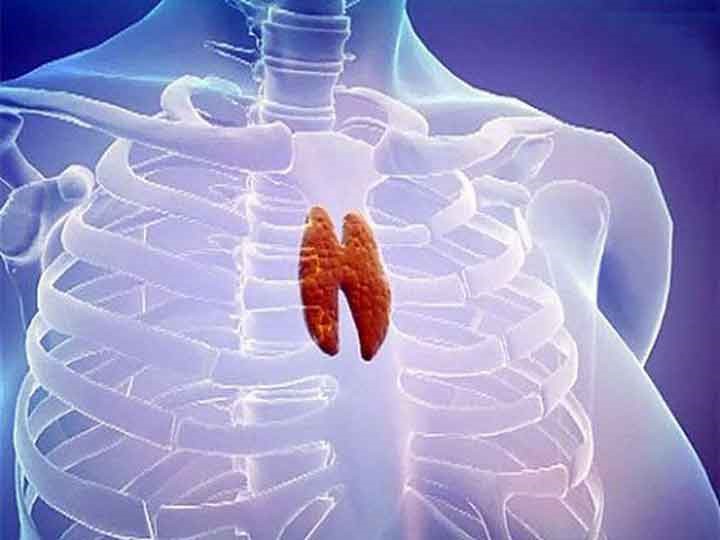
Тимус (или вилочковая железа) – один из главных органов иммунной системы, расположенный у человека за грудиной ниже ключиц, который отвечает за образование Т-клеток иммунной системы в лимфоидных тканях организма (рис.2).
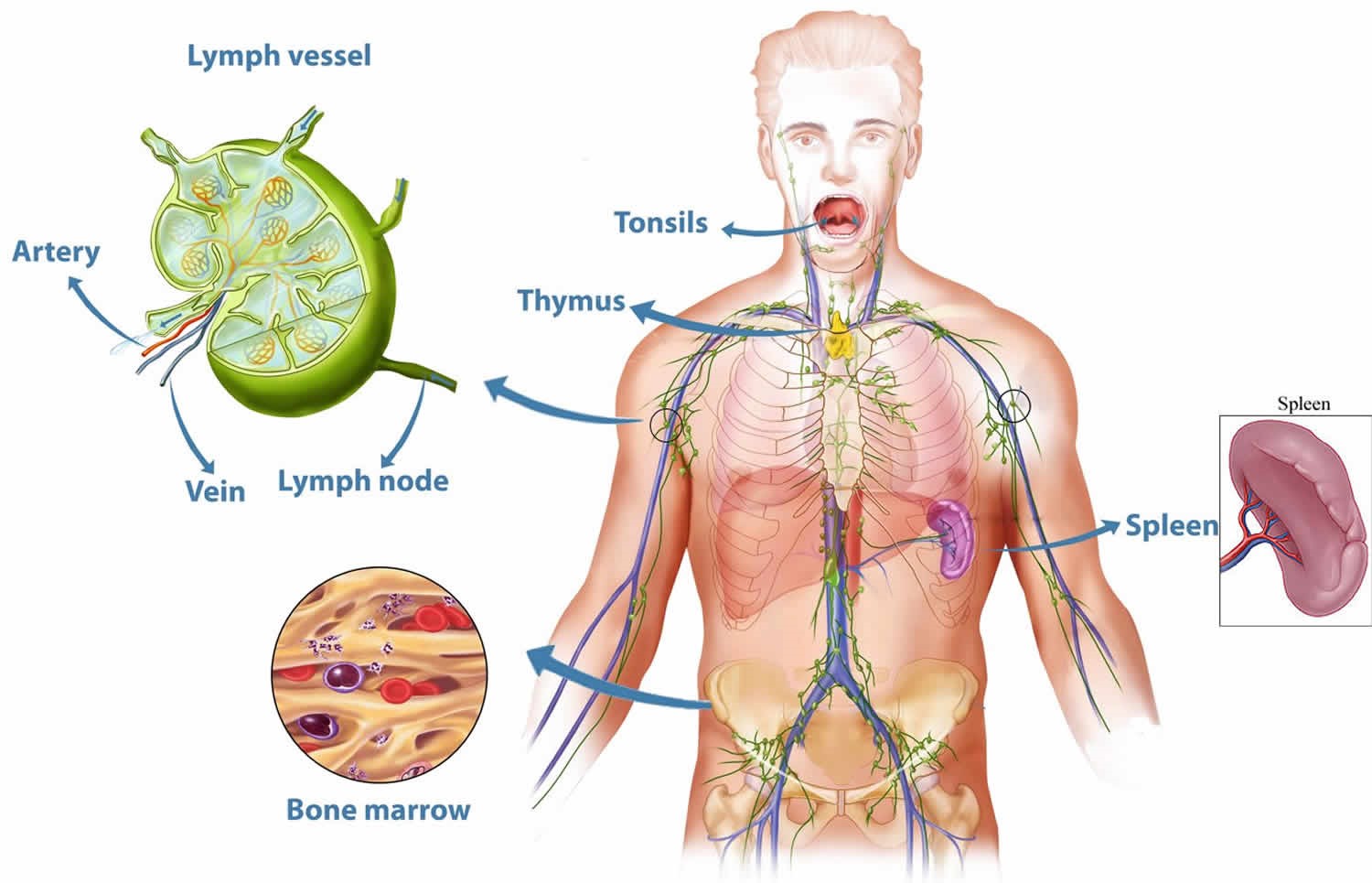
К периферическим органам относятся селезенка, миндалины и лимфоузлы, в которых находятся зоны созревания иммунных клеток.
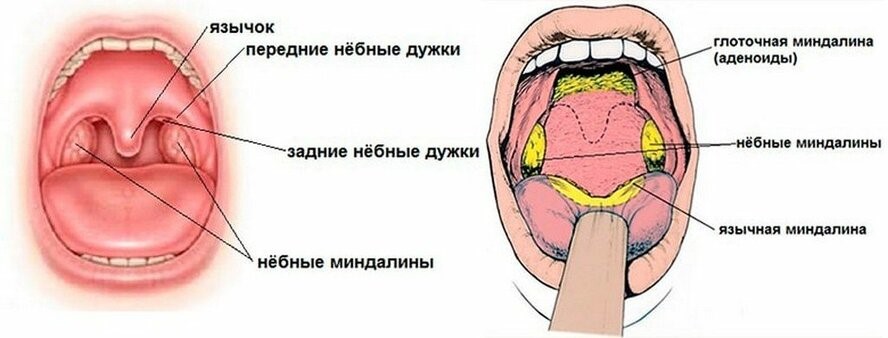
Миндалины, получившие свое название из-за внешней схожести с миндалем, представляют собой скопление лимфоидной ткани в верхней части носоглотки. У человека шесть миндалин: две небные, две грудные и по одной носоглоточной и язычной.
Самыми крупными из них являются небные миндалины, или гланды, которых легко осмотреть самостоятельно в зеркале, если достаточно широко раскрыть рот (рис.3).
Рис. 3. Небные миндалины
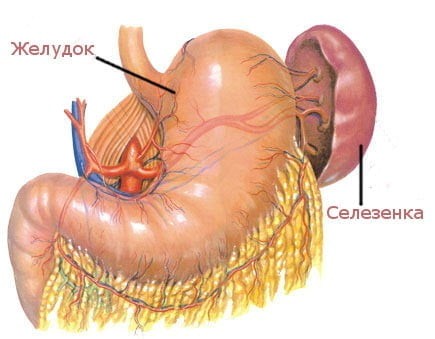
Селезенка является самым крупным лимфоидным органом (рис. 4). Кроме того, она может накапливать некоторое количество крови. В экстренных ситуациях селезенка способна послать свои запасы в общий кровоток. Это позволяет улучшить качество и скорость иммунных реакций организма. Селезенка очищает кровь от бактерий и перерабатывает всевозможные вредные вещества. В ней полностью разрушаются эндотоксины, а также остатки умерших клеток при ожогах, травмах или других повреждениях тканей. У людей, оставшихся по какой-либо причине без селезенки, ухудшается иммунитет.
Лимфатические узлы представляют собой небольшие образования округлой формы (рис. 5), расположенные в грудной полости (бронхолегочные, бронхотрахеальные) и брюшной полости (пейеровы бляшки, аппендикс и другие), окологрудные на поверхности грудной клетки, на шее и на конечностях. Лимфоузел – это один из барьеров на пути инфекций и раковых клеток, играющий роль своеобразной таможни (рис. 5). В нем образуются лимфоциты – специальные клетки, которые принимают активное участие в уничтожении вредных веществ.
Центральные органы иммунной системы отвечают за образование и созревание клеток, а периферические органы обеспечивают защиту, то есть иммунный ответ. Периферические и центральные органы иммунной системы выполняют свои работу только вместе и если выходит из строя какой-либо один из этих органов, то организм лишится защитного барьера.
Компоненты иммунной системы
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции (сущности).
Врожденный (видовой) иммунитет – наследственно закрепленная система защиты организма человека от патогенных и непатогенных микроорганизмов, а также продуктов тканевого распада. Клетки врожденного иммунитета распознают патоген по специфичным для него молекулярным маркёрам – так называемым «образам патогенности». Эти маркёры не позволяют точно определить принадлежность патогена к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с возмутителями спокойствия: чужаком или своим, но ставшим для организма предателем (рис.6).
Рис.6. Врожденный иммунитет: главное – спокойствие!
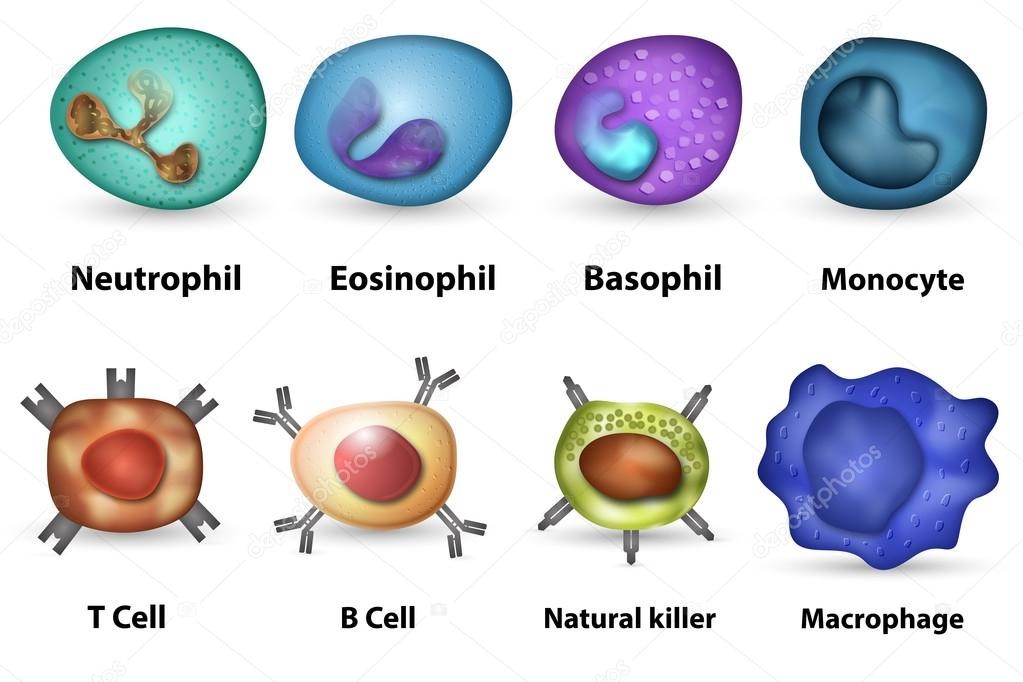
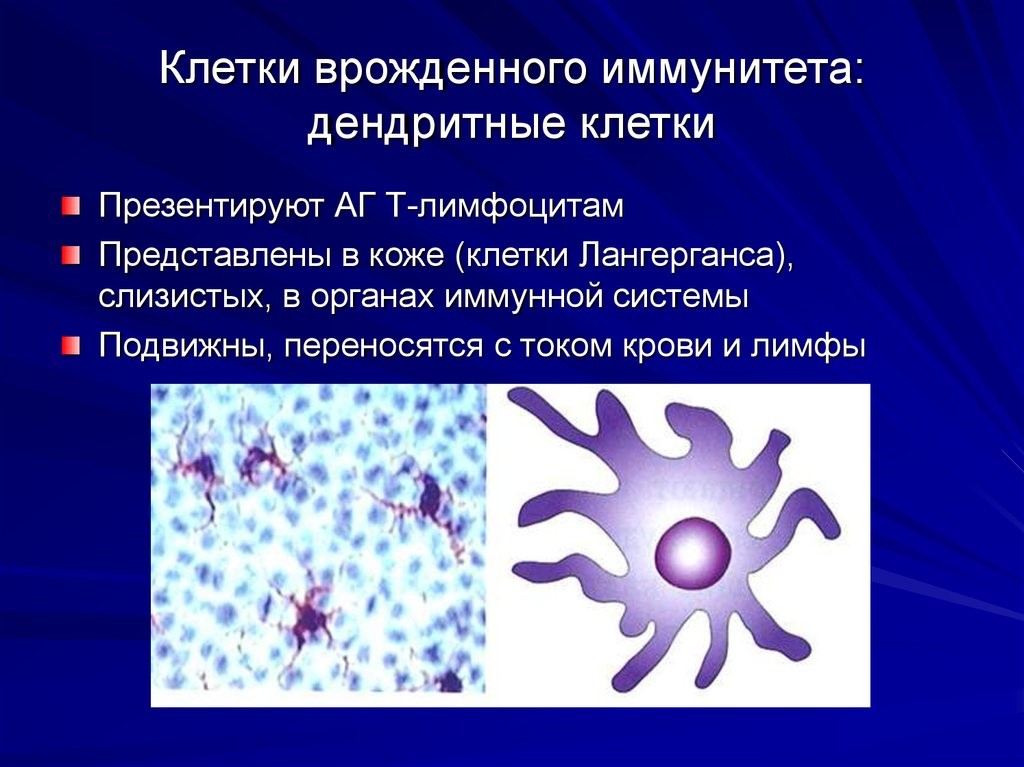
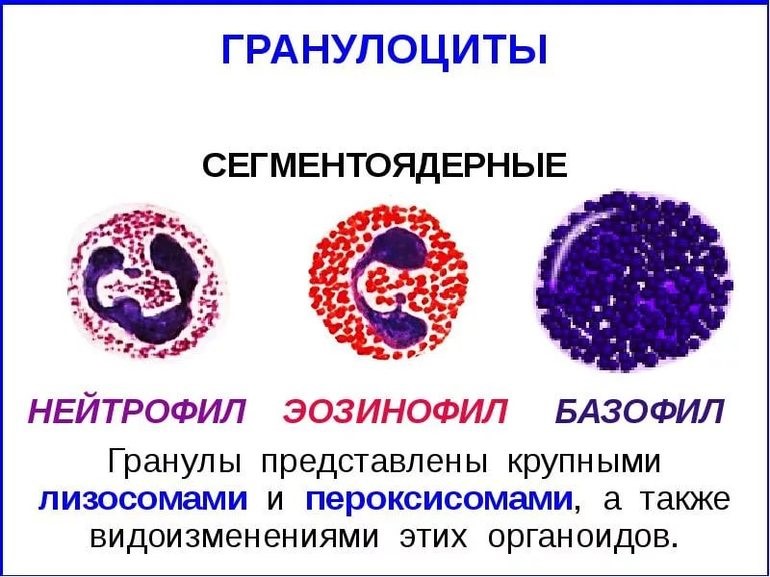
Врожденный иммунитет на клеточном уровне представляют:
Рис.8. Дендритная клетка и
Нейтрофилы – самые многочисленные иммунные клетки в крови человека. Они циркулируют в крови всего 8-10 часов и бόльшую часть своей жизни путешествуют по тканям организма. При встрече с патогеном они его захватывают и переваривают, после чего обычно сами погибают. Из разрушенных нейтрофилов высвобождаются гранулы, содержащие антибиотические вещества.
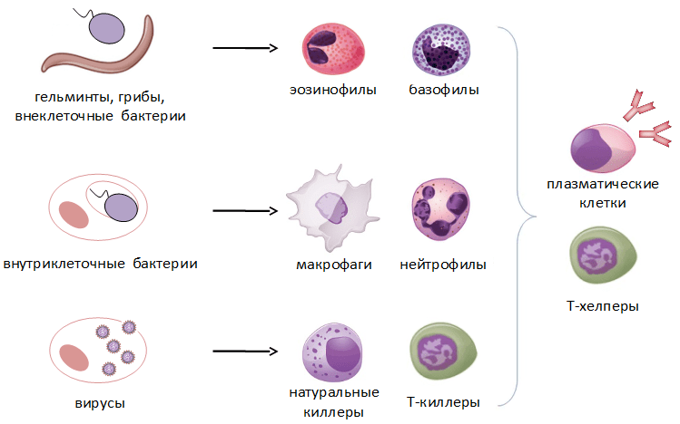
Гранулы эозинофилов и базофилов осуществляют химическую защиту организма от крупных патогенов, например, паразитических червей, грибов, внеклеточных бактерий. Однако при чрезмерной активности могут участвовать и в развитии аллергической реакции;
Рис.10. Натуральный киллер
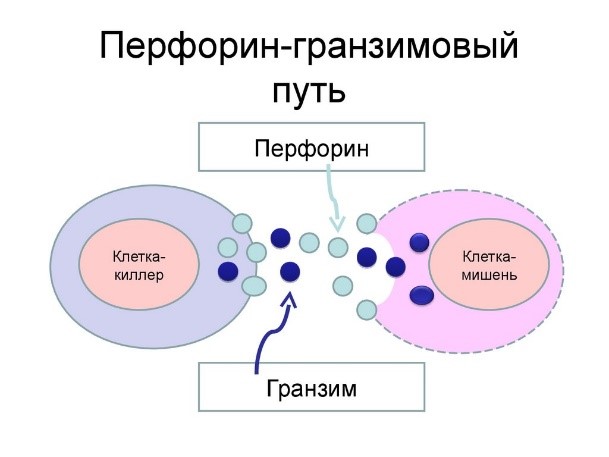
Действуют натуральные киллеры с помощью агрессивных веществ перфорина и гранзима, которые наподобие буравчиков «кусают» и разрушают пораженную клетку, ставшую для них мишенью (рис.11)
Рис.11. Проникновение перфорина и гранзима в раковую клетку и ее уничтожение
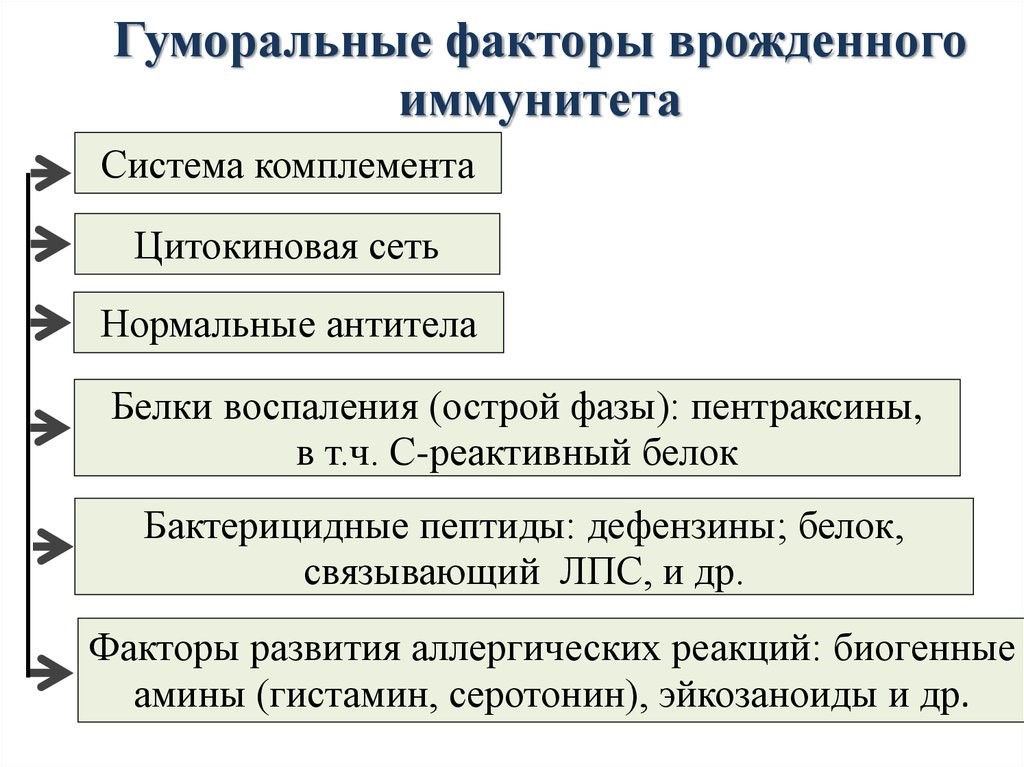
Молекулярными(гуморальные) факторами врожденного иммунитета являются (рис.12):
Рис.12.Гуморальные факторы врожденного иммунитета
Система комплемента – это многокомпонентная самособирающаяся система более 20 сывороточных белков, которые в норме находятся в неактивном состоянии.
После активации проявляются биологические эффекты комплемента: образование мембраноатакающего комплекса для лизиса патогенов, выброса медиаторов воспаления для привлечения фагоцитов и усиления их поглотительной способности.
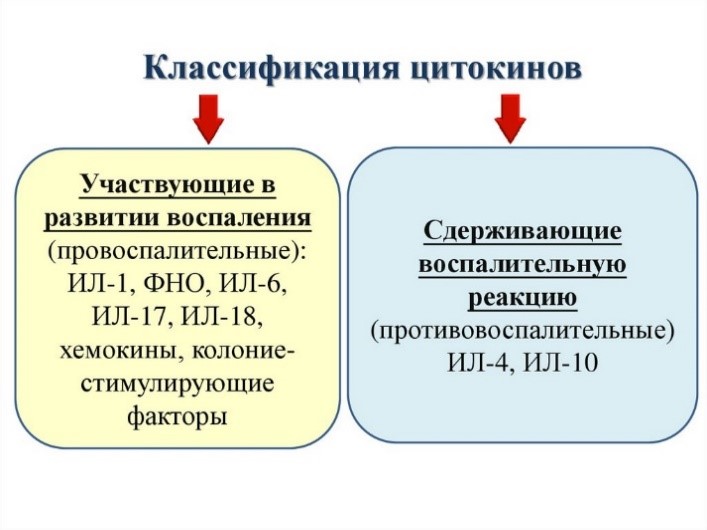
Цитокины – это система низкомолекулярных белков организма, синтезируемых преимущественно активными клетками иммунной и кроветворной систем, регулирующих межклеточные взаимодействия «универсальный» язык для всех клеток), представленные на рис.13 и 14.
Рис. 13. Цитокины: ИЛ – интерлейкины, которых в настоящее время насчитывается 34 разновидности;
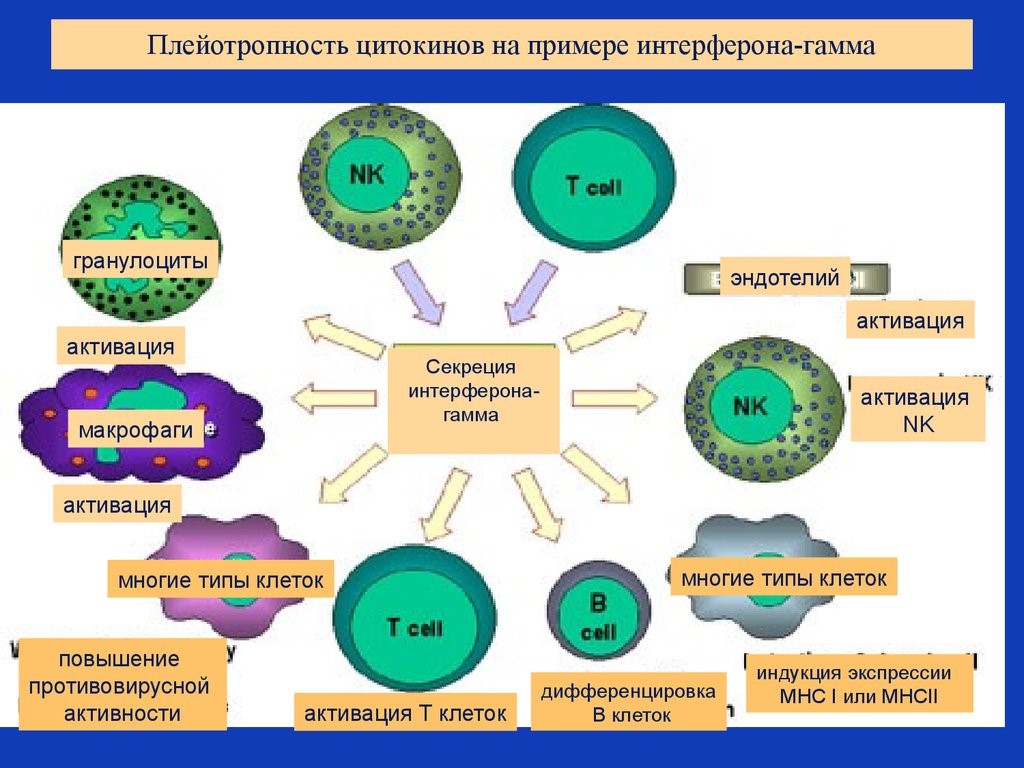
Рис. 14. Разнонаправленность действия цитокинов на примере гамма-интерферона
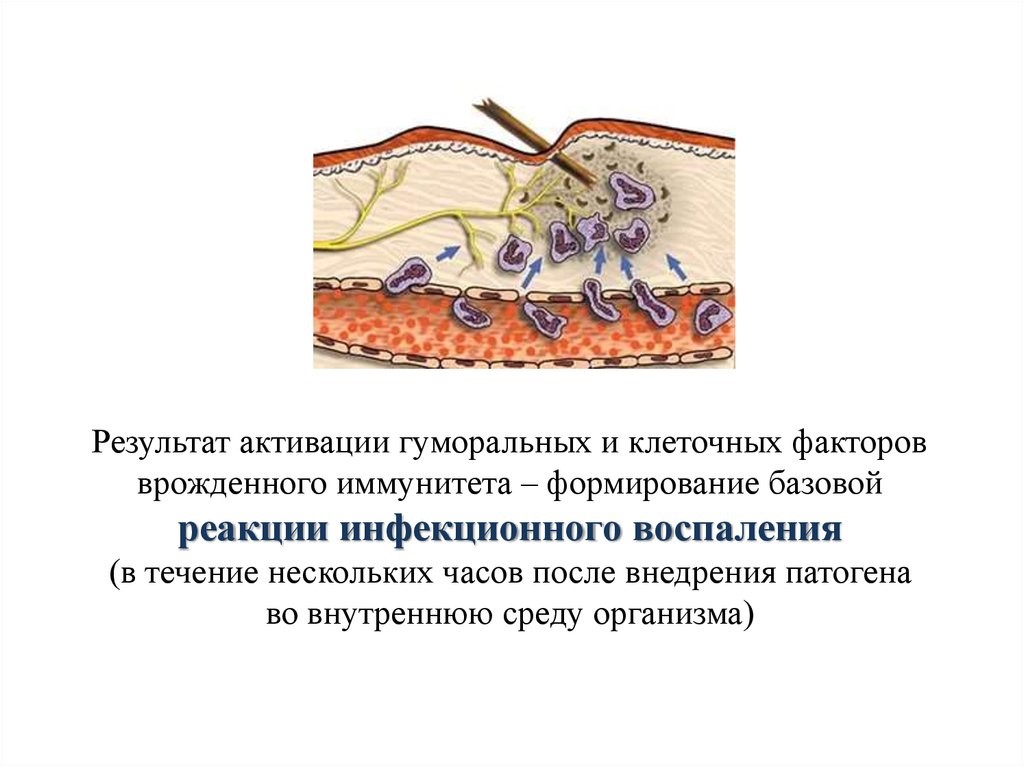
В результате активации гуморальных и клеточных факторов врожденного иммунитета в течение нескольких часов после внедрения патогена во внутреннюю среду организма формируется базовая реакция инфекционного воспаления (рис. 15)
Рис. 15. Инфекционное воспаление ткани на месте внедрения инородного тела с целью его удаления
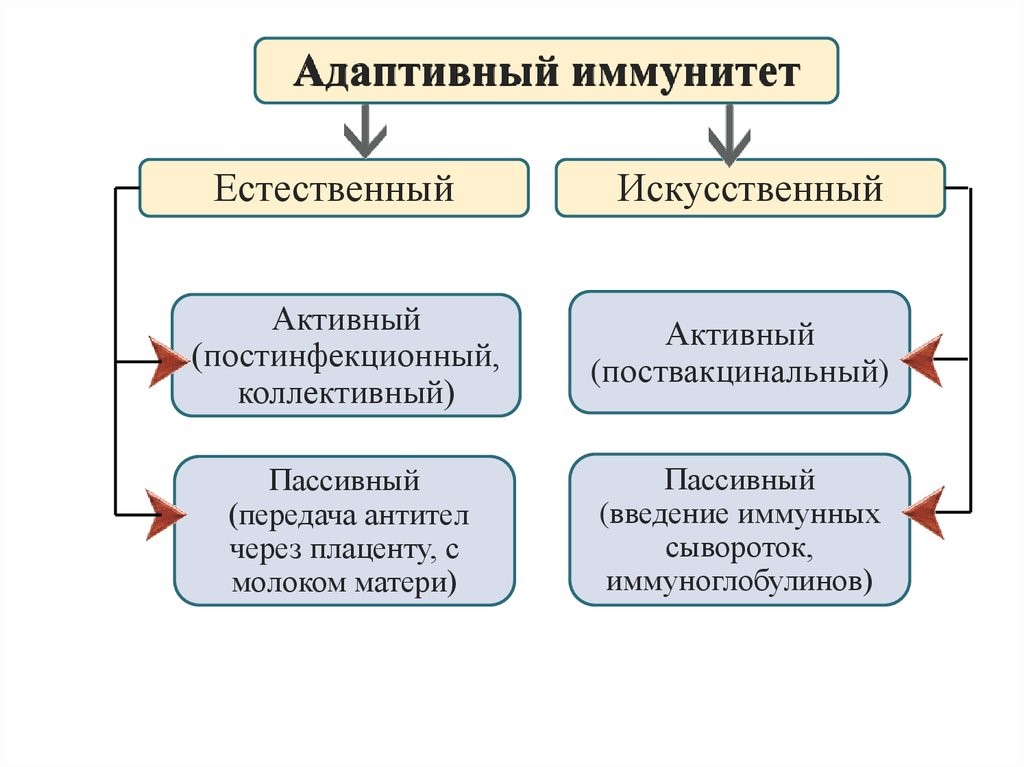
Приобретенный иммунитет (или адаптивный – от франц. adapter «приспосабливать») формируется индивидуально в течение жизни под влиянием антигенной стимуляции и, в свою очередь, подразделяется на естественный и искусственный (рис.16).
Естественный иммунитет формируется при встрече с патогеном, в результате чего в организме вырабатываются защитные иммунные факторы (активный естественный иммунитет), либо они попадают в готовом виде из материнского оргазма в период внутриутробного развития или при грудном вскармливании (пассивный естественный иммунитет).
Искусственный иммунитет создается путем введения вакцин или анатоксинов, которые стимулируют выработку антител против конкретных патогенов или их ядов. При этом с профилактической целью воспроизводится процесс реакции иммунной системы пациента на патоген, но в бессимптомной или легкой клинической форме с сохранением их защитной иммунной силы в течение нескольких месяцев, лет или даже пожизненно (искусственный активный иммунитет). Когда необходимо быстро и на короткое время защитить пациента от реального риска встречи с патогеном во время эпидемии или нейтрализовать уже проникший в его организм патоген применяются иммуноглобулины (антитела) как в очищенном виде, так и в дозированных объемах плазмы или сыворотки, полученных из крови донора (человека или животного). Применение готовых антител формирует пассивный искусственный иммунитет, сохраняющийся 2-3 недели.
Адаптивный иммунитет основывается на трех главных процессах:
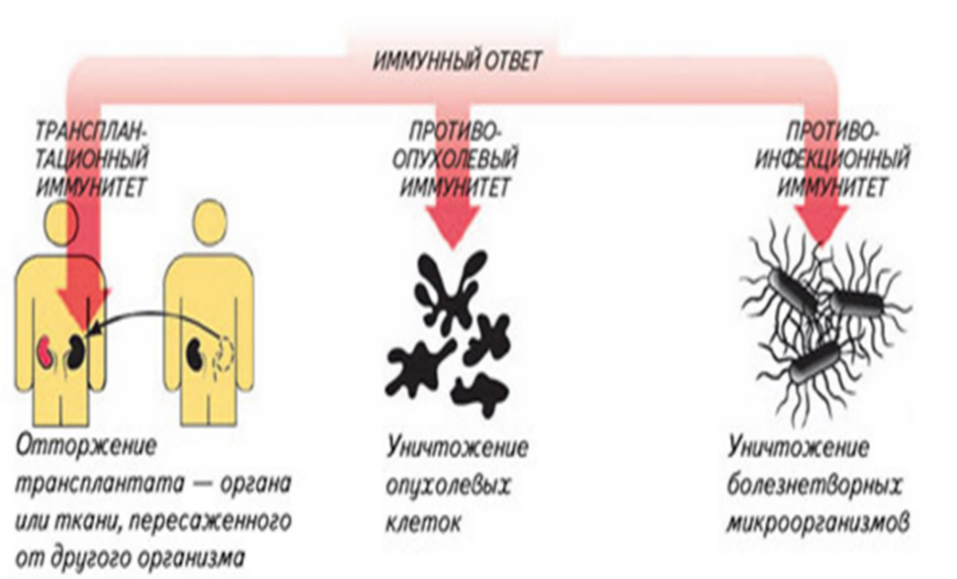
Рис.17.Варианты реагирования иммунной системы на пересадку органов или тканей, возникновение злокачественных новообразований и инфекций
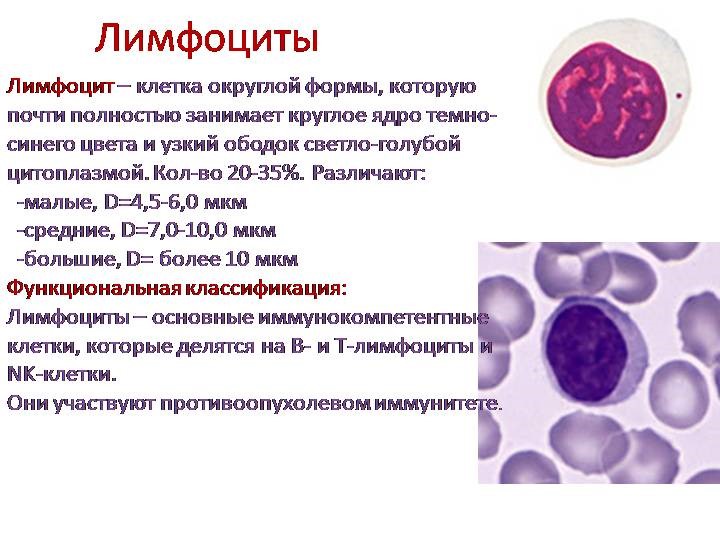
Иммунокомпетентными клетками адаптивного иммунитета являются лимфоциты, которые живут в организме человека от нескольких месяцев до несколько лет. По функциям клетки подразделяются на Т-лимфоциты – 80% и В-лимфоциты – 20%.
То, что Т-лимфоцит распознает только чужеродные антигены, а не молекулы собственного организма, является следствием процесса, называемого селекцией, которая происходит в тимусе, где завершают свое развитие Т-клетки. Суть селекции такова: клетки, окружающие юный, или наивный, лимфоцит, показывают (презентируют) ему пептиды собственных белков. Тот лимфоцит, который слишком хорошо или слишком плохо узнает эти белковые фрагменты, уничтожается. Выжившие же клетки (а это менее 1% всех предшественников Т-лимфоцитов, пришедших в тимус) обладают промежуточным сродством к антигену, следовательно, они, как правило, не считают собственные клетки мишенями для атаки, но имеют возможность среагировать на подходящий чужеродный пептид.
Для активации Т-лимфоцита нужно, чтобы он получил специальные сигналы от рецепторов лейкоцитарной антигенной системы и коктейля из множества провоспалительных цитокинов.
С помощью специальных реагентов определяются маркеры поверхностных белков лейкоцитов определенного типа, которые называются кластерами дифференциации (Сluster of differentiation) – CD. В настоящее время известно 350 CD-антигенов и их подтипов (табл. 1).
Таблица 1. Главные идентификациионные СD-маркёры клеток
Лимфоидная стволовая клетка
CD19, CD72, CD79 и др.
Т-лимфоциты распознают клетки, несущие чужеродные антигены, и уничтожают их после непосредственного контакта (атаки), а также выполняют функцию регуляции иммунного ответа.
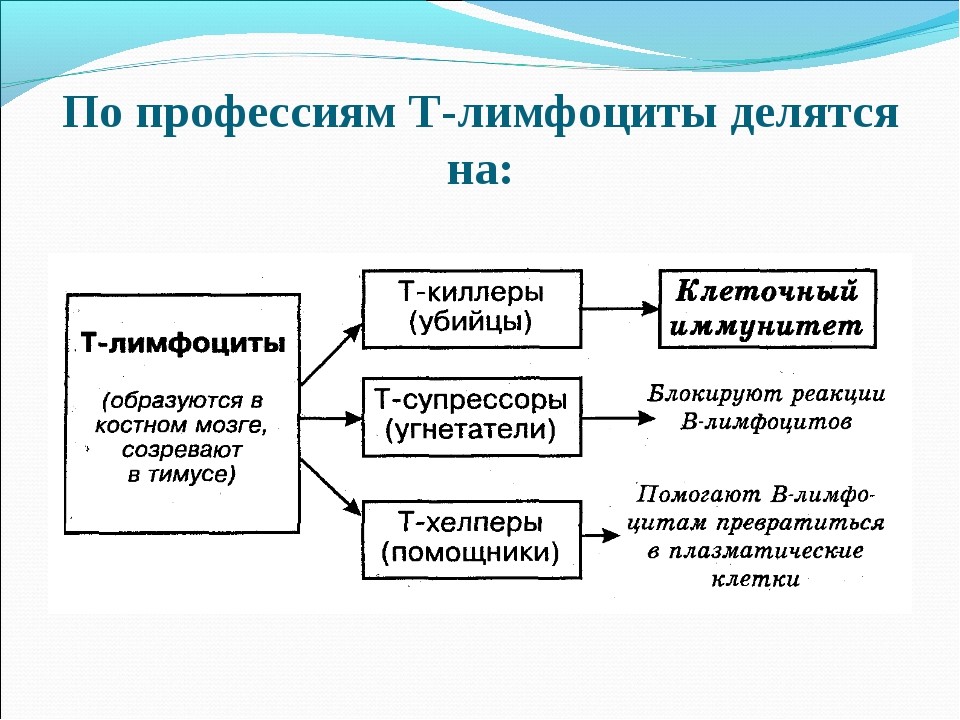
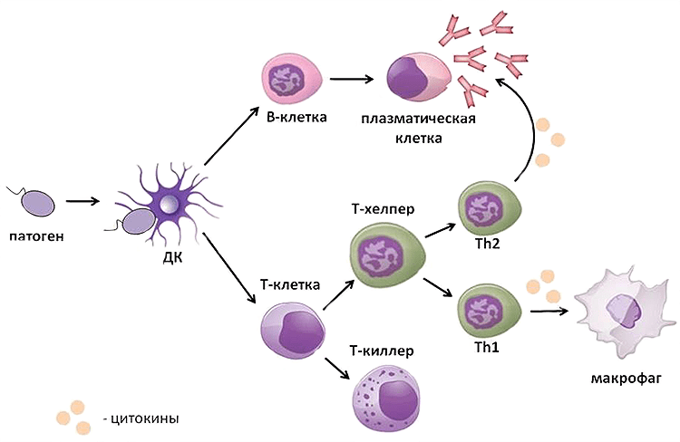
Т-лимфоциты имеют подтипы (рис. 18):
Рис. 18. Подтипы Т-лимфоцитов и их функции
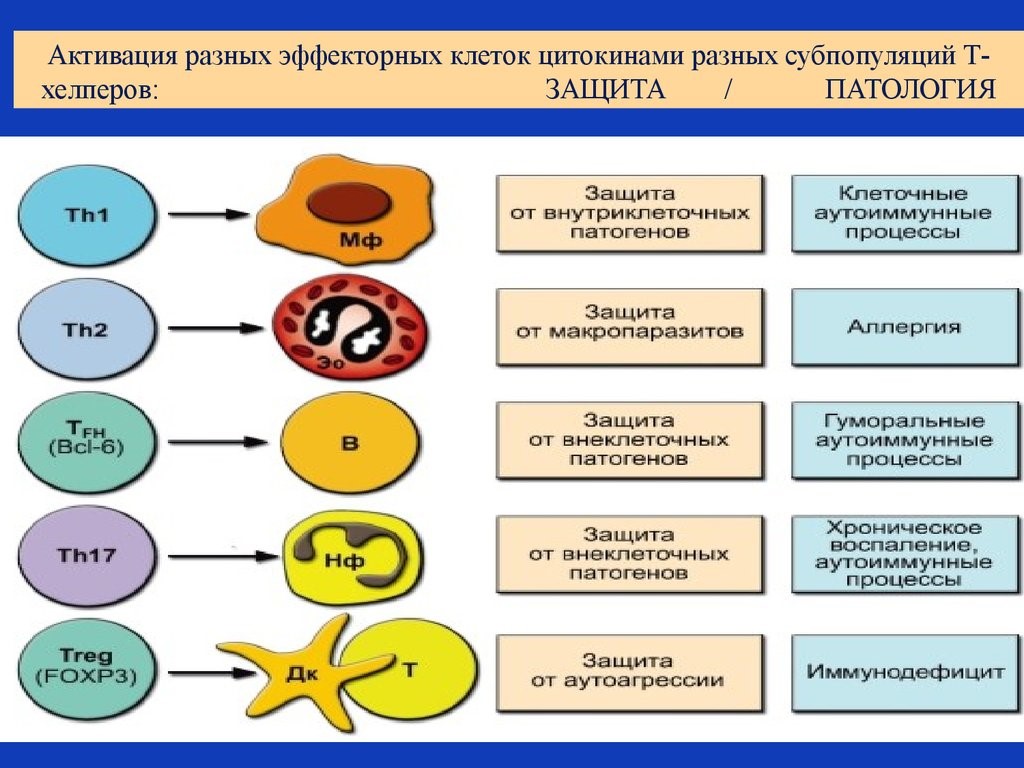
Рис. 19. Активация цитокинами разных субпопуляций Т-хелперов
Соотношение количества клеток CD4/CD8 называют иммунорегуляторным индексом (ИРИ). Если у пациента ИРИ повышен (более 2,2), то это говорит о чрезмерной активности T-хелперов и ослаблении регулирующей функции T-киллеров. При таком показателе иммунные клетки могут разрушать собственные ткани организма. Повышенный ИРИ чаще всего отмечается у пациентов с аутоиммунными болезнями (системной красной волчанкой, склеродермией, ревматоидным артритом и др.). Причиной чрезмерной активности T-хелперов может также стать опухоль вилочковой железы. При этой патологии продуцируется избыточное количество лимфоцитов. Высокие показатели ИРИ отмечаются при остром лимфобластном лейкозе. Это тяжелое онкологическое заболевание сопровождается неконтролируемым увеличением количества незрелых лимфоцитов.
Если иммунорегуляторный индекс понижен (менее1,6), то это говорит о серьезном ухудшении работы иммунитета. Низкие показатели ИРИ свидетельствуют о том, что в организме ослаблена функция защитных клеток, а регуляция со стороны T-киллеров чрезмерна. Обычно это отмечается при следующих патологиях, сопровождающихся иммунодефицитом: инфекционных болезнях (в том числе ВИЧ-инфекции); врожденном иммунодефиците; любых затяжных и хронических болезнях; опухолях костного мозга.
В-лимфоциты ответственны за гуморальное звено иммунитета – продукцию антител. После антигенного стимула В-лимфоцит превращается в лимфобласт – клетку, способную к делению. Часть лимфобластов дифференцируется в В-лимфоциты памяти, другая часть превращается в плазматические клетки, которые осуществляют продукцию антител.
В-лимфоциты несут на своей поверхности В-клеточный рецептор. При контакте с антигеном эти клетки активируются и превращаются в особый клеточный подтип – плазматические клетки, живущие до трех недель и обладающие уникальной способностью секретировать в этот срок тысячи антител.
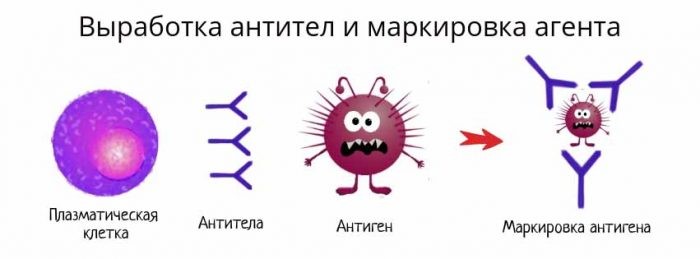
Антитело имеет сродство к распознаваемому им антигену, как бы «прилипает» к нему. Это дает возможность антителам обволакивать (опсонизировать) клетки и вирусные частицы, покрытые молекулами антигена, привлекая макрофаги и другие иммунные клетки для уничтожения патогена. Антитела также умеют активировать специальный каскад иммунологических реакций, называемый системой комплемента, который приводит к перфорации клеточной мембраны патогена и его гибели.
Рис. 20. Выработка антител и маркировка патогена
Различают несколько классов антител (иммуноглобулинов). Первыми после антигенного раздражения, вызывающих агглютинацию бактерий и нейтрализацию вирусов, появляются иммуноглобулины М (IgM). В длительном иммунитете участвуют иммуноглобулины G(IgG).
В табл.2 представлена интерпретация лабораторных исследований на наличие патогена на молекулярном уровне и с помощью тестов на иммуноглобулины М и G.
Таблица 2. Интерпретация лабораторных исследований на наличие патогена на молекулярном уровне
Результат молекулярного исследования
Инфицированный или повторно инфицированный пациент
Ранние стадии инфекции. Требуется дополнительное исследование
Инфекция. Требуется дополнительное исследование
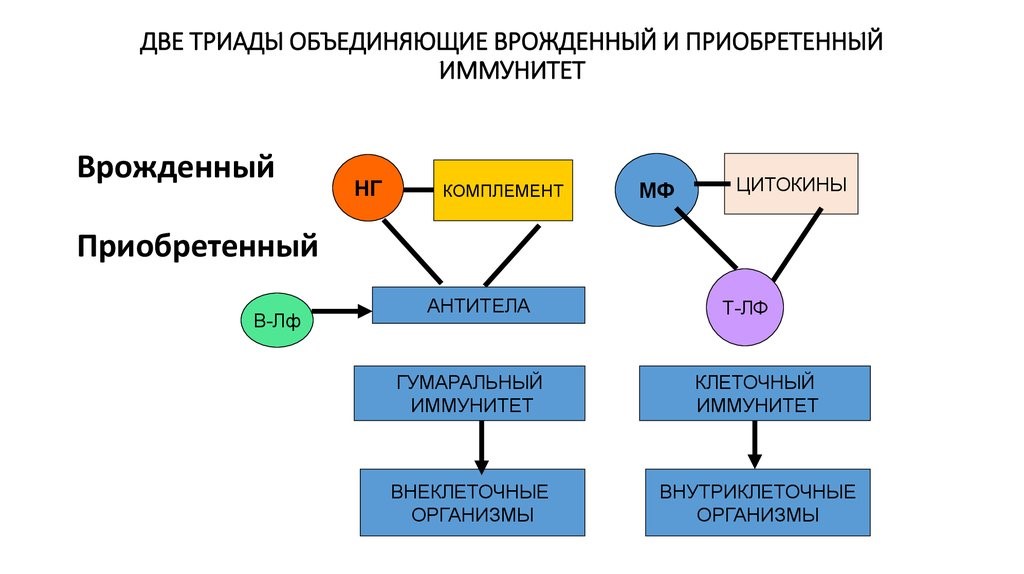
Врожденный и приобретенный виды иммунитета имеют точки соприкосновения, которые представляют две триады (рис.21)
Рис. 21. Две триады, объединяющие врожденный и приобретенный виды иммунитета
Развитие адаптивного иммунного ответа требует достаточно много времени (от нескольких дней до двух недель), и для того чтобы организм мог защищаться от уже знакомой инфекции быстрее, из Т- и В-клеток, участвовавших в прошлых битвах, формируются так называемые клетки памяти. Они, подобно ветеранам, в небольшом количестве присутствуют в организме, и, если появляется знакомый им патоген, вновь активируются, быстро делятся и целой армией выходят на защиту границ (рис.22).
Рис.22. Т-клетки памяти быстро формирует вторичный иммунный ответ
Иммунологическая толерантность
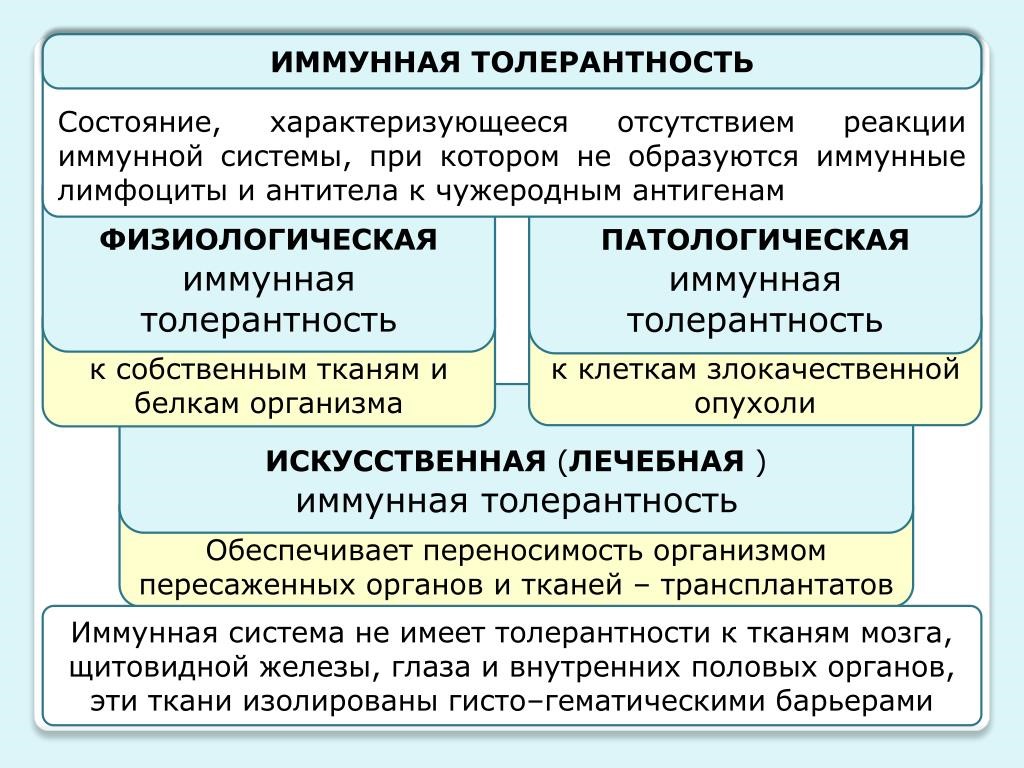
Под иммунологической толерантностью (терпимостью, ареактивностью) понимают отсутствие иммунного ответа на специфический антиген. Перечень антигенов, к которым может развиваться толерантность, практически неотличим от набора антигенов, против которых развивается специфический иммунный ответ (рис.23).
Рис. 23. Иммунная толерантность
Механизмы толерантности необходимы, поскольку иммунная система продуцирует огромное число разнообразных антиген специфичных рецепторов, и некоторые из них оказываются специфичными к собственным антигенам организма; толерантность предотвращает нежелательные реакции против собственных органов и тканей, также для нормального протекания беременности.
Нарушения иммунной системы у человека
Нарушения в работе иммунной системы можно подразделить на три категории: иммунодефициты, аутоиммунные заболевания и реакции гиперчувствительности.
Иммунодефициты
Иммунодефицит – снижение количественных показателей и/или функциональной активности основных компонентов иммунной системы, приводящее к нарушению защиты организма от патогенных микроорганизмов и проявляющееся повышенной инфекционной заболеваемостью.
Первичные иммунодефициты (ПИД) – наследственные заболевания, обусловленные дефектами генов, контролирующих иммунный ответ. В основном ПИД заявляют о себе уже в раннем детском возрасте, но иногда лишь к 30-40 годам жизни.
По механизмам развития выделяют 4 основные группы ПИД (табл.3):
Таблица 3. Некоторые первичные иммунодефициты
Частые бактериальные инфекции
Дефицит или полное отсутствие В-лимфоцитов
Антибиотики, пожизненное введение IgG
Частые респираторные инфекции, отиты
Дефекты Т- и В- лимфоцитов
Антибиотики, пожизненное введение IgG
Атаксия-телеангиоэкстазия (синдром Луи-Бар)
Аномалия двигательной функции, слабость мышц, нарушение речи
Дефицит Т- и В- лимфоцитов
ПИД, обусловленные дефектами фагоцитоза
Хроническая гранулёматозная болезнь
Частые пневмонии, гнойные инфекции
Пожизненная антибактериальная и противогрибковая терапия, интерферон гамма
ПИД, обусловленные дефектами в системе комплемента
Наследственный ангионевротический отек
Отеки губ и век при отсутствии зуда. Отеки гортани, носа, языка опасны для жизни
Низкая концентрация ингибитора эстеразы С1
Введение концентрата ингибитора эстеразы С1
Как следует из табл.3, основным и часто единственным методом лечения большинства пациентов с первичными В-клеточными иммунодефицитами являются иммуноглобулины. Это лекарственные средства, получаемые из плазмы крови человека. Они призваны заменить защитные антитела, отсутствующие в иммунной системе, с целью предотвращения или остановки развития тяжелых инфекционных заболеваний. Сегодня в арсенале врача имеются иммуноглобулины, различающиеся по концентрации активного вещества (5 и 10%), а также по способу введения (внутривенный и подкожный).
ПИД может проявиться в любом возрасте. В зависимости от этого у пациента возникают своеобразные проблемы, требующие определенных видов поддержки на протяжении всей жизни (табл. 4).
Таблица 4. Необходимость в видах поддержки пациента с ПИД в различных возрастных группах
В возрасте от 0 до 14 лет требуется уход со стороны родителей, направленный на профилактику инфекций и на период лечения. Могут потребоваться: обучение на дому; оказание психологической помощи; социальная поддержка в приобретении лекарственных средств.
В подростковом возрасте (14-18 лет) дополнительно могут возникнуть потребности в продолжении непрерывного обучения, профессиональной ориентации, налаживании взаимоотношений со сверстниками, организации досуга.
В возрасте от 18 до 65 лет у пациентов чаще возникают инфекционные осложнения, а с ними и расходы на приобретение лекарственных средств, не подлежащих восполнению, а также проблемы с трудоустройством.
В пожилом возрасте (старше 65 лет) возникают потребности в материальной, социальной и психологической поддержке пациента с ПИД.
Аутоиммунная патология
Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом. Заболеваниями такого типа страдает около 5% человечества. В организме пациента развиваются боевые действия, напоминающие гражданскую войну: в атаку идут «свои против своих». В этой борьбе победителей нет – одни страдания.
Селекция Т-лимфоцитов в тимусе, а также удаление аутореактивных клеток на периферии (центральная и периферическая иммунологическая толерантность), о которых мы говорили ранее, не могут полностью избавить организм от аутореактивных Т-лимфоцитов. Что же касается В-лимфоцитов, вопрос о том, насколько строго осуществляется их селекция, до сих пор остается открытым. Поэтому в организме каждого человека обязательно присутствует множество аутореактивных лимфоцитов, которые в случае развития аутоиммунной реакции могут повреждать собственные органы и ткани.
В качестве аналога можно привести созданную турками в ХIV веке янычарскую пехоту, в которую набирали юношей-христиан 8-16 лет, воевших против своих сородичей.
Т-клеточная аутоиммуннная агрессия хорошо изучена при ревматоидном артрите, сахарном диабете первого типа, рассеянном склерозе и многих других болезнях.
Такие же клетки-янычары, не помнящие своего родства, прослеживаются среди В-лимфоцитов:
Например, вследствие срыва иммунологической толерантности происходит активация В-лимфоцитов, продуцирующих антитела. Это приводит к выраженному повышению выработки тиреоидных гормонов (Т4 и Т3), а также к увеличению щитовидной железы в размерах (гипертрофии). Патология носит название болезнь Грейвса.
Еще одним примером может быть миастения гравис, которая характеризуется слабостью скелетной мускулатуры вследствие образования аутоантител против структур, отвечающих за холинергическую передачу и сокращение мышечного волокна;
Как правило, аутоиммунное заболевание возникает внезапно, и невозможно точно определить, что стало его причиной. Считается, что триггером для запуска может послужить практически любая стрессовая ситуация, будь то перенесенная инфекция, травма или переохлаждение. Значительный вклад в вероятность возникновения аутоиммунного заболевания вносит как образ жизни человека, так и генетическая предрасположенность – наличие определенного варианта какого-либо гена.
Гиперчувствительность
Под гиперчувствительностью понимают чрезмерный иммунный ответ на какой-либо антиген. Реакции гиперчувствительности подразделяют на несколько типов в зависимости от их длительности и механизмов, лежащих в их основе:
Эффективные методы воздействия на иммунитет:
Спекулятивные методы вокруг иммунитета:
Заключение
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным со сложнейшими взаимодействиями между ними.
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный (адаптивный) виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции, которые представляют собой микроорганизмы, злокачественные опухолевые клетки, пересаженные органы и ткани.
Адаптивный иммунитет основывается на трех главных процессах: распознавание антигенов, их удаление (элиминация) и формирование иммунологической памяти.
Поломки в структуре иммунной системы приводят к развитию иммунодефицитов, аутоиммунным заболеваниям или реакции гиперчувствительности.
Иммунодефицит на генетическом уровне (первичный) или приобретенный (вторичный) может проявиться в любом возрасте и привести к повышенной инфекционной заболеваемости. В последние годы появились средства заместительной терапии, которые продлевают жизнь этим пациентам. Для повышения качества их жизни требуется не только обеспечение дорогостоящим лечением, но и организация поддержки со стороны семьи, психологов и социальных институтов.
Аутоиммунные заболевания и гиперчувствительность – это неспособность организма противостоять разбушевавшейся иммунной системе, которая перепутала свое и чужое.
К сожалению, ни одно из заболеваний иммунной системы медицина еще не научилась излечивать, а только применять заместительную терапию.
Эффективными профилактическими методами воздействия на иммунную систему являются вакцинация и здоровый образ жизни. Купить иммунитет в аптеке пока никому не удалось.