Кислородный концентратор при лечении и реабилитации после COVID-19. Лекция для врачей
Для лечения и реабилитации новой коронавирусной инфекции (COVID-19), у пациентов с сатурацией ниже 93-94% рекомендовано начинать кислородотерапию с помощью кислородного концентратора.
Сатурация — показатель, определяющий уровень насыщения крови кислородом.
Для проведения кислородотерапии необходима консультация врача назначающего индивидуальный план лечения.
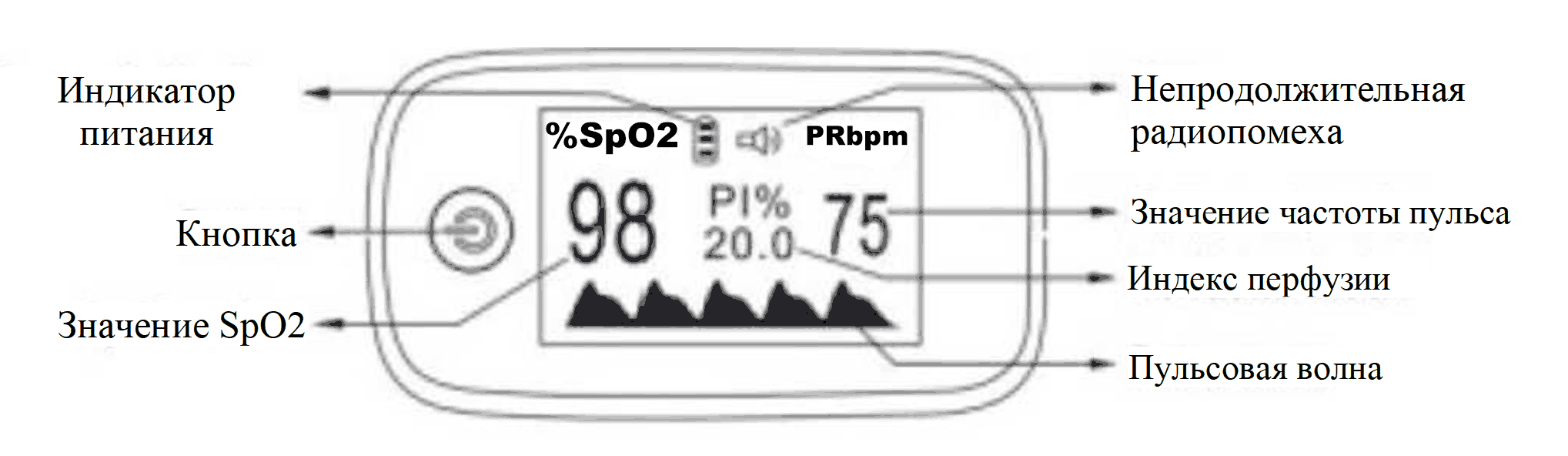
Определение сатурации производят с помощью прибора пульсоксиметра. Пульсоксиметр — прибор для определения уровня содержания кислорода в крови, надеваемого на палец. С помощью специального диода свет проникает сквозь мягкие ткани в кровь и определяет уровень снабжение крови кислородом.
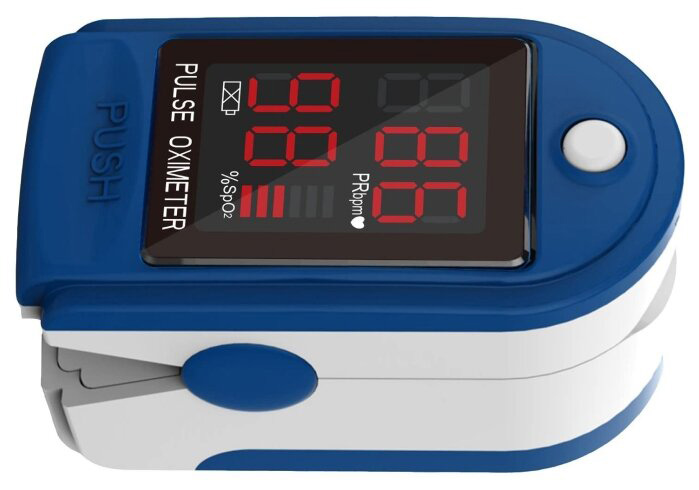
Как измерять сатурацию пульсоксиметром?
• Откройте зажим и вставьте палец в изделие, затем осторожно отпустите зажим
• Нажмите кнопку, чтобы включить пульсоксиметр и появится интерфейс измерения
• Примерно через 8 секунд результат измерения можно будет считать прямо с экрана дисплея
• Перед считыванием параметров убедитесь в том, что цифры не исчезают в течение более 4 секунд
PRbpm – показывает силу пульса, измеряемого в количестве ударов в одну минуту.
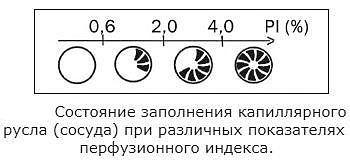
Индекс перфузии (PI, ПИ) зависит от интенсивности кровотока в месте измерения, заполнения сосудов кровью, количества работающих капилляров. Этот параметр свидетельствует от отношения окружающей среды и организма к готовности к корректному измерению сатурации.
Индекс перфузии (импульсной модуляции) может иметь значения от 0,3 % до 20 %. Данный показатель индивидуален у каждого человека и колеблется в зависимости от места проведения измерения и физического состояния пользователя. Очень низкое значение этого параметра (меньше 4%) может искажать результаты измерения сатурации и свидетельствует, например, о переохлаждении пальца, о наличии болезней сосудов, о шоковых состояниях. Показатель более 7% говорит о избыточной перфузии.
Состояние пациента
Показатели
Нормальная сатурация кислорода у взрослого
Дыхательная недостаточность 1-й степени
Дыхательная недостаточность 2-й степени
Дыхательная недостаточность 3-й степени
Основной метод кислородотерапии при коронавирусной инфекции — введение кислорода через дыхательные пути. Данный метод осуществляется с помощью специальной кислородно-дыхательной аппаратуры кислородного концентратора.
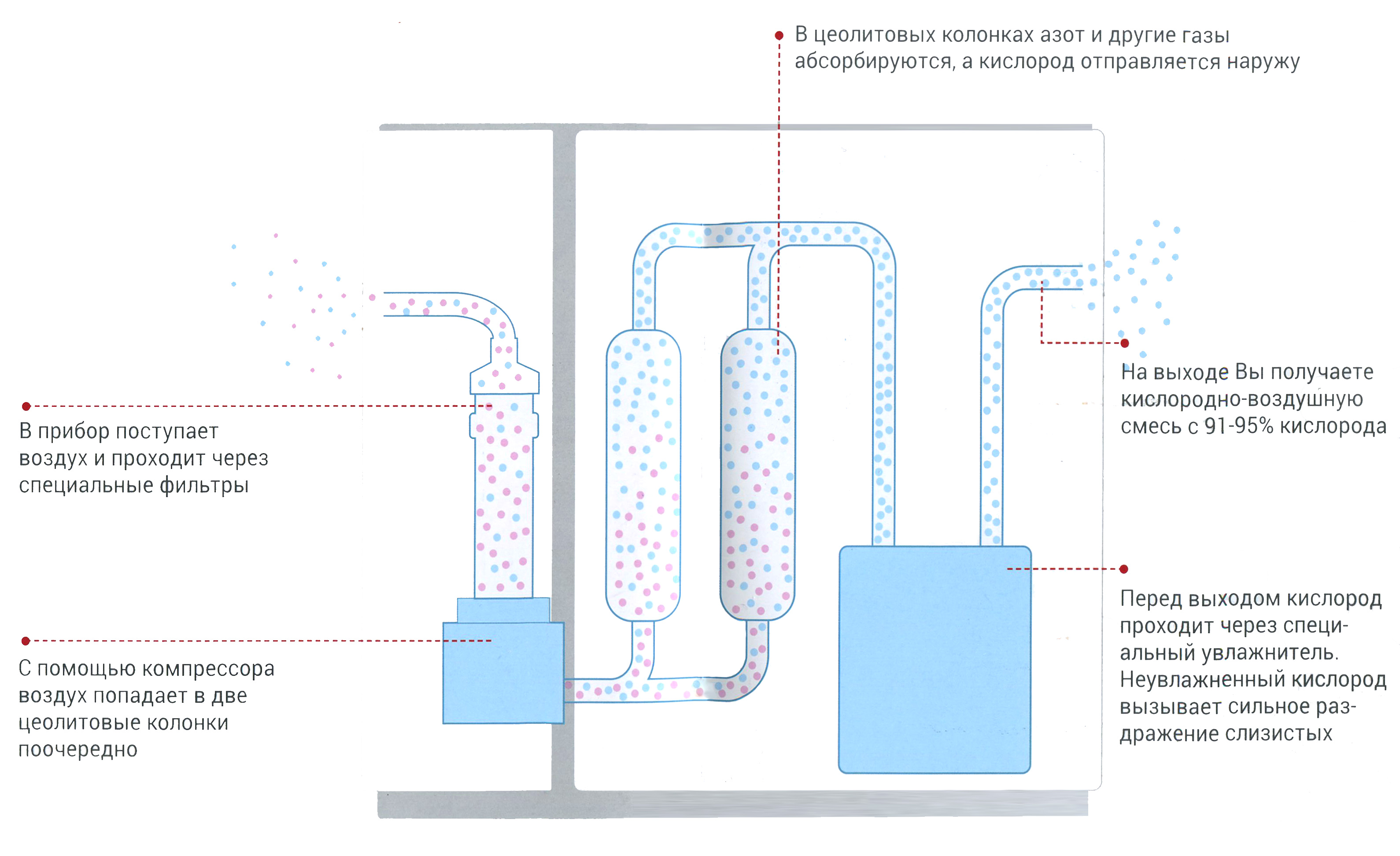
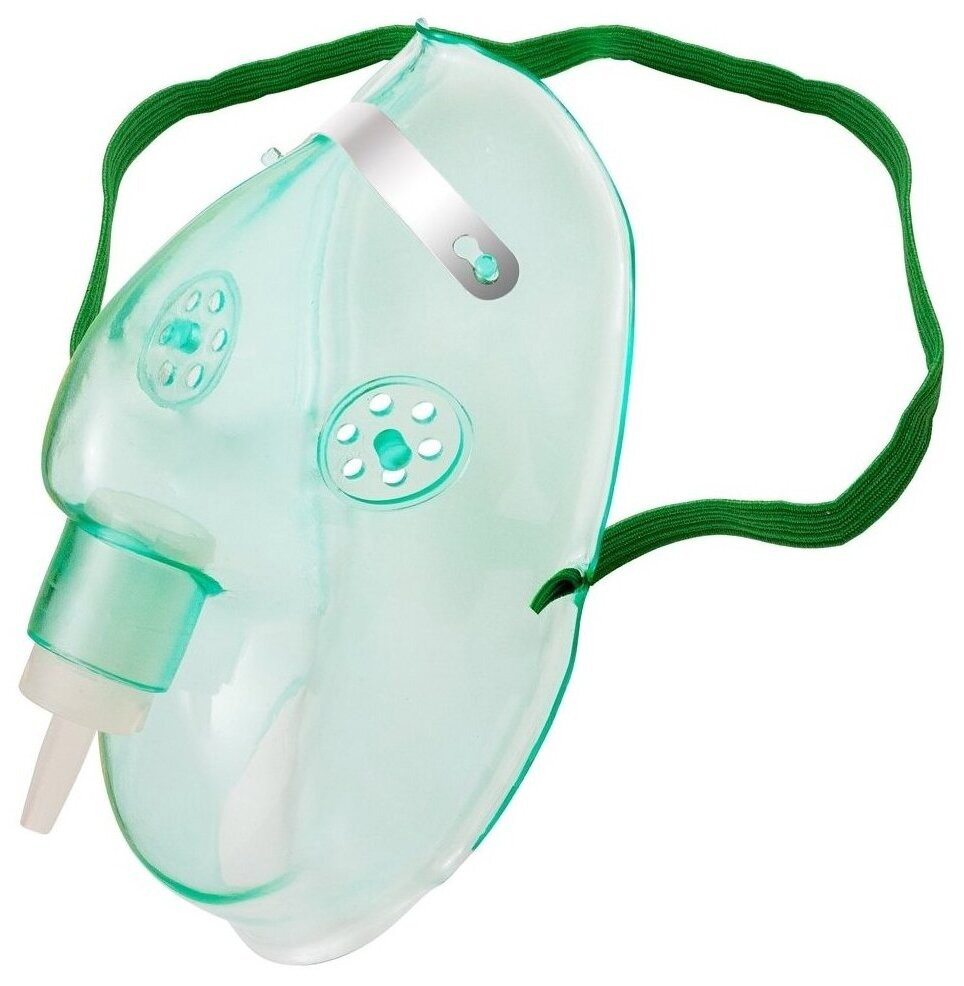
Кислородный концентратор предназначен для проведения кислородной (кислородно-воздушной) терапии или аэрозольной ингаляции жидкими лекарствами пострадавшему (больному) с лечебной целью.
Схема кислородного концентратора
При лечении и реабилитации COVID-19 используют кислородные концентраторы, которые производят кислород с концентрацией 90-95% со скоростью около 5-6 литров в минуту. Они используются для длительной кислородной терапии при тяжелой и среднетяжелой формах коронавирусной инфекции. Кислородные концентраторы эффективны и при этом просты в использовании.
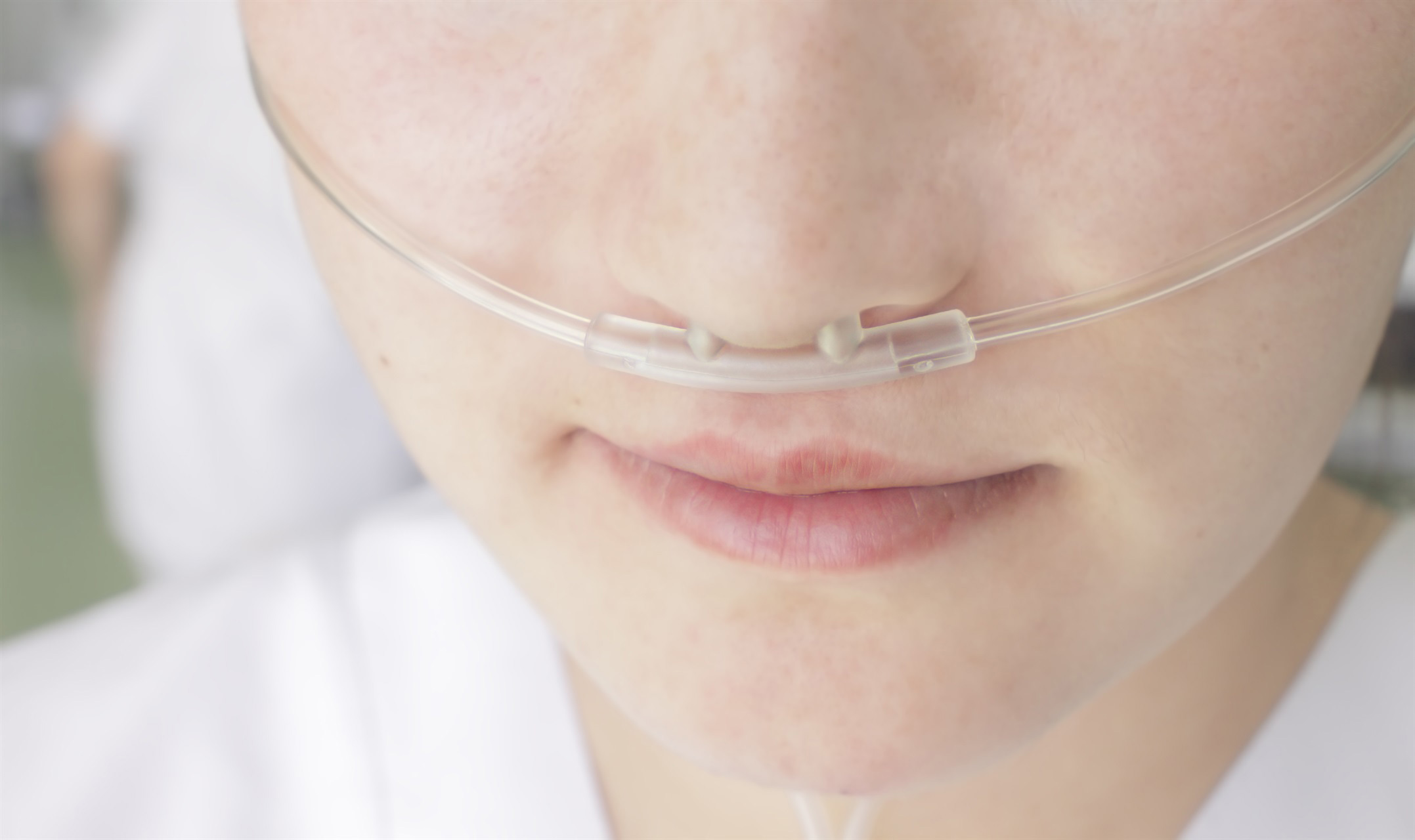
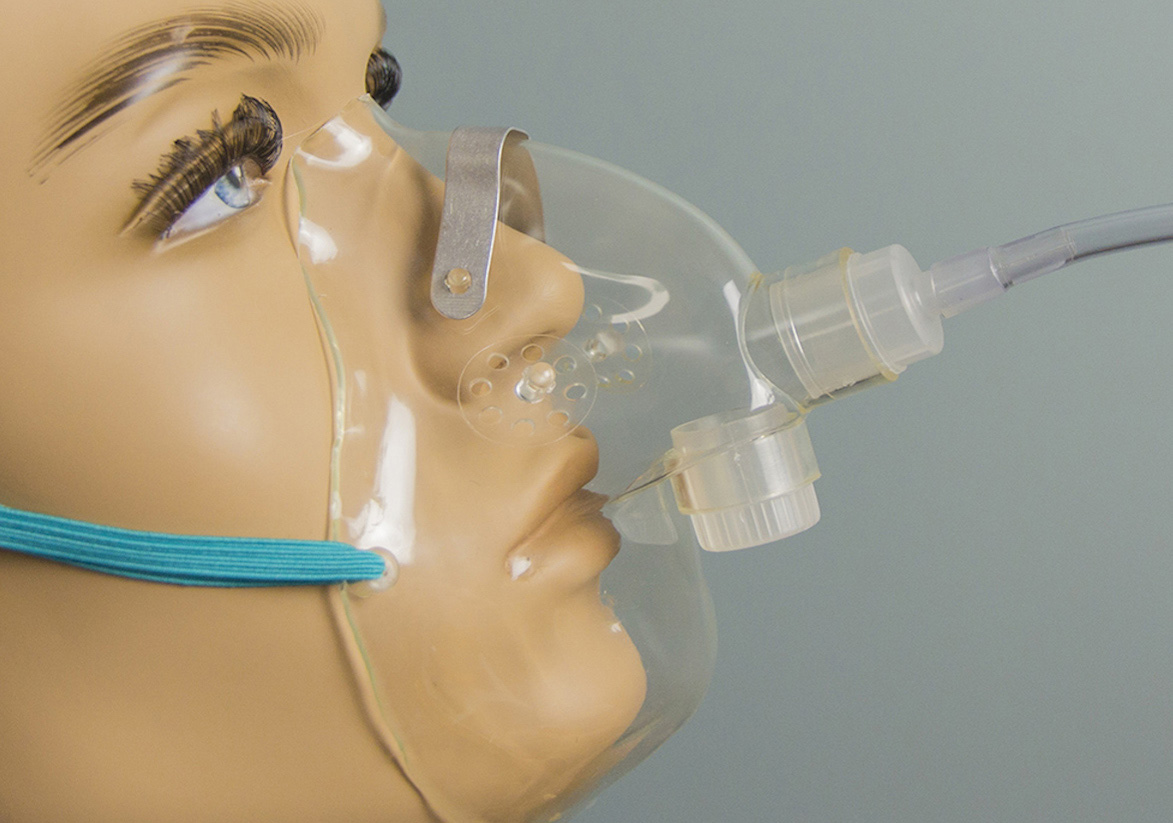
Кислород из кислородного концентратора поступает через кислородную маску или назальную канюлю
Назальная канюля в носу у пациента
Кислородная маска надета
Как оценивают работу легких после COVID-19?
Понять, что после ковида нужна кислородная терапия или другие методы поддержки организма, можно по следующим признакам:
Для оценки дыхательных функций лечащий врач может использовать следующие виды диагностики:
Какой кислородный концентратор покупать для реабилитации?
Производительность должна быть до 5л/мин. Все остальные параметры это дополнительные функции, которые повышают комфорт: пульт дистанционного управления, уровень шума компрессора, габариты, вес, встроенный выход для ингаляции.
Примеры кислородных концентраторов имеющих производительность до 5 литров/мин
Концентратор кислорода Армед 8F-5
Тип: медицинское оборудование
Вид оборудования: концентратор кислорода
Область медицины: хирургия, терапия, пульмонология
Длина: 39 см
Ширина: 34 см
Высота: 59 см
Вес: 23.4 кг
Дополнительная информация воздушный поток (производительность) на выходе КВС 0-5 л/мин; концентрация КВС на выходе при максимальной производительности ≥ 93 %; время выхода концентратора на рабочий режим 3-5 мин; средняя потребляемая мощность 600 Вт; частота сети 50 Гц; питание сети 220 ± 22 В; уровень шума (не более) 55 дБ; объем увлажнителя (не более) 250 мл; срок службы 10 лет; материал корпуса: ударопрочный пластик; колесные опоры.
Срок службы 120 мес.
Концентратор кислорода Армед 8F-5AW с пультом ДУ
Тип: медицинское оборудование
Вид оборудования: концентратор кислорода
Область медицины: хирургия, терапия, пульмонология
Длина: 39 см
Ширина: 34 см
Высота: 59 см
Вес: 23.4 кг
Дополнительная информация
воздушный поток (производительность) на выходе КВС 0-5 л/мин; концентрация КВС на выходе при максимальной производительности ≥ 93 %; время выхода концентратора на рабочий режим 3-5 мин; средняя потребляемая мощность 600 Вт; частота сети 50 Гц; питание сети 220 ± 22 В; уровень шума (не более) 55 дБ; объем увлажнителя (не более) 250 мл; срок службы 10 лет; материал корпуса: ударопрочный пластик; колесные опоры.
Срок службы 120 мес.
Кислородный концентратор BITMOS OXY 6000. Компактный, тихий, но более дорогой
Поток: 0.1-6 литров в минуту
Электронный расходомер!
Эргономичный
Удобный в переноске
Бесшумный: (
При какой сатурации подключают кислород при ковиде
Пациент А., 49-ти лет, поступил в ФГБУ «НМИЦ Кардиологии» МЗ РФ Центр COVID-19 с жалобами на кашель с трудноотделяемой мокротой, одышку, нехватку воздуха, боль в груди, головную боль и повышение температуры до 39,4 о С, SpO2 93-94% на атмосферном воздухе. У пациента был положительный назофаренгеальный мазок на SARS-CoV-2.
В течение нескольких дней у пациента нарастала симптоматика дыхательной недостаточности, по данным компьютерной томографии увеличился процент поражения легких до 90% (КТ-4).
Пациент находился на антибактериальной терапии, антикоагулянтной терапии, специфической терапии: гидроксихлорохином, азитромицином, лопинавир-ритонавиром. В последующем, в связи с развитием цитокинового «шторма» больному вводился тоцилизумаб.
Пациент пробыл в блоке интенсивной терапии 6 дней и в дальнейшем учитывая стабилизацию клинического состояния – отсутствие необходимости в проведении респираторной поддержки с применением СРАР – терапии, пациент был переведен в отделение.
При контрольном КТ исследовании: выраженная положительная динамика в виде частичного разрешения вирусной пневмонии, новых участков инфильтрации в паренхиме легких не определяется. Средне-тяжелая степень, процент поражения легочной ткани – 50-60% (КТ2).
Учитывая стабилизацию состояния, отсутствие признаков дыхательной недостаточности и хорошее самочувствие, пациент был выписан из стационара.
Во время проведения СРАР – терапии врачами и медицинским персоналом применялись следующие защитные средства: респиратор FFP3, очки, щиток, костюм индивидуальной защиты влагонепроницаемый, перчатки (2-3 пары). За время использования пациентом СРАР – терапии и в течение 14 дней после ни один сотрудник не заболел, положительных назофаренгиальных мазков на SARS-CoV-2 так же зафиксировано не было.
После выписки пациент выразил благородность всему коллективу ФГБУ «НМИЦ кардиологии».
Полностью клинический пример планируется к публикации в журнале «Анестезиология и реаниматология», ссылка на номер будет размещена на сайте.
Случай предоставлен Литвиным Александром Юрьевичем и Елфимовой Евгенией Михайловной.
При какой сатурации подключают кислород при ковиде
Проблема поражения легких при вирусной инфекции, вызванной COVID-19 является вызовом для всего медицинского сообщества, и особенно для врачей анестезиологов-реаниматологов. Связано это с тем, что больные, нуждающиеся в реанимационной помощи, по поводу развивающейся дыхательной недостаточности обладают целым рядом специфических особенностей. Больные, поступающие в ОРИТ с тяжелой дыхательной недостаточностью, как правило, старше 65 лет, страдают сопутствующей соматической патологией (диабет, ишемическая болезнь сердца, цереброваскулярная болезнь, неврологическая патология, гипертоническая болезнь, онкологические заболевания, гематологические заболевания, хронические вирусные заболевания, нарушения в системе свертывания крови). Все эти факторы говорят о том, что больные поступающие в отделение реанимации по показаниям относятся к категории тяжелых или крайне тяжелых пациентов. Фактически такие пациенты имеют ОРДС от легкой степени тяжести до тяжелой.
В терапии классического ОРДС принято использовать ступенчатый подход к выбору респираторной терапии. Простая схема выглядит следующим образом: низкопоточная кислородотерапия – высокопоточная кислородотерапия или НИМВЛ – инвазивная ИВЛ. Выбор того или иного метода респираторной терапии основан на степени тяжести ОРДС. Существует много утвержденных шкал для оценки тяжести ОРДС. На наш взгляд в клинической практике можно считать удобной и применимой «Берлинскую дефиницую ОРДС».
Общемировая практика свидетельствует о крайне большом проценте летальных исходов связанных с вирусной инфекцией вызванной COVID-19 при использовании инвазивной ИВЛ (до 85-90%). На наш взгляд данный факт связан не с самим методом искусственной вентиляции легких, а с крайне тяжелым состоянием пациентов и особенностями течения заболевания COVID-19.
Тяжесть пациентов, которым проводится инвазивная ИВЛ обусловлена большим объемом поражения легочной ткани (как правило более 75%), а также возникающей суперинфекцией при проведении длительной искусственной вентиляции.
Собственный опыт показывает, что процесс репарации легочной ткани при COVID происходит к 10-14 дню заболевания. С этим связана необходимость длительной искусственной вентиляции легких. В анестезиологии-реаниматологии одним из критериев перевода на спонтанное дыхание и экстубации служит стойкое сохранение индекса оксигенации более 200 мм рт. ст. при условии, что используются невысокие значения ПДКВ (не более 5-6 см. вод. ст.), низкие значения поддерживающего инспираторного давления (не более 15 см. вод. ст.), сохраняются стабильные показатели податливости легочной ткани (статический комплайнс более 50 мл/мбар), имеется достаточное инспираторное усилие пациента ( p 0.1 более 2.)
Достижение адекватных параметров газообмена, легочной механики и адекватного спонтанного дыхания является сложной задачей, при условии ограниченной дыхательной поверхности легких.
При этом задача поддержания адекватных параметров вентиляции усугубляется присоединением вторичной бактериальной инфекции легких, что увеличивает объем поражения легочной ткани. Известно, что при проведении инвазинвой ИВЛ более 2 суток возникает крайне высокий риск возникновения нозокомиальной пневмонии. Кроме того, у больных с COVID и «цитокиновым штормом» применяются ингибиторы интерлейкина, которые являются выраженными иммунодепрессантами, что в несколько раз увеличивает риск возникновения вторичной бактериальной пневмонии.
В условиях субтотального или тотального поражения дыхательной поверхности легких процент успеха терапии дыхательной недостаточности является крайне низким.
Собственный опыт показывает, что выживаемость пациентов на инвазивной ИВЛ составляет 15.3 % на текущий момент времени.
Алгоритм безопасности и успешности ИВЛ включает:
В связи с тем, что процент выживаемости пациентов при использовании инвазивной ИВЛ остается крайне низким возрастает интерес к использованию неинвазивной искусственной вентиляции легких. Неинвазивную ИВЛ по современным представлениям целесообразно использовать при ОРДС легкой степени тяжести. В условиях пандемии и дефицита реанимационных коек процент пациентов с тяжелой формой ОРДС преобладает над легкой формой.
Тем не менее, в нашей клинической практике у 23% пациентов ОРИТ в качестве стартовой терапии ДН и ОРДС применялась неинвазивная масочная вентиляция (НИМВЛ). К применению НИМВЛ есть ряд ограничений: больной должен быть в ясном сознании, должен сотрудничать с персоналом. Допустимо использовать легкую седацию с целью обеспечения максимального комфорта пациента.
Критериями неэффективности НИМВЛ являются сохранение индекса оксигенации ниже 100 мм рт.ст., отсутствие герметичности дыхательного контура, возбуждение и дезориентация пациента, невозможность синхронизации пациента с респиратором, травмы головы и шеи, отсутствие сознания, отсутствие собственного дыхания. ЧДД более 35/мин.
В нашей практике успешность НИМВЛ составила 11.1 %. Зав. ОАИР: к.м.н. Груздев К.А.
При какой сатурации подключают кислород при ковиде
Высокопоточная назальная канюля (HFNC) обычно используется при лечении гипоксической дыхательной недостаточности и связано с бóльшим количеством дней без подключения к аппарату ИВЛ и более низкой смертностью по сравнению со стандартной оксигенотерапией или неинвазивной вентиляцией.
Тем не менее, использование высокопоточной назальной канюли для терапии пациентов с коронавирусным заболеванием- 2019 (COVID-19) затруднительно в связи с повышенным риском распространения микрочастиц (особенно во время приступов кашля), возможным истощением запаса кислорода и обеспокоенностью по поводу того, что она вряд ли изменит естественный ход развития вирусной пневмонии.
Эти факторы привели к призывам отказаться от использования HFNC в пользу ранней интубации. Хотя эти сомнения и являются обоснованными, они могут иметь определенные последствия при нынешней пандемии, что связано с ростом пациентов, которым требуется интенсивная терапия и возможным развитием ситуации, когда аппаратов для проведения ИВЛ не будет хватать для всех. Выполнение больничных правил, предписывающих проведение ранней интубации пациентов с COVID-19, ускорит истощение и других ресурсов в отделениях реанимации и интенсивной терапии (ОРИТ), включая седативные препараты и человеческие ресурсы. И, наконец, снижение порога возможности проведения интубации и приема в ОРИТ скрывает истинную степень тяжести заболевания и искажает модель пандемии.
Появляющиеся данные свидетельствуют, что у пациентов с COVID-19 развивается атипичный острый респираторный дистресс-синдром (ОРДС) с относительно хорошо сохраненной механикой и комплайнсом легких, несмотря на тяжелую гипоксемию по причине фракции шунта. Также дополнительно известно, что пронпозиция может улучшить насыщение кислородом и уменьшить фракцию шунта. Поэтому рядом авторов сейчас предполагается, что в случае лечения пациентов без усиленной работы дыхания использование канюли HFNC сможет обеспечить потребность в кислороде, при этом позволяя пациентам без посторонней помощи изменять положение своего тела, самостоятельно переходя в пронпозицию (положение на животе). Проблема дополнительной генерации аэрозоля, спровоцированной HFNC, может быть частично решена за счет принятия следующих мер: надетая на пациента хирургическая маска для ограничения диапазона распространения частиц, усиленный комплект средств индивидуальной защиты для персонала, группирование пациентов, а также использование помещений с отрицательным давлением.
В недавно полученном отчете из Италии описаны два фенотипических проявления пневмонии, вызванной COVID-19. Изначально у многих пациентов проявляется тяжелая гипоксемия при отсутствии одышки и сохранении комплаенса легких, с малой массой легких, низким соотношением вентиляции / перфузии (V/Q) и низкой рекрутируемостью легких (определяемая как L-фенотип). Со временем у некоторых из этих пациентов развивается более классический фенотип ОРДС, характеризующийся низким комплаенсом легких, высокой массой легких, значительным шунтом справа налево и высокой рекрутируемостью легких (определяемый как H-фенотип). Предполагаемая причина появления гипоксемии в случае L-фенотипа заключается в дисрегуляции легочной перфузии и утрате гипоксической вазоконстрикции. Как известно, дорсальные отделы легких характеризуются большим количеством легочной ткани и более развитой сосудистой сетью, что приводит к более низкому местному легочному сопротивлению и более слабой гипоксической легочной вазоконстрикции ввиду повышенной эндотелиальной экспрессии оксида азота. Пронпозиция позволяет достичь более равномерного распределения легочной ткани между дорсальной и вентральной осями, что приводит к более однородной альвеолярной архитектуре. Более того, она также способствует более равномерному распределению легочной перфузии.
Улучшение насыщения кислородом также может восстановить гипоксическую легочную вазоконстрикцию, которая нарушается при более низких уровнях насыщения кислородом, далее улучшая соотношение V/Q. И, наконец, улучшенное насыщение кислородом, возможно, предотвратит ухудшение одышки, а перераспределение легочной ткани при самостоятельном принятии пронпозиции изменит взаимоотношение между напряжением и деформацией в легком и интраторакальными силами, замедляя формирование отека легких и прогрессирования заболевания от L к H-фенотипу.
Помимо сохранения мощностей ИВЛ в условиях загруженности ресурсов, описываемый метод респираторной терапии может найти важное применение в странах с ограниченными ресурсами, где более сложные технологии ОРИТ могут быть недоступны.
Хроники пандемии: три причины скрытой гипоксии при CoViD-19
Продолжаются исследования многих неясных аспектов патогенеза коронавирусной болезни. Одним из наиболее важных открытых вопросов остается механизм развития «тихой гипоксии», – малосимптомного дефицита кислорода в клетках и тканях. Если это состояние длится достаточно долго без соответствующего медицинского вмешательства, могут наступить необратимые изменения в жизненно важных органах. Группа специалистов в области биомедицинской инженерии из Бостонского университета, работающая в сотрудничестве с коллегами из Университета Вермонта (США), пытаются найти ответы с использованием технологий компьютерного моделирования.
Во многих случаях люди, инфицированные вирусом SARS-CoV-2 и имеющие опасно низкий уровень насыщения крови кислородом, не обнаруживают никаких признаков одышки или затрудненного дыхания. Термин «тихая гипоксия» появился именно в связи с этой тенденцией. Принято считать, что первоначально вирус повреждает легкие, лишая определенные их участки способности полноценно выполнять свои функции. Пораженные легочные ткани теряют кислород и больше не могут оксигенировать кровоток. Но как именно возникает этот эффект, до сих пор было неясно. Особую тревогу вызывал тот факт, что при несовместимой с жизнью гипоксии сканирование легких зачастую не обнаруживало практически никаких серьезных аномалий.
Объединенная исследовательская группа протестировала на математических моделях три различных сценария, объясняющих, как и почему легкие перестают поставлять кислород в кровоток. Результаты, опубликованные в Nature Communications, позволяют предполагать, что при CoViD-19 в легочных тканях пациентов одновременно протекают несколько патологических процессов.
Известно, что легкие выполняют жизненно важную функцию внешнего газообмена, при вдохе обеспечивая поступление кислорода для каждой клетки и при выдохе избавляя организм от углекислого газа. Здоровые легкие насыщают кровь кислородом на уровне 95-100% от максимально возможного. Уровень сатурации ниже 95 процентов уже является тревожным сигналом, а падение ниже 92 процентов создает показания к искусственной оксигенации. На ранних этапах пандемии, когда в потоке медицинской информации стали появляться первые сообщения о феномене тихой гипоксии, бытовые пульсоксиметры были буквально сметены с аптечных полок: очень многие люди осознали, что им, возможно, придется бороться с инфекцией в домашних условиях, и готовились отслеживать у себя и своих близких уровень насыщения крови кислородом.
Первоочередным объектом исследования было влияние CoViD-19 на способность легких регулировать основные потоки крови. Нормальным является то, что в инфицированном участке легочной ткани, если он не способен собирать достаточно кислорода, кровеносные сосуды сужаются. Этот механизм был выработан в ходе эволюции, и его задачей является перенаправление кровотока в наиболее оксигенированные участки легких, благодаря чему последствия инфекции частично или полностью компенсируются. Но при CoViD-19, как предполагают авторы, у некоторых пациентов легкие утрачивают способность ограничивать приток крови к уже поврежденной ткани; напротив, кровеносные сосуды там дополнительно расширяются, – т.е. происходит нечто такое, что очень трудно увидеть при стандартной компьютерной томографии.
Вычислительное моделирование подтверждает эту гипотезу.
Было также изучено влияние свертываемости крови на кровоснабжение различных участков легкого. Когда слизистые оболочки сосудистых стенок воспаляются в ответ на коронавирусную инфекцию, внутри легких могут образовываться микроскопические сгустки, размеры которых не позволяют увидеть их на томографических сканах. Компьютерное моделирование подтверждает и такую возможность, но одного этого патогенетического механизма было бы недостаточно, чтобы оксигенация крови снизилась до реально наблюдаемых у пациентов уровней.
Наконец, было исследовано влияние коронавирусной болезни на эффективность передачи кислорода в кровь, – в объемах, достаточных для нормального функционирования организма. Эта пропорция нарушается при многих заболеваниях дыхательной системы, – например, при бронхиальной астме, – что может быть одним из факторов тихой гипоксии и при CoViD-19. Результаты вычислительного моделирования свидетельствуют о том, что для развития тихой гипоксии эффективность передачи кислорода в кровь должна быть снижена, в том числе, и в тех участках легких, которые при визуализирующей диагностике не выглядят поврежденными или измененными.
В целом, одновременное сочетание всех трех факторов и становится, по всей вероятности, причиной тяжелых гипоксий у пациентов с CoViD-19. В настоящее время, с учетом полученных данных, изучается возможность предотвратить такой сценарий, в том числе посредством т.н. низкотехнологичного вмешательства, – например, в позе лежа на животе задние отделы легких усваивают больше кислорода и в какой-то степени компенсируют недостаточную пропорцию между притоком воздуха и сатурацией крови. Как утверждают авторы, очень важно понимать все возможные причины гипоксии, чтобы в каждом конкретном случае выбрать наиболее эффективный терапевтический ответ, – в частности, назначить сосудосуживающие и/или тромболитические препараты.