Избыток жира влияет на половое созревание и менструальный цикл
У девочек с избыточным весом, половое созревание протекает специфически, как с точки зрения репродуктивных гормонов, так и с точки зрения процесса созревания молочных желез. К данным вывода пришло исследование, проведенное Национальным Институтом Здоровья (NIH) в Дареме, Северная Каролина.
Предыдущие исследования показывали, что девочки с ожирением начинают половое созревание и испытывают свою первую менструацию раньше, чем девочки с нормальным весом. В данном исследовании оценивалось, может ли избыток жира влиять не только на время полового созревания, но и на уровень репродуктивных гормонов и развитие репродуктивных органов, таких как грудь, яичники и матка.
«Мы обнаружили, что в середине и конце полового созревания девочки с большим количеством жира в организме демонстрировали более высокий уровень некоторых репродуктивных гормонов, включая фолликулостимулирующий гормон, ингибин В и мужские гормоны, например, тестостерон”, — заявил один из авторов исследования доктор Натали Ди Шоу.
В качестве подопечных наблюдались 90 девочек в возрасте от 8 до 15 лет (36 с ожирением, 54 с нормальным весом). Наблюдения длились 4 года. Кроме расчета общего жира в организме (DXA-сканирование), отслеживалось половое созревание (стадирования Таннера), проводились ультразвуковые исследования груди и таза, измерялся уровень гормонов.
У девочек с ожирением в организме наблюдаются различия в уровне репродуктивных гормонов, грудь развивается медленнее и первые месячные наступают раньше, чем у девочек с более низким весом.
При этом не было обнаружено значимых различий в созревании яичников и матки в зависимости от объема жировых отложений. У некоторых девушек с лишним весом отмечался более высокий уровень тестостерона, что приводило к нарушениям менструального цикла и избытку волос на теле.
Самым эффективным методом лечения ожирения, (в том числе и у детей) современная медицинам признают бариатрическую хирургию.
Признаки гормонального сбоя у женщин
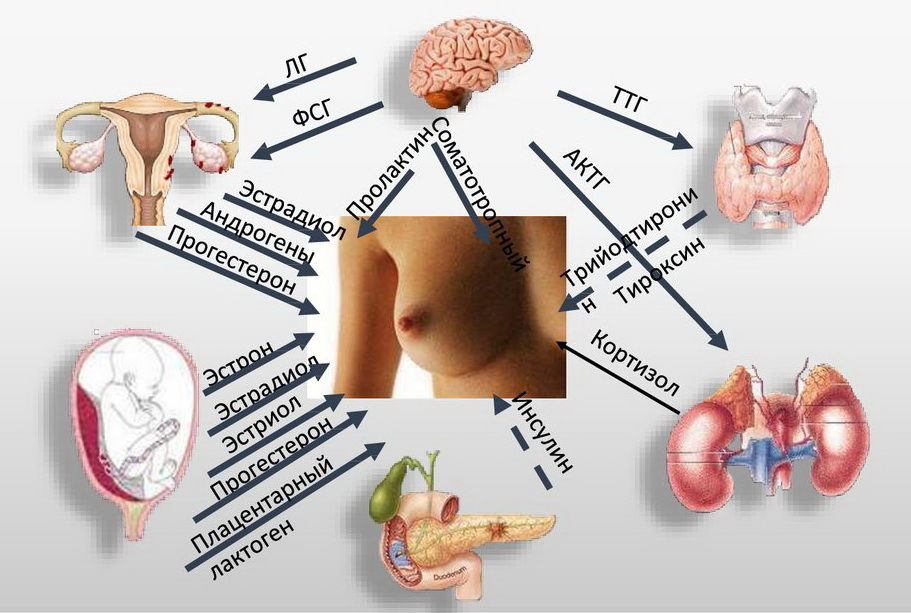
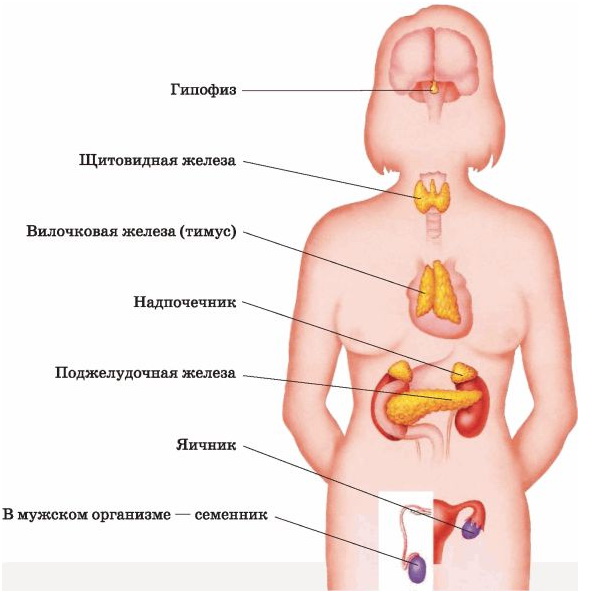
Гормональная система женщины хрупка. Существует очень много причин для нарушения гормонального баланса. Найти причину сбоя не всегда удается быстро, потому что за правильное соотношение гормонов в теле женщины отвечают несколько органов и систем:
В зависимости от того, где именно произошел сбой, отличается и симптоматика. Но так как мы говорим о женском здоровье, то рассмотрим симптомы гормонального сбоя, при котором нарушен баланс половых гормонов, вырабатываемых яичниками.
Симптомы дисбаланса половых гормонов женщины
Половые гормоны определяют внешний вид женщины, ее голос, поведение, отвечают за репродуктивную функцию. Самый главный женский гормон — эстроген — ответственен за мягкие очертания тела, крупные молочные железы, широкие бедра, высокий голос. Тестостерон также есть в женском теле, но в меньшем количестве, чем у мужчин. Женский организм вырабатывает прогестероны, пролактин, гонадотропный гормон, гонадотропин-рилизинг-гормон.
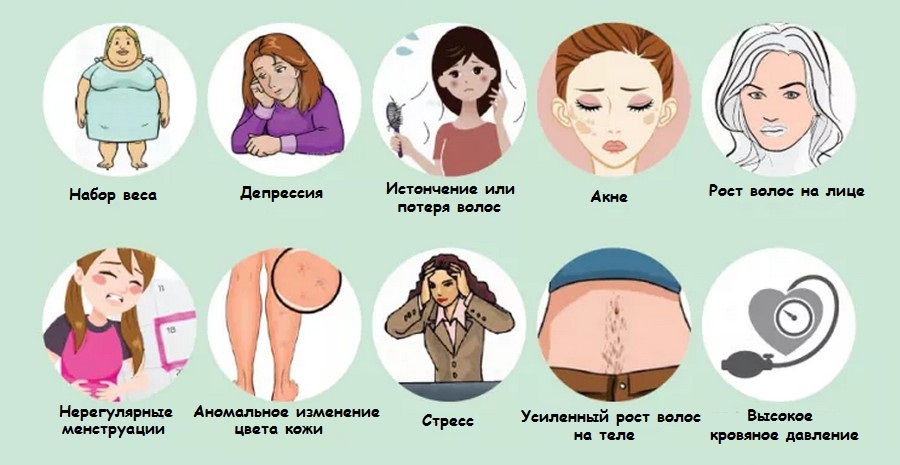
Дисбаланс часто виден невооруженным глазом. Вот типичные симптомы гормонального сбоя у женщин:
Акне также говорит о том, что в крови много свободного тестостерона, но это далеко не всегда свидетельствует о гормональном сбое, это распространенная ситуация в пубертате.
Чаще всего о том, что в организме женщины не все в порядке с гормонами, говорят следующие признаки:
Если у женщины есть выделения из сосков, это может говорить о том, что у нее повышен пролактин из-за пролактиномы — доброкачественной опухоли гипофиза. Оволосение по мужскому типу, редкие менструации, лишний вес, бесплодие могут быть признаки поликистозных яичников.
Общие признаки гормональных нарушений
Кроме специфических симптомов гормонального сбоя, есть и менее типичные, которые могут, тем не менее, говорить о некорректной работе щитовидной железы, либо быть частью картины дисбаланса половых гормонов:
Для сбоя гормонального фона у женщин характерна картина, при которой одновременно появляются сразу несколько тревожных признаков. Страдает и половая сфера, и внешний вид, и активность.
При каком весе пропадают месячные при ожирении
Кафедра акушерства и гинекологии им. С.Н. Давыдова Северо-Западного государственного медицинского университета им. И.И. Мечникова Минздрава России, Санкт-Петербург
Роль ожирения в развитии нарушений менструальной и репродуктивной функций
Журнал: Российский вестник акушера-гинеколога. 2014;14(2): 43-51
Ковалева Ю. В. Роль ожирения в развитии нарушений менструальной и репродуктивной функций. Российский вестник акушера-гинеколога. 2014;14(2):43-51.
Kovaleva Iu V. Role of obesity in the development of menstrual and reproductive dysfunctions. Russian Bulletin of Obstetrician-Gynecologist. 2014;14(2):43-51.
Кафедра акушерства и гинекологии им. С.Н. Давыдова Северо-Западного государственного медицинского университета им. И.И. Мечникова Минздрава России, Санкт-Петербург
Ожирение оказывает неблагоприятное влияние на репродуктивное здоровье женщин. Установлена взаимосвязь ожирения с нарушениями функции яичников, проявляющимися ановуляцией, нарушением ритма менструаций и почти трехкратным увеличением частоты эндокринного бесплодия. Наличие ожирения у женщин увеличивает риск развития рака молочной железы и эндометрия. Несмотря на многочисленность сообщений о нарушениях функций репродуктивной системы у женщин с ожирением, до настоящего времени их генез точно не определен. В последние годы опубликовано большое число работ, посвященных взаимосвязи гиперинсулинемии с яичниковой гиперандрогенией. Большинство исследователей признают, что инсулинорезистентность и гиперинсулинемия способствуют формированию синдрома поликистозных яичников. В настоящем обзоре подробно рассматриваются патогенетические аспекты влияния ожирения на функцию репродуктивной системы и обмен половых гормонов у женщин.
Кафедра акушерства и гинекологии им. С.Н. Давыдова Северо-Западного государственного медицинского университета им. И.И. Мечникова Минздрава России, Санкт-Петербург
В настоящее время ожирение рассматривается в качестве одной из основных причин нарушений функции репродуктивной системы у женщин, ведущих к снижению фертильности, патологическому течению беременности и родов.
Одно из самых ранних исследований, которое показало связь между ожирением и нарушением репродуктивной функции, было опубликовано в начале XX века H. Evans и K. Bishop (1922). При этом авторами было отмечено, что фертильность восстанавливалась на фоне снижения избыточной массы тела. Взаимосвязь между нарушениями репродуктивной системы и ожирением была изложена в 1934 г. в классической статье Штейна и Левенталя при описании синдрома поликистозных яичников. В 1952 г. J. Rogers и G. Mitchell представили результаты наблюдения за женщинами с ожирением, ановуляторными менструальными циклами и олиго- или аменореей. После консультации диетологов у большинства похудевших пациенток ритм менструаций восстановился; у тех, кому не удалось похудеть, сохранялась олигоменорея. Хотя эти наблюдения были относительно случайными, они заложили основу для последующих исследований связи ожирения с ановуляцией. В последующие годы исследователи неоднократно подчеркивали высокую частоту нарушений менструального цикла, бесплодия, привычного невынашивания беременности у женщин с избыточной массой тела.
Патологическое влияние ожирения на репродуктивную систему прослеживается с самого начала ее функционирования. Частота нарушений менструальной функции у девушек с ожирением значительно выше, чем у подростков с нормальной и низкой массой тела.
Процессы пубертатного периода в норме ассоциированы с накоплением жировой ткани и изменениями продукции лептина [17, 61]. Примерно в 10-11 лет у здоровых девочек происходит резкое повышение уровня лептина в сыворотке крови, что совпадает с физиологическим скачком роста. Лептин действует как сигнальная система от жировой ткани к головному мозгу, «информируя» его о том, что критическая масса жировой ткани достигнута для инициации пубертата и дальнейшего становления репродуктивной функции [2, 22, 26]. Увеличение образования лептина адипоцитами в препубертатном периоде у девочек ответственно за повышение образования кисспептина в нейронах аркуатного и передневентрально-паравентрикулярного ядер гипоталамуса. Это способствует началу пульсирующей секреции гонадотропин-рилизинг-гормона (ГнРГ) в гипоталамусе с последующим циклическим образованием гонадотропинов и наступлению менархе. Менархе в среднем наступает в 12,5 года, когда в организме накапливается определенное количество жира. После менархе уровень лептина снижается и вновь начинает нарастать с периода половой зрелости вплоть до менопаузы.
Снижение чувствительности тканей к инсулину также является физиологическим феноменом для пубертата. Вклад в развитие инсулинорезистентности у подростков вносят повышенные уровни половых гормонов, гормона роста и кортизола, свойственные пубертатному становлению. В этот период изменения образа жизни, ведущие к нарушению баланса потребления и расхода энергии, могут спровоцировать прибавку массы тела.
Наличие ожирения у девочек-подростков отражается на процессе полового созревания. Этот процесс у подростков с избыточной массой тела начинается раньше, чем у девушек с нормальной массой тела [5], в частности, раньше наступает менархе. Так, при избыточной массе тела менархе начинается на 1,4±0,2 года раньше, чем у девочек с нормальной массой тела, т.е. возраст наступления менархе снижается до 9-11 лет [1]. Причем ускорение темпов полового созревания не соответствует темпам развития генитального аппарата. Ранний возраст менархе можно рассматривать как независимый прогностический фактор нарастания индекса массы тела (ИМТ) и других осложнений ожирения. По данным ряда авторов, своевременное наступление менархе у женщин с различными формами ожирения и нарушениями репродуктивной функции наблюдается лишь в 31% случаев. Но с течением времени данная тенденция меняется на противоположную, в результате чего девушки с ожирением вступают в репродуктивный период позже, чем их здоровые сверстницы, а впоследствии формируется хроническая ановуляция, риск развития которой находится в прямой зависимости от величины ИМТ.
Кроме того, у девочек с избыточной массой тела могут наблюдаться отклонения в порядке появления половых признаков. У них встречается изолированное пубархе, частота которого доходит до 33%, в то время как в популяции этот показатель составляет 15%. Эндокринной основой несвоевременной манифестации полового оволосения является чрезмерное адренархе.
При ожирении примерно в 3 раза чаще отмечается ановуляторное бесплодие, значительно снижается эффективность различных видов терапии, направленной на восстановление фертильности. Так, в Европейском многоцентровом исследовании, проведенном под руководством J. Rich-Edwards и соавт. (1994), было показано, что у женщин с ИМТ ≥30 кг/м 2 распространенность бесплодия в 2,7 раза выше, чем у женщин с нормальной массой тела. Частота и выраженность нарушений репродуктивной функции, как и других сопутствующих ожирению заболеваний, возрастает с увеличением степени ожирения и количества жировой ткани, особенно в висцеральной области. Роль ожирения в патогенезе нарушений функций репродуктивной системы подтверждается восстановлением овуляторного менструального цикла после нормализации массы тела [11, 35, 42, 45, 46].
Особую значимость приобретает проблема ожирения в период перименопаузы. Поскольку жировая ткань является местом конверсии биоактивных эстрогенов из андрогеновых предшественников, казалось бы, у женщин с ожирением реже должны развиваться такие проявления климактерических расстройств, как вегетососудистые нарушения, остеопороз. Однако результаты ряда исследований показали, что у женщин с ожирением повышение уровня ФСГ и снижение концентрации эстрогенов наступает в среднем на 4 года раньше, поэтому у женщин 40-44 лет, страдающих ожирением, «приливы» отмечаются чаще по сравнению с женщинами, имеющими нормальную массу тела, и лишь к 50-55 годам эти различия стираются [57].
Несмотря на многочисленность сообщений о нарушениях функции репродуктивной системы у женщин с ожирением, до настоящего времени механизмы развития этих расстройств пока еще не вполне ясны, а выраженность не всегда коррелирует с ИМТ, традиционно используемым для диагностики ожирения. Вместе с тем становится все более очевидным, что жировая ткань, особенно висцерального происхождения, играет важную роль как в метаболизме половых гормонов, так и в синтезе биологически активных веществ (лептин, адипонектин, резистин и др.), обладающих эндокринной и паракринной активностью [10].
Установлено, что ожирение ассоциировано с рядом аномалий в эндокринном балансе (рис. 1). 
Прежде всего при ожирении развивается гиперлептинемия [19, 20, 27, 40, 51, 60], важнейшими следствиями которой являются:
— нарушение характера пульсирующей секреции ГнРГ, а следовательно, и характера образования гонадотропинов;
— подавление стероидогенеза в клетках яичников;
— нарушение механизмов обратной связи в регуляции менструального цикла;
— нарушение процессов питания эмбриона и увеличение вероятности его гибели при наступлении беременности.
Гиперлептинемия может оказывать стимулирующее действие на некоторые гипоталамические рилизинг-факторы, в частности на кортикотропин-рилизинг-гормон (КТРГ). Повышение секреции КТРГ может приводить к нарушению секреции ФСГ и ЛГ, в результате чего подавляются созревание доминантного фолликула и овуляция.
Рецепторы к лептину обнаружены на поверхности гранулезных клеток, клеток теки и интерстициальных клеток яичников. Так, R. Zachow и D. Magoffin (1997), принимая во внимание данные о наличии мРНК-рецепторов лептина в овариальной ткани, продемонстрировали прямое действие указанного гормона на стероидогенез клеток гранулезы крыс in vitro. При этом было показано дозозависимое подавляющее действие лептина на инсулиноподобный фактор роста 1-го типа (ИФР-1), потенциированное увеличением стимулированного ФСГ-синтеза эстрадиола клетками гранулезы. Эти данные подтверждают гипотезу о том, что повышение уровня лептина у лиц с ожирением может противодействовать созреванию доминантного фолликула и овуляции.
Весьма интересными являются данные L. Spicer и C. Francisco (1997), свидетельствующие о том, что лептин в нарастающих концентрациях (10-300 нг/мл) ингибирует инсулинзависимую продукцию эстрадиола и прогестерона в культуре клеток гранулезы. Этот эффект обусловлен наличием специфических сайтов связывания для лептина.
Таким образом, лептин подавляет процессы стероидогенеза в гранулезных клетках и клетках теки [3], проявляя антагонизм по отношению к ИФР-1, инсулину, ЛГ и трансформирующему фактору роста-β (ТФР-β). Кроме того, независимо от влияния на механизмы стероидогенеза, высокие концентрации лептина подавляют развитие доминантного фолликула и нарушают овуляцию.
У женщин с ожирением уровень циркулирующего глобулина, связывающего половые гормоны (ГСПГ), снижен, что является ответом печени на увеличенные уровни циркулирующего тестостерона и инсулина [3, 61]. Инсулин непосредственно ингибирует синтез ГСПГ в гепатоцитах. Распределение жира также играет важную роль в изменении концентрации ГСПГ. У женщин с центральным (андроидным) ожирением уровень ГСПГ в плазме крови обычно ниже, чем у женщин того же возраста и с сопоставимой массой тела с периферическим (гиноидным) ожирением.
Ожирение также сочетается с повышенной продукцией эстрогенов. Еще в 1978 г. P. Siiteri и P. MacDonald обнаружили, что в жировой ткани происходит ароматизация андрогенов и таким путем образуется ⅓ циркулирующих эстрогенов. Связь между количеством жировой ткани и содержанием эстрогенов была выявлена в ряде исследований. Выраженность ароматизации существенно коррелирует с массой жира. При ожирении повышается активность ароматазы в адипоцитах и увеличивается конверсия андрогенов в эстрогены. Помимо этого, гиперэстрогению обусловливает снижение уровня ГСПГ и изменение метаболизма эстрогенов, ведущее к относительному увеличению биологически активных фракций. Таким образом, 3 механизма обеспечивают присутствие в крови повышенного количества биологически активного эстрадиола при ожирении:
— повышенная продукция эстрадиола из эстрона в периферических (экстраовариальных) тканях, поддерживающая увеличенные уровни циркулирующего эстрадиола;
— повышенный уровень биологически активного циркулирующего эстрадиола вследствие сниженного уровня ГСПГ;
— локальная конверсия эстрона в эстрадиол в тканях-мишенях. Этот локальный механизм физиологически значим в таких тканях-мишенях, как молочная железа, в которой развивается пролиферация ткани в ответ на действие эстрогенов.
При ожирении соотношение эстрон/эстрадиол меняется в сторону эстрона, что предрасполагает к нарушению нормального функционирования механизма обратной связи. Гиперэстрогенемия сенсибилизирует гонадотрофы гипофиза к ГнРГ и снижает пороговый уровень овариального эстрадиола, необходимый для начала овуляторного подъема ЛГ. Гиперстимуляция незрелых фолликулов, вероятно, лежит в основе их кистозного перерождения [6].
Увеличение частоты нарушений менструальной функции при прогрессировании ожирения обусловлено изменением экстрагландулярного образования эстрона из андрогенов и ингибированием циклической секреции ЛГ.
Кроме того, ожирение сочетается с меньшим образованием неактивных метаболитов эстрадиола (2-гидроксиэстрогенов) и высокой продукцией активных метаболитов. На фоне гиперэстрогении и прогестерон-дефицитного состояния удлиняется время пролиферации эндометрия, что приводит к развитию его гиперплазии, проявляющейся кровотечениями у 50-60% женщин с ожирением. При ожирении возникает повышенный риск развития не только гиперпластических процессов, но и рака эндометрия и молочных желез.
Важнейшими следствиями гиперэстрогенемии являются нарушение механизмов обратной связи в регуляции менструального цикла, нарушение овуляции, усиление пролиферации эпителиальных клеток протоков молочных желез и клеток эндометрия, маточные кровотечения.
В механизмах нарушений репродуктивной функции при ожирении важную роль играют гиперинсулинемия и инсулинорезистентность [43, 53, 57]. Увеличение образования и секреции инсулина β-клетками поджелудочной железы при ожирении вызвано, в частности, β-эндорфином вследствие повышения активности опиоидергической системы мозга, а также высокими концентрациями свободных жирных кислот и глюкозы [51].
Инсулинорезистентность при андроидном ожирении обусловлена повышением содержания свободных жирных кислот в крови и подавлением захвата инсулина гепатоцитами вследствие увеличения образования андрогенов. Кроме того, повышенное образование лептина адипоцитами стимулирует липолиз в жировой ткани и скелетных мышцах и подавляет действие инсулина в периферических органах и тканях. Кстати, в физиологических условиях лептин ослабляет продукцию инсулина в поджелудочной железе, но при ожирении этого не происходит из-за лептинорезистентности [59].
Важнейшие следствия гиперинсулинемии:
— увеличение количества мРНК Р450с17α;
— повышение синтеза андрогенов в тека-клетках яичников, пролиферация тека-клеток;
— ФСГ-стимулированный синтез эстрогенов;
— повышение уровня секреции ЛГ;
— активация гена ГнРГ;
— снижение синтеза печенью ГСПГ;
— повышение уровня свободного тестостерона;
— увеличение риска развития рака эндометрия и/или молочных желез.
При инсулинорезистентности и гиперинсулинемии инсулин проникает в область гипоталамуса, что приводит к повышенному выбросу КТРГ, который запускает ряд гормональных изменений в гипофизе и периферических эндокринных железах [58]. При этом усиливается секреция адренокортикотропного гормона (АКТГ), пролактина в гипофизе и снижается секреция гормона роста и тиреотропного гормона (ТТГ). Под воздействием повышенной стимуляции АКТГ усиливается продукция кортизола надпочечниками. Повышение секреции КТРГ также может приводить к нарушению секреции ФСГ и ЛГ. Избыток инсулина усиливает выброс ЛГ в ответ на стимуляцию гипофиза гонадолиберином.
Роль инсулина в овариальной функции сводится к усилению ЛГ-зависимого синтеза тестостерона. Избыток инсулина подавляет продукцию ГСПГ в печени, тем самым повышая содержание в крови биологически активных фракций тестостерона. Таким образом, инсулин увеличивает уровень свободного тестостерона через 2 независимых механизма: увеличение яичниковой секреции предшественников тестостерона (например, андростендиона) и супрессию ГСПГ.
Однако неясно, каким образом инсулин стимулирует продукцию андрогенов в яичниках, в то время как организм «резистентен» к действию инсулина. Для объяснения этой парадоксальной ситуации был предложен ряд гипотез:
1) инсулин действует на яичник не только через рецепторы инсулина, но также через рецепторы ИФР-1 в яичниках;
2) так как инсулин обладает множеством функций, можно предположить селективный дефект некоторых из них;
3) может наблюдаться органоспецифичность чувствительности к инсулину;
4) инсулин может связываться с гибридным инсулиновым рецептором (подобное маловероятно, так как гибридные рецепторы к инсулину не были идентифицированы в яичниках человека).
Показано, что ИФР-1 оказывает свое действие в физиологических концентрациях, в то время как инсулин в нормальных концентрациях подобного действия на организм не оказывает, за исключением его синергического воздействия на ЛГ-индуцированный синтез андрогенов тека-клетками. Несмотря на то что рецепторы инсулина и ИФР-1 являются продуктами деятельности разных генов, в результате их структурного сходства инсулин может связываться с рецепторами ИФР-1, хотя с меньшим сродством, чем с собственными рецепторами [12, 13]. Однако при гиперинсулинемии, а также в ситуации, когда рецепторы инсулина блокированы или имеется их дефицит, можно ожидать, что инсулин будет связываться с рецепторами ИФР-1 в большей степени и активировать ферментные процессы, аналогично этому фактору. Таким образом, в условиях гиперинсулинемии эффект инсулина опосредуется через рецепторы ИФР-1, инсулин имитирует его действие, повышая синтез андрогенов в яичниках [3, 4, 43].
Идея о том, что инсулин стимулирует продукцию андрогенов яичниками путем прямой активации своих собственных рецепторов, подтверждается сообщениями группы S. Franks (1999), показавшей на культуре гранулезных клеток человека, что влияние инсулина на стероидогенез в яичниках опосредовано собственными инсулиновыми рецепторами, а не рецепторами к ИФР-1.
W. Miller и соавт. [38] выявили сериновое фосфорилирование Р450с17α у человека. Если один и тот же фактор фосфорилирует серин инсулинового рецептора, приводя к инсулинорезистентности, также фосфорилирует серин Р450с17α, приводя к гиперандрогении, это могло бы объяснить взаимосвязь ожирения и инсулинорезистентности через единый генетический дефект.
Возможно, механизмы стимуляции инсулином и ИФР-1 стероидогенеза в яичнике могут быть разделены на неспецифические и специфические. Неспецифические заключаются в классическом действии инсулина на метаболизм глюкозы, аминокислот и синтез ДНК. В результате повышается жизнеспособность клетки и, следовательно, усиливается синтез гормонов. Специфические механизмы включают прямое действие инсулина / ИФР-1 на стероидогенные ферменты, синергизм между инсулином и ЛГ/ФСГ и влияние на количество рецепторов к ЛГ.
Инсулин и ИФР-1, действуя синергично с ФСГ, стимулируют ароматазную активность клеток гранулезы, тем самым увеличивают синтез эстрадиола. Кроме того, они приводят к повышению содержания рецепторов к ЛГ, усиливая ЛГ-зависимый синтез андростендиона тека- и стромальными клетками.
У женщин с ожирением определяется повышенная активность гипоталамо-гипофизарно-надпочечниковой оси, что сопровождается увеличением синтеза кортизола и надпочечниковых андрогенов [4].
Андрогены нарушают нормальное развитие фолликулов, приводя к множественной атрезии. Возрастающая концентрация андрогенов в яичнике вызывает постепенную элиминацию эстрогенпродуцирующих клеток гранулезы с последующей гиперплазией текальных клеток и лютеинизацией интерстициальной ткани яичника, которые являются местом продукции андрогенов. Этим объясняется то, что стимуляция яичникового стероидогенеза инсулином проявляется преимущественно в виде гиперандрогении. Кроме того, возможно, имеет место подавление инсулином апоптоза, в результате чего атрезирующиеся фолликулы, которые в иных условиях погибли бы, получают возможность длительно функционировать.
Наиболее выраженные гормональные нарушения имеются у больных с ожирением и СПКЯ [20, 25, 28, 32, 55]. По сравнению с пациентками с «чистым» ожирением у женщин с СПКЯ выявляются более высокие уровни ЛГ, тестостерона и индекса свободных андрогенов [3]. Вероятно, выявленные изменения можно объяснить большей степенью гиперинсулинемии у больных с СПКЯ, чем с «чистым» ожирением, и ингибирующим влиянием инсулина на секрецию ГСПГ [47, 54]. Таким образом, наличие СПКЯ является определяющим фактором в генезе нарушений эндокринной функции репродуктивной системы у больных с ожирением, что в значительной степени связано с инсулинорезистентностью и гиперсекрецией инсулина.
При ожирении увеличивается продукция провоспалительных цитокинов: фактора некроза опухолей α (ФНО-α), интерлейкина-6 (ИЛ-6) клетками жировой ткани. Постоянное увеличение уровня провоспалительных цитокинов в крови способствует нарушению функционирования репродуктивной системы [31].
В овариальной ткани in vitro ФНО-α в зависимости от дозы потенцирует действие инсулина и ИФР-1, стимулируя стероидогенез и пролиферацию в клетках-теки. Не исключено участие ФНО-α в механизме апоптоза фолликулярных клеток, индуцирующем ановуляцию в эксперименте [21].
Ожирение нарушает репродуктивную функцию не только через механизмы нарушения овуляции: снижение фертильности отмечается и у пациенток с овуляторными регулярными циклами. К другим механизмам относятся [4, 19, 47] следующие:
— комплексное воздействие психосоциальных факторов: и ожирение, и бесплодие сопровождаются депрессивным синдромом, что способствует стрессорной гиперпролактинемии и отражается на нормальном росте и созревании преовуляторного фолликула, на овуляции и процессе созревания желтого тела, преимплантационной подготовке эндометрия;
В заключение следует отметить, что при любой форме ожирения имеет место патология гипоталамо-гипофизарной системы, которая приводит к овариальной недостаточности [30, 35]. Установлено, что у женщин с ожирением, особенно с андроидным типом распределения жировой ткани, имеют место:
— инсулинорезистентность и гиперинсулинемия;
— гиперандрогения (повышение содержания тестостерона и андростендиона);
— повышение процессов ароматизации андрогенов в эстрогены на периферии;
— нарушение нейрорегуляции гипоталамо-гипофизарно-яичниковой оси;
— нарушение секреции гонадотропинов;
— снижение концентрации ГСПГ;
— снижение концентрации гормона роста;
— снижение концентрации ИФРСБ;
— повышение уровня лептина;
— повышение уровня кортизола;
— снижение уровня прогестерона.