Закон Бойля — Мариотта
Закон Бойля — Мариотта
Закон Бо́йля — Марио́тта — один из основных газовых законов, открытый в 1662 году Робертом Бойлем и независимо переоткрытый Эдмом Мариоттом в 1676 году. Закон является частным случаем уравнения состояния идеального газа.
Закон Бойля — Мариотта гласит:
В математической форме это утверждение записывается следующим образом
где p — давление газа; V — объём газа.
Важно уточнить, что в данном законе газ рассматривается, как идеальный. На самом деле, все газы в той или иной мере отличаются от идеального. Чем выше молекулярная масса газа, тем больше это отличие.
Полезное
Смотреть что такое «Закон Бойля — Мариотта» в других словарях:
Закон Бойля-Мариотта — Закон Бойля Мариотта один из основных газовых законов. Закон назван в честь ирландского физика, химика и философа Роберта Бойля (1627 1691), открывшего его в 1662, а также в честь французского физика Эдма Мариотта (1620 1684), который открыл… … Википедия
ЗАКОН БОЙЛЯ-МАРИОТТА — ЗАКОН БОЙЛЯ МАРИОТТА, закон, согласно которому объем газа при постоянной температуре обратно пропорционален давлению. Это означает, что по мере возрастания давления объем газа уменьшается. Впервые этот закон был сформулирован в 1662 г. Робертом… … Научно-технический энциклопедический словарь
ЗАКОН БОЙЛЯ МАРИОТТА — один из основных газовых законов, согласно которому при постоянной температуре Т для данной массы m идеального (см.) произведение давления р на занимаемый им объём V есть величина постоянная: pV = const … Большая политехническая энциклопедия
закон бойля-маріотта — закон Бойля Мариотта Boyle’s and Mariotte’s law *Boyle Mariottesches Gesetz – закон iдеальних газiв, згiдно з яким добуток тиску на об єм незмiнної маси такого газу при сталiй температурi є величина стала: (pV) т = const. У певних межах… … Гірничий енциклопедичний словник
Закон Бойля — Воздух (или ин … Википедия
закон Бойля-Мариотта — Boilio ir Marioto dėsnis statusas T sritis Standartizacija ir metrologija apibrėžtis Idealiųjų dujų dėsnis: suslėgtų dujų slėgio ir tūrio sandauga, kai temperatūra pastovi, nekinta, t. y. pV = const. Realiosioms dujoms galioja tik apytiksliai… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
закон Бойля-Мариотта — Boilio ir Marioto dėsnis statusas T sritis fizika atitikmenys: angl. Boyle and Mariotte law; Boyle Mariotte law vok. Boyle Mariottesches Gesetz, n rus. закон Бойля Мариотта, m pranc. loi de Boyle Mariotte, f … Fizikos terminų žodynas
закон Бойля-Мариотта и Гей-Люссака — Boilio, Marioto ir Gei Liusako dėsnis statusas T sritis fizika atitikmenys: angl. Boyle Charles law; Boyle Gay Lussac law vok. Boyle Charlessches Gesetz, n; Boyle Mariotte Gay Lussacsches Gesetz, n rus. закон Бойля Мариотта и Гей Люссака, m pranc … Fizikos terminų žodynas
Бойля-Мариотта закон — закон, связывающий изменения объема газа при постоянной температуре с изменениями его упругости. Этот закон, открытый в 1660 г. англ. физиком Бойлем и позже, но, независимо от него, Мариоттом во Франции, по своей простоте и определенности… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ЗАКОН ИДЕАЛЬНОГО ГАЗА — ЗАКОН ИДЕАЛЬНОГО ГАЗА, закон, определяющий соотношение давления, температуры и объема идеального газа: pV = nRT, где п количество молекул газа, a R универсальная ГАЗОВАЯ ПОСТОЯННАЯ; закон гласит, что при постоянной температуре (Т) произведение… … Научно-технический энциклопедический словарь
Закон Бойля-Мариотта: формула и пример задачи
При изучении газового состояния вещества в современной физике используют сравнительно простую модель. Она базируется на принципах молекулярно-кинетической теории, предложенной в середине XVIII века Даниилом Бернулли. В рамках этой модели исследуется поведение систем во время разных преобразований. В данной статье приведем формулу закона Бойля-Мариотта и название изопроцесса, к которому он применим.
Модель идеального газа
Она основана на теории, которая полагает молекулы и атомы материальными точками, движущимися во всех направлениях с одинаковой скоростью. Кинетическая энергия частиц системы обуславливает наличие температуры в ней, а их постоянные столкновения со стенками сосуда приводят к возникновению давления. Считается, что в идеальной газовой модели частицы системы не взаимодействуют друг с другом, то есть их потенциальная энергия равна нулю.
Поведение любого реального газа хорошо описывается этой теорией только в том случае, если он образован химически инертными молекулами или атомами, его давление является невысоким, а температура находится в пределах комнатной или превышает ее.
Закон Бойля-Мариотта: формула и формулировка
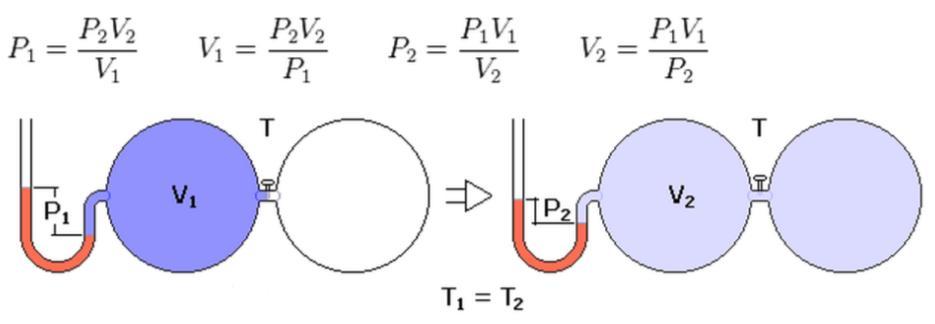
Во второй половине XVII века француз Эдм Мариотт и англичанин Роберт Бойль независимо друг от друга установили следующее соотношение между давлением P и объемом V газовой системы:
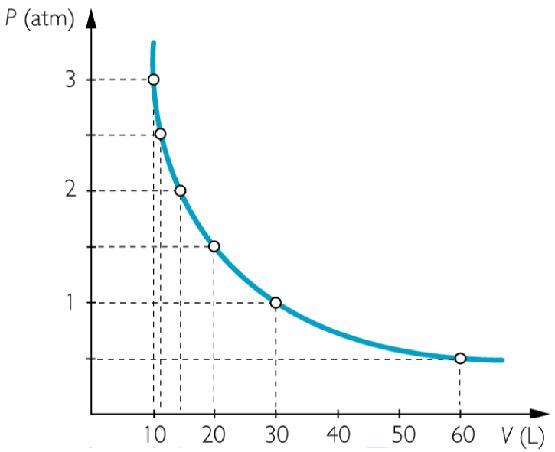
Это равенство выполнялось с высокой точностью для всех исследуемых газов только в том случае, если поддерживалась постоянной температура t. В физике такой процесс называется изотермическим. Соответствующим графиком для него будет изотерма P(V).
Из формулы закона Бойля-Мариотта следует, что при изотермическом изменении одного равновесного состояния на другое давление в системе возрастает (уменьшается) ровно во столько раз, во сколько уменьшается (увеличивается) ее объем.
Хотя рассматриваемый закон был получен экспериментально, в настоящее время он может быть легко выведен из уравнения состояния идеального газа (закон Клапейрона-Менделеева), который имеет форму:
Пример графика, соответствующего рассматриваемому закону, приведен выше. Кривая P(V) называется изотермой и представляет собой гиперболу.
Пример задачи
Покажем, как следует пользоваться формулой закона Бойля-Мариотта для решения задач.
Известно, что в результате изотермического процесса давление в системе с идеальным газом уменьшилось с 105 Па до 104 Па. Насколько изменился ее объем при этом, если в начале процесса он был равен 10 литрам.
Запишем закон изотермического расширения газа в следующей форме:
Отсюда можно выразить значение объема V2 и вычислить его:
V2 = 105/104*10 = 100 литров.
Бойля-Мариотта закон
Бойля-Мариотта закон
| Уравнение состояния |
|---|
 |
| Статья является частью серии «Термодинамика». |
| Уравнение состояния идеального газа |
| Уравнение Ван-дер-Ваальса |
| Уравнение Дитеричи |
| Разделы термодинамики |
| Начала термодинамики |
| Уравнение состояния |
| Термодинамические величины |
| Термодинамические потенциалы |
| Термодинамические циклы |
| Фазовые переходы |
| править |
Уравнение состояния идеального газа (иногда уравнение Клапейрона или уравнение Клапейрона — Менделеева) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
Так как 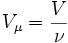
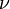
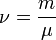
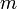
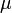
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
В случае постоянной массы газа уравнение можно записать в виде:
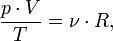
Последнее уравнение называют объединённым газовым законом. Из него получаются законы Бойля — Мариотта, Шарля и Гей-Люссака:
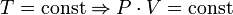
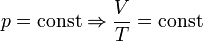
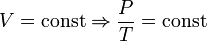
С точки зрения химика этот закон может звучать несколько иначе: Объёмы вступающих в реакцию газов при одинаковых условиях (температуре, давлении) относятся друг к другу и к объёмам образующихся газообразных соединений как простые целые числа. Например, 1 объём водорода соединяется с 1 объёмом хлора, при этом образуются 2 объёма хлороводорода:
1 объём азота соединяется с 3 объёмами водорода с образованием 2 объёмов аммиака:
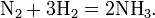
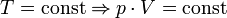
Закон Бойля — Мариотта назван в честь ирландского физика, химика и философа Роберта Бойля (1627—1691), открывшего его в 1662 г., а также в честь французского физика Эдма Мариотта (1620—1684), который открыл этот закон независимо от Бойля в 1676 году.
В некоторых случаях (в газовой динамике) уравнение состояния идеального газа удобно записывать в форме
где 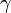

Эмиль Амага обнаружил, что при высоких давлениях поведение газов отклоняется от закона Бойля — Мариотта. И это обстоятельство может быть прояснено, как считал ещё М. В. Ломоносов, на основании молекулярных представлений.
С одной стороны, в сильно сжатых газах размеры самих молекул являются сравнимыми с расстояниями между молекулами. Таким образом, свободное пространство, в котором движутся молекулы, меньше, чем полный объем газа. Это обстоятельство увеличивает число ударов молекул в стенку, так как благодаря ему сокращается расстояние, которое должна пролететь молекула, чтобы достигнуть стенки.
С другой стороны, в сильно сжатом и, следовательно, более плотном газе молекулы заметно притягиваются к другим молекулам гораздо большую часть времени, чем молекулы в разреженном газе. Это, наоборот, уменьшает число ударов молекул в стенку, так как при наличии притяжения к другим молекулам молекулы газа движутся по направлению к стенке с меньшей скоростью, чем при отсутствии притяжения. При не слишком больших давлениях. более существенным является второе обстоятельство и произведение 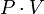
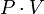
Связь с современной физикой
При каком условии справедлив закон бойля мариотта
Хорошо известный закон Бойля-Мариотта был установлен английским физиком Бойлем в 1662 г. и независимо от него французским ученым Мариоттом в 1679 г.

МАРИОТТ Эдм (1620-1684)
Французский физик, член Парижской Академии Наук (1666), один из ее основателей. В 1676 г. установил закон изменения объема данной массы газа от давления при постоянной температуре (закон Бойля-Мариотта). Предсказал разнообразные применения этого закона, в частности, расчет высоты местности по данным барометра. Доказал увеличение объема воды при замерзании. Обнаружил слепое пятно в глазу, исследовал цвета, в частности, цветные кольца вокруг Солнца и Луны, изучал радугу, дифракцию света.

Роберт БОЙЛЬ (1627-1691)
Бойль был одним из основателей и соучредителей Королевского общества, выросшего из кружка молодых оксфордских ученых. Провел целый ряд новаторских химических экспериментов, включая эксперименты по детальному изучению свойств кислот и оснований. По некоторым данным, первым выдвинул гипотезу о существовании химических элементов. Доказал, что воздух необходим для горения и дыхания.
Для данной массы газа m при неизменной температуре Т произведение давления на объем есть величина постоянная:
 . . |
Закон, связывающий объем газа V и его температуру t, измеренную в градусах Цельсия, был установлен французским ученым Гей-Люссаком в 1802 г.

Жозеф-Луи Гей-Люссак (1778-1850)
Французский химик и физик. Работы Гей-Люссака относятся к различным областям химии и физики (газовые законы).
Для данной массы m при постоянном давлении р объем газа линейно зависит от температуры:
 Рис. 2.2 |
 , , |
График этого процесса, называемого изобарическим, представлен на рис. 2.2. Коэффициент α для всех газов равен
 . . |
Закон, связывающий давление газа р и его температуру t, установлен Шарлем.

Жак Александр Сезар ШАРЛЬ (1746-1823)
Французский физик, химик, инженер и воздухоплаватель. Заинтересовавшись воздухоплаванием, разработал монгольфьеры современной конструкции, подъемная сила которых обусловлена расширением нагретого горелкой воздуха внутри шара. Он же одним из первых стал наполнять воздушные шары водородом (который во много раз легче воздуха и обеспечивает значительно большую подъемную силу, нежели горячий воздух), установив благодаря этому рекорды высоты подъема (более 3 000 м) и дальности полета (43 км). Именно занятия воздухоплаванием заставили Шарля заинтересоваться исследованиями свойств газов. Закон, носящий его имя, Шарль сформулировал в 1787 г. после ряда опытов с кислородом, азотом, водородом и углекислым газом.
Для данной массы m при постоянном объеме V давление газа линейно зависит от температуры:
 , , |
График этого процесса, называемого изохорическим, представлен на рис. 2.3. Коэффициент β для всех газов равен
 , , |
 Рис. 2.4 |
Опытные законы Бойля-Мариотта, Гей-Люссака и Шарля справедливы для широкого интервала давлений, объемов и температур. Однако когда давления превышают атмосферное в 300-400 раз, или температуры очень высоки, наблюдаются отклонения от этих законов. Тем не менее, во многих случаях эти законы удобны для практического применения.
Если бы существовал газ, для которого не было бы отклонений от этих законов, то такой газ был бы идеальным газом.
При каком условии справедлив закон бойля мариотта
| Законы идеальных газов |   |
| В XVII – XIX веках были сформулированы опытные законы идеальных газов. Кратко напомним их. Изопроцессы идеального газа – процессы, при которых один из параметров остаётся неизменным. 1. Изохорический процесс. Закон Шарля. V = const. Изохорическим процессом называется процесс, протекающий при постоянном объёме V. Поведение газа при этом изохорическом процессе подчиняется закону Шарля: При постоянном объёме и неизменных значениях массы газа и его молярной массы, отношение давления газа к его абсолютной температуре остаётся постоянным: P/Т = const. График изохорического процесса на РV-диаграмме называется изохорой. Полезно знать график изохорического процесса на РТ— и VT-диаграммах (рис. 1.6). Уравнение изохоры: Изобарическим процессом называется процесс, протекающий при постоянном давлении Р. Поведение газа при изобарическом процессе подчиняется закону Гей-Люссака: При постоянном давлении и неизменных значениях массы и газа и его молярной массы, отношение объёма газа к его абсолютной температуре остаётся постоянным: V/T = const. График изобарического процесса на VT-диаграмме называется изобарой. Полезно знать графики изобарического процесса на РV— и РT-диаграммах (рис. 1.8). Изотермическим процессом называется процесс, протекающий при постоянной температуре Т. Поведение идеального газа при изотермическом процессе подчиняется закону Бойля – Мариотта: При постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV = const. График изотермического процесса на РV-диаграмме называется изотермой. Полезно знать графики изотермического процесса на VT— и РT-диаграммах (рис. 1.10). Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой. 5. Политропический процесс. Процесс, при котором теплоёмкость газа остаётся постоянной. Политропический процесс – общий случай всех перечисленных выше процессов. 6. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится одинаковое число молекул. В одном моле различных веществ содержится NA=6,02·10 23 молекул (число Авогадро). 7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов: При В соответствии с законами Бойля – Мариотта (1.4.5) и Гей-Люссака (1.4.3) можно сделать заключение, что для данной массы газа |


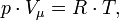
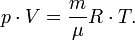
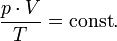
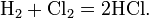
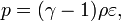


 , давление смеси газов:
, давление смеси газов:


