Изопроцессы в газах.
Изопроцессами называются процессы, протекающие при неизменном значении одного из параметров: давления (p), объема (V), температуры (T).
В идеальном газе эти процессы подчиняются газовым законам.
Газовыми законами называются количественные зависимости между двумя параметрами газа при фиксированном значении третьего параметра.
Изобарный процесс.
Изобарный (или изобарический) процесс — это изменение термодинамической системы с условием не изменения давления (P = const). Изобарой называют линию, которая отображает изобарический процесс на графике. Этот процесс описывает закон Гей-Люссака.
Изохорный процесс.
Изохорный (или изохорический) процесс — это изменение термодинамической системы с условием не изменения объема (V = const). Изохорой называют линию, которая отображает изохорический процесс на графике. Этот процесс описывает закон Шарля.
Изотермический процесс.
Изотермический процесс — это изменение термодинамической системы с условием не изменения температуры (T = const). Изотермой называют линию, которая отображает изотермический процесс на графике. Этот процесс описывает закон Бойля-Мариотта.
Изоэнтропийный процесс.
Изоэнтропийный процесс — это изменение термодинамической системы с условием не изменения энтропии (S = const). Изоэнтропийным является, например, обратимый адиабатический процесс: в таком процессе не происходит теплообмена с окружающей средой. Идеальный газ в таком процессе описывается следующим уравнением:
где γ — показатель адиабаты, определяемый типом газа.
Первый закон термодинамики.
Первое начало (первый закон) термодинамики — это закон сохранения и превращения энергии для термодинамической системы.
Согласно первому началу термодинамики, работа может совершаться только за счет теплоты или какой-либо другой формы энергии. Следовательно, работу и количество теплоты измеряют в одних единицах — джоулях (как и энергию).
Первое начало термодинамики было сформулировано немецким ученым Ю. Л. Манером в 1842 г. и подтверждено экспериментально английским ученым Дж. Джоулем в 1843 г.
Первый закон термодинамики формулируется так:
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
где ΔU — изменение внутренней энергии, A — работа внешних сил, Q — количество теплоты, переданной системе.
При любых процессах, происходящих в изолированной системе, ее внутренняя энергия остается постоянной.
Если работу совершает система, а не внешние силы, то уравнение (ΔU = A + Q) записывается в виде:

Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Первое начало термодинамики может быть сформулировано как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника (т. е. только за счет внутренней энергии).
Следует помнить, что как работа, так и количество теплоты, являются характеристиками процесса изменения внутренней энергии, поэтому нельзя говорить, что в системе содержится определенное количество теплоты или работы. Система в любом состоянии обладает лишь определенной внутренней энергией.
Рассмотрим применение первого закона термодинамики к различным термодинамическим процессам.
Изохорный процесс.
Зависимость р(Т) на термодинамической диаграмме изображается изохорой.
Изохорный (изохорический) процесс — термодинамический процесс, происходящий в системе при постоянном объеме.
Изохорный процесс можно осуществить в газах и жидкостях, заключенных в сосуд с постоянным объемом.
При изохорном процессе объем газа не меняется (ΔV= 0), и, согласно первому началу термодинамики 
т. е. изменение внутренней энергии равно количеству переданного тепла, т. к. работа (А = рΔV=0) газом не совершается.
График изотермического процесса. Основные термодинамические процессы
Главным предметом изучения термодинамики газовых систем является изменение термодинамических состояний. В результате таких изменений газ может совершать работу и запасать внутреннюю энергию. Изучим в приведенной ниже статье разные термодинамические переходы в идеальном газе. Особое внимание будет уделено изучению графика изотермического процесса.
Идеальные газы
Уже судя по самому названию, можно сказать, что 100-процентных идеальных газов в природе не существует. Однако многие реальные вещества удовлетворяют этой концепции с приемлемой для практики точностью.

Идеальным называется любой газ, в котором можно пренебречь взаимодействиями между его частицами и их размерами. Оба условия удовлетворяются только в том случае, если кинетическая энергия молекул будет намного превышать потенциальную энергию связей между ними, а расстояния между молекулами будут намного больше размеров частиц.
Чтобы определить, является ли изучаемый газ идеальным, можно воспользоваться простым эмпирическим правилом: если температура в системе выше комнатной, давление не сильно отличается от атмосферного или меньше него, а составляющие систему молекулы являются химически инертными, то газ будет идеальным.
Главный закон
Речь идет об уравнении идеального газа, которое также называется законом Клапейрона-Менделеева. Записано это уравнение было в 30-е годы XIX века французским инженером и физиком Эмилем Клапейроном. Спустя несколько десятилетий оно было приведено русским химиком Менделеевым к современному виду. Это уравнение имеет следующий вид:
Закон Клапейрона-Менделеева впервые был получен из результатов предыдущих газовых законов, то есть в его основе лежала исключительно экспериментальная база. С развитием современной физики и кинетической теории текучих сред уравнение идеального газа может быть выведено из рассмотрения микроскопического поведения частиц системы.
Изотермический процесс
Касательно газа идеального отметим, что изотермический переход для него называется законом Бойля-Мариотта. Обнаружен этот закон был экспериментальным путем. Причем он стал первым в этой области (вторая половина XVII века). Его может получить каждый школьник, если рассмотрит поведение газа в закрытой системе (n = const) при постоянной температуре (T = const). Пользуясь уравнением состояния, получаем:
Последнее равенство представляет собой закон Бойля-Мариотта. В учебниках по физике можно также встретить такую форму его записи:
При переходе из изотермического состояния 1 в термодинамическое 2 произведение объема на давление остается постоянным для закрытой газовой системы.
Изучаемый закон говорит об обратной пропорциональности между величинами P и V:
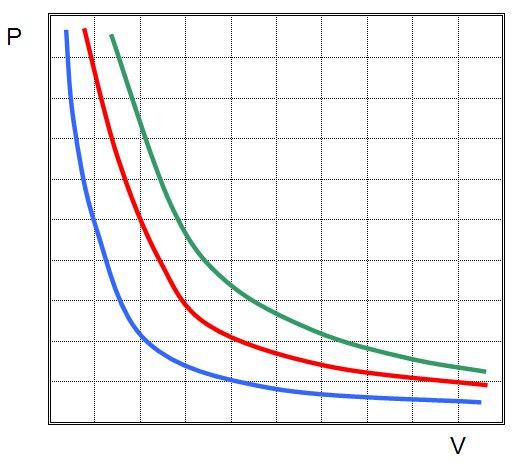
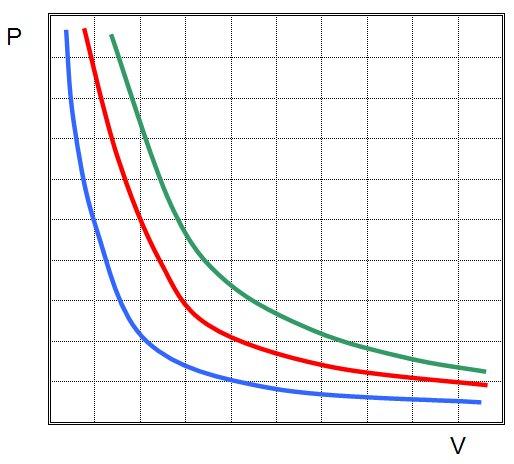
Это означает, что графиком изотермического процесса в идеальном газе будет кривая гипербола. Три гиперболы изображены на рисунке ниже.
Изменение внутренней энергии при изотермическом процессе
В физике идеальных газов под внутренней энергией понимают энергию кинетическую, связанную с вращательным и поступательным движением молекул. Из кинетической теории несложно получить следующую формулу для внутренней энергии U:
В случае процесса изотермического температура остается постоянной, значит, единственной причиной изменения внутренней энергии является выход или приход в систему частиц вещества. Таким образом, в закрытых системах во время изотермического изменения их состояния внутренняя энергия сохраняется.
Изобарный и изохорный процессы
Помимо закона Бойля-Мариотта, существуют еще два основных газовых закона, которые также были открыты экспериментальным путем. Они носят фамилии французов Шарля и Гей-Люссака. Математически их записывают так:
V / T = const при P = const;
P / T = const при V = const.
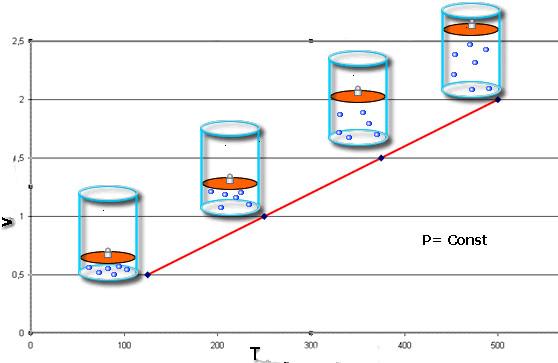
Закон Шарля говорит о том, что во время изобарного процесса (P = const) объем линейно зависит от абсолютной температуры. Закон Гей-Люссака свидетельствует о линейной зависимости между давлением и абсолютной температурой при изохорном переходе (V = const).
Из приведенных равенств следует, что от процесса изотермического графики изобарного и изохорного переходов отличаются существенным образом. Если изотерма имеет форму гиперболы, то изобара и изохора являются прямыми линиями.
Изобарно-изотермический процесс
Рассматривая газовые законы, иногда забывают, что, помимо величин T, P и V, также может изменяться и величина n в законе Клапейрона-Менделеева. Если зафиксировать давление и температуру, то мы получим уравнение изобарно-изотермического перехода:
n / V = const при T = const, P = const.
Линейная зависимость между количеством вещества и объемом говорит о том, что при одинаковых условиях разные газы, содержащие одно и то же количество вещества, занимают равные объемы. Например, при нормальных условиях (0 oC, 1 атмосфера) молярный объем любого газа составляет 22,4 литра. Рассмотренный закон называется принципом Авогадро. Он лежит в основе закона Дальтона об идеальных газовых смесях.
Термодинамическая система
Системой в термодинамике принято называть некоторую совокупность составляющих ее элементов, которые могут обмениваться между собой энергией. Как правило, этими элементами являются атомы и молекулы. Система находится в термодинамическом равновесии, когда все ее макроскопические характеристики не меняются во времени.

Системы бывают открытые, закрытые и изолированные. В открытых происходит обмен энергией и веществом с внешней средой, в закрытых системах возможен только обмен энергией с окружающей средой. Наконец, изолированные системы полностью предоставлены самим себе. Их энергия и количество вещества сохраняются с течением времени.
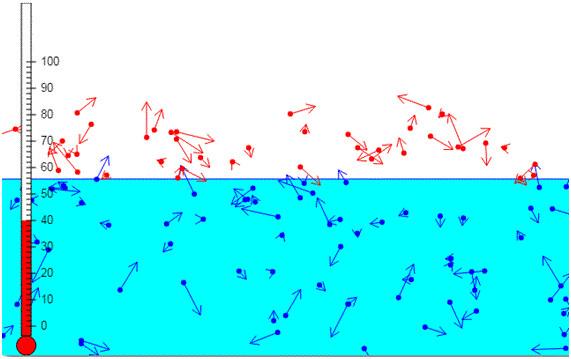
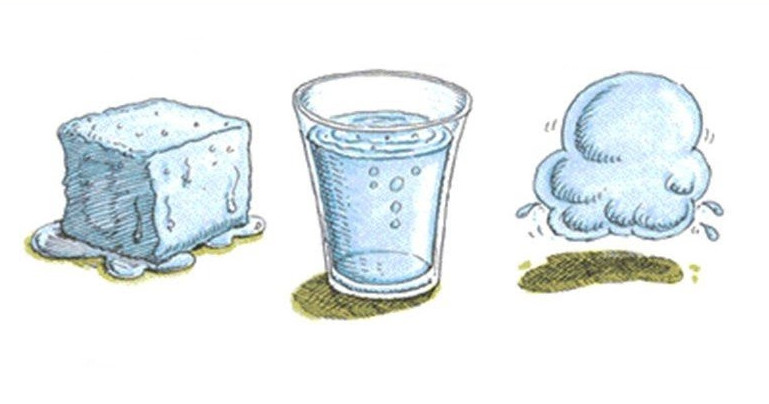
Отметим, что понятие термодинамической системы не связано с агрегатным состоянием материи. Так, вода и водяной пар в закрытом сосуде или лед, плавающий в стакане с водой, являются примерами термодинамических систем, в которых в равновесии одновременно находятся два агрегатных состояния одного и того же химического вещества.
Термодинамические параметры

Рассмотрим каждый из них подробнее в статье.
Закон Бойля-Мариотта
Во второй половине XVII века англичанин Роберт Бойль и француз Эдм Мариотт независимо друг от друга экспериментально установили следующее отношение для газовых систем:
В экспериментах они использовали разные газы. При этом произведение давления на объем всегда оставалось постоянным. Это уравнение называется законом Бойля-Мариотта. Графически функция P(V) представляет собой гиперболическую зависимость.
Мы только что рассмотрели изотермический процесс в идеальном газе. Понять выражение выше несложно, если вспомнить, как выглядит универсальное уравнение состояния для газовой системы:
Принцип Авогадро
В 1810 году, экспериментируя с разными газами, Амедео Авогадро пришел к удивительному выводу. Оказалось, что занимаемый газом объем является функцией только количества вещества при определенном давлении и температуре. Не важно, из каких молекул и атомов состоит газовая система, 1 моль любого газа всегда занимает один и тот же объем, если P=const и T=const.
Понять изложенный принцип не сложно, если обратиться снова к универсальному уравнению для идеального газа. Имеем:
V/n = R*T/P = const при P=const, T=const
Рассмотренный процесс является изобарно-изотермическим.
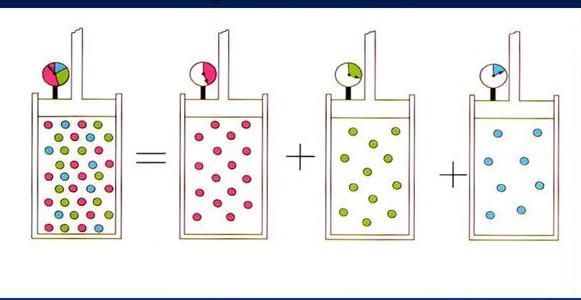
Принцип Авогадро положен в основу закона Дальтона. Если проводить смешение двух идеальных газов при постоянной температуре в сосуде с некоторым фиксированным объемом, то абсолютное давление в системе будет равно сумме парциальных давлений каждого компонента. В свою очередь парциальное давление компонента прямо пропорционально атомной доле его частиц в смеси:
P = ∑i=1m(Pi) = R*T/V*∑i=1m(ni)
Переход между агрегатными состояниями вещества
Речь идет о процессах плавления твердого тела или кристаллизации жидкости, о процессах кипения жидкости или конденсации газа. Все эти переходы происходят либо с выделением, либо с поглощением тепла. Так, в результате кристаллизации молекулы жидкости теряют энергию, выделяя ее в окружающую среду. Последнее приводит к уменьшению кинетической энергии молекул и формированию из них определенной структуры (аморфной, кристаллической). Наоборот, плавление является эндотермическим процессом, то есть он идет с поглощением теплоты. Эта теплота расходуется на разрушение химических связей между молекулами и атомами в твердом теле.
Определение теплового эффекта перехода между агрегатными состояниями
Все термодинамические расчеты процессов кристаллизации, плавления, конденсации и кипения проводятся с использованием следующей формулы:
Изотермический процесс
Из Википедии — свободной энциклопедии
Изотермический [1] или изотермный [2] процесс (от др.-греч. ἴσος «равный» и θέρμη «жар») — термодинамический изопроцесс, происходящий в физической системе при постоянной температуре.
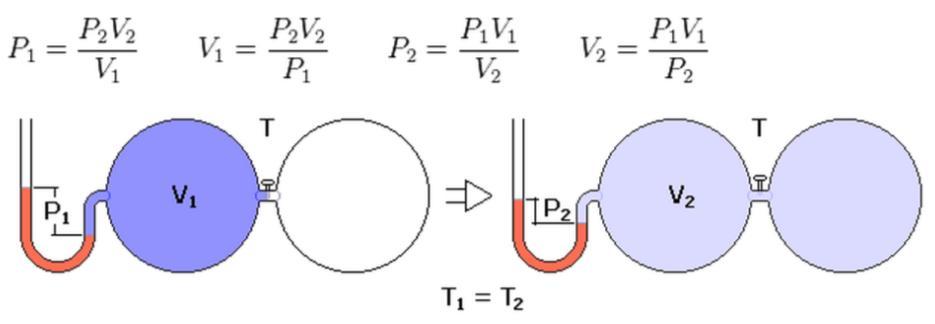
В идеальном газе при изотермическом процессе для неизменной массы газа произведение давления на объём постоянно (закон Бойля-Мариотта):
откуда при изменении объёма или давления, имеем:
P 1 ∗ V 1 = P 2 ∗ V 2 <\displaystyle P_<1>*V_<1>=P_<2>*V_<2>>
В твёрдом теле и большинстве жидкостей изотермические процессы очень мало изменяют объём тела, если только не происходит фазовый переход.
Первый закон термодинамики для изотермического процесса записывается в виде:
где учитывается, что внутренняя энергия системы в изотермическом процессе не изменяется. Таким образом, в изотермическом процессе вся теплота, полученная системой, расходуется на совершение системой работы над внешними телами.