какой металл не относится к группе платиновых
Платина, палладий или родий — во что лучше вложиться и как это сделать
При упоминании слова «платиноиды» в голову приходит платина — драгоценный металл, самый дорогой в ювелирных магазинах. На самом деле семейство платиноидов более разнообразно, и платина в нем сейчас занимает далеко не самое почетное место. Мало того, что она дешевле золота, но еще и сильно дешевле других металлов той же группы — палладия и родия. Чем эти материалы заслужили благосклонность потребителей и инвесторов, которая позволила им вырасти в цене в 5–15 раз за последние пять лет?
Спрос на палладий и родий
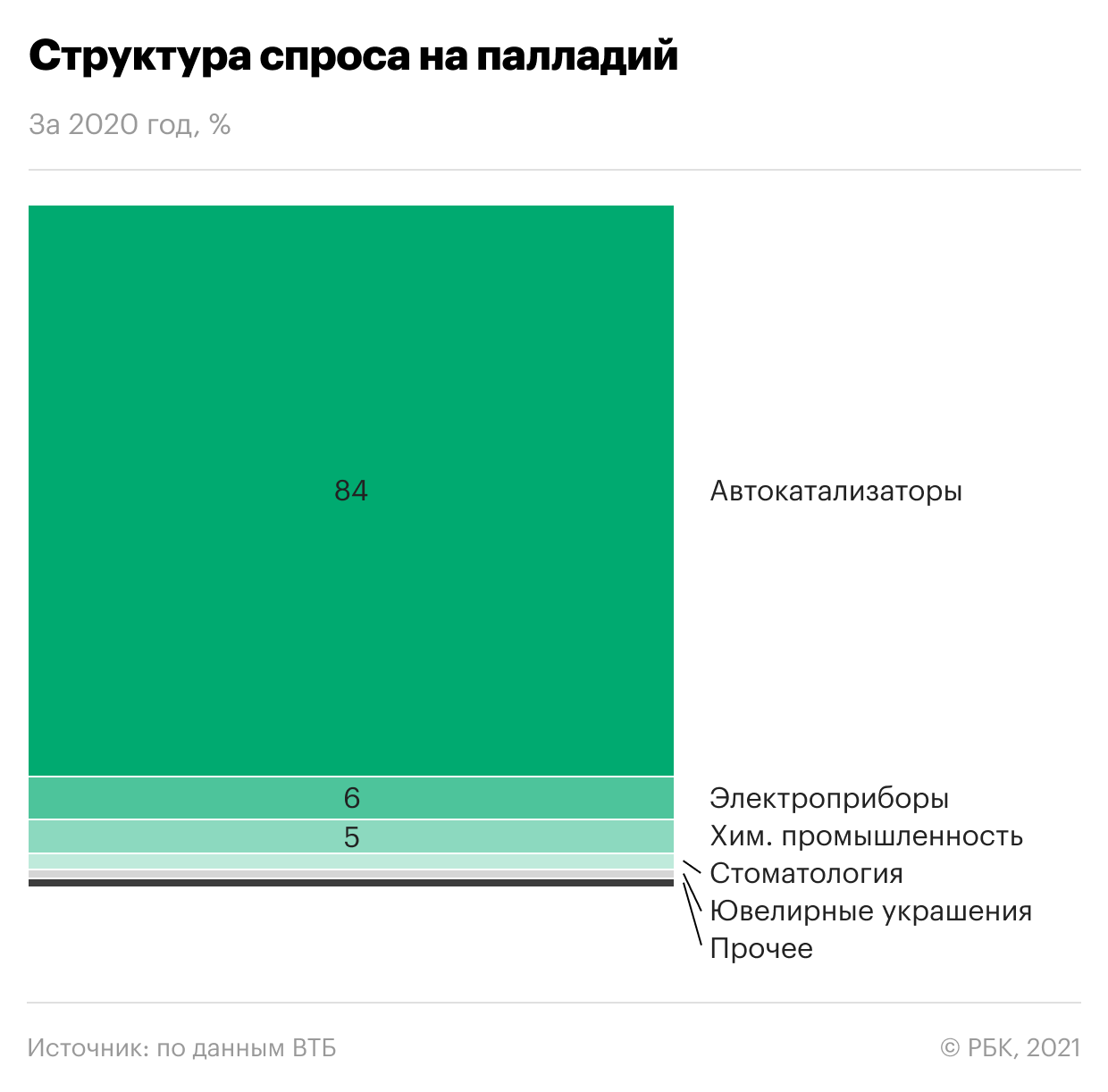
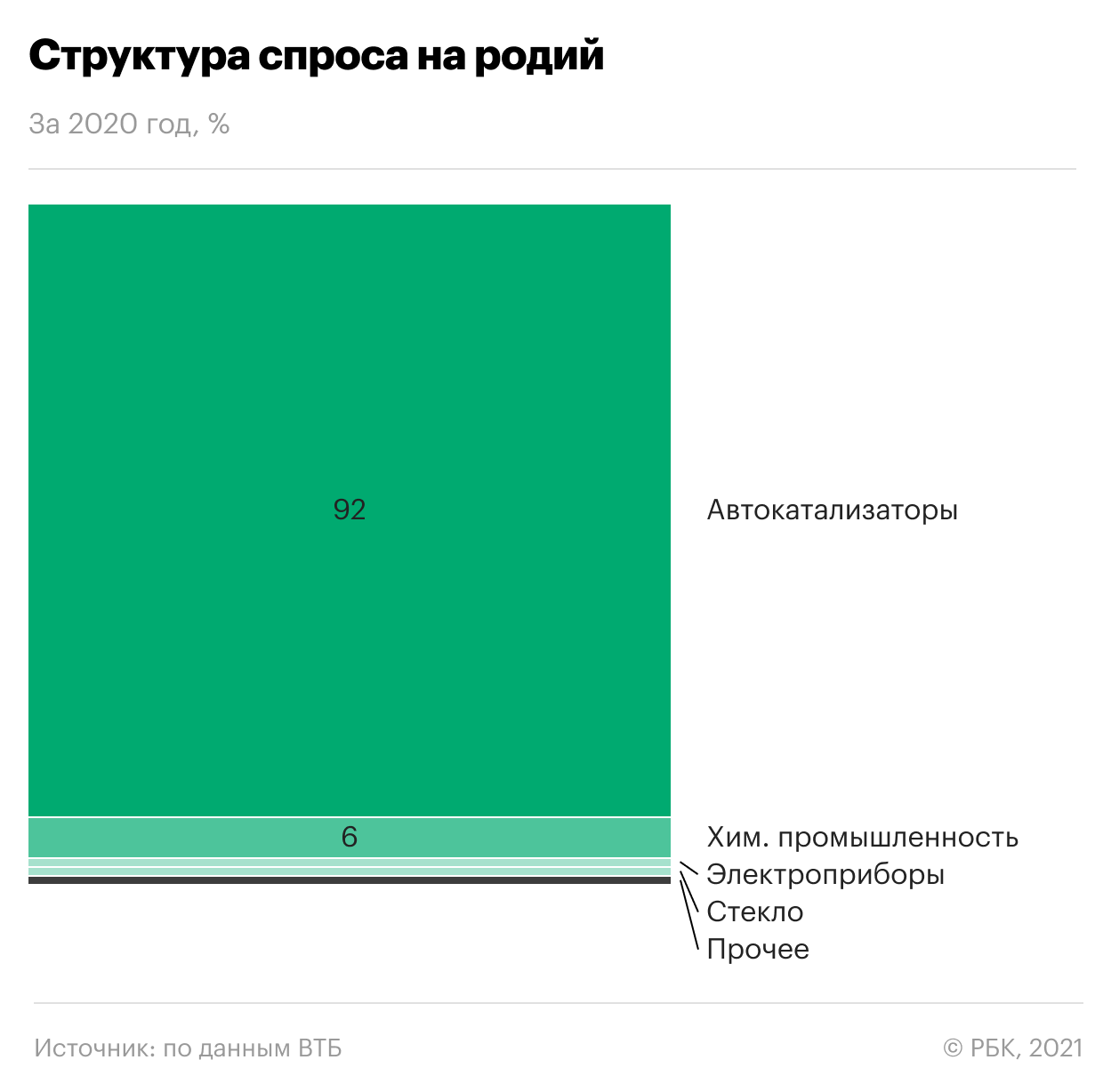
Хотя формально палладий и родий являются драгметаллами, по факту они уже давно стали индустриальными металлами, ведь больше 85% их потребления приходится на нужды автомобильной промышленности. Этот сдвиг произошел за последние десять лет, когда производители катализаторов для систем выхлопа автомобилей начали массово использовать эти два металла. Теперь практически в каждой выхлопной системе находится достаточно большое количество родия и палладия, которые отвечают за улавливание выходящих из двигателя и загрязняющих окружающий мир веществ, продуктов горения.
В последнее время во всем мире идет беспощадная борьба за очищение городского воздуха. Все регуляторы с каждым годом ужесточают требования по количеству выбросов загрязняющих элементов из автомобилей. Так появляются стандарты Euro-5, Euro-6, China-5, China-6 и прочие, которые обновляются в разных регионах с разной периодичностью, но требуют с каждым разом все более строгого контроля за выбросами.
Для производителей автомобилей это означает, что нужно добавлять все больше палладия и родия в выхлопные системы. Этим и объясняется такой растущий интерес к данным металлам, которые больше почти нигде не используются. При этом их производство практически не росло в последние годы, а исторические запасы в России и Швейцарии подошли к концу, что и привело к взлету цен.
Основной риск для спроса на палладий — это, как ни странно, действия все тех же регуляторов, но уже в борьбе с изменением климата. В соответствии с Парижским соглашением все страны мира должны существенно сократить выбросы парниковых газов, в первую очередь углекислого газа (CO 2 ), а автомобили с двигателями внутреннего сгорания являются одним из крупнейших источников выбросов. Основным способом сократить выбросы видится повсеместная замена автомобилей с двигателями внутреннего сгорания (ДВС) на автомобили с электродвигателями. Регуляторы всеми правдами и неправдами стараются сделать автомобили с ДВС более дорогими, а электромобили — более дешевыми для потребителей.
В России, например, отсутствует импортная пошлина на электромобили, владельцы не платят налоги за свои электрокары, а парковка в Москве для них бесплатна, не говоря уже о том, что электричество дешевле бензина. В итоге рост рынка электромобилей во всем мире идет опережающими темпами, происходит это за счет сокращения рынка классических.
По нашим прогнозам, рынок авто с ДВС (как и спрос на палладий и родий) перестанет расти с 2024 года, а с 2025 года начнет постепенно снижаться. Производство электромобилей растет со средним темпом 50% в год последние пять лет, и в 2020 году продажи электромобилей составили 3% от общих продаж. Но если такие темпы сохранятся, то уже в 2025 году их доля вырастет до 15–20%, а количество проданных авто с ДВС начнет сокращаться, что в свою очередь может повлечь и снижение спроса на палладий и родий.
Спрос на платину
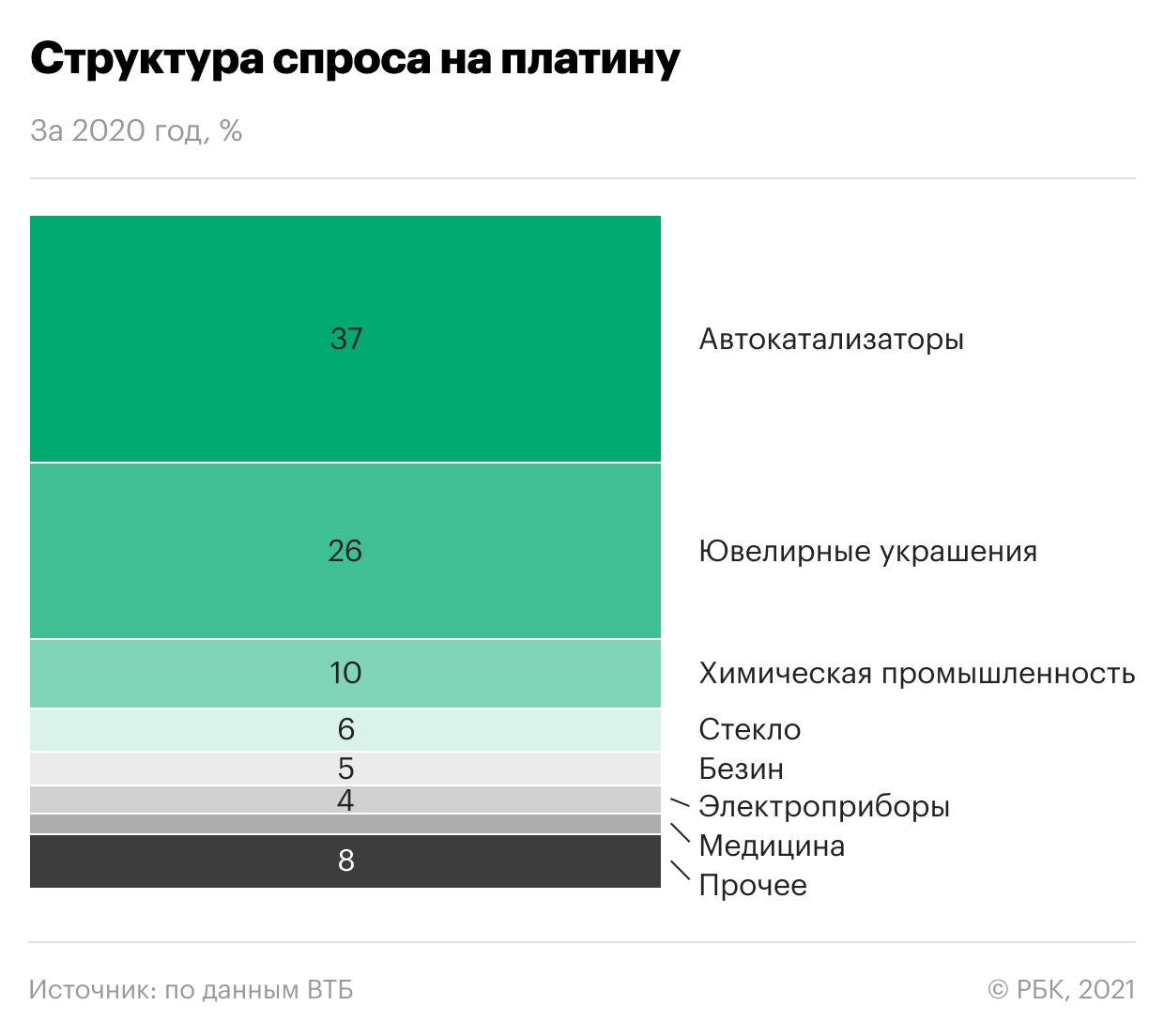
С платиной ситуация не столь очевидная. Структура спроса достаточно диверсифицирована, и на автокатализаторы приходится только порядка 40%, в то время как на ювелирные украшения — 30%, а оставшиеся 30% поделены между применениями в химической, стекольной, электротехнической, топливной промышленности и медицине.
Катализаторы на основе платины активно используются в дизельных автомобилях (палладий и родий — в бензиновых), и после «дизельгейта», произошедшего пять лет назад, производство дизельных автомобилей в мире и, как следствие, потребление платины в автокатализаторах сократилось на 25%. Именно это и привело к тому, что цена на платину с тех пор упала, в то время как цены на родий и палладий выросли в несколько раз. При этом запасы платины в мире, по разным источникам, составляют от шести месяцев до двух лет мирового потребления, поэтому какого-то критического дефицита в ближайшие годы не ожидается. Из потенциальных темных лошадок для спроса на платину можно упомянуть водородные двигатели, еще одного конкурента двигателей с ДВС.
Технология водородных двигателей (fuel cells) развивается параллельно с электромобилями и также позволяет сильно снизить выбросы вредных веществ и парниковых газов при использовании автомобиля. В перспективе эта технология может стать большим потребителем платины, которая активно в ней используется. Пока темпы роста производства таких автомобилей сильно отстают от темпа роста производства электромобилей, но оба рынка на данный момент очень малы относительно рынка автомобилей с двигателями внутреннего сгорания, поэтому делать выводы относительно того, какая технология победит, преждевременно.
Планы основных регионов выглядят агрессивно: в ЕС — 5 млн машин с водородными двигателями к 2030 году (сейчас 1400), в Китае и США — по 1 млн автомобилей к 2030-му. Но пока выглядит так, что электромобили победят, и большинство усилий государств приходится сейчас именно на развитие инфраструктуры под электромобили, а инвестировать параллельно в инфраструктуру под водородные двигатели никто не будет.
Производство платиноидов
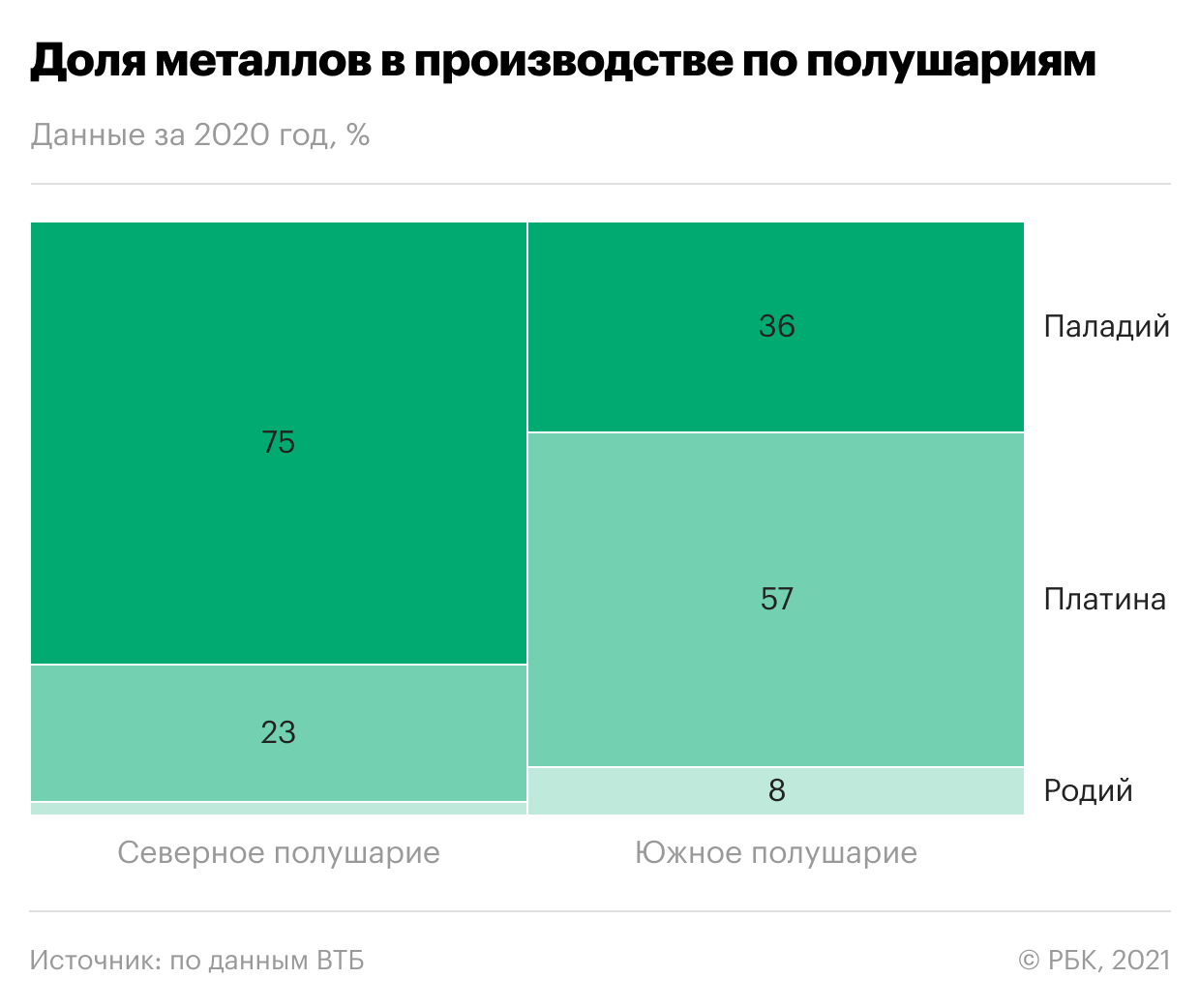
С точки зрения производства платиноидов ситуация очень простая, ведь мировое производство сконцентрировано в нескольких ключевых регионах. Южная Африка производит 50% мировых платиноидов. «Норильский никель» — 30%, а остальное производство разделено в основном между Зимбабве и Северной Америкой. При этом в южном полушарии в производстве превалируют платина и родий, а большая часть палладия приходит из северного полушария и 40% мирового палладия производит «Норникель». Инвестиции в рост производства в последние десять лет были минимальными из-за низких цен на металлы, поэтому производство в мире остановилось, а в Южной Африке даже сокращалось.
Металлы платиновой группы
СВОЙСТВА И ПРИМЕНЕНИЕ ПЛАТИНОВЫХ МЕТАЛЛОВ
Платина (Pt) открыта в 1783 г. Название элемента происходит от испанского слова «плата» — серебрецо, серебряный за внешнее сходство с серебром.
Палладий (Pd) открыт в 1803 г. и назван по имени малой планеты Паллада, обнаруженной за год до открытия элемента.
Родий (Rh) — металл серебристо-голубого цвета, напоминающий алюминий. Элемент открыт в 1803 г. Название его происходит от греческого слова «родос»— розовый (цвет за розовую окраску своих солей).
Осмий (Os) открыт в 1803 г. Название элемента происходит от греческого слова «осме» — пахнущий за резкий запах осмиевого ангидрида.
Рутений (Ru) — серебристо-белый металл, похожий на платину. Элемент открыт в 1884 г. русским химиком Клауссом и назван им в честь России, латинское название которой — Рутения.
Четыреххлористая платина при растворении в соляной кислоте образует платино- хлористоводородную кислоту. Соли этой кислоты — хлороплатинаты. Хлороплатинат аммония (NH4)2[PtCl6] мало растворим в водных растворах и очень малорастворим в растворах хлористого аммония, что имеет большое значение при аффинаже платиновых металлов. При диссоциации в результате термического разложения из хлор- платината удаляется хлористый аммоний и хлор в виде газов, а платина остается в виде металлической губки.
Палладий при растворении в царской водке образует хлористый палладий, который с соляной кислотой дает палладохло- ристоводородную кислоту H2PtCl6. Соль — хлорпалладозамин [Pd(NH3)2Cl2], которая
ТАБЛИЦА. ФИЗИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ ПЛАТИНОВОЙ ГРУППЫ
Плотность, кг/ м3 · 10-3
Теплота плавления, кал/г
Удельная теплоемкость при 20°С,Кал/(г*град)
Теплопроводность, кал/ (см · сек · град)
Удельное электросопротивление при 25°С, мком/см
Платина и палладий обладают хорошей пластичностью при комнатной температуре и легко обрабатываются давлением, пластичность их сохраняется при высоких степенях обжатия. Иридий и родий непластичны при комнатной температуре и могут быть прокатаны и протянуты в проволоку лишь при 1200—1400°С. Рутений и осмий непластичны даже при 1500°С.
Платина, так же как золото и серебро, не окисляется на воздухе даже при плавлении; осмий и рутений при нагревании на воздухе легко окисляются. Иридий, палладий и родий при нагревании на воздухе также окисляются, но в меньшей степени, чем осмий и рутений.
Иридий, рутений и родий не растворяются в кислотах и в кипящей царской водке. Платина устойчива в кислотах, но растворяется в царской водке. Палладий корродирует под действием горячих азотной, соляной и серной кислот. При нагревании металлы платиновой группы образуют хрупкие сплавы с углеродом.
На платину воздействуют расплавленные едкие щелочи и фосфор. С серой платина образует сернистую и двусернистую платину— PtS и PtS2. С хлором платина образует четыреххлористую платину PtCl4, устойчивую до 370°С. При более высокой температуре она переходит в PtCl3, а нагревание до 435°С приводит к образованию хлористой платины PtCl2. При температурах >582°С двухвалентная платина разлагается с выделением металлической платины· PtCl2-*»Pt+Cl2.
получается после последовательной обработки палладохлористоводородной кислоты и образующихся при этом соединений, имеет малую растворимость и поэтому используется для выделения палладия из растворов. При термическом разложении хлорпалладоза(М1ин диссоциирует, при этом хлористый аммоний и хлористый водород удаляются в газовую фазу, а палладий остается в виде металлической губки.
Иридий при температурах красного каления взаимодействует с хлором, в результате чего получается хлорный и хлористый иридий — 1гС14 и 1гС13. Этим соединениям соответствуют иридиевохлористоводородная кислота Н21гС16 и иридистохлористоводо- родная кислота Н31гС1б. При добавлении к раствору Н21гС1б избытка хлористого аммония выпадает хлороиридат аммония (NH4)2IrCl6, который имеет незначительную растворимость в растворах хлористого аммония. Это используют при разделении платиновых металлов. Хлороиридат аммония при обработке сернистым водородом, щавелевой кислотой и другими восстановителями переходит в хлороиридит, что позволяет отделить иридий от платины, которая не образует подобного типа соединений.
Осмий при сплавлении его со смесью щелочи и перекиси натрия или бария образует сплав, растворяющийся в воде. При обработке этого раствора спиртом образуется осминат натрия Na2[OsC4].
При восстановлении гипосульфитом раствора осмии а та натрия и обработкой хлористым аммонием получают осмилтетрамиихлорид [0s02(NH3)4]Cl2, который является исходным соединением для получения порошка осмия.
В тонкоизмельченном состоянии осмий при прокаливании в атмосфере воздуха образует четырехокись осмия 0s04, которая испаряется при 120°С и обладает специфическим запахом. Водородом она восстанавливается до двуокиси ОэОг.
Рутений с кислородом образует летучую четырехокись Ru04, которая имеет едкий запах и испаряется при 65°С. Четырехокись рутения —сильный окислитель и при соприкосновении с концентрированным аммиаком или спиртом восстанавливается с сильным взрывом. При растворении Ru04 в соляной кислоте и воздействии на раствор хлористого калия получают легко растворимую соль хлористого рутения K2[RuC15OH]. Из растворов этой соли при действии хлористого аммиака или калия выпадают малорастворимые гексахлорорутенаты (ЫН4)г [RuCls], K2[RuC16].
Металлы платиновой группы находят самое широкое применение в технике и промышленности.
Платину применяют для изготовления лабораторной посуды и аппаратуры для химических Лабораторий, в качестве нерастворимых анодов в производстве перекиси водорода, перхлоратов ή др., в качестве защитного покрытия для плакировки реакторов, используемых в производстве особо чистых продуктов, при переработке фторсодержащих материалов, в пищевой промышленности. Платиновые катализаторы используют в основной химии для реакций гидрогенизации и дегидрогенизации, восстановления нитросоединений и галоидных соединений, в производстве серной кислоты контактным способом, при получении синильной кислоты, а также в процессах пиролиза газообразных углеводородов, каталитической полимеризации, гидрогенизации, алкилировавния, крекинг- и реформинг-процессов очистки от серы.
В производстве аммиака и азотной кислоты применяют катализаторные сетки, изготовленные из сплавов платины с родием и палладием, а в производстве синильной кислоты — сетки из сплава платины с родием. При гидрировании целлюлозы или полисахаридов в качестве катализатора применяют рутений, а при гидрировании некоторых органических соединений — осмий. Палладиевые покрытия применяют для изготовления сосудов для перегонки плавиковой кислоты.
Платину, платиновые металлы и их сплавы широко используют при изготовлении кантактов, катодов и антикатодов рентгеновских трубок, электросопротивлений, плавких предохранителей, деталей астрономических приборов, аппаратуры связи, термопар.
Высокую отражательную способность родия используют для покрытия рефлекторов. Рутениевые покрытия, нанесенные на вольфрамовые нити, значительно увеличивают срок их службы. Рутений применяют также в приборостроении при изготовлении деталей, требующих высокой прочности. Сплав палладия с 18% 1г обладает большой упругостью, поэтому из него в авиационном приборостроении изготовляют пружинящие контакты. Сплавы осмия с иридием используют в приборостроении для изготовления некоторых деталей морских точных приборов. Мощные постоянные магниты делают из магнитного сплава платина- кобальт.
Какой металл не относится к группе платиновых
Металлы платиновой группы (МПГ, Платиновая группа, Платиновые металлы, Платиноиды) — коллективное обозначение шести переходных металлических элементов (рутений, родий, палладий, осмий, иридий, платина), имеющих схожие физические и химические свойства, и, как правило, встречающихся в одних и тех же месторождениях. В связи с этим, имеют схожую историю открытия и изучения, добычу, производство и применение. Металлы платиновой группы являются благородными и драгоценными металлами. В природе, чаще всего встречаются, в полиметаллических (медно-никелевых) рудах, а также в месторождениях золота и платины. Иногда, металлы платиновой группы подразделяют на две триады:
рутений, родий и палладий — лёгкие платиновые металлы, а
платина, иридий и осмий — тяжёлые платиновые металлы.
Платина и металлы её группы встречаются в природе в весьма рассеянном состоянии. Геохимически все эти элементы связаны с ультраосновными и основными породами. Известно около полусотни минералов платиновой группы. Платина, иридий, палладий в горных породах и месторождениях развиты как в самородном виде, так и в виде твёрдых растворов и интерметаллических соединений с Fe, Ni, Cu, Sn, реже Au, Os, Pb, Zn, Ag.
Генетические группы и промышленные типы месторождений
1. Магматические
а. хромит-платиновые месторождения (уральский тип)
б. месторождения комплексных платина-хромит-медно-никелевых руд (бушвельдский тип)
в. ликвационные медь-никель-платиновые месторождения (норильский тип)
2. Гидротермальные
3. Россыпи
Все платиновые металлы светло-серые и тугоплавкие, платина и палладий пластичны, осмий и рутений хрупкие. Красивый внешний вид благородных металлов обусловлен их инертностью.
Платиновые металлы обладают высокой каталитической активностью в реакциях гидрирования, что обусловлено высокой растворимостью в них водорода. Палладий способен растворить до 800—900 объёмов водорода, платина — до 100.
Все платиновые металлы химически довольно инертны, особенно платина. Они растворяются лишь в «царской водке» с образованием хлоридных комплексов:
Промышленное производство платины первоначально велось в Америке. Лишь в 1819 году платиновые россыпи были впервые обнаружены на Урале близ Екатеринбурга. С тех пор Россия становится ведущим производителем платины, а, с момента открытия, и платиноидов.
В настоящее время, почти 90 % всего объема производства металлов платиновой группы разделено между платиной и палладием, остальные добываются и продаются в небольших количествах.
95 % запасов и 90 % производства МПГ сосредоточены в двух крупных месторождениях —
Бушвельдском комплексе, находящемся на территории Южно-Африканской Республики, и в
Норильском рудном районе, расположенном в России.
В рудах Бушвельда содержание платины втрое выше, чем палладия,
в то время как в Норильске наблюдается обратное соотношение.
Поэтому, ЮАР является крупнейшим мировым производителем платины, а Россия — палладия.
Запасы
Содержание платиновых металлов в земной коре (кларк) оценивается, как 10−8 % для платины, 10−9 % для палладия и 10−11 % для остальных платиновых металлов.
Общие запасы металлов платиновой группы на начало 2009 года оцениваются в 100 млн кг.
Причем распределены они, также неравномерно:
ЮАР (63,00 млн кг разведанных запасов при 70,00 млн кг общих),
Россия (6,20/6,60),
США (0,90/2,00),
Канада (0,31/0,39).
В России почти вся добыча металлов платиновой группы целиком сосредоточена в рамках «Норильского никеля» (15 % мирового производства платины и 55 % производства палладия).
С середины 1970−х годов главной сферой применения платины и палладия стала автомобильная промышленность.
В электротехнической промышленности из металлов платиновой группы изготовляют контакты с большой степенью надёжности (стойкость против коррозии, устойчивость к действию образующейся на контактах кратковременной электрической дуги).
В технике слабых токов при малых напряжениях в цепях используются контакты из сплавов золота с платиной, золота с серебром и платиной. Для слаботочной и средненагруженной аппаратуры связи широко применяют сплавы палладия с серебром (от 60 до 5 % палладия).Магнитные сплавы металлов платиновой группы с высокой коэрцитивной силой употребляют при изготовлении малогабаритных электроприборов. Сопротивления (потенциометры) для автоматических приборов и тензометров делают из сплавов металлов платиновой группы (главным образом палладия с серебром, реже с другими металлами). У них малый температурный коэффициент электрического сопротивления, малая термоэлектродвижущая сила в паре с медью, высокое сопротивление износу, высокая температура плавления, они не окисляются.
Металлы платиновой группы идут на изготовление деталей, работающих в агрессивных средах — технологические аппараты, реакторы, электрические нагреватели, высокотемпературные печи, аппаратуру для производства оптического стекла и стекловолокна, термопары, эталоны сопротивления и др.
При изготовлении инструментов металлы платиновой группы позволяют получить уникальные свойства по прочности, корозостойкости и долговечности.
Металлы платиновой группы используются в чистом виде, как биметалл и в сплавах (см. Платиновые сплавы). Химические реакторы и их части делают целиком или только покрывают фольгой из металлов платиновой группы. Покрытые платиной аппараты применяют при изготовлении чистых химических препаратов и в пищевой промышленности. Когда химической стойкости и тугоплавкости платины или палладия недостаточно, их заменяют сплавами платины с металлами, повышающими эти свойства: иридием (5-25 %), родием (3-10 %) и рутением (2-10 %). Примером использования металлов платиновой группы в этих областях техники является изготовление котлов и чаш для плавки щелочей или работы с соляной, уксусной и бензойной кислотами; автоклавов, дистилляторов, колб, мешалок и др.
Сплавы иридия с осмием, а также золота с платиной и палладием используют для изготовления компасных игл, напаек «вечных» перьев.
Высокие каталитические свойства некоторых металлов платиновой группы позволяют применять их в качестве катализаторов, например, платину применяют при производстве серной и азотной кислот.
Металлы платиновой группы (МПГ)
Металлы платиновой группы или платиноиды, представляют собой 6 драгоценных химических элементов, благородного вида. Они располагаются в периодической системе в один ряд и являются переходными металлами 8-10 групп 5-6 периода. Внешне металлы схожи друг с другом.
Главными особенностями металлов платиновой группы, являются:
Основными источниками платиновых металлов являются минералы редких элементов. Сегодня драгоценные платиновые металлы используют в ювелирном производстве, но в разной степени, а биологически активные соединения платиновых металлов в медицине.
Платина
Платина известна издревле, а название произошло с испанского языка: «маленькое серебро». Конкистадоры, это первые европейцы, которые познакомились с платиной в середине 16 века в Южной Америке. А в 1735 году король Испании издал указ, по которому следовало топить платину в реке и не ввозить в страну. Позже речку назвали Платино-дель-Пинто. Указ был отменен только через сорок лет, для фальсифицирования золотых и серебряных монет мадридскими властями. Позже с платиной познакомились алхимики, но посчитали ее непригодной. Но во Франции она все же нашла свое применение в виде эталона метра, а затем килограмма. В России металл назвали белым золотом, найдя его в россыпном золоте.
Платина, это один из редчайших металлов, ведь в земной коре ее содержания невелико. Главными месторождениями платины являются: Россия, США (2 крупных рудника: Stillwater, East Bouder), Китай, Зимбабве (9 тонн), ЮАР (Бушвельский комплекс).
В России данный металл МПГ обладает уникальной базой, с огромным количеством месторождений, основной из которых расположен в Зареченске (Мурманской области).
Добыча платины это трудоемкий процесс, двух видов:
Платина это драгоценный металл, который используют в ювелирном деле и промышленности. Свойства платины широки:
Область применения платины достаточно широкое и не ограничивается ювелирным производством, ведь она обладает уникальной красотой и благородством. В настоящее время рост на металл растет, так как используют ее и в промышленности. Итак, применения платины:
Палладий
На сегодня, палладий самый дорогой металл платиновой группы, который используется в промышленности.
Название металл получил в честь астероида. Этот металл платиновой группы встречается в природе очень редко в чистом в виде. А чаще в комплексе с другими металлами (золото, серебро, платина).
Добывают металл также двумя способами:
Главные месторождения палладия:
В России также происходит добыча палладия, сконцентрированная на Урале. Главными свойствами палладия являются:
Области применения палладия
Родий
Родий получил свое название с греческого языка: роза. Добыча родия производится вместе с платиной/золотом. Основными источниками родия являются золотые месторождения Мексики, залежи родиевого Невьянскита.
Родий представляет собой металл серебристо-белого оттенка и относится к благородным металлам платиновой группы.
Свойства родия
Так как родий, это драгоценный и уникальный металл, то и область его применения различна:
Рутений
Добыча рутения всегда сопровождает добычу платины на россыпных и коренных месторождениях. Присутствует в качестве примесей в составе никелевой руды, медной руды. Также существуют искусственные источники добычи рутения, т.е. отходы ядерной промышленности. Основное месторождение данного металла платиновой группы, это ЮАР, Канада, Россия, Зимбабве.
Основные характеристики рутения:
Область применения металла
Иридий
В начале 19 века химики были заинтересованы неочищенной платиной и всеми возможными элементами содержащиеся в ней. Тогда Дескотиль, Фуркруа и Вокелен стали изучать сырой металл, сплавив его с едким кали, получив частично растворимые в воде соединения неизвестных металлов. Теннант пошел этим же способом, и смог выделит два новых металла: иридий и осмий.
Иридий получил свое название с греческого: радуга, благодаря тому, что соединения данного металла были окрашены в разные цвета. Осмий же в связи с растворение щелочного сплава осмиридия в кислоте (или в воде) сопровождался сильным запахом. С греческого языка, получив название: запах.
Иридий очень редкий металл платиновой группы, который добыть практически невозможно. Добыча его сопровождается попутчиками: платиной или осмием и рутением или палладием. Он встречается в медных и никелевых рудах. Место добывания иридия: Канада (Британская Колумбия), США (Калифорния), ЮАР (Трансвааль), Остров Тасмания, Новая Гвинея, остров Калимантан.
Осмий
Чистого осмия в природе нет, он находится в комплексе с родием. Месторождения осмия сконцентрированы в: Африке (юг), Тасмании, Австралии, США, Канаде, Россие, Колумбия, ЮАР (самые большие запасы).
Область применения
Металлы платиновой группы, редкие и уникальные металлы, которые не так часто встречаются в природе, но широко и активно применяются в разных сферах жизни, тем самым помогая человечеству.