Клостридии вызывают острые кишечные инфекции.
Бактерии рода Клостридий вырабатывают наиболее сильные из известных ядов – ботулотоксин, тетаноспазмин и другие.
Клостридии – бактерии в составе постоянной собсвтенной микрофлоры кишечника. Растут строго без доступа воздуха и их очень трудно идентифицировать.
В организме человека клостридии являются стимуляторами Т-регуляторных клеток, которые снижают аллергическую настроенность организма. Один из клостридиальных метаболитов – бутират –защищает нас через интерлейкин 10. к
Кроме того, клостридии учавствуют в обмене липидов, в обмене желчных кислот и их частичном выведении из организма, подавляют рост и развитие в ЖКТ болезнетворных бактерий, расщепляют до молекулярного состояния белки.
В кишечнике новорожденных детей клостридии появляются к 6-7 дню жизни.
У детей на грудном вскармливании уровень клостридий держится в норме.
У детей при раннем введении смешанного или искусственного вскармливании клостридий превышает норму.
Анализ на дисбактериоз
Количество клостридий у взрослых:
Повышенное содержание клостридий часто наблюдается у людей старшего возраста на фоне физиологического снижения бифидобактерий.
Также повышенное содержание мясных продуктов в диете может спровоцировать рост клостридий с превышением естественной нормы.
При дисбактериозах надо регулировать эубактерии, клостридии, бифидо- и лактобактерии.
Лечшими препаратами для коррекции микрофлоры в сторону нормы являются жидкие синбиотики бифидум баг и трилакт. В них запредельное количество живых бактерий плюс жидкая среда в качестве пребиотика.
Живые культуры бифидо- и лактобактерий вместе с частью культуральной среды работают как биокатализаторы, стимулирующие восстановление кишечного гомеостаза в сторону нормы.
Людям старшего возраста необходимо 2 раза в год проводить профилактические курсы бифидум баг+трилакт для восстановления бифидобактерий, латофлоры, клостридий и др. А также регулярно употреблять в пищу кисломолочные продукты.
Трилакт и Бифидум БАГ – это безопасная микробиологическая профилактика и терапия дисбиотических нарушений ЖКТ.
Клостридия клостридии волк: С. difficile vs С. scindens
Клостридия клостридии волк: С. difficile vs С. scindens
Автор
Редактор
Тело человека населено триллионами микроорганизмов, совокупность которых называют микробиомом. Микробиом выполняет множество важных функций — от синтеза витаминов до расщепления сложных компонентов пищи. «Здоровая» микрофлора постоянно конкурирует за ограниченные питательные ресурсы с патогенными микроорганизмами, тем самым подавляя их рост. Однако из-за приема антибиотиков или других причин нормальный состав микробиома может нарушаться, и тогда патогены получают возможность размножаться неконтролируемо, вызывая болезни. Один из таких патогенов — бактерия Clostridium difficile, возбудитель псевдомембранозного колита. Борьба с С. difficile осложняется ее устойчивостью к большинству известных антибиотиков. Но недавно было показано, что рост С. difficile можно успешно подавлять не лекарствами, а при помощи родственного ему вида — С. scindens. Это открытие послужит основой для создания «умных» лекарств-пробиотиков: эффективных против С. difficile, но безопасных для полезной микрофлоры.
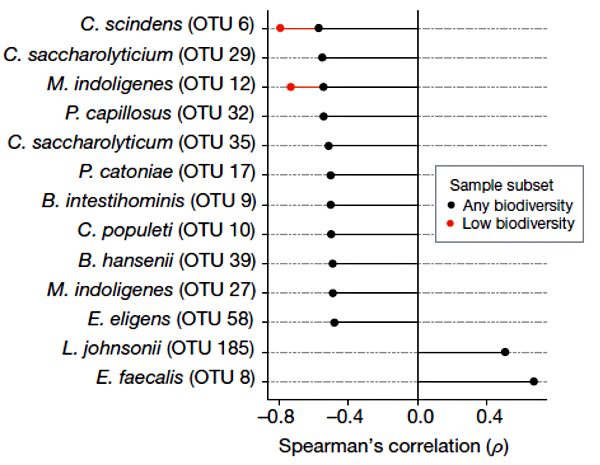
Рисунок 1. Корреляция между присутствием конкретных бактериальных таксонов в микробиоме и устойчивостью к заражению C. difficile [3].
Антибиотики эффективны в борьбе со множеством смертельных заболеваний, но вместе с тем они наносят существенный урон микробиому человека. После курса антибиотиков человек, как правило, более подвержен заражению различными патогенами. Clostridium difficile — грамположительная подвижная бактерия, основной возбудитель острых внутрибольничных кишечных инфекций. За последние 15 лет число смертельных случаев, обусловленных размножением С. difficile, возросло по меньшей мере в 10 раз, особенно среди пожилых и ослабленных людей [1]. Борьба с С. difficile осложняется тем, что при неблагоприятных условиях этот вид образует споры, выдерживающие действие антибиотиков. Такая особенность позволяет бактериям повторно колонизировать кишечник спустя несколько недель и даже месяцев после окончания лечения.
Недавно было показано, что трансплантация микробиомов здоровых доноров вылечивает тяжелые инфекции C. difficile [2]. Однако оставалось неизвестным, какие именно члены микробиома восстанавливают устойчивость организма к инфекции C. difficile и какими механизмами. И вот наконец вышла статья, которая проливает свет на довольно необычный механизм межвидовых взаимодействий в микробиоме [3].
О мышах и людях
C. difficile — не только человеческая беда, но и мышиная. Для начала микробиомы мышей пробовали травить разными антибиотиками и смотрели, как от этого меняется восприимчивость к C. difficile. В целом антибиотики не столько уменьшают суммарное число бактерий в кишечнике, сколько существенно нарушают расстановку сил — соотношение разных таксономических групп. Оказалось, что восприимчивость к C. difficile четко коррелирует с общим снижением видового разнообразия микробима. Удалось выделить горстку из 11 условных видов (операционных таксономических единиц), ассоциированных с устойчивостью к заражению C. difficile (рис. 1). Многие из них оказались тоже клостридиями (кластер Clostridium XIVa). Ученые обратили внимание на один таксон, присутствие которого сильнее всего коррелировало с резистентностью к C. difficile, даже у животных с экстремально низким видовым разнообразием микробиома. Героем оказался Clostridium scindens.
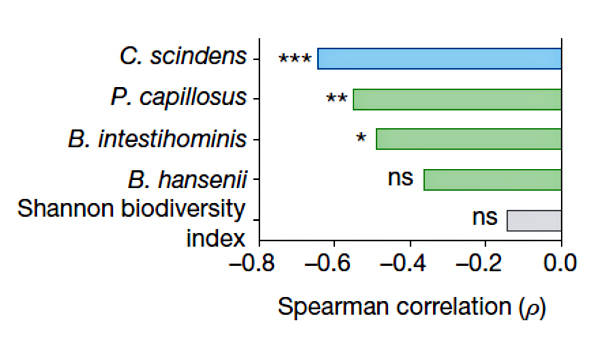
Рисунок 2. Корреляция между приживлением видов-кандидатов в микробиоме и устойчивостью к C. difficile [3].
Но то у мышей. Как же обстоят дела у человека? Для определения видов, связанных с устойчивостью к инфекции C. difficile, исследовали микробиомы пациентов, перенесших аллогеную трансплантацию гемопоэтических стволовых клеток. Большинство из них проходило химиотерапию и/или лучевую терапию одновременно с курсом антибиотиков во время трансплантации. Ослабленный иммунитет и снижение видового разнообразия микробиома делают этих пациентов легкой мишенью для C. difficile. У человека удалось найти два основных вида, с которыми не уживались C. difficile. Наиболее сильным ингибитором оказался C. scindens, как и у мышей. Как будто бы победа?
Для проверки ингибирующего эффекта C. scindens вместе с несколькими другими перспективными бактериями запустили в кишечники животных, недавно принимавших антибиотики (рис. 2). Оказалось, что такая микробная трансплантация существенно облегчила течение инфекции, вызванной C. difficile, а также положительно сказалась на снижении смертности и увеличении массы тела по сравнению с контролем. Наиболее заметную устойчивость к C. difficile обеспечивал, как и ожидалось, C. scindens. Приживление трасплантированных бактерий в микробиоме отслеживали по наличию гена соответствующей 16S рРНК. Устойчивость к C. difficile росла прямо пропорционально обилию C. scindens. То есть улучшение приживаемости C. scindens может повысить защиту против C. difficile. Примечательно, что такая аккуратная замена плохой клостридии на очень похожую, но хорошую, не нарушает существующий в микробиоме баланс (ни качественный, ни количественный). Своеобразная антидотная терапия, только на уровне микробиома. Все это открывает искрящиеся горизонты для разработки безопасных лекарств против C. difficile. Но как именно C. scindens противостоит C. difficile?
Механизм ингибирующего действия
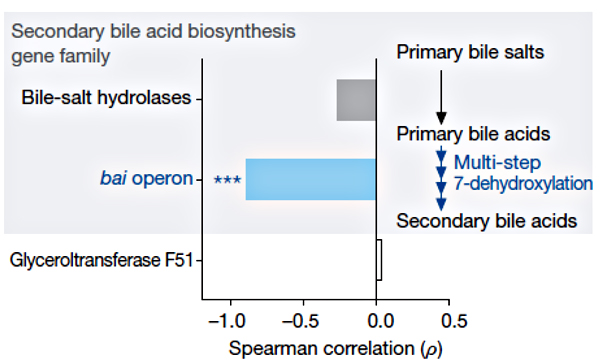
Рисунок 3. Корреляция между устойчивостью к C. difficile и наличием семейств генов, необходимых для синтеза вторичных желчных кислот [3].
Известно, что некоторые вторичные желчные кислоты могут ухудшать рост C. difficile in vitro [4]. У очень большого числа микробиомных бактерий есть ген bsh, кодирующий гидролазу желчных кислот. Однако у редкой бактерии (ужасно малой доли микробиомных организмов) есть все гены, необходимые для осуществления полного пути биосинтеза желчных кислот. Редкой бактерией, конечно же, оказалась C. scindens, обладающая критическим для синтеза вторичных желчных кислот геном 7α-гидроксистероид-дегидрогеназы (рис. 3). Именно на этой уникальной биохимической особенности и зиждется защитный механизм C. scindens против C. difficile. Внедрение C. scindens в микробиом животных, восприимчивых к C. difficile, восстанавливает необходимый уровень и соотношение вторичных желчных кислот: дезоксихолевой (DCA) и литохолевой (LCA). Обе эти кислоты подавляют рост C. difficile пропорционально своей концентрации. Примечательно, что C. scindens повышает количество вторичных желчных кислот до физиологического уровня и препятствует росту C. difficile даже у животных, прошедших курс антибиотикотерапии. Этот механизм консервативен — реализуется как в микробиоме мыши, так и в микробиоме человека.
Терапевтические перспективы
* — О черных делишках кишечных микробов-диверсантов, сокращающих пул желчных кислот и стимулирующих развитие атеросклероза, читайте в статье «Не доверяйте рекламе, или потенциальная связь метаболизма и развития атеросклероза» [6] — Ред.
Clostridium ramosum что это такое
Из не опубликованного
ОБНАРУЖЕНИЕ МАРКЕРОВ НЕКУЛЬТИВИРУЕМЫХ МИКРООРГАНИЗМОВ В ТКАНЯХ ВНУТРЕННИХ ПОЛОВЫХ ОРГАНОВ
Анализ и аналитическое описание Осипова Г.А.
По данным из научной литературы, воспалительные процессы внутренних половых органов составляют 62,5% в структуре гинекологической заболеваемости, причем у 9,5% женщин диагностируют гнойные воспалительные заболевания маточных труб и яичников.
Отмечается, что инфекционные заболевания редко вызываются одним возбудителем, и также возрастает роль условно-патогенных возбудителей. Смешанные инфекции составляют примерно 20-30% в структуре инфекционных заболеваний нижнего отдела половых путей, т.е. почти у каждой третьей пациентки выявляется инфекционный процесс, вызванный несколькими возбудителями. В таких случаях клинические проявления заболевания нетипичны и определяются характером взаимодействия между различными возбудителями, приводящим к угнетению или стимуляции одного вида микроорганизма другим. Гнойные воспалительные заболевания придатков матки относят к смешанным полимикробным инфекциям, важнейшими возбудителями которых, по данным Всемирной организации здравоохранения, являются анаэробно-аэробные микроорганизмы (42,5%), Neiseria gonorrhoeae (37,5%), Chlamydia trachomatis (27,5%), Mycoplasma hominis (до 15%) и др. В последние годы именно анаэробной инфекции уделяют особое внимание, поскольку она приобретает реальную значимость в клинической практике. При острых хронических воспалительных заболеваниях придатков матки и околоматочного пространства наиболее часто (82,5%) выделяют облигатные анаэробные микроорганизмы. По данным В.И. Удовиченко и соавт. (1997), 80% женщин из числа гинекологических больных, обращающихся в женскую консультацию с различными видами вульвовагинитов, цервицитов, уретритов, имеют смешанную бактериально-грибково-трихомонадную инфекцию.
Большинство патогенных организмов являются компонентами нормальной микрофлоры человека, этот факт подтверждает эндогенный путь трансмиссии инфекции. Подавляющее большинство воспалительных заболеваний органов малого таза обусловлено собственной условно-патогенной микрофлорой, ведущая роль в развитии которых принадлежит наиболее вирулентным анаэробам, энтеробактериям и коккам (Сидорова, 2007). В микрофлоре влагалища могут присутствовать гнилостные бактерии родов Bacillus, Proteus, Clostridium, Spirochaeta. По данным Wilkins M.et.al, 1984, количество анаэробов преобладает над аэробами в 10 раз в микробиоценозе вагины.
В свете этих данных представляет интерес изучение состава микробных сообществ матки и придатков, включающих в себя как нормальную, условно-патогенную, патогенную микрофлору. Изучение состава микрофлоры УГТ в норме и патологии в динамике может позволить оценить иммунологический, гормональный статус и гомеостаз макроорганизма. Знание микробных взаимоотношений помогают врачу определить истинную причину инфекционного процесса и подбирать адекватную терапию.
Участие в этом сообществе бактерий, относящихся к разным родам и группам, а также простейших делает затруднительным анализ состава этого сообщества традиционными методами, включающими микробиологический метод селективных сред с биохимическими тестами, и генетическими методами. Традиционные методы идентификации микроорганизмов не являются универсальными и требуют часто длительного времени исполнения.
На этом фоне выглядит перспективным выявление специфических веществ (маркеров) — структурных компонентов микроорганизмов — на фоне биологических жидкостях организма человека, и использование их состава для индикации микроорганизмов с помощью метода газовой хроматографии и масс-спектрометрии (ГХ-МС). Методом ГХ-МС с высокой точностью и чувствительностью определяется качественный и количественный состав микробиоценозов в экологии и медицине по жирным кислотам, оксикислотам, альдегидам и стеринам мембран клеток микроорганизмов и их профилям, относящимся к определенным видам сообщества. Метод детектирования микроорганизмов по ЖК-маркерам сродни генетическому (ПЦР, определение последовательности нуклеотидов 16sРНК, FISH и пр.), поскольку состав жирных кислот детерминирован в ДНК и воспроизводится путем репликации участка генома транспортными РНК и последующего синтеза ЖК по матричным РНК (Уотсон, Молек биол клетки, 5т). Поэтому профиль ЖК бактерий является их визитной карточкой или фингерпринтом как отпечатки пальцев людей (Митрука, 1978). Он так же консервативен, как строение ДНК, но и так же подвержен мутациям под действием факторов окружающей среды. Стабильность набора жирных кислот, составляющих клетки микробов, подтверждается исследованиями в области бактериальной палеонтологии, которые показывают, что до глубины времен в 2,5 млрд лет состав ЖК отдельных микробов и пула их жирных кислот в целом остается постоянным (Shekhovtsova, 2003).
Ранее описаны примеры обнаружения микроорганизмов при инфекционных процессах методом ГХ-МС, в том числе для анализа вагинальной микрофлоры [32] [Вестник РАМН, 1996, № 2]. В результате исследование состава жирных кислот вагинального содержимого показано, что его минорные компоненты относятся к микроорганизмам, колонизирующим половые органы в норме и патологии. Оценена их диагностическая значимость при микробной диагностике хронических вагинитов (Крымцева, 2003, Осипов, 2005).
В настоящей работе этот метод применен для исследования инфекционной составляющей патологического процесса эндометрия матки, приводящего к необходимости оперативного решения проблемы вынашивания плода. Целью исследования является выявление и определение в послеоперационном материале численности анаэробов и других, редко культивируемых микроорганизмов, наряду с традиционными объектами клинической микробиологии.
Методы
В основной группе больных исследованы 24 соскобов из полости матки от пациенток, перенесших операции по поводу проблем беременности.
Режим анализа подробно описан ранее (Осипов, 2010; Годков, 2011). Коротко, он состоит в следующем. Материал в количестве 0,04 г подвергали кислому метанолизу в 0,4 мл 1,2 М HCl в метаноле в течение 45 мин при 80°С. В результате реакции метанолиза жирные кислоты, входящие в состав сложных липидов пробы освобождаются в виде метиловых эфиров. Их экстрагировали в 400 мкл гексана, экстракт высушивали и обрабатывали в 20 мкл N,О-бис(триметилсилил)-трифторацетамида в течение 5 мин при 80 °С для получения триметилсилильных эфиров гидрокси-кислот и стеролов. Смесь эфиров в количестве 2 мкл вводили в инжектор ГХ-МС системы HP-5880/5975 Agillent Technologies (США) в модификации «Микробиологический анализатор «МАЭСТРО» ООО Интерлаб (Россия). Для управления и обработки данных использовали штатные
программы прибора. Хроматографическое разделение пробы осуществляли на капиллярной колонке с метилсиликоновой привитой фазой HP-5ms Agillent Technologies. Длина колонки 25м, внутренний диаметр 0.25 мм. Режим анализа — программированый, скорость нагрева термостата колонки — 5 град/мин в диапазоне 130 — 320°С.
Площади пиков маркеров на масс-фрагментограммах интегрировали автоматически по заданной программе. Затем эти данные вводили в программу расчета, подготовленную в электронных таблицах EXCEL по технологии масс-спектрометрии микробных маркеров (МСММ, Разрешение Росздравнадзора ФС 2010/038 от 24.02.2010) (Осипов, 2010). Для количественного расчета использовали дейтерированную тридекановую кислоту в качестве внутреннего стандарта и собственный банк данных состава жирных кислот клинических изолятов микроорганизмов.
Ошибка количественных измерений численности микроорганизмов из-за погрешности в подготовке проб и анализа, несоответствия состава жирных кислот чистых культур банка данных и изучаемого сообщества in situ может составлять 20%.
Метод характеризуется следующими показателями:
· Определение более 50 микроорганизмов одновременно в одном анализе
· Время анализа – 2,5 часа
· Чувствительность 103-104 клеток в пробе
· Селективность – до вида при наличии маркера
· Анализ непосредственно в материале без высевания или подращивания микроорганизмов
· Не требует биологических и биохимических тестовых материалов – культуральных сред, ферментов, тестовых субстратов, праймеров и т.п.
Результаты измерения концентраций микробных маркеров в соскобах матки с последующей реконструкцией микробного сообщества позволили определить состав микст-инфекции в очаге поражения (табл 1).
Результаты анализа состава локальной микст-инфекции в соскобах из полости матки (N=24). Данные в размерности [клеток/мл х105]
Из 54 таксонов микроорганизмов, контролируемых в процессе анализа, в итоговую таблицу выведены 48, из которых 38 показывают избыточный рост (инфекцию), Клинически значимыми считали более чем двойное превышение нормы на основании статистического распределения концентрации маркеров микроорганизмов у больных и здоровых людей (Белобородова, 1999). Такие изменения отмечены в таблице затенением клетки. Как видно, инфицирование каждого исследованного материала включает несколько (до двадцати двух, Пожарская, GBT-1559) таксонов микроорганизмов. Это подтверждает тезис литературного обзора о смешанном характере инфекции половых органов женщин. Данные таблицы 1 подтверждают также сформировавшееся представление о доминировании анаэробов. Их доля составляет 70-90% по нашим измерениям и соответствует оценке других авторов. В отличие от предыдущих работ наши измерения носят количественный характер, что позволяет выявить микробные доминанты воспалительного процесса на одной и той же пробе инфицированного материала, а также сопоставлять данные анализов разных пациентов. В данном случае доминантами у большинства пациентов оказались бактерии видов Propionibacterium/Cl. subterminale, представителей родов Eubacterium, Clostridium, Lactobacillus, Ruminococcus. Такой тип инфекции показан на рис 1, где в графическом выражении лучше иллюстрируется количественные изменения относительно нормы и других составляющих микробного сообщества. За неимением возможности оценить уровень колонизации слизистых оболочек полости матки и придатков у здоровых женщин, мы приняли в качестве максимально возможного уровня данные нормы по крови. Тем более, что проба носит явно насыщенный кровяной характер.
По кратности превышения нормы выделяются бактерии кишечной группы (рис 1), для которой наблюдается многократное увеличение концентрации маркеров клостридий группы Clostridium ramosum, групп Eubacterium/Cl. сoccoides, Propionibacterium/Cl. subterminale в соскобе из полости матки по сравнению с их уровнем в крови в норме. Пересчетное значение численности этих микроорганизмов по технологии МСММ достигает уровня 10 9 – 10 10 клеток\мл. Расчетная численность C. ramosum в десяти случаях превышает норму в десять-двадцать раз. Из трудно культивируемых микроорганизмов, которые позволяет выявить масс-спектрометрический метод, следует отметить еще анаэробы Streptococcus mutans, численность которых в 11 пробах более 5 раз выше нормальной. В большинстве случав в составе микст-инфекции присутствуют анаэробные актинобактерии Actinomyces viscosus.
Число случаев более чем двукратного превышения расчетной численности микроорганизмов соскобах из полости матки по сравнению с нормой крови
| № | Микроорганизм | Число клин. значимых | в % | Максимальная численность | Максимальное превышение нормы, раз | Найдено в бакпосеве, КОЕ |
| 1 | Streptococcus | 3 | 13 | 1.1×10 8 | 4,5 | |
| 2 | Eubacterium lentum | 22 | 96 | 1.8×10 9 | 271,3 | |
| 3 | Clostridium hystolyticum | 5 | 22 | 7×10 7 | 7,5 | |
| 4 | Peptostreptococcus anaerobius | 8 | 35 | 9×10 5 | 9,0 | |
| 5 | Acinetobacter | 19 | 83 | 9,5×10 6 | 9,5 | |
| 6 | Pseudomonas aeruginosa | 23 | 100 | 2,3×10 6 | 22,0 | |
| 7 | Clostridium propionicum | 3 | 13 | 3,7×10 8 | 14,0 | |
| 8 | Stenotrophomonas maltophilia | 3 | 13 | 2×10 5 | 2,0 | |
| 9 | Актиномицеты | 3 | 13 | 3,6×10 7 | 4,7 | |
| 10 | Streptomyces | 6 | 26 | 4,9×10 7 | 7,9 | |
| 11 | Clostridium ramosum | 21 | 91 | 4.1×10 9 | 20,5 | |
| 12 | Haemophylus/Burkholderia | 23 | 100 | 7,6×10 6 | 76,0 | |
| 13 | Alcaligenes | 14 | 61 | 3,1×10 7 | 6,4 | |
| 14 | Rhodococcus | 5 | 22 | 2,7×10 8 | 6,3 | |
| 15 | Corineform CDC-group XX | 1 | 4 | 1.3×10 8 | 2,1 | |
| 16 | Lactobacillus | 6 | 26 | 3.1×10 9 | 4,8 | |
| 17 | Campylobacter mucosalis | 1 | 4 | 2,2×10 7 | 2,2 | |
| 18 | Candida | 2 | 9 | 1.4×10 8 | 2,5 | |
| 19 | Clostridium 12:0group* | 8 | 35 | 1.7×10 8 | 6,8 | |
| 21 | Грибы (Aspergillus-тип) | 4 | 17 | 7,4×10 7 | 6,8 | |
| 22 | Prevotella/Burkholderia | 1 | 4 | 1.3×10 7 | 3,4 | |
| 23 | Eubacterium/Cl. Coccoides | 20 | 87 | 1.6×10 10 | 23,1 | |
| 24 | Staphylococcus | 17 | 74 | 1.3×10 8 | 11,2 | |
| 25 | Bifidobacterium | 3 | 13 | 1.6×10 9 | 3,1 | |
| 26 | Helicobacter pylory | 13 | 57 | 1.2×10 7 | 8,5 | |
| 27 | Clostridium perfringens | 11 | 48 | 7,3×10 6 | 6,1 | |
| 28 | Enterococcus | 1 | 4 | 1.3×10 8 | 4,5 | |
| 29 | Propionibacterium/Cl. subterminale | 19 | 83 | 8,7×10 9 | 19,5 | |
| 30 | Streptococcus mutans (анаэробные) | 19 | 83 | 5,6×10 8 | 24,7 | |
| 31 | Herpes | 16 | 70 | 1.1×10 8 | 18,1 | |
| 32 | Nocardia asteroides | 14 | 61 | 4.1×10 8 | 15,0 | |
| 33 | Ruminicoccus | 8 | 35 | 6,6×10 8 | 10,3 | |
| 35 | Blautia coccoides | 7 | 30 | 1.6×10 7 | 15,7 | |
| 36 | Kingella | 3 | 13 | 1.0×10 7 | 10,0 | |
| 37 | Actinomyces viscosus | 9 | 39 | 1.5×10 9 | 12,5 |
Здесь под C. ramosum подразумевается целая группа клостридий, объединенная общим маркером – специфической ненасыщенной жирной кислотой ω9-гексадеценовой. Это C. inocuum, C. clostridieforme, C. subterminale, C. sordellii, C. septicum, C. paraputrificum, C. celatum, C. cochlearium, C. limosum, C. fallax, C. difficile. Другая группа Clostridium 12:0group имеет общий маркер – додекановую кислоту и (С12:0) и включает виды Clostridium perfringens, С. putrefacience, C. hystolyticum, C. tetani. Свои маркеры имеют клостридии других видов: C. histolyticum, C. coccoides вместе с большой группой родственных эубактерий (род Eubacterium), а также C. propionicum, C. perfringens и C. subterminale вместе с частью видов Propionibacterium. В сумме клостридии составляют около 74% микробного сообщества, то есть, как принято в хирургии, это анаэробная клостридиальная инфекция (АКИ).
По данным реконструкции микробного сообщества эндометрия по маркерам в соскобе из полости матки численность ряда микроорганизмов многократно превышает таковую в крови той же пациентки (Рис 2). Основываясь на данных предыдущих исследований методом МСММ (Лазебник, 2008; Прохорова, 2012) мы полагаем, что имеет место транслокация микроорганизмов кишечника по крови и/или восходящая инфекция из вагины с последующим размножением уже в самом органе – матке.
Рис.2. Сравнение состава реконструкции микробного сообщества в соскобе матки и крови одной и той же пациентки методом МСММ.
Таким образом, применение метода масс-спектрометрии микробных маркеров позволило дополнить картину инфицирования верхних половых органов женщин таксонами, которые оказались доминирующими в микробном сообществе, а также расширить список участников инфекционного процесса. Ими оказались, как и предполагалось другими исследователями, представители кишечной микробиоты. Кроме того, в отличие от предыдущих исследований, мы дали их количественную оценку, показав рейтинговый ряд агентов инфекции и подтвердив доминирование анаэробов родов Propionibacterium, Eubacterium, Clostridium и Bifidobacterium. Вряд ли следует сразу зачислять в патогенны доминантные микроорганизмы кишечной микробиоты: бифидобактерии, лактобациллы,эубактерии и пропионобактерии. Также оставим за скобками клостридии группы C. ramosum, поскольку их роль в организме явно выглядит двоякой. Пока не будем осложнять задачу их транслокацией в полость матки. Попробуем выделить явных патогенов.
Для этого исключим из таблицы перечисленные выше кишечные доминантные бактерии и микробы, которые в норме, и оставим те, что превышают норму, а также те, что часто встречаются в бакпосеве – для возможного сопоставления.
Тогда для соскоба GBT-1559 получим следующую сокращенную таблицу (рис 3):
Рис. 3. Наиболее вероятные агенты инфекции эндометрия, за исключением микробов, доминирующих в микробиоте кишечника.
Это реальные кандидаты в агенты инфекции, которая препятствуют нормальному протеканию беременности.
Если посмотреть в таком ключе остальные анализы соскобов, то будет видно, что везде такими агентами являются обязательно Clostridium perfringens, H. pylori, одна или несколько актинобактерий родов Streptomyces, Nocardia, Pseudonocardia. В примере на рисунке 3 это Actinomyces viscosus, Nocardia asteroids и Rodococcus. В этой группе известные разрушители клеток животных. Они обнаружили себя в амбулаторной практике в качестве агентов, препятствующих оплодотворению и развитию яйцеклетки в плод, в том числе при экстракорпоральном оплодотворении.
Тем не менее, нельзя исключать участие в патогенезе и «хороших» бактерий: лактобацилл, бифидобактерий, пропионобактерий и части клостридий. Можно найти десятки документированных случаев участия в инфекционном процессе любого микроба, обитающего в теле человека. В том числе лактобацилл и бифидобактерий. Особенно лактобациллл. Действительно, по литературным данным они зафиксированы как возбудители при эндокардите, бактериемии, бактериурии, перитонитах, абсцессах и менингитах. Наиболее часто выявляются L. casei и L. rhamnosus (Cannon, 2005). Eubacterium – родственные клостридиям микроорганизмы, являющиеся одними из основных обитателей кишечника. Условные патогены с развитой системой видов и штаммов с универсальными свойствами. Эубактерии участвуют в качестве основных агентов во многих воспалительных процессах и синдромах: воспаления неизвестной этиологии, себорея, атопический дерматит, кахексия, воспаление кишечника, глютеновая энтеропатия, воспаление десен, средиземноморская семейная лихорадка, Yang Xiao-xia’s “mysteriuos disease”, синдром раздраженного кишечника, воспаление легких, бактеремия, хронический синусит, болезнь Крона, периодонтит, артрит, простатит, муковисцидоз, эндометрит, эндокардит, неспецифический вагинит, врожденный порок сердца и другие. Основными функции эубактерий в организме человека являются: образование водорода, высвобождение гистамина, биотрансформация желчных кислот, индуцирование продукции провоспалительных цитокинов и TNF-alfa, а также противовоспалительного цитокина IL-10 (как ЛПС или клеточные токсины Грам+ патогенов) и другие. Патогенность клостридий более известна в клинической практике. Они обладают широким набором экзотоксинов. У C.perfringens их насчитывается двенадцать. С. ramosum обладает близкой активностью, в том числе также может вызывать газовую гангрену, язвенный и некротизирующий колиты. Они известны как агенты септицемии, нефропатии, бактериемии и менингита (Brook, 1995; в Атласе, 2003).
Анкирская А. С. Бактериальный вагиноз. Акушерство и гинекология. №3 2005 с. 10-13
Анкирская А.С., Прилепская В.Н., Байрамова Г.Р. Бактериальный вагиноз: особенности клинического течения, диагностика и лечение. // Рус мед журнал, 1999; 5: 276–82.
Атлас по медицинской микробиологии, вирусологии и иммунологии. Под ред А.А. Воробьева и А.С. Быкова. – М., Медицинское информационное агентство, 2003. – 236 с.: ил.
Годков М.А., Осипов Г.А., Федосова Н.Ф., Лядов К.В. Возможности масс-спектрометрии микробных маркеров в лабораторном мониторинге дисбиозов и инфекций. Справочник заведующего КДЛ. 2011, № 7, С. 35-44.
Лазебник Л.Б., Винницкая Е.В., Осипов Г.А. Дроздов В.Н., Петраков А.В. Новые подходы к диагностике спонтанного бактериального перитонита при циррозе печени. Экспериментальная и клиническая гастроэнтерология. №2. 2008. стр. 32-39.
Крымцева Т.А., Осипов Г.А., Бойко Н.Б., Соколов Я.А., Демина А.М., Радюшина Т.В., Осипов Д.Г.. Минорные жирные кислоты биологических жидкостей урогенитальных органов и их значимость в диагностике воспалительных процессов. Журн. Микроб. Эпидем. Иммун. 2003, № 2: 92-101
Митрука Б.М. Применение газовой хроматографии в микробиологии и медицине. М. Медицина, 1978.
Муравьева В. В. Микробиологическая диагностика бактериального вагиноза у женщин репродуктивного возраста // Дисс. Канд. мед. наук., Москва, — 1997.
Осипов Г.А. Хромато-масс-спектрометрический анализ микроорганизмов и их сообществ в клинических пробах при инфекциях и дисбиозах. / В книге: Химический анализ в медицинской диагностике.- М.: Наука, 2010.- С.293-368.
Осипов Г.А., Крымцева Т.А., Осипов Д.Г., Столярова О.Н. Функциональные изменения жирнокислотного состава урогенитальных жидкостей организма человека при дисбиозах. Прометей. Москва, 2005
Прохорова Е. С., Выборнов Д.Ю., Бойко Н.Б., Федосова Н.Ф., Лядов К.В., Осипов Г.А. Изучение эндогенного пути инфицирования посттравматических артритов у детей с применением масс-спектрометрии микробных маркеров. Детские инфекции. 2012, том 11, № 1, С. 55-60
Journal of General Microbiology (1990), 136, 241-247.
JP Cannon, TA Lee, JT Bolanos, and LH Danziger. Pathogenic relevance of Lactobacillus: a retrospective review of over 200 cases. Eur J Clin Microbiol Infect Dis, January 1, 2005; 24(1): 31-40
Shekhovtsova N.V., Osipov G.A., Verkhovtseva N.V., Pevzner L.A. Analysis of lipid biomarkers in rocks of the Archean crystalline basement //Proceedings of SPIE.- 2003.- Vol.4939.- P. 160 – 168
Wilkins M., Thin R. N., Tabaqchall S. Quantitave bacteriology of the vaginal flora in genital disease // J. Med. Microbiol. 1984, 18:2, 217-231.
В этом можно усматривать специфику инфицирования внутренних половых органов, так как при вагинитах в слизистой влагалища их рост хотя и происходит, но не в такой степени. Для вагины более характерна инфекция Clostridium perfringens. При воспалениях, напоминающих по клиническим проявлениям кандидоз, их численность до 30 крат превышают уровень колонизации слизистой оболочки в норме.
Клиническая микробиология и антимикробная химиотерапия, Том 3, N 1, 2001
стр. 39-47
Экологические аспекты чувствительности к антибиотикам анаэробных бактерий
М. Качерес 1,2 , К.Э. Норд 1 , А. Веинтрауб 1