Цитокиновый шторм: ученые выяснили, почему COVID-19 губит молодых и здоровых
Средний возраст людей, ставших жертвами коронавируса, молодеет, и все чаще в применении к этим случаям звучит выражение «цитокиновый шторм». О том, что это такое, пишет New York Times.
Ирина Зиганшина
Когда организм впервые сталкивается с вирусом или бактерией, иммунная система активизируется и начинает бороться с «захватчиком». Рядовые в этой борьбе – молекулы, называемые цитокинами, благодаря которым клетки получают сигнал о том, что необходима ответная реакция.
Как правило, чем сильнее иммунный ответ, тем больше шансов победить инфекцию, – это отчасти объясняет, почему дети и молодые люди менее уязвимы для коронавируса. Как только враг побежден, иммунная система отключается.
Однако есть пациенты – по некоторым данным, среди тех, кто борется с любой серьезной инфекцией, их бывает до 15%, – чья иммунная система продолжает бороться и после того, как вирус уже обезврежен. Цитокины продолжают высвобождаться, атакуя множество органов, включая легкие и печень, и изнуряя организм.
Иными словами, главную опасность для таких пациентов представляет не вирус, а чрезмерная реакция их организма, и закончиться все это может смертью. Цитокиновый шторм настигает людей любого возраста, однако некоторые ученые считают, что именно этот феномен может объяснить, почему среди жертв эпидемий «испанки», атипичной пневмонии, БВРС и нынешнего COVID-19 так много молодых и здоровых людей.
Этот неконтролируемый всплеск иммунных молекул, зачастую приводящий к фатальному отключению органов, помимо цитокинового шторма, называют также гиперцитокинемией и цитокиновым каскадом. В последние дни эти слова звучат все чаще, однако еще недавно далеко не все врачи были знакомы с этим состоянием и не знали, как его лечить.У пациента, борющегося с цитокиновым штормом, может быть учащенное сердцебиение, лихорадка и падение кровяного давления.
Кроме того, анализ крови может показать повышенные уровни таких маркеров, как интерлейкин-6, интерлейкин-1, С-реактивный белок и фактор некроза опухоли-альфа. Через некоторое время цитокиновый шторм становится очевидным. Но чем раньше врачи поймают его и вылечат, тем больше шансов, что пациент выживет: если начать лечение слишком поздно, состояние может выйти из-под контроля.
Существует относительно простой, быстрый и доступный тест, который может определить, подвергся ли организм пациента цитокиновому шторму, – это биохимический анализ на ферритин. Высокие уровни этого белка могу быть показателем воспалительного заболевания. Если врач имеет основания предполагать, что налицо цитокиновый шторм, он назначает лечение.
Во время нынешней эпидемии коронавируса уже было описано несколько случаев молодых пациентов в Китае и Италии с цитокиновым штормом, иммунную систему которых «успокаивали» препаратом под названием тоцилизумаб.
Классический пример, описанный в журнале Annals of Oncology: после всего лишь двух доз препарата, с интервалом в восемь часов, лихорадка пациента быстро исчезла, уровень кислорода повысился, а сканирование грудной клетки показало, что его легкие очистились, – свидетельствует о том, что тоцилизумаб может быть эффективным противоядием от коронавируса у некоторых людей.
До появления COVID-19 тоцилизумаб использовался для лечения ревматоидного артрита и некоторых видах рака: он приглушает активность специфического цитокина под названием интерлейкин-6, который связан с чрезмерно интенсивным иммунным ответом.Сейчас уже как лекарство от COVID-19 тоцилизумаб проходит клинические испытания в Китае (где его уже одобрили для лечения серьезных случаев) и США.
Также ученые тестируют другие препараты, которые могут быть полезны прицитокиновых бурях, например анакинру, гидроксихлорохин (тот самый препарат от малярии, который на минувшей неделе нам представили как изобретение российских медиков) и кортикостероиды.
Последние, однако, известны тем, что подавляют иммунный ответ целиком, а это опасно, поскольку оставляет пациента беззащитным перед другими инфекциями, а они вероятны, особенно в больнице.
Цель успешного лечения при цитокиновых бурях – установить правильный баланс: подавить чрезмерно буйный иммунный ответ, сохранив при этом иммунитет достаточно сильным, чтобы он мог бороться с вирусом. Как показывает опыт, это достаточно сложно из-за индивидуальных реакций пациентов: например, некоторые больные коронавирусом не показали никаких улучшений от терапии тоцилизумабом. Испытания должны показать, на каких пациентах препараты работают.
Цитокиновый шторм при коронавирусе
Важное о коронавирусе
Коронавирусная инфекция в первую очередь опасна своими осложнениями. Вирус агрессивно действует на ткани, негативно влияет на работу иммунной системы, провоцирует сердечно-сосудистые и неврологические нарушения. Одним из грозных последствий заболевания врачи называют цитокиновый шторм при ковиде, который протекает очень тяжело и может быть потенциально смертельным.
Что такое цитокиновый шторм при коронавирусе
Медики описывают это состояние как системную воспалительную реакцию, которая протекает бесконтрольно и характеризуется чрезмерной выработкой воспалительных цитокинов. Если объяснять простыми словами, цитокиновый шторм — слишком активная работа иммунной системы, когда организм начинает атаковать сам себя.
Чтобы было понятнее, стоит поговорить о том, что такое цитокины. Так называются регуляторные белковые молекулы, которые вырабатываются иммунными клетками, контролируют процессы воспаления и клеточной защиты от чужеродных веществ и патогенных возбудителей. В норме они синтезируются в умеренном количестве, помогают организму справляться с болезнями.
Если таких молекул образуется слишком много, вместо реакции с вирусами или бактериями, они начинают взаимодействовать с собственными тканями организма, вызывая ухудшение здоровья и отягощая симптомы коронавируса.
Кандидат биологических наук, врач-иммунолог Борис Донской для описания гиперцитокинемии приводит метафору с физической нагрузкой: “Вы требуете от сердца «обслужить» дополнительную нагрузку? Оно будет пытаться выполнить ваше требование, запустив «режим» высокого пульса в 200 ударов в минуту и высокого давления. Но не каждое сердце может это выдержать и на определенном этапе функционирования в таком режиме оно само себя и убьет. Примерно то же происходит и при цитокиновом шторме”.
Причины шторма
Гиперцитокинемия возникает не только при коронавирусной инфекции. Она сопровождает многие тяжелые заболевания, которые приводят к нарушениям защитных сил организма и развитию аутоагрессии. Ученые предполагают, что провоцирующим фактором шторма является недостаток отдельных фракций Т-лимфоцитов, отвечающих за регуляцию иммунного ответа, на фоне чего формируется неконтролируемый выброс провоспалительных агентов.
Причины неадекватного цитокинового выброса:
Недавно американские ученые установили еще одно возможное звено патогенеза выброса цитокинов. Врачи выявили, что увеличение уровня молекул микроРНК miR-155 повышает риск развития синдрома, причем такая особенность более характерна для мужчин.
Кто в группе риска
Чаще всего патология возникает у пожилых пациентов, у которых нарушен нормальный иммунный ответ и не хватает Т-лимфоцитов, которые могли бы регулировать образование цитокинов. В такой ситуации формируется “порочный круг”, когда повышенное количество цитокинов стимулирует новые клетки иммунные системы, которые в свою очередь продуцируют очередные порции провоспалительных молекул.
Парадоксально, что в группе риска также находятся молодые люди спортивного телосложения. Врач Олег Назар поясняет ситуацию: “Кстати, у спортсменов тоже может не хватать иммунных клеток, потому что белок, из которого они строятся, идет на постройку мышечной массы”. Вероятность развития шторма в этой группе еще больше повышается, если человек недополучает белок, придерживается вегетарианского рациона.
Выделяют и другие факторы риска:
Симптомы цитокинового шторма
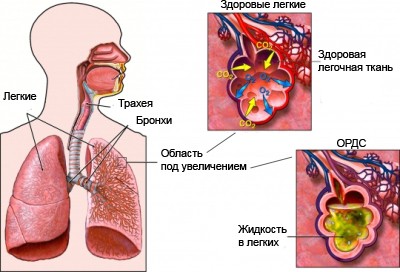
Патологическая иммунная реакция негативно влияет на все органы и системы, но первыми повреждаются легкие — развивается острый респираторный дистресс-синдром. Как объясняет медицинский директор “СберЗдоровье” Владислав Мохаммед Али: “Цитокиновый шторм — это каскад биохимических реакций, в котором задействованы факторы, «отвечающие» за воспалительные процессы в организме. При цитокиновом шторме поражаются в первую очередь легкие, но также страдают и другие органы”.
У человека с гиперцитокинемией на фоне КОВИД-19 могут быть такие клинические проявления:
Как выявляют
По клиническим проявлениям невозможно с точностью определить заболевание, поэтому пациенту назначают лабораторное тестирование. Результаты анализов крови при цитокиновом шторме:
Дополнительно при гиперцитокинемии проводится КТ легких, в котором обнаруживают очаговые инфильтраты или тотальное поражение паренхимы по типу “матового стекла”.
На какой день начинается
Чаще всего выброс цитокинов происходит на фоне пневмонии при коронавирусе, но может возникать и при легком течении КОВИД-19. Самым опасным считается период с 8 по 10 день заболевания. В это время при положительном сценарии происходит регресс симптоматики, а в случае неблагоприятного течения возникают осложнения.
Обратите внимание! Зачастую перед появлением признаков цитокинового шторма при коронавирусе возникает временное улучшение состояния, что вводит пациента в заблуждение.
Сколько длится
Продолжительность нарушений зависит от своевременности и полноты терапии, исходного состояния иммунной системы, наличия сопутствующих болезней у коронавирусного пациента. Если проявления замечены на ранней стадии, комплексной терапией их удается купировать за 2-3 суток, а в тяжелых случаях пациенты лечатся в течение 3-4 недель.
Что происходит в результате цитокинового шторма?
При гиперцитокинемии симптомы вызваны не самим вирусом, а вторичными реакциями, которые он запустил при взаимодействии с иммунными клетками. В результате накопления большого количества провоспалительных агентов поражается ткань альвеол, наблюдается интерстициальное воспаление и пропотевание жидкости из сосудов в ткани, из-за чего нарушается газообмен.
Цитокиновый синдром при коронавирусной инфекции всегда сопровождается тяжелыми нарушениями дыхания и гипоксией, что приводит к неврологическим и полиорганным нарушениям.
Еще один механизм негативного влияния гиперцитокинемии — повреждение тромбоцитов и эритроцитов. При этом нарушается свертываемость крови, могут возникать тромбозы или спонтанные кровотечения.
Лечение цитокинового шторма при ковиде
При наличии хотя бы одного настораживающего признака и подозрении на гиперцитокинемию пациента немедленно госпитализируют в стационар. Терапию начинают после сокращенного обследования, врачи стараются как можно раньше начать патогенетические препараты.
В протоколах по ведению цитокинового шторма при коронавирусе указаны такие группы медикаментов:
Помимо этих лекарств, пациенту могут назначать противовирусные, кардиотропные, общеукрепляющие препараты. Для предупреждения вторичной бактериальной инфекции используются антибиотики пенициллинового ряда или макролида.
Сосудистые нарушения при выбросе цитокинов зачастую сопровождаются снижением артериального давления и шоковым состоянием. Для его коррекции вводятся вазопрессоры (Норадреналин, Добутамин).
Можно ли остановить цитокиновый шторм
С гиперцитокинемией возможно бороться в условиях интенсивной терапии с применением большого количества специфических медикаментов. Чем раньше будет диагностирована болезнь и чем быстрее начнется лечение, тем больше у человека шансов полностью выздороветь.
К сожалению, цитокиновый синдром не всегда поддается лечению. Это патологическое состояние составляет до 70% причин смерти коронавирусных пациентов.
Последствия цитокинового шторма
Цитокиновая буря негативно влияет на весь организм, вызывая такие патологические состояния:
Все указанные последствия при гиперцитокинемии могут возникать в короткие сроки, поэтому очень важно знать, как проявляется цитокиновый шторм при коронавирусе, чтобы вовремя обратиться к врачу.
Как предотвратить цитокиновый шторм при COVID-19
Учитывая сложные патогенетические механизмы и множество провоцирующих факторов, специфические профилактические меры при гиперцитокинемии отсутствуют. Чтобы минимизировать риски для пациента, необходимо проводить правильное и комплексное лечение типичного сценария коронавируса, выполняя все предписания клинических рекомендаций Минздрава РФ.
Профессор Медицинской школы Университета Кейс Вестерн (США) Майкл Ледерман обращает внимание на раннюю диагностику иммунных нарушений, которая поможет избежать развернутой клинической картины цитокиновой бури. Врач указывает на решающее значение уровней Д-димера, СРБ интерлейкинов, который нужно оценивать в динамике. Это позволяет с высокой точностью спрогнозировать начало гиперцитокинемии и вовремя предпринять меры.
Советы врачей при цитокиновом шторме
Врач-терапевт Людмила Лапа предостерегает пациентов, что в список лекарств, которые нельзя принимать при COVID-19, входят витамины. Эти на первый взгляд безобидные препараты могут вызывать нарушения в иммунном ответе и запустить каскад патологических реакций.
Профессор МГМСУ им. Евдокимова Андрей Мальвин напоминает о важности регулярного контроля сатурации у пациентов, которые лечатся дома. По словам специалиста, снижение показателя менее 95% — фактор риска развития цитокинового шторма, поэтому такому больному нужно немедленно связаться с врачом для принятия решения о госпитализации.
Кандидат медицинских наук, аллерголог-иммунолог Дарья Фомина на онлайн-конференции, посвященной гиперцитокинемии при ковиде. подчеркнула важность раннего назначения иммуносупрессивной терапии. Врач пояснила, что в таком случае появляется шанс на более быстрое выздоровление пациентов и снижается вероятность жизнеугрожающих осложнений.
Отзывы переболевших с цитокиновым штормом
Я раньше в эту заразу не особо верил, думал, что это обычный грипп, как мы каждый год болеем. Но теперь, когда пролежал 3 недели в больнице, понимаю, что все намного страшнее. У меня сначала была пневмония, но без сильной одышки и кислород в крови в норме, поэтом лечился дома. Через неделю резко подскочила температура, стала сильно болеть грудь и был постоянный кашель. Меня забрали в больницу, там сделали анализы и выяснили, что кроме воспаления легких есть цитокиновая буря. Мне уже было так плохо, что почти все время лежал под кислородной маской, постоянно кололи лекарства. Через неделю полегчало, но выписался только через 3 недели.
Валерий, 48 лет
Я переболела в средней форме, все время была дома. Купила себе пульсоксиметр, постоянно следила за кислородом и была на связи с врачом по вайберу. А вот мужу моему не повезло. Его забрали в стационар с двусторонней пневмонией, потом сказали, что начался шторм и нужно давать гормоны. Он был сначала на кислороде, а потом несколько дней на ИВЛ. Всего лечение заняло более 1,5 месяцев. Сейчас муж уже дома, но очень слабый, у него обострились проблемы с почками.
Ольга, 57 лет
Вот уж не думала, что у меня будет ковид, да еще и в тяжелой форме, поскольку я вообще редко болею, несколько лет закаляюсь и занимаюсь спортом. Но болезнь оказалась очень коварной. Меня из дома забрали на скорой с температурой под 40 градусов и сильной одышкой. В больнице лечили противовирусными и гормонами. На фоне цитокинового шторма были сильно повреждены легкие, поэтому я неделю лежала с кислородной маской. К счастью, вроде бы все обошлось, после выздоровления никаких осложнений у меня не нашли.
Диана, 25 лет
Мы с мужем оба тяжело переболели, в больнице провели почти месяц, и большую часть времени были на кислороде. Как нам терапевт уже потом объяснил, кроме пневмонии и проблем с сердцем, начался цитокиновый шторм, поэтому были осложнения на все органы. У меня после ковида начались проблемы с почками, и врач сказал, что это тоже из-за цитокинов.
Наталья, 63 года
Цитокиновый шторм после коронавируса — опасное и потенциально смертельное осложнение, возникающее при неадекватной реакции иммунной системы и накоплении в крови провоспалительных веществ. Состояние проявляется фебрильной лихорадкой, дыхательной недостаточностью, нарушениями свертываемости крови, патологиями внутренних органов. При гиперцитокинемии нужно как можно раньше начинать лечение иммуносупрессорами, чтобы сохранить жизнь и здоровье пациенту.
Видео о главных ошибках в лечении ковида
Цитокиновый шторм при различных вариантах течения COVID-19
В декабре 2019 года в городе Ухань, Китай, был обнаружен новый штамм коронавируса, вызывающий тяжелый острый респираторный синдром — коронавирус 2 (SARS-CoV-2). Наряду с SARS-CoV и коронавирусом, ассоциированным с ближневосточным респираторным синдромом — (MERS-CoV), SARS-CoV-2 является третьим коронавирусом, вызывающим тяжелые респираторные заболевания у людей, объединенных под названием «коронавирусная болезнь 2019 года» (COVID-19). Эта вспышка была признана Всемирной организацией здравоохранения (ВОЗ) в марте 2020 года пандемией и оказала значительное влияние на экономику и здравоохранение во всем в мире.
Хотя ситуация развивается стремительно, тяжелое течение заболевания, проявляющееся лихорадкой и пневмонией, приводящее к острому респираторному дистресс-синдрому (ОРДС), было описано в 20 % случаев COVID-19. Это напоминает течение ОРДС, вызванного синдромом выброса цитокинов (цитокиновый шторм), и вторичный гемофагоцитарный лимфогистиоцитоз, наблюдаемый у пациентов с SARS-CoV и MERS-CoV, а также у пациентов с лейкемией, получающих Т-клеточную терапию. Учитывая этот опыт, необходимо создание терапевтических средств, основанных на подавлении синдрома выброса цитокинов, таких как тоцилизумаб, которые прошли клинические испытания для лечения COVID-19.
SARS-CoV-2 — это бета-коронавирус, который наиболее тесно связан с SARS-CoV. Оба вируса используют рецептор ангиотензинпревращающего фермента, связанный с карбоксипептидазой (ACE2), чтобы проникнуть в клетки. Этот рецептор повсеместно экспрессируется в сердечной и легочной ткани, а также в некоторых кроветворных клетках, включая моноциты и макрофаги. Ключевой особенностью инфекции COVID-19 является лимфопения (низкий уровень лимфоцитов в крови), которая коррелирует с клинической тяжестью процесса. При SARS-CoV инфицируются моноциты и дендритные клетки, тогда как при MERS-CoV инфицируются моноциты и Т-клетки через дипептидилпептидазу 4 (DPP4). Возможно, что SARS-CoV-2 также поражает дендритные клетки. Апоптоз и истощение пула Т-клеток в результате нарушения процессов активации из-за дисфункции дендритных клеток может способствовать патологии иммунной системы при COVID-19. Однако лимфопения не является специфическим биомаркером неблагоприятного прогноза при COVID-19, поскольку она также является биомаркером, который коррелирует с летальным исходом в пандемии гриппа A (H1N1) 2009 года.
Было установлено, что цитокиновый шторм является основным фактором тяжелого течения SARS-CoV и MERS-CoV у пациентов. Повышенные сывороточные концентрации интерлейкина-6 (IL-6) и других провоспалительных цитокинов являются признаками тяжелого течения инфекции MERS-CoV. Синдром высвобождения цитокинов часто встречается у пациентов с COVID-19, а повышенный уровень IL-6 в сыворотке коррелирует с дыхательной недостаточностью, ОРДС и неблагоприятными клиническими исходами. Повышенный уровень C-реактивного белка (CРБ),экспрессия которого стимулируется IL-6, также является биомаркером тяжелой бета-коронавирусной инфекции.
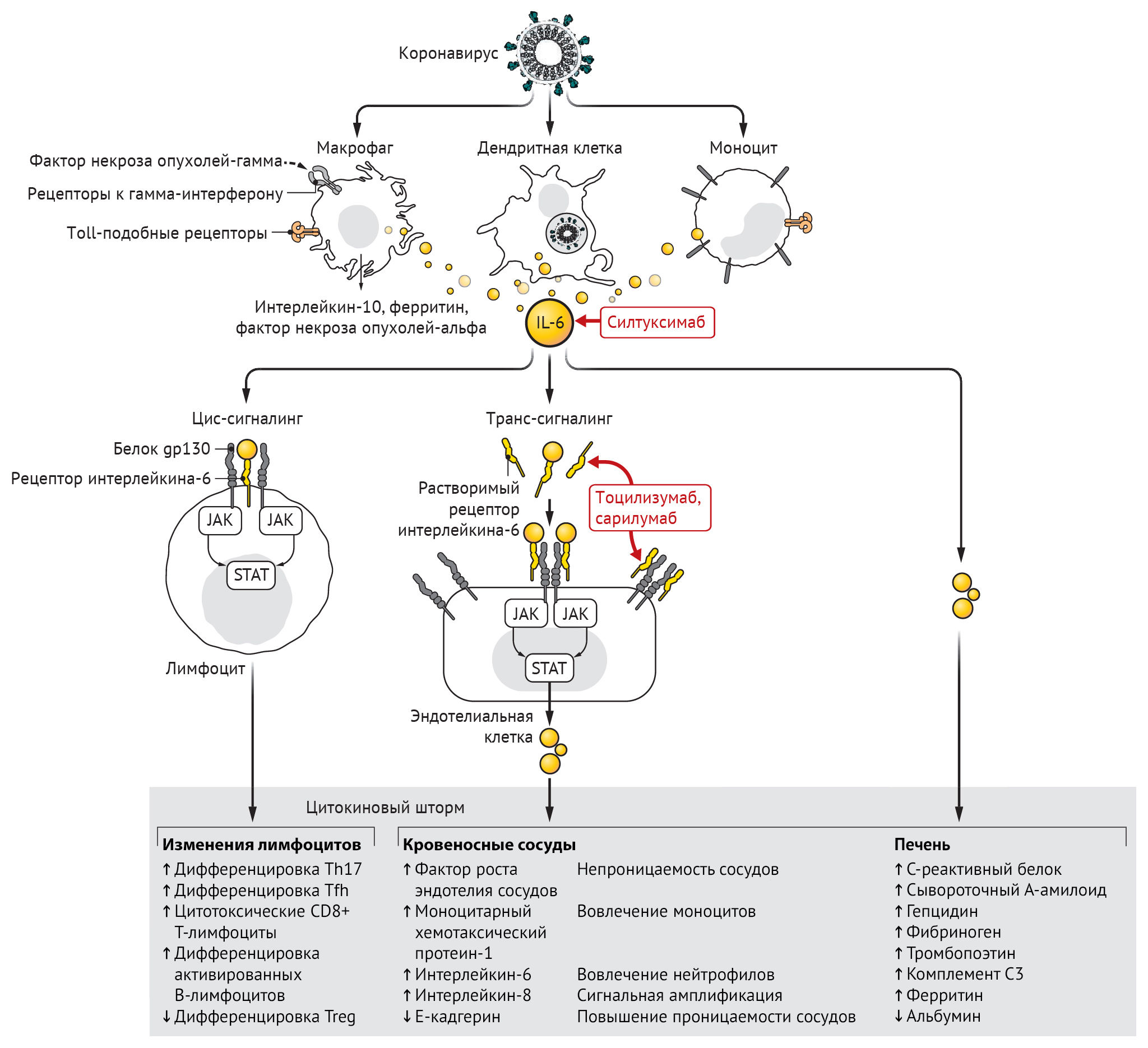
Инфицирование бета-коронавирусом моноцитов, макрофагов и дендритных клеток приводит к их активации и секреции IL-6 и других провоспалительных цитокинов. IL-6 обладает выраженными провоспалительными свойствами (см. рис. 1). IL-6 может передавать сигналы по двум основным путям, которые называются классической цис-передачей или транс-передачей. При передаче цис-сигналов IL-6 связывается с мембраносвязанным рецептором IL-6 (mIL-6R) в комплексе с gp130; нисходящая сигнальная трансдукция опосредуется, в свою очередь, JAKs (Janus kinases) и STAT3 (сигнальный преобразователь и активатор транскрипции-3). Связанный с мембраной комплекс gp130 экспрессируется повсеместно, в отличие от mIL-6R, экспрессия которого ограничена в основном иммунными клетками. Активация передачи сигналов в рамках цис-передачи приводит к плейотропным эффектам на приобретенный иммунитет (В- и Т-клетки), а также врожденную иммунную систему [нейтрофилы, макрофаги и естественные клетки-киллеры (NK)], которые могут вносить вклад в возникновение цитокинового шторма.
При передаче сигналов высокие концентрации циркулирующих IL-6 связываются с растворимой формой IL-6R (sIL-6R), образуя комплекс с димером gp130 на всех клеточных поверхностях. В результате сигнальный каскад IL-6-sIL-6R-JAK-STAT-3 активируется в клетках, которые не экспрессируют mIL-6R, таких как эндотелиальные клетки. Это приводит к системному «цитокиновому шторму», включающему секрецию сосудистого эндотелиального фактора роста (VEGF), хемоаттрактантного белка моноцитов–1 (МСР-1), IL-8 и дополнительного IL-6, а также снижение экспрессии E-кадгерина на эндотелиальные клетки. VEGF и пониженная экспрессия E-кадгерина способствуют проницаемости сосудов, которые участвуют в патофизиологии гипотонии и легочной дисфункции при ОРДС.
Вторичный гемофагоцитарный лимфогистиоцитоз — это гипервоспалительный синдром, характеризующийся высвобождением цитокинов, цитопенией (низкое количество клеток крови) и полиорганной недостаточностью (включая печеночную). У взрослых вторичный гемофагоцитарный лимфогистиоцитоз чаще всего связан с тяжелыми вирусными инфекциями, но также встречается у пациентов с лейкемией, получающих специальную Т-клеточную терапию. В дополнение к повышенным уровням цитокинов для вторичного гемофагоцитарного лимфогистиоцитоза характерны высокие уровни ферритина в сыворотке крови. Экспрессирующие CD163 макрофаги выступают в качестве источника ферритина. Учитывая их роль в передаче сигналов ретикулоэндотелиального железа, вторичный гемофагоцитарный лимфогистиоцитоз известен также как синдром активации макрофагов. Ретроспективное исследование пациентов с COVID-19 показало, что повышение сывороточного ферритина и IL-6 коррелировало с уровнем выживаемости и наблюдалось у погибших.
У пациентов, получающих CART-терапию (лечение Т-клетками химерного рецептора антигена (chimeric antigen receptor — CAR)), также могут развиться как цитокиновый шторм, так и вторичный гемофагоцитарный лимфогистиоцитоз. CART-терапия включает перепрограммирование Т-лимфоцитов пациента с целью повышения экспрессии на них молекул CAR, которые распознают антигены на опухолевых клетках. При переливании этих перепрограммированных клеток обратно пациенту они нацеливаются на опухолевые клетки, тем самым активируя противоопухолевый иммунный ответ. Эмили Уайтхед, первый пациент, получивший CD19-нацеленные Т-клетки CAR-19 с целью лечения острого лимфобластного лейкоза в 2012 году, побочным эффектом получила тяжелую форму цитокинового шторма и вторичного гемофагоцитарного лимфогистиоцитоза, что привело к развитию ОРДС, полиорганной недостаточности и гипотонии, которая была невосприимчива к стандартному лечению стероидами. Из-за значительного повышения сывороточного IL-6 у этой пациентки эмпирически было принято решение о начале терапии тоцилизумабом, антагонистом IL-6R, одобренным в то время для лечения ревматических состояний, таких как ювенильный идиопатический артрит. Она получала однократную дозу тоцилизумаба на 7-й день после введения CARТ-лимфоцитов. Спустя несколько часов у пациентки снизилась температура, после чего было принято решение об отмене лечения гипотонии и отказ от поддержки ИВЛ после разрешения ОРДС. В настоящее время тоцилизумаб с подтвержденной эффективностью и минимальными побочными эффектами у сотен пациентов одобрен Управлением по контролю за продуктами и лекарствами США (FDA) для лечения заболеваний, протекающих с синдромом цитокинового шторма, вызванного CARТ-терапией.
Эффективность антагонистов IL-6-IL-6R для лечения цитокинового шторма и вторичного гемофагоцитарного лимфогистиоцитоза подчеркивает центральную роль передачи сигналов IL-6 в патофизиологии цитокин-управляемых гипервоспалительных синдромов. Тяжелые случаи COVID-19 можно лечить как раз путем ингибирования пути IL-6, учитывая связанные с цитокиновым штормом и подобным вторичному гемофагоцитарному лимфогистиоцитозу повышения цитокинов в сыворотке крови. Действительно, предварительные результаты исследования 21 пациента с COVID-19, получавшего тоцилизумаб в Китае, обнадеживают: лихорадка спадала у всех пациентов в течение первого же дня приема тоцилизумаба. Потребность в кислороде была снижена у 75 % пациентов.
Во всем мире проводятся контролируемые клинические испытания с целью тестирования эффективности антагонистов IL-6 и IL-6R для лечения пациентов с COVID-19 с тяжелыми респираторными осложнениями. Один вопрос, который необходимо решить, заключается в том, будет ли иметь место дифференциальная эффективность между антагонистами IL-6 и антагонистами IL-6R. Относительно этого поднимается вопрос, что ингибиторы IL-6R могут подавлять как цис-, так и транс-передачу сигналов, а также транс-презентацию, недавно описанный третий способ передачи сигналов. Транс-презентация включает связывание IL-6 с mIL-6R, экспрессируемым на иммунной клетке, которая образует комплекс с gp130 на клетках T-хелпера-17 (TH17), что приводит к передаче сигналов Т-клеток вниз по каскаду, который может приводить к ОРДС. Однако ингибиторы IL-6 могут подавлять только цис- и транс-передачу сигналов. Непосредственная цель применения антагонистов IL-6 состоит в том, чтобы облегчить течение тяжелых случаев COVID-19 и свести к минимуму потребности в интенсивной терапии данных пациентов. Долгосрочная цель должна заключаться в разработке противовирусных препаратов и вакцин, которые предотвращают инфекцию или облегчают ее течение.
Есть ряд предостережений, которые необходимо брать во внимание, учитывая глобальную потребность в терапии COVID-19. При сепсис-ассоциированном ОРДС часто назначают кортикостероиды. Однако применение кортикостероидов у пациентов с SARS и MERS не улучшило показатели выживаемости и не привело к каким-либо изменениям вирусного клиренса. В результате консенсус экспертов-инфекционистов из профильных институтов и ВОЗ рекомендует клиницистам избегать системных кортикостероидов у пациентов с COVID-19 в настоящее время. Теоретическая возможность состоит в том, что подавление воспаления антагонистами IL-6 может задержать выведение вируса из организма. Однако блокада IL-6 также приводит к быстрому снижению сывороточного IL-10, иммуносупрессивного цитокина, секретируемого макрофагами, что может смягчить опасения по поводу продления клиренса вируса. Более того, одна или две дозы антагониста IL-6 вряд ли приведут к таким осложнениям, как грибковые инфекции или остеонекроз челюсти, возникающие у пациентов, которым ежемесячно вводят эти препараты для лечения хронических состояний, например, ревматоидного артрита. Примечательно, что тоцилизумаб был впервые одобрен для лечения ревматических заболеваний, а затем — цитокинового шторма у пациентов, получающих CARТ-терапию, и в настоящее время подвергается «перепрофилированию» для борьбы с пандемией COVID-19. Вполне возможно, что направленная на IL-6 терапия будет использоваться в лечении пациентов на случай будущих пандемий, вызванных другими вирусами, таких как грипп и лихорадка Эбола.