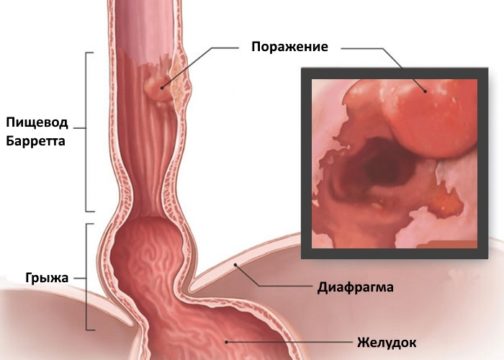
Цилиндроклеточная метоплазия пищевода
Добрый день. Делал гастроскопию с биописей. Пришел такой результат.
«цилиндроклеточная метоплазия слизистой пещевода». Все документы с иследованием прикрепил к вопросу.
Гастранэнтеролог назначил лечение. Пантопразол 20 мг по 1 таблетки в день в течении 4 недель.
Но я как то поднапрегся от диагноза, меня ничего не беспокоит. Я не пью, не курю. Это часто встречается? Какой прогноз? можно ли полностью избавится? мне 29 лет всего
Хронические болезни: удален жп, невроз (ОКР)
На сервисе СпросиВрача доступна консультация гастроэнтеролога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
Можете прочитать о клпассификациии метаплазии пищевода вводя в поисковик следующий заголовок :
Пражская классификация метаплазии в пищеводе (2004)
Можно ли вылечить Пищевод Барретта? (Выпуск 4)
Пищевод Барретта определяется как замещение слизистой пищевода слизистой желудочного типа (цилиндроклеточной метаплазии) с наличием среди нее очагов кишечных клеток (кишечной метаплазии).
Вопрос века
Если развитие цилиндроклеточной метаплазии уже состоялось, можно ли на фоне лечения добиться, чтобы на этом месте образовался нормальный эпителий пищевода? Решению вопроса о том, можно ли вылечить пищевод Барретта было посвящено множество исследований и, к сожалению, на сегодня ни медикаментозное, ни хирургическое лечение обеспечить этого с доказательной достоверностью не могут. В ряде исследований отмечено о появлении даже островков нового эпителия пищевода, но неполное его восстановление. Некоторые авторы сообщали о полной регрессии цилиндроклеточной метаплазии, но только у 2 пациентов из 190 наблюдавшихся.
Можно ли вылечить пищевод Барретта разрушением очагов болезни?
Перспективным и современным методом лечения пищевода Барретта рассматривается в настоящее время различные формы абляции (разрушение очагов пищевода Барретта различными методами). К этим методам прибегают только при прогрессировании пищевода Барретта, т.е. обнаружении на фоне цилиндроклеточной метаплазии, кишечной метаплазии в сочетании с дисплазией.
Также следует отметить, что данные процедуры делаются под контролем зрения человека, не на микроскопическом уровне. Возникает пресловутый «человеческий фактор», когда невозможно точно и повсеместно определить все очаги поражения. Описаны не единичные случаи остаточных микроскопических очагов пищевода Барретта, которые не были разрушены. Поверх этих очагов образовывался новый эпителий пищевода, а под ним из неразрушенных остатков пищевода Барретта продолжал развиваться процесс, который при последующей эндоскопии никак не определялся.
Можно ли вылечить пищевод Барретта изменением мировозрения?
Нужно помнить, что развитие пищевода Барретта – это своеобразный защитный механизм организма от агрессии кислотой и желчью. К этому агрессивному воздействию клетки слизистой пищевода не адаптированы, вот и образуются в этом месте такие клетки (клетки желудка и кишки), которые привычны к кислоте и/или желчи. Поэтому, чтобы вылечить данное состояние, необходимо не только прием лекарственных препаратов для ликвидации уже приобретенных изменений, но и глубоко изменение образа жизни и, если хотите, мировозрения.
Поэтому, отвечая на этот вопрос, сегодня с уверенностью можно сказать: медицине пока это не подвластно. При подозрении и обнаружении пищевода Барретта необходимо проводить пожизненную медикаментозную терапию с оптимальным сочетанием хирургических вмешательств, и при возникновении диспластических процессов в слизистой пищевода Барретт прибегать к из разрушению, т.е абляции.
Пищевод Барретта: симптомы, прогноз, лечение
Пищевод Барретта (ПБ, синдром Барретта) — это изменение слизистой нижнего отдела пищевода по цилиндрическому типу любой длины, так называемая метаплазия. Эти изменения могут быть распознаны при эндоскопическом исследовании, после взятия биопсии из измененных участков и гистологического подтверждения.
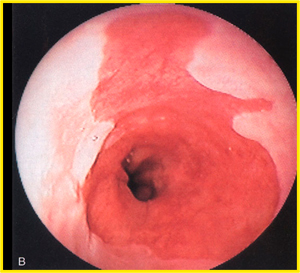 | 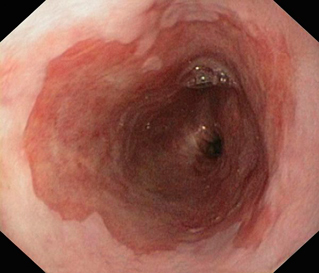 |
Причины и симптомы заболевания
Пищевод Барретта — это заболевание которое возникает в течении жизни, зачастую по причине следующих факторов:
Наиболее частые формы патологических изменений слизистой оболочки пищевода, которые могут привести к ПБ:
Основные жалобы пациентов и признаки пищевода Барретта
Не следует игнорировать перечисленные симптомы и откладывать поход к врачу, лучше профилактировать заболевание и начать лечение на ранних этапах, ведь процессы, происходящие на клеточном уровне не обратимы.
Диагностика пищевода Барретта
Основной и наиболее эффективный метод диагностики синдрома Барретта — эндоскопический. Его цель — получение биопсийного материала. При этом морфологическое исследование направлено на:
Для определения более точных границ измененной слизистой во время эндоскопического исследования используют хромоскопию, это окраска слизистой. Обычно используют раствор Люголя, при аллергии на йод — метиленовый синий, уксусную кислоту.
Лечение пищевода Барретта
Применяют следующие методы лечения пищевода Барретта:
Еще один применяемый и весьма радикальный метод — удаление нижней части пищевода.
Профилактика
Не существует специфической профилактики синдрома Барретта.
Предупредить его развитие помогает своевременная диагностика и лечение гастроэзофагеальной рефлюксной болезни, регулярные и своевременные посещения гастроэнтеролога, обследования и стойкое динамическое наблюдение.
После эффективного консервативного и хирургического лечения пищевода Барретта всем пациентам необходимо проходить ежегодное эндоскопическое обследование с биопсией эпителия.
Авторская публикация:
ВИНЦКОВСКАЯ АЛЕКСАНДРА ИГОРЕВНА
онколог, эндоскопист
НМИЦ онкологии им Н.Н. Петрова
Новости пищевода Барретта. Метапластическая мозаика пищевода Барретта. Часть 3
Метапластическая мозаика пищевода Барретта
Метапластическая мозаика пищевода Барретта
Кажущееся простым гистопатологическое определение ПБ как метапластического состояния, при котором нативный плоский эпителий дистального отдела пищевода замещается цилиндрическим эпителием, представляет собой гораздо более сложную микроскопическую картину.
На самом деле, вместо одного фенотипа, гистология слизистых оболочек пищевода пациентов показывает ряд цилиндрических фенотипов.
Важно подчеркнуть, что, несмотря на традиционный акцент на клеточном составе эпителия как такового, сегмент Барретта имеет кажущееся однообразным расположение желез, как и все слои слизистой оболочки желудочно-кишечного тракта.
Структура каждой железы выстраивается благодаря уникальной популяции стволовых клеток, и поэтому каждая железа является единственной уникальной развивающейся единицей внутри слизистой оболочки. Эти метапластические железистые единицы появляются в различных проявлениях, но, что важно, (1) морфология различных типов железистых единиц инвариантна внутри и между пациентами, и (2) морфология этих типов метапластических желез часто имитирует типы желез, найденные в других отделах желудочно-кишечного тракта, либо первично, либо, вторично в патологических условиях.
Классический фенотип железы, ассоциированный с ПБ, представляет собой смешанную эпителиальную выстилку, состоящую из рассеянных бокаловидных клеток (клетки Гоблета) на фоне цилиндрический клеток с муцинозными свойствами, неотличимыми от желудочных фовеолярных клеток (рис. 1). Этот смешанный желудочный и кишечный рисунок эпителиальной дифференцировки отражается в его муциновом основном пептиде и экспрессии фактора трилистника (TFF) в клетках Гоблета, продуцирующими муцин типа MUC2, а также фактор трилистника 3 (TFF3), в то время как фовеолярные клетки продуцируют муцин типа MUC5AC и фактор трилистника 1 (TFF1). Эти MUC протеины содержат многочисленные олигосахаридные боковые цепи, которые позволяют протеинам связывать большое количество воды после их секретирования в просвет кишки. MUC протеины в дальнейшем будут подвергаться спонтанной агрегации, что создает густой вязко-эластичный гель, который обволакивает подлежащий эпителий. Этот своеобразный рисунок смешанного желудочного и кишечного ростка дифференциаций был широко описан как “специализированный эпителий” или “специализированная метаплазия”, или, в общем употреблении в патогистологических заключениях, “кишечная метаплазия”. Отметим, что в более свежих публикациях это может быть отнесено к неполной кишечной метаплазии II или III типа, однако этот гистохимический подтип в настоящее время считается устаревшим.
В отличие от крипт в тонкой и толстой кишке, где стволовые клетки находятся строго у основания железы и продвигаются вверх по крипте (и ворсинке) по мере своей дифференцировки и созревания, в железах Барретта отсек стволовых клеток расположен примерно на одну треть вверх по высоте железы. А линии зрелых клеток показывают двунаправленный поток от этого отсека стволовых клеток как к просвету, так и к основанию железы. Причем, в эксперименте было показано, что клеточная миграция в сторону основания железы происходит намного медленнее, чем в сторону поверхности крипты железы. Стоит отметить, что примерно за неделю поверхностная миграция была в этих железах утеряна, а неделящиеся клетки обнаруживались до 10 недель в основании железы. Основание железы Барретта выстлано популяцией столбчатых клеток, которые производят не только MUC6, но и бикарбонат (HCO3−). Это создает защитную зону от разъедающего рефлюктата и, вместе с коллоидным гелем, покрывающим метапластический эпителий, защищает слизистую оболочку дистального отдела пищевода. Такое разделение имеет отношение к полному пониманию уникальных функциональных свойств канонической железы Барретта. Обратите внимание, что это двунаправленное разделение никоим образом не уникально в желудочно-кишечном тракте и напоминает основную архитектуру пилорических желез в антральном отделе желудка.
Есть небольшое количество других типов желез, которые в совокупности составляют метапластическую мозаику пищевода, выстланного цилиндрическим эпителием (рис. 2). Наиболее изученной из них является кардиальная железа (также называемая переходной железой или цилиндроклеточная столбчатая железа без клеток Гоблета). По сути, эпителиальная выстилка и двунаправленная архитектура железы кардиального типа идентичны описанным выше каноническим железам Барретта, за исключением отсутствия в них бокаловидных клеток. Таким образом, они являются простейшими с точки зрения дифференцированных типов эпителиальных клеток из всех типов желез Барретта, проявляя только MUC5AC/TFF1 фовеолярные клетки вдоль поверхностного криптового отсека железы и MUC6/TFF2 клетки вдоль основания железы. Они достаточно широко изучены, так как этот тип желез, наиболее часто встречающийся в биопсиях пациентов с коротким сегментом ПБ и в биопсиях у пациентов со столбчатой (цилиндрической) метаплазией в сформированном новым дистальном отделе после резекции пищевода.
Исходя из вышесказанного, данный тип желез можно назвать самым ранним узнаваемым (“ранним ответчиком”) типом железы при развитии ПБ. Это также железы, которые неразличимы с точки зрения железистой архитектуры и клеточного состава от репаративных желез, известных как псевдо-пилорическая метаплазия, например, при терминальном илеите при болезни Крона.
Остальные типы желез – это их вариации. Железы по кардиальному типу могут проявлять кислото-продуцирующей дифференцировкой в виде рассеянных париетальных клеток, в этот момент железа по существу сопоставима с аналогичными железами, обнаруженными в переходной слизистой оболочке угла желудка или пилорического отдела желудка (обратите внимание, что вопреки распространенному мнению, париетальные клетки не ограничены слизистой оболочкой тела желудка и в изобилии встречаются в нормальной пилорической зоне слизистой желудка человека). Зрелые главные клетки могут также быть найдены в этих железах, которые указывают на полный набор типов клеток, нормально найденных в теле и своде желудка, хотя нерегулярное расположение этих желез ясно показывает, что это не родная, поствоспалительная слизистая оболочка.
Действительно, во многих случаях эти железы могут быть найдены в контексте однозначных ориентиров анатомического пищевода, таких как подслизистые комплексы желез, что позволяет предположить, что эти железы фундального типа развились как часть метапластической мозаики.
Независимо от того, развиваются ли эти метапластические кислото-продуцирующие железы из кардиальных желез, и, если это так, то представляют ли они истинные метаплазии стволовых клеток, или являются проявлением переменных уровней дифференцировки кислото-продуцирующих желез, они предполагают гибкие уровни дифференцировки этих архетипических желудочных желез с важными последствиями для динамики железистой метаплазии в атрофической слизистой желудка.
Наконец, можно увидеть железы, демонстрирующие зрелую кишечную дифференцировку, для которой характерны клетки Панета в основании железы и энтероциты вдоль поверхностного криптового отсека. Эти железы единственные, которые совершенно лишены желудочного муцинового основного пептида и, также являются самыми редкими из всех типов желез описанных выше, хотя пациенты с обильной дифференциацией клеток Панета изредка встречаются.
Цилиндрическая метаплазия пищевода что это такое
Мерзляков М. В., Шапкин. А. А., Перминов А. А., Хапаева Т. Н., Бураго А. Ю.
ГАУЗ Кемеровская областная клиническая больница
ГБОУ ВПО Кемеровская государственная медицинская академия
ГУЗ Кемеровское патологоанатомическое бюро
г. Кемерово
Введение:
Распространенность гастроэзофагеальной рефлюксной болезни (ГЭРБ) в России среди взрослого населения составляет от 17 до 60 % (Минушкин О. Н., 2008). У 45–80 % пациентов ГЭРБ обнаруживается эзофагит различной степени выраженности (Васильев Ю. В., 2001)
В 90 — Х годах 20 столетия в странах Европы и США число пациентов с тяжелыми рефлюкс-эзофагитами увеличилось в 3 раза (Буеверов А. О., Лапина Т. Л., 2006).
Грыжа пищеводного отверстия диафрагмы достаточно частая причина развития гастроэзофагеальной рефлюксной болезни. По данным W. Wienbeck и j. Bamert (1989), хиатальная грыжа обнаруживается у 50 % обследуемых в возрасте старше 50 лет и у 63–84 % из них эндоскопически определяются признаки рефлюкс-эзофагита.
Под хиатальной грыжей принято понимать смещение желудка, а иногда и других органов брюшной полости, через расширенное пищеводное отверстие диафрагмы в заднее средостение.
По частоте встречаемости: аксиальная хиатальная грыжа (99,2 %), параэзофагеальная грыжа (0,4 %), короткий пищевод (0,4 %). Осложнения от общего числа больных ГЭРБ: стриктуры пищевода (7–23 %), язвенные поражения (5 %), кровотечения из эрозий и язв (2 %), пищевод Баррета (8–13 %), аденокарцинома пищевода (0,5–8 %). (Маева И. В., Вьюченкова М. И. (2004), Буркова С. Г. (2008)
Аденокарцинома пищевода и дисплазия высокой степени развивается: 0,4–0,6 % при кишечной метаплазии, 0,5 % при низкой степени дисплазии эпителия, 6 % при дисплазии высокой степени, менее чем у 0,1 % — без дисплазии.
Пищевод Барретта — состояние метапластического цилиндрического эпителия в пищеводе, под воздействием агрессивного желудочного содержимого приводящее к развитию аденокарциномы пищевода. Доказано, что только кишечная метаплазия единственный тип цилиндрического эпителия в пищеводе, достоверно предрасполагающий к малигнизации. Существуют работы демонстрирующие, что кардиальный тип эпителия в пищеводе так же может приводить к малигнизации, однако риск этого остается не выясненным.
В настоящее время нет достаточно данных, чтобы сделать значимые рекомендации по ведению пациентов с исключительно кардиальным типом эпителия в пищеводе, и не рекомендуется использовать термин «пищевод Барретта” для этих пациентов.
При длительном применении ингибиторов протонной помпы (ИПП) возможно обратное развитие из кишечного в многослойный плоский эпителий (Gore S, Healey CJ, Sutton R et al.. Ailment Pharmacol Therap 1993). Применение ингибиторов протоновой помпы, неспецифических противовоспалительных средств, статинов снижает риск развития аденокарциномы (Nguyen DM Gastroenterology. 2010 Jun;138 (7):2260–6. Epub 2010 Feb 23.).
Патологоанатомические критерии, используемые для различения степени дисплазии от пищевода Барретта без дисплазии, при наличии воспаления пищевода, основаны в первую очередь на степени архитектурных и цитологических отклонений, весьма субъективны. В настоящее время нет четко определенных критериев для дифференцировки степени дисплазии. (American Gastroenterological Association Medical Position Statement on the Management of Barrett’s Esophagus. Gastroenterology. 2011;140:1–1091.) В связи с этим, при выявлении дисплазии при пищеводе Барретта рекомендуется повторное исследование с забором биоптатов по протоколу, после курса лечения ГЭРБ.
Внутрипросветное эндоскопическое лечение безопасная и эффективная альтернатива традиционному хирургическому лечению, для пациентов с пищевом Барретта и дисплазией высокой степени (Menon et al. BMC Gastroenterology 2010). Современные подходы к лечению пищевода Барретта: абляция слизистой оболочки, резекция слизистой оболочки, диссекция слизистой оболочки. Аргоноплазменная коагуляция в сочетании с интенсивным подавлением кислоты — эффективный метод лечения при пищеводе Барретта (Pereira-Lma J. C.Am J Gastroenterol. 2000)
Рекомендуется комбинация аргоноплазменной коагуляции и энтирефлюксной хирургии при лечении пищевода Барретта (Tigges H., Fuchs K. H., Maroske J. et al J Gastrointest Surg. 2001). Электрохирургический, монополярный, бесконтактный метод воздействия на биологические ткани высокочастотным током с помощью ионизированого аргона. По разным данным (Madisch A. 2005, Mork H. 2007) эффективность составляет 87–98 % повторный рецидив 12–66 %.
Возможные осложнения:
Дисфагия, боль, пневмомедиастинум без видимой перфорации, реактивный плеврит.
Пациенты и методы:
2011–2014 годах в Клинике хирургии ГАУЗ КОКБ пролечен 21 пациент с наличием дисплазии в области зубчатой линии при наличии гастроэзофагеальной рефлюксной болезни. Женщин 15, возраст 27–74 года. Мужчин 6, возраст 32–66 лет.
19 пациентам выполнены лапароскопические фиксирующие операции в различных модификациях. Эзофагокардиофундопликация по Дору 3 человека. Парциальная циркулярная эзофагофундопликация по Ниссену (floppy-Nissen) 8 пациентов. Задняя и передняя крурорафия в варианте с эзофагокардиофундопликацией (по Дору или Ниссену) 5 пациентам. Протезирование пищеводного отверстия диафрагмы протезом «экофлон», «surgipro» 1 пациенту. Низведение желудка в сочетании с крурораффией (задней, передней и задней, протезированием пищеводного отверстия диафрагмы протезом, и эзофагокардиофундопликацией по Дору, Ниссену 2 пациентам.
Два пациента пролечены только медикаментозно из-за наличия противопоказаний к проведению анестезиологического пособия.
У всех пациентов площадь очагов метаплазии не превышала ультракороткий — с распространением метаплазии менее чем на 1 см проксимальнее уровня истинного кардиоэзофагеального перехода. Кардиальный тип метаплазии эпителия наблюдали у трёх оперированных пациентов и одного не оперированного пациента. Фундальный тип метаплазии циллиндроклеточного эпителия был у 12 оперированных и одного не оперированного пациента. Истинный пищевод Барретта с кишечным типом метаплазии и низкой степенью дисплазии был у двух пациентов, оба пациента подверглись хирургической антирефлюксной коррекции. Вторичные изменения пищевода (эндоскопические признаки укорочения пищевода) наблюдались у 2 пациентов с клиническими проявлениями ГЭРБ более 10 лет.
Антирефлюксную хирургическую коррекцию выполняли через 2 месяца стандартной медикаментозной терапии ГЭРБ. Аргоноплазменную абляцию выполняли через 6 месяцев после хирургического лечения. Проводилась местная анестезия 2 % раствором лидокаина 2.0 мл. Использовался видеогастроскоп Olympus НL 180 с возможностью узкоспектрального светового излучения, инструментальным каналом 2,3 мм. Аргоноплазменная установка Soring в режиме потока газовой смеси 35 литров в минуту, со стандартным аргоновым зондом. Под визуальным контролем, в синем спектре светового излучения, проводилась бесконтактная абляция очагов метаплазии по достижении посткоагуляционного струпа.
Повторный осмотр проводился через 2 месяца после абляции, в режиме узкого спектра светового излучения с инстилляцией 1,5 % раствора уксусной кислоты, всем пациентам проведена биопсия из любого патологически измененного участка слизистой оболочки, включая эрозии, язвы, полиповидные, узловые изменения или стриктуры, согласно «Клиническим рекомендациям» профильной комиссии по специальности «Гастроэнтерология» МЗ РФ. Рецидивов возникновения метаплазии пищеводного циллиндрического эпителия не отмечено.
Осложнений после аргоноплазменной деструкции очагов метаплазии в нашей практике не отмечено
Выводы:
Аргоноплазменная деструкция недорогой, доступный метод лечения пищевода Барретта.
Для стойкого клинического эффекта деструкции очагов метаплазии, предварительно должна проводится антирефлюксная хирургическая коррекция, после общепринятой медикаметозной терапии.
При наличии ГЭРБ и отсутствии хиатальной грыжи алгоритм ведения пациента должен начинаться с медикаментозной терапии, вторым этапом проводится аргоновая абляция