Гемоглобин
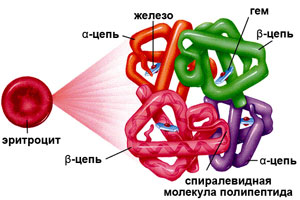
Строение гемоглобина
Гемоглобин состоит из двух цепей глобина типа альфа и двух цепей другого типа (бета, гамма или сигма), соединенными с четырьмя молекулами гемма, содержащего железо. Структура гемоглобина записывается буквами греческого алфавита: α2γ2.
Обмен гемоглобина
Гемоглобин образуется эритроцитами в красном костном мозге и циркулирует с клетками в течение всей их жизни – 120 дней. Когда селезенкой удаляются старые клетки, компоненты гемоглобина удаляются из организма или поступают обратно в кровоток, чтобы включиться в новые клетки.
Типы гемоглобина
К нормальным типам гемоглобина относится гемоглобин А или HbA (от adult — взрослый), имеющий структуру α2β2, HbA2 (минорный гемоглобин взрослого, имеющий структуру α2σ2 и фетальный гемоглобин (HbF, α2γ2. Гемоглобин F – гемоглобин плода. Замена на гемоглобин взрослого полностью происходит к 4-6 месяцам (уровень фетального гемоглобина в этом возрасте менее 1%). Эмбриональный гемоглобин образовывается через 2 недели после оплодотворения, в дальнейшем, после образования печени у плода, замещается фетальным гемоглобином.
Функция гемоглобина
Основная функция гемоглобина – доставка кислорода от легких к тканям и углекислого газа обратно.
Формы гемоглобина
Эффект был описан датским физиологом Христианом Бором http://en.wikipedia.org/wiki/Christian_Bohr (отцом знаменитого физика Нильса Бора).
Христиан Бор заявил, что при большей кислотности (более низкое значение рН, например, в тканях) гемоглобин будет меньше связываться с кислородом, что позволит его отдать.
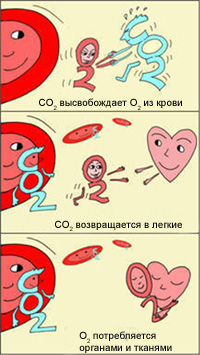
В легких, в условиях избытка кислорода, он соединяется с гемоглобином эритроцитов. Эритроциты с током крови доставляют кислород ко всем органам и тканям. В тканях организма с участием поступающего кислорода проходят реакции окисления. В результате этих реакций образуются продукты распада, в том числе, углекислый газ. Углекислый газ из тканей переносится в эритроциты, из-за чего уменьшается сродство к кислороду, кислород выделяется в ткани.
Эффект Бора имеет громадное значение для функционирования организма. Ведь если клетки интенсивно работают, выделяют больше СО2, эритроциты могут снабдить их большим количеством кислорода, не допуская кислородного «голодания». Следовательно, эти клетки могут и дальше работать в высоком темпе.

В каждом миллилитре крови содержится около 150 мг гемоглобина! Уровень гемоглобина меняется с возрастом и зависит от пола. Так, у новорожденных гемоглобин значительно выше, чем у взрослых, а у мужчин выше, чем у женщин.
Что еще влияет на уровень гемоглобина?
Некоторые другие состояния также влияют на уровень гемоглобина, например, пребывание на высоте, курение, беременность.
С какими газами воздуха гемоглобин образует соединения
Мы, рискуя навлечь справедливые нарекания, позволим себе заявить, что основными системами, обеспечивающими поддержания жизнедеятельности больного при критических состояниях, являются системы органов дыхания и кровообращения. Это утверждение в аспекте тематики настоящей монографии становится обоснованным, если учесть, что при современном уровне интенсивной терапии критических состояний основное внимание реаниматолога направлено на поддержание или протезирование функций именно данных систем.
Поэтому-то большинство методов мониторинга при критических состояниях направлены на регистрацию функциональных параметров газообмена и гемодинамики.
Далее мы намеренно ограничили изложение физиологии и патологии дыхания и кровообращения только освещением вопросов, связанных с газообменной функцией организма, поскольку именно она является основным объектом мониторинга критических состояний. Поэтому основное внимание будет посвящено проблеме газотранспортной функции органов дыхания, крови и насосной функции сердца, обеспечивающих транспорт газов. В связи с этим изложение материала было разделено на две части.
Первая глава посвящена физиологии и патологии газотранспортной функции крови и системы органов дыхания, вторая — насосной функции сердца — основному механизму, обеспечивающему транспорт газов к органам и тканям.
Детальное описание физиологии и патологии дыхания и кровообращения можно найти в известных монографиях отечественных и зарубежных авторов, посвященных тщательному анализу основных вопросов этой проблемы и на нашем сайте МедУнивер.
В плазме крови при нормальном атмосферном давлении кислород растворен в минимальных количествах, всего в 0,03% (9 мл на 3 литра циркулирующей крови).
В эритроцитах крови находится сложное белковое вещество — гемоглобин, которое, в свое время, великий английский физиолог Дж.Баркрофт назвал «чудесным». Своеобразие этого вещества состоит в том, что, во-первых, оно обладает повышенным сродством к кислороду (1 грамм гемоглобина способен присоединить 1,34-1,37 мл кислорода) и при нормальном содержании гемоглобина 150 г 1 л крови может связать около 200 мл кислорода.
Во-вторых, степень сродства гемоглобина к кислороду меняется в зависимости от парциального давления (напряжения) кислорода. Чем меньше напряжение кислорода, тем больше к нему сродство гемоглобина и тем быстрее он присоединяет кислород.
Эта особенность гемоглобина имеет большой физиологический смысл. При напряжении кислорода в 27 мм Нд гемоглобин насыщается кислородом на 50%, а при напряжении кислорода 60-70 мм Нд гемоглобин почти полностью насыщен кислородом. Отсюда следует, что транспорт кислорода полностью обеспечивается даже в случае 30-40% дефицита поступающего в организм кислорода. Поистине Дж. Баркрофт был прав, назвав гемоглобин чудесным веществом.
Углекислый газ находится в плазме крови в виде раствора и в химической связи в виде легко диссоциирующего гидрокарбоната натрия. Растворимость углекислоты приблизительно в 20 раз больше, чем у кислорода, в связи с этим ее транспорт осуществляется в основном путем диффузии из плазмы.
Однако при некоторых состояниях, сопровождающихся недонасыщением крови кислородом (гипоксемия), традиционный транспорт углекислого газа может дополняться и транспортом в связанном состоянии с гемоглобином.
С какими газами воздуха гемоглобин образует соединения
В учебнике в соответствии с программой представлены все разделы физиологии человека. Наиболее полно изложены главы «Вегетативная нервная система», «Железы внутренней секреции», «Центральная нервная система», «Анализаторы». В главе «Физиология дыхания» дается новая полная классификация гипоксии, созданная одним из авторов. В учебнике впервые излагаются основы физиологических функций организма в связи с данными по фармакологической коррекции их нарушений. Для студентов медицинских и биологических факультетов и медицинских институтов, обучающихся по специальностям «Лечебное дело», «Стоматология» и «Фармация».
Николай Александрович Агаджанян
Сокращения в тексте
Глава 1. История физиологии. Методы физиологических исследований
Глава 2. Физиология возбудимых тканей
Биоэлектрические явления в возбудимых тканях. Природа возбуждения
Изменения мембранного потенциала. Пороговые и подпороговые раздражители
Изменения возбудимости при возбуждении
Законы раздражения возбудимых тканей
Физиология нервов и нервных волокон
Механизм мышечного сокращения
Фармакологические влияния на возбудимые ткани
Глава 3. Физиология центральной нервной системы
Организация нервной системы
Общие закономерности деятельности центральной нервной системы
Рефлекторный принцип регуляции
Торможение в центральной нервной системе и его виды
Классификация видов торможения
Принципы координационной деятельности центральной нервной системы
Частная физиология центральной нервной системы
Нейроны спинного мозга
Собственные функции спинного мозга
Проводниковая функция спинного мозга
Собственные функции продолговатого мозга
Вегетативные функции продолговатого мозга
Проводниковые функции продолговатого мозга
Собственные функции варолиева моста
Проводниковая функция варолиева моста
Проводниковая функция гипоталамуса
Собственные функции гипоталамуса
Функции лимбической системы
Кора больших полушарий
Локализация функций в коре больших полушарий
Электрическая активность коры головного мозга
Функции гематоэнцефалического барьера
Факторы, повышающие проницаемость гематоэнцефалического барьера
Особенности морфологического строения гематоэнцефалического барьера
Фармакологические препараты, регулирующие функцию центральной нервной системы
Глава 4. Вегетативная (автономная) нервная система
Различия между вегетативной и соматической нервными системами
Структура и функции вегетативной нервной системы
Симпатический отдел вегетативной нервной системы
Парасимпатический отдел вегетативной нервной системы
Внутриорганный отдел (энтеральный, метасимпатический)
Медиаторы вегетативной нервной системы
Вегетативные (автономные) рефлексы
Центры регуляции вегетативных функций
Средства, влияющие на синаптическую передачу
Глава 5. Железы внутренней секреции
Общая физиология желез внутренней секреции
Механизмы действия гормонов.
Регуляция функций желез внутренней секреции
Частная физиология желез внутренней секреции
Гормоны передней доли гипофиза
Гормоны задней доли гипофиза
Околощитовидные (паращитовидные) железы
Гормоны коры надпочечников
Гормоны мозгового слоя надпочечников
Мужские половые гормоны (андрогены)
Женские половые гормоны
Овариально-менструальный (менструальный) цикл
Гормональные средства, используемые в фармакологические целях
Глава 6. Физиология крови
Основные функции крови
Объем и физико-химические свойства крови
Кислотно-основное состояние крови (КОС).
Форменные элементы крови
Гемоглобин и его соединения
Скорость оседания эритроцитов (СОЭ)
Фармакологическая коррекция нарушений гемопоэза и гемостаза
Средства, влияющие на гемопоэз
Средства, влияющие на гемостаз
Глава 7. Крово- и лимфообращение
Свойства сердечной мышцы
Электрическая активность клеток миокарда и проводящей системы сердца
Проводимость и сократимость
Классификация сосудов. Основы гемодинамики
Транссосудистый обмен веществ
Движение крови в венах
Нейрогуморальная регуляция кровообращения
Регуляция деятельности сердца
Внутрисердечные механизмы регуляции
Характер влияний блуждающих и симпатических нервов на работу сердца
Гуморальная регуляция деятельности сердца
Регуляция тонуса сосудов
Местные регуляторные механизмы
Центральные механизмы регуляции
Гуморальная регуляция сосудистого тонуса
Рефлекторная регуляция деятельности сердца и сосудистого тонуса
Методы исследования сердечно-сосудистой системы
Регуляция коронарного кровотока
Функции лимфатической системы
Нервная регуляция лимфообразования
Гуморальная регуляция лимфотока и лимфообразования
Фармакологическая коррекция нарушений некоторых физиологических показателей системы кровообращения
Средства, влияющие на возбудимость, проводимость сердечной мышцы и ритм сердечных сокращений
Средства, влияющие на сократимость сердечной мышцы
Средства, улучшающие коронарный кровоток и метаболизм миокарда
Средства, нормализующие кровяное давление
Средства, влияющие на метаболизм сосудистой стенки и ее проницаемость
Глава 8. Физиология дыхания
Состав и свойства дыхательных сред
Внутриплевральное и внутрилегочное давление
Вентиляция легких и легочные объемы
Газообмен и транспорт газов
Регуляция внешнего дыхания
Локализация и функциональные свойства дыхательных нейронов
Рефлекторная регуляция дыхания
Рефлексы с проприорецепторов дыхательных мышц
Гуморальная регуляция дыхания
Дыхание в измененных условиях
Дыхание при высоком атмосферном давлении
Патологические типы дыхания
Негазообменные функции воздухоносных путей и легких
Фармакологическая коррекция патологии органов дыхания
Глава 9. Пищеварение
Функции желудочно-кишечного тракта
Общие принципы регуляции процессов пищеварения
Гемоглобин и его соединения



Гемоглобин (Нв) – основной компонент эритроцитов, благодаря которому эритроциты выполняют дыхательную функцию и поддерживают рН крови. По химической природе он относится к хромопротеидам. У мужчин в крови содержится в среднем 130-160 г/л гемоглобина, у женщин – 120-150 г/л. Молекулярная масса гемоглобина составляет около 60000 Да. Гемоглобин состоит из белка глобина и 4 молекул гема. Гем имеет в своем составе атом железа, способный присоединять или отдавать молекулу кислорода.
В скелетных и сердечной мышцах находится мышечный гемоглобин, называемый миоглобином. Он играет важную роль в снабжении кислородом работающих мышц, его можно рассматривать, как депо О2 в мышцах.
Имеется несколько форм гемоглобина, отличающихся строением белковой части – глобина. Первые 7-12 нед. внутриутробного развития зародыша его красные кровяные тельца содержат примитивный гемоглобин. У плода содержится гемоглобин F (80 %) или фетальный гемоглобин (от англ. Faetus – плод) гемоглобин. Он обладает более высокой способностью связывать кислород. Это помогает плоду не испытывать гипоксии при относительно низком парциальном напряжении кислорода в его крови. После рождения гемоглобин F практически полностью заменяется на взрослый – гемоглобин А (от англ. adult – взрослый). В эритроцитах взрослого человека содержатся гемоглобин А (95-98 % Hb A1 и 2-3 % HbA2 ).
Гемоглобин может вступать в соединение и с другими газами. Соединение гемоглобина с угарным газом (СО) называется карбоксигемоглобином — это патологическое соединение, в норме его не существует, т.к. в атмосфере отсутствует СО. Является прочным соединением. Гемоглобин блокирован в нем угарным газом и не способен осуществлять перенос кислорода. Сродство гемоглобина к угарному газу выше его сродства к кислороду, поэтому даже небольшое количество угарного газа в воздухе является опасным для жизни. При этом более критическим является не концентрация угарного газа, а длительность его вдыхания. Даже предельно низкое содержание СО в воздухе, но при длительном вдыхании, например, во время сна может оказаться летальным. Вследствие своего высокого сродства угарный газ в виде карбоксигемоглобина способен циркулировать в крови предельно долго.
Часто отравления угарным газом возникают у водителей при длительном нахождении в закрытом гараже с включенным двигателем автомобиля. Другим распространенным клинически значимым источником СО являются древесный дым, а также сырой кирпич печей изб и свежий печной лак. Поэтому при первом или после длительного перерыва протапливании таких печей необходимо тщательное проветривание помещения.
Особенностью угарного газа является то, что он не обладает запахом, поэтому отравление развивается незаметно. Часто пострадавший осознает это, когда проявляется миорелаксирующее (расслабление скелетной мускулатуры) действие угарного газа, при этом человек не может самостоятельно покинуть помещение.

Первая помощь при отравлении угарным газом. Пострадавшего следует переместить на свежий воздух. Следует учитывать, что при значительном отравлении сохранность самостоятельного дыхания не снимает необходимости проведения дальнейших действий по оказанию помощи. Наиболее оптимальным будет подача воздуха с повышенным содержание О2, например, из кислородной подушки. При отсутствии таковой – произвести искусственное дыхание. Во время искусственного дыхания в легкие потерпевшего воздух нагнетается под давлением, большим атмосферного.
При этом парциальное давление О2 в таком воздухе оказывается большим, чем в норме, что способствует его большему растворению в крови, а также лучшему вытеснению угарного газа из связи с гемоглобином. Если же пострадавший будет дышать самостоятельно, парциальное давление О2 во вдыхаемом воздухе окажется меньшим (примерно, 100 мм рт.ст.), что окажется недостаточным для вытеснения из карбоксигемоглобина угарного газа, т. к. сродство Нb к СО значительно выше, чем О2. В дальнейшем пострадавший должен быть доставлен в больницу.
При воздействии на гемоглобин экзогенных сильных окислителей происходит окисление железа гема с переходом его в 3-х валентную форму. В результате этого образуется метгемоглобин, который не способен присоединять ни О2, ни СО2. В результате окисления гемоглобин прочно удерживает кислород и теряет способность отдавать его тканям, что может привести к гибели организма.
К подобным сильным окислителем относятся нитраты и нитриты, содержащиеся, например, в химических удобрениях, также опасность представляют пероксиды, нитрокраски, анилиновые красители и ряд других веществ бытовой химии. В норме ежедневно около 0,5 % всего гемоглобина превращается в метгемоглобин, но затем она снова восстанавливается в гемоглобин специальным ферментом метгемоглобинредуктазой. Встречаются наследственные метгемоглобинемии, когда снижена активность метгемоглобинредуктазы в эритроцитах, что вызывает кислородное голодание. Метгемоглобин, также как карбоксигемоглобин, относится к группе патологических соединений гемоглобина.