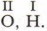§ 13. Валентность химических элементов. Определение валентности в бинарных соединениях
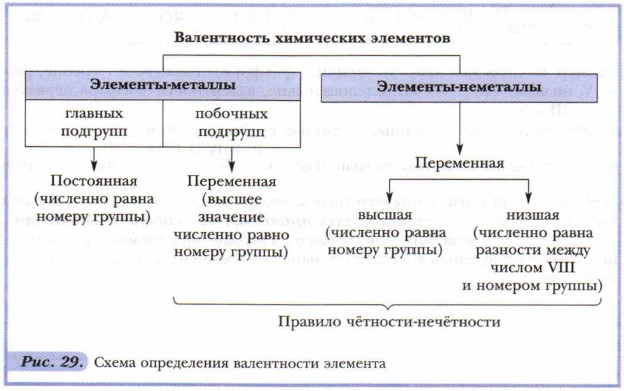
Способность элементов проявлять то или иное значение валентности определяется строением их атомов. Поскольку строение атомов мы будем изучать позднее, научимся определять валентность, исходя из положения элементов в периодической системе (рис. 29, табл. 7).
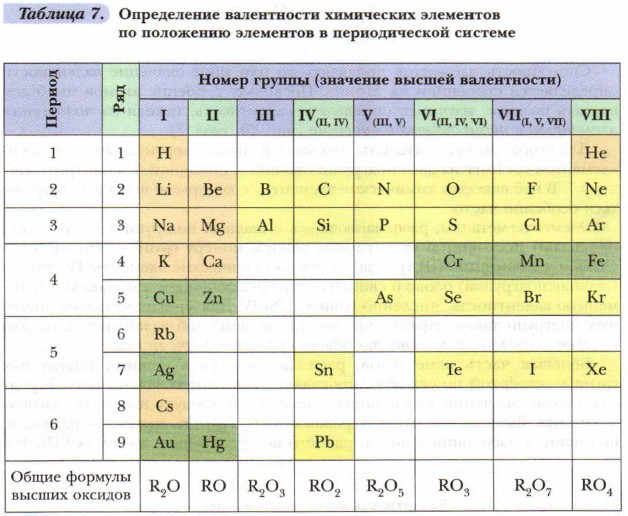
Для этого следует учитывать, что каждая группа (вертикальный столбец) элементов состоит из двух подгрупп: главной и побочной. Рассмотрите таблицу 7. В неё внесены химические элементы, с которыми вы будете встречаться особенно часто.
Элементы-металлы, располагающиеся в главных подгруппах I и II групп, проявляют постоянную валентность, равную номеру группы. Это же относится и к алюминию (III группа). А вот металлические элементы IV группы (главная подгруппа) олово и свинец служат исключением и проявляют переменную валентность, численно равную II и IV. Для многих металлов побочных подгрупп также характерно наличие переменной валентности, однако высшее значение валентности обычно равно номеру группы!
Элементы, расположенные в группах с чётными номерами, проявляют чётные значения валентности 

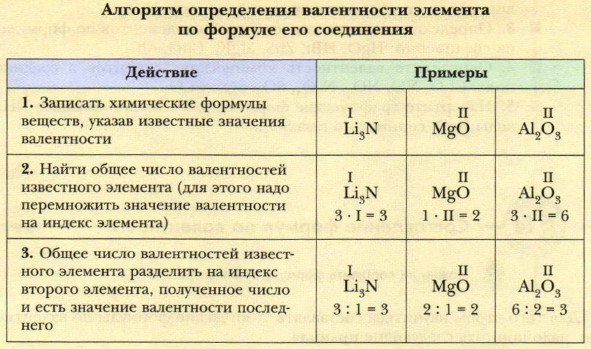
По формуле бинарного (состоящего из атомов двух элементов) соединения можно определить валентность одного из элементов, если известна валентность другого.
1. Валентность — свойство атомов присоединять определённое число других атомов.
2. В зависимости от строения атомов элементы проявляют постоянную или переменную валентность.
3. Металлы главных подгрупп проявляют постоянную валентность, равную номеру группы.
4. Валентность кислорода и водорода постоянна:
5. В случаях переменной валентности высшее её значение равно номеру группы.
6. Для определения значения низшей валентности элементов-неметаллов следует из числа VIII вычесть номер группы.
Валентность: постоянная, переменная • Правило чётности-нечётности





§ 13. Валентность химических элементов. Определение валентности в бинарных соединениях
Способность элементов проявлять то или иное значение валентности определяется строением их атомов. Поскольку строение атомов мы будем изучать позднее, научимся определять валентность, исходя из положения элементов в периодической системе (рис. 29, табл. 7).
Для этого следует учитывать, что каждая группа (вертикальный столбец) элементов состоит из двух подгрупп: главной и побочной. Рассмотрите таблицу 7. В неё внесены химические элементы, с которыми вы будете встречаться особенно часто.
Элементы-металлы, располагающиеся в главных подгруппах I и II групп, проявляют постоянную валентность, равную номеру группы. Это же относится и к алюминию (III группа). А вот металлические элементы IV группы (главная подгруппа) олово и свинец служат исключением и проявляют переменную валентность, численно равную II и IV. Для многих металлов побочных подгрупп также характерно наличие переменной валентности, однако высшее значение валентности обычно равно номеру группы!
Элементы, расположенные в группах с чётными номерами, проявляют чётные значения валентности 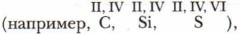
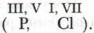
По формуле бинарного (состоящего из атомов двух элементов) соединения можно определить валентность одного из элементов, если известна валентность другого.
1. Валентность — свойство атомов присоединять определённое число других атомов.
2. В зависимости от строения атомов элементы проявляют постоянную или переменную валентность.
3. Металлы главных подгрупп проявляют постоянную валентность, равную номеру группы.
4. Валентность кислорода и водорода постоянна:
5. В случаях переменной валентности высшее её значение равно номеру группы.
6. Для определения значения низшей валентности элементов-неметаллов следует из числа VIII вычесть номер группы.
Валентность: постоянная, переменная • Правило чётности-нечётности





Рассмотрите таблицу 7 какие металлы обладают постоянной валентностью какие элементы первой группы
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1 Рассмотрите таблицу 7. Какие металлы обладают постоянной валентностью?
Металлы, располагающиеся в главных подгруппах I и ІІ групп, а также алюминий, располагающийся в главной подгруппе I ІІ группы, проявляют постоянную валентность, равную номеру группы.
Какие элементы первой группы обладают переменной валентностью?
Медь (Cu), серебро (Ag) и золото (Au) обладают переменной валентностью.
Какую подгруппу они образуют?
Они образуют побочную подгруппу.
Задание 2 Используя таблицу 7, составьте формулы кислородсодержащих соединений известных вам элементов.
І группа: H2O, Li2O, Na2O, K2O, Rb2O, Cs2O
ІІ группа: BeO, MgO, CaO
ІІI группа: B2O3, Al2O3
ІV группа: CO2, SiO2, SnO2, PbO2
V группа: N2O5, P2O5, As2O5
VІ группа: SO3, SeO3, TeO3
VIІ группа: Cl2O7, Br2O7, I2O7
Объяснение: воспользуйтесь общими формулами высших оксидов, располагающиеся в нижней строке таблицы 7.
Как определить валентность.
В этой статье рассмотрим способы и поймем, как определить валентность элементов таблицы Менделеева.
В химии принято, что валентность химических элементов можно узнать по группе (колонке) в таблице Менделеева. В действительности не всегда валентность элемента соответствует номеру группы, но в большинстве случаев определенная валентность по такому методу даст правильный результат часто элементы, в зависимости от разных факторов, имеют не одну валентность.
За единицу валентности принята валентность атома водорода, равная 1, то есть водород одновалентен. Поэтому валентность элемента указывает на то, со сколькими атомами водорода соединён один атом рассматриваемого элемента. Например, HCl, где хлор – одновалентен; H2O, где кислород – двухвалентен; NH3, где азот – трёхвалентен.
Как определить валентность по таблице Менделеева.
Таблица Менделеева содержит в себе химические элементы, которые размещены в ней по определенным принципам и законам. Каждый элемент стоит на месте, который определяется его характеристиками и свойствами и каждый элемент имеет свой номер. Горизонтальные линии называются периодами, которые возрастают от первой строки вниз. Если период состоит из двух рядов (что указано сбоку нумерацией), то такой период называется большим. Если он имеет только один ряд, то называется малым.
Валентностью называют способность атома образовывать некоторое количество химических связей с атомами других элементов. Как определить валентность по таблице Менделеева поможет понять знание видов валентности.
Виды валентности
Постоянная (у металлов главных подгрупп)
Переменная (у неметаллов и металлов побочных подгрупп)
Высшая (равна номеру группы)
Низшая (равна разности между числом 8 и номером группы)
Для элементов побочных подгрупп (а к ним относятся только металлы) валентность нужно запоминать, тем более что в большинстве случае она равна I, II, реже III. Также придется заучить валентности химических элементов, которые имеют более двух значений. Или постоянно держать под рукой таблицу валентности элементов.
Алгоритм определения валентности по формулам химических элементов.
1. Записать формулу химического соединения.
2. Обозначить известную валентность элементов.
3. Найти наименьшее общее кратное валентности и индекса.
4. Найти соотношение наименьшего общего кратного к количеству атомов второго элемента. Это и есть искомая валентность.
5. Сделать проверку путём перемножения валентности и индекса каждого элемента. Их произведения должны быть равны.
Пример: определим валентность элементов сульфида водорода.
2. Обозначим известную валентность:
3. Найдём наименьшее общее кратное:
4. Найдём соотношение наименьшего общего кратного к количеству атомов серы:
Валентность.
Валентность – свойство атомов одного химического элемента присоединять или замещать определённое количество атомов другого.
За единицу валентности принята валентность атома водорода, равная 1, то есть водород одновалентен. Поэтому валентность элемента указывает на то, со сколькими атомами водорода соединён один атом рассматриваемого элемента. Например, HCl, где хлор – одновалентен; H2O, где кислород – двухвалентен; NH3, где азот – трёхвалентен.
Таблица элементов с постоянной валентностью.
Валентности
Элементы
O, Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd
Формулы веществ можно составлять по валентностям входящих в них элементов. И наоборот, зная валентности элементов, можно составить из них химическую формулу.
Алгоритм составления формул веществ по валентности.
1. Записать символы элементов.
2. Определить валентности входящих в формулу элементов.
3. Найти наименьшее общее кратное численных значений валентности.
4. Найти соотношения между атомами элементов путём деления найденного наименьшего общего кратного на соответствующие валентности элементов.
5. Записать индексы элементов в химической формуле.
Пример: составим химическую формулу оксида фосфора.
2. Определим валентности:
3. Найдём наименьшее общее кратное:
4. Найдём соотношения между атомами:
Алгоритм определения валентности по формулам химических элементов.
1. Записать формулу химического соединения.
2. Обозначить известную валентность элементов.
3. Найти наименьшее общее кратное валентности и индекса.
4. Найти соотношение наименьшего общего кратного к количеству атомов второго элемента. Это и есть искомая валентность.
5. Сделать проверку путём перемножения валентности и индекса каждого элемента. Их произведения должны быть равны.
Пример: определим валентность элементов сульфида водорода.
2. Обозначим известную валентность:
3. Найдём наименьшее общее кратное:
4. Найдём соотношение наименьшего общего кратного к количеству атомов серы: