Ферментативный катализ имеет свои особенности
Этапы катализа
В ферментативной реакции можно выделить следующие этапы:
1. Присоединение субстрата (S) к ферменту (E) с образованием фермент-субстратного комплекса (E-S).
2. Преобразование фермент-субстратного комплекса в один или несколько переходных комплексов (E-X) за одну или несколько стадий.
3. Превращение переходного комплекса в комплекс фермент-продукт (E-P).
4. Отделение конечных продуктов от фермента.
Механизмы катализа
1. Кислотно-основной катализ – в активном центре фермента находятся группы специфичных аминокислотных остатков, которые являются хорошими донорами или акцепторами протонов. Такие группы представляют собой мощные катализаторы многих органических реакций.
2. Ковалентный катализ – ферменты реагируют со своими субстратами, образуя при помощи ковалентных связей очень нестабильные фермент-субстратные комплексы, из которых в ходе внутримолекулярных перестроек образуются продукты реакции.
Типы ферментативных реакций
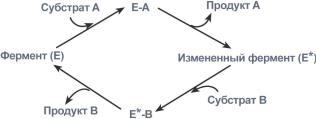
Ферментативная реакция по типу «пинг-понг»
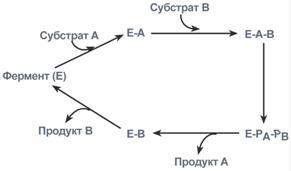
2. Тип последовательных реакций – к ферменту последовательно присоединяются субстраты А и В, образуя «тройной комплекс», после чего осуществляется катализ. Продукты реакции также последовательно отщепляются от фермента.
Ферментативная реакция по типу «последовательных реакций»
3. Тип случайных взаимодействий – субстраты А и В присоединяются к ферменту в любом порядке, неупорядоченно, и после катализа так же отщепляются.
ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ
ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ (биокатализ), ускорение биохим. р-ций при участии белковых макромолекул, называемых ферментами (энзимами). Ферментативный катализ- разновидность катализа, хотя термин «ферментация» (брожение)известен с давних времен, когда еще не было понятия хим. катализа.
Первое исследование ферментативного катализа как хим. процесса было выполнено К. Кирхгофом, к-рый в 1814 продемонстрировал фер-ментативную конверсию крахмала в растворимые углеводы.
Заметный вклад в представление о природе ферментативного катализа внесли работы И. Берцелиуса и Э. Мичерлиха, к-рые включили ферментативные р-ции в категорию хим. каталитич. процессов. В кон. 19 в. Э. Фишер высказал гипотезу о специфичности ферментативных р-ций и тесном стерич. соответствии между субстратом и активным центром фермента. Основы кинетики ферментативных р-ций были заложены в работах Л. Михаэ-лиса (1913).
В 20 в. происходит интенсивное изучение хим. основ ферментативного катализа, получение ферментов в кристаллич. состоянии, изучение структуры белковых молекул и их активных центров, исследование большого числа конкретных ферментативных р-ций и ферментов.
В простейшем случае ур-ние р-ции с участием фермента имеет вид:
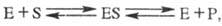
Превращение субстрата в продукт происходит в комплексе Михаэлиса. Часто субстрат образует ковалентные связи с функц. группами активного центра, в т. ч. и с группами кофермента (см. Коферменты). Большое значение в механизмах ферментативных р-ций имеет основной и кислотный катализ, реализуемый благодаря наличию имидазольных групп остатков гистидина и карбоксильных групп дикарбоно-вых аминокислот.
Большинство ферментов обладает высокой субстратной специфичностью, т. е. способностью катализировать превращение только одного или неск. близких по структуре в-в. Специфичность определяется топографией связывающего субстрат участка активного центра.
Активность ферментов регулируется в процессе их биосинтеза (в т.ч. благодаря образованию изоферментов, к-рые катализируют идентичные р-ции, но отличаются строением и каталитич. св-вами), а также условиями среды (рН, т-ра, ионная сила р-ра) и многочисленными ингибиторами и активаторами, присутствующими в организме. Ингибиторами и активаторами могут служить сами субстраты (в определенных концентрациях), продукты р-ции, а также конечные продукты в цепи последоват. превращений в-ва (см. Регуляторы ферментов).
Осн. направления совр. исследований ферментативного катализа- выяснение механизма, обусловливающего высокие скорости процессов, высокую селективность (специфичность действия ферментов), изучение механизмов контроля и регуляции активности ферментов. Оказалось, в частности, что р-ции ферментативного катализа включают большое число стадий с участием лабильных промежут. соед., времена жизни к-рых изменяются в нано- и миллисекундном диапазонах. На активных центрах ферментов протекают быстрые (нелимитирующие) стадии, в результате чего понижается энергетич. барьер для наиб. трудной, лимитирующей стадии.
Установлен механизм регулирования ферментативной активности путем действия ингибитора (или активатора) на специфичный центр белковой молекулы с опосредованной передачей воздействия на активный центр фермента через белок. Обнаружены эффекты кооперативного взаимод. неск. молекул субстрата на белковой матрице. Найден способ «жесткого» выведения фермента из процесса посредством индуцированной субстратом необратимой инактивации.
Ф ерментативный катализ- основа мн. современных хим. технологий, в частности крупномасштабных процессов получения глюкозы и фруктозы, антибиотиков, аминокислот, витаминов и регуляторов, а также тонкого орг. синтеза. Разработаны методы, позволяющие проводить ферментативные р-ции в орг. р-ри-телях, обращенных мицеллах (см. Мицеллообразование). С ферментативным катализом связаны перспективы развития иммуноферментного и биолюминесцентного анализа, применения биосенсоров. Созданы методы, позволившие придать каталитич. активность антителам, обнаружена каталитич. активность у рибонуклеи-новой к-ты (абзимы, рибозимы соотв.).
Лит.: Б е r е з и н И. В., Исследования в области ферментативного катализа и инженерной этимологии, M., 1990. См. также лит. к ст. Биотехнология^ Генетическая инженерия, Ферментативных реакций кинетика, Ферменты.
Ферментативный катализ в биологических системах
Зачастую говоря о витаминах, минералах и других полезных для человеческого организма элементах упоминаются вещества, которые называются ферментами. Что такое ферментативный катализ и как он происходит в организме человека вы узнаете, дочитав эту статью до конца.
Строение атома и химические связи
Вспомним некоторые сведения о строении атомов и природе химических связей, удерживающих атомы в молекуле. Основу строения атома составляют центральное положительно заряженное ядро и вращающиеся вокруг него по орбитам отрицательно заряженные электроны. Самый простой атом (водорода) имеет один электрон, самый тяжелый из встречающихся в природе атомов — атом урана — 92 электрона. Способность атомов различных элементов вступать в реакцию между собой объясняется тем, что они, так сказать, «делятся» электронами своих внешних орбит: возникает пара электронов, общих для «объединяющихся» атомов — через эти общие электроны образуется химическая связь между ними.
Существуют и другие типы связей между атомами, но описанная, так называемая ковалентная связь, является наиболее прочной. Какое действие оказывают вещества, «атакующие» химические связи? Они нарушают распределение внешних электронов, увеличивая силы отталкивания или притяжения. Следствием этого является ослабление или разрыв связей. Электроны перераспределяются, и возникают новые связи.
Взаимодействие молекул
Чтобы молекулы вступили во взаимодействие и перераспределились внешние электроны составляющих их атомов, разорвались одни связи и замкнулись другие, этим им необходимо находиться в достаточно активном состоянии. Известно, что повышение температуры ускоряет химические реакции. Это объясняется тем, что тепловая энергия увеличивает число молекул, находящихся в активированном состоянии. Количество энергии, которое вещества должны получить дополнительно для того, чтобы между ними пошел процесс, называется энергией активизации. Это количество энергии, достаточное для того, чтобы большинство молекул преодолело так называемый энергетический барьер. Когда взаимодействие заканчивается, ее продукты находятся на более низком энергетическом уровне, чем исходные вещества, то есть в более устойчивом состоянии.
Как работают катализаторы?
Сущность действия катализаторов состоит в том, что они понижают энергетический барьер реакции, направляют ее как бы в обход этого барьера.
Представьте себе лыжника, стоящего перед лестницей к трамплину, с которого ему предстоит прыгнуть. Чтобы начать спуск, ему необходимо предварительно затратить некоторое количество энергии, для попадания на площадку перед трамплином. И тогда ему хватит небольшого толчка, для полета.
Теперь допустим, что перед нашим лыжником имеется ровная тропинка, ведущая на спуск с трамплина в обход лестницы. Чтобы начать спуск, пройдя этой тропинкой, ему требуется гораздо меньшая затрата энергии, чем для подъема на площадку по лестнице; стоящий перед ним энергетический барьер окажется менее высоким. Но при этом величина свободной энергии спуска будет такой же, как при спуске с площадки.
Для чего нужны ферменты и что такое ферментативный катализ
Ферментативный катализ отличается от катализа неферментативного тремя важными особенностями.
Первая — это большая специфичность ферментов (катализаторов). Если катализатор-нефермент, так сказать, облегчает осуществление множества различных хим. реакций, убыстряя их, то фермент катализирует химические превращения веществ, имеющих строго специфическое строение и не оказывает воздействие на остальные субстраты (вещества, химические превращения которых катализируются определенным ферментом).
Вторая – заключается в том, что ферменты действуют при мягких условиях внешней среды. Они не требуют высоких температур, резко кислой или очень щелочной реакции среды, повышенного во много раз давления — условий, при которых невозможна жизнь.
Третья – чрезвычайно высокая молекулярная активность ферментов; 1 молекула фермента катализирует за 1 минуту превращения множество молекул субстрата. Под действием биологических катализаторов — ферментов реакции идут в десятки тысяч, подчас в миллионы раз быстрей, чем под влиянием неорганических-катализаторов.
Ферментативный катализ по эффективности более высок по сравнению с неорганическими. Это объясняется тем, что он сильней уменьшает энергию активации. Также эффективней облегчается преодоление энергетического барьера реакции, увеличивает число активированных, способных к реакции молекул, и потому ее ускоряет.
Ферментативный катализ на первое его стадии заключается в том, что фермент соединяется с субстратом и образуется фермент-субстратный комплекс.
Формирование и последующее превращения фермент-субстратного комплекса разделяют на несколько стадий:
Освободившаяся молекула фермента способна вновь вступать в оборот — соединяться с новой порцией субстрата.
Непосредственное участие в каталитическом действии принимает не вся молекула фермента, а лишь часть ее, которая называется активным центром фермента. Важнейшая составная часть активного центра — его каталитически активный участок, непосредственно взаимодействующий с субстратом. Наряду с этим принято выделять в составе активного центра так называемый контактный, или якорный участок (площадку), который обеспечивает связывание фермента с субстратом. Для многих ферментов уже выяснено, какие аминокислоты входят в состав их активных центров.
Как происходит ферментативный катализ на химическом уровне
Как протекает ферментативный катализ изучен еще не до конца, в частности не совсем ясно, каким образом активируется субстрат, какой вид приобретает его молекула в том активированном, переходном состоянии, при котором облегчен разрыв и замыкание связей в молекуле. Одни из объяснений дает так называемая теория деформации субстрата.
Возьмем соединение А—В. Связь между A и В разорвана с присоединением к А—В молекулы воды. При этом вода присоединяется таким образом, что за счет освободившейся валентности к А присоединяется одна часть молекулы воды — группа ОН (гидроксильная группа), а к молекуле В — второй атом водорода, входивший в молекулу воды. Такой тип химических реакций называется реакциями гидролиза — распад молекулы с присоединением к продуктам распада остатков молекулы воды. Ферменты, катализирующие такой тип реакции, называют гидролитическими ферментами. К такому типу реакций относятся реакции расщепления белков, углеводов и жиров в органах пищеварения. Например, молекула обычного сахара состоит из двух простых сахаров: глюкозы и фруктозы, соединенных между собой.
Если связь между ними с присоединением воды разорвется, молекула сахарозы расщепится на молекулу глюкозы и молекулу фруктозы. Таким образом, под соединением А—В мы можем подразумевать сахарозу, под А — глюкозу и под В — фруктозу. Реакция гидролиза сахарозы катализируется ферментом сахаразой, который является каталитически активным белком.
При соединении субстрата (сахарозы) с ферментом он располагается в соответствующих участках молекулы последнего таким образом, что связь между частями А и В (остатками глюкозы и фруктозы) в молекуле (сахарозы) растягивается наподобие того, как растягивали тело пытаемого человека на дыбе средневековые палачи (отсюда название «теория дыбы»); связь эта становится рыхлой. В силу происходящей при этом деформации, изменения конфигурации (как принято говорить, конформации) молекулы субстрата (сахарозы), в ней перераспределяются электроны, и это приводит к изменению расположения электрических зарядов. В итоге этого связь между А и В разрывается и при этом по освободившимся связям к обломку А присоединяется ОН, а к обломку В — водород. Источником гидроксила и водорода служит молекула воды. Сахароза распалась на глюкозу и фруктозу.
Ферментативный катализ хорошо объясняется теорией «дыбы». Для других типов подобных реакций механизм активирующего влияния фермента на субстрат менее ясен.
Как происходит ферментативный катализ в организме человека
По местам освободившихся связей к молекуле субстрата или ее остатку могут присоединяться другие атомы или группа атомов — синтезируются новые соединения. Такие реакции катализируются особым классом ферментов — синтетазами. Отщепившиеся от молекулы атомы и их группы за счет действия ферментов, именуемых трансферазами, могут быть перенесены на молекулы других соединений с образованием при этом новых молекул.
За счет действия ферментов, называемых оксидоредуктазами, продукты расщепления белков, углеводов, жиров подвергаются глубокому распаду путем их окисления. В результате такого процесса углерод пищевых веществ окисляется до углекислоты, водород — до воды, азот восстанавливается до аммиака. Те продукты обмена веществ (метаболиты), которые в организме подвергаются далее тем или иным превращениям, называются промежуточными продуктами, а те что дальнейшим превращениям не подвергаются, а удаляются из организма являются конечными.
Например: крахмал пищи под действием пищеварительных ферментов подвергается гидролизу, расщепляясь при этом на большое число молекул глюкозы. Глюкоза поступает в клетки тела. В них она подвергается многочисленным превращениям, в ходе которых она преобразуется в различные необходимые организму продукты: холестерин, гормоны и многие другие. Основная же масса продуктов распада глюкозы в итоге многоэтапных превращений, на разных стадиях катализируемых различными ферментами, вступает в конце концов в окислительно-восстановительные реакции и полностью окисляются до углекислоты и воды. В ходе этого окисления глюкозы освобождается необходимая для жизнедеятельности энергия.
Вообще процессы распада пищевых веществ идут с освобождением энергии. Такие реакции называются экзэргоническими. Процессы биологического синтеза протекают с потреблением энергии и называются эндэргоническими. Наиболее эффективный способ освобождения энергии пищевых веществ — глубокий их распад путем окисления. Энергия для этих процессов используется организмом как для производства различных видов работы (сокращение мышц и др.), так и для процессов биосинтеза.
Вывод
Таким образом, превращение того или иного вещества в организме является многоступенчатым процессом, требующим для каждого этапа действия соответствующих ферментов. По современным данным, в одной клетке нашего тела содержится в среднем 100 000 молекул ферментов, при помощи которых осуществляется 1—2 тысячи различных химических реакций. Следовательно, на одну реакцию приходится 50—100 молекул ферментов. Синтез или распад того или иного продукта обеспечивается своего рода ферментной системой. Продукт предшествующей ферментативной реакции служит субстратом для действия следующего фермента этого конвейера. Многоступенчатым, «поточным» является и синтез того или иного вещества в организме.
На это мы закончим. В этой статье по подробно разобрали что такое ферментативный катализ и как он происходит. Если вам статья понравилась и стала полезной, поделитесь ей со своими знакомыми и друзьями в соц сетях.
Ферментативный катализ | Биокатализ
Высокоизбирательные активные катализаторы для экологически чистой химии
Что такое ферментативный катализ или биокатализ?
Под биокатализом, или ферментативным катализом, понимается применение биологически активных соединений для ускорения химических превращений. Биокатализ ускоряет различные реакции, где основным компонентом выступают соединения на основе углерода. Эти реакции происходят в различных средах: от бесклеточных, протекающих полностью in vitro, до опосредованных ферментацией процессов в культуре живых клеток.
Биокатализ может стать полезной альтернативой обычному химическому катализу по ряду причин. Ферментативные биокаталитические реакции:
Направленная разработка биокатализаторов улучшает их стабильность в растворителях при повышенной температуре, обеспечивая широкое применение биокатализа в фармацевтической, химической, биотопливной и пищевой промышленности.
В чем ценность ферментативного катализа?
Биокатализ относится к области «зеленого», экологически ответственного и рентабельного производства химических продуктов. В отличие от химического катализа, биокатализаторам изначально присущи определенные преимущества с точки зрения синтеза:
Ферменты-биокатализаторы обладают важными, свойствами, которые часто оказываются полезны и включают:
A) Связывание и распознавание других биопрепаратов или малых молекул, сайт-специфичное или по функциональным группам
B) Облегчение ассоциации или вытеснения других биопрепаратов или малых молекул
C) Структурные или электростатические свойства, облегчающие перенос ионов
D) Способность к преобразованиям с изменением степени упорядоченности и, следовательно, каталитической активности
E) Аллостерические и непрямые модификации, которые индуцируют или подавляют активность ферментов
Исследования улучшенных или модифицированных рекомбинантных биокатализаторов продолжают расширять возможности их применения в агрессивных химических средах, улучшать условия проведения реакции, устойчивость ферментов и возможность их повторного использования. В настоящее время имеются природные и искусственно созданные биокатализаторы для таких важных химических превращений, как образование связей C — C, амидных связей, образование хиральных аминов и функционализация C — H.
Биокатализ, ферменты и биотрансформации
Сфера применения ферментов-биокатализаторов чрезвычайно широка и охватывает практически все отрасли, включая пищевую промышленность, фармацевтику, производство текстиля, биотоплива, бумаги, бытовой химии и товаров для дома. В тонком химическом синтезе, химии фармацевтических препаратов и связанных с ними промежуточных продуктов биокатализ (ферментативный или ферментно-опосредованный катализ) быстро стал передовой технологией. Имеются ферменты для различных биотрансформаций, таких как окисление, восстановление, присоединение и отщепление.
Шесть основных классов ферментов и примеры их использования:
1. Оксидоредуктазы — ферменты, катализирующие окислительно-восстановительные реакции. Монооксигеназы, катализирующие реакции присоединения одного атома кислорода, позволяют образовывать связи C — O. Разработаны специальные ферменты для окисления спиртов, кетонов, альдегидов и аминов. Что касается восстановления, то кеторедуктазы (KREDS) и дегидрогеназы позволяют синтезировать энантиоспецифичные спирты. Другие ферменты восстанавливают группы, такие как C = N, превращая нитрилы в амины.
2. Трансферазы применяются для переноса функциональных групп из одной молекулы в другую. Киназа и фосфатазы (добавление и удаление фосфатов) особенно важны для молекулярных сигнальных каскадов, репликации ДНК, транскрипции РНК и других процессов. Существует также множество биологически значимых трансфераз, которые выполняют функции, например, превращения кетонов или альдегидов в амины, в том числе стереоселективно.
3. Гидролазы катализируют гидролиз различных субстратов. Нуклеазы или протеазы проявляют активность в процессах рециклинга нуклеиновых кислот и пептидов. Такие гидролазы, как липаза, протеаза и ацилаза, действуют как катализаторы реакций 1,4-присоединения Михаэля, широко используемых для образования связей C — C и углерод — гетероатом.
4. Лиазы обычно катализируют реакции образования и разрыва двойных связей. В отличие от реакций замещения, катализируемых гидролазами, для биокаталитического присоединения или удаления CO2 в фармацевтическом синтезе обычно используются карбоксилазы или декарбоксилазы. Их, как и C-N-лиазы, можно использовать для образования аминокислот, включая замещенные аспарагиновые кислоты и аланины.
5. Изомеразы способствуют перегруппировке атомов в молекулах. Например, рацемазы инвертируют стереохимию целевого хирального углерода, а цис-транс-изомеразы катализируют изомеризацию цис-транс-изомеров в алкенах и циклоалканах. Превращение глюкозы во фруктозу с помощью глюкозоизомеразы является примером важного промышленного применения ферментативной биотрансформации.
6. Лигазы способствуют образованию новых химических связей, когда две молекулы соединяются в одну, более крупную. Одно из наиболее важных направлений — использование ДНК-лигазы, в дополнение к эндо- или экзонуклеазам, для получения рекомбинантных молекул ДНК.
Вспомогательные процессы
Производство ферментных катализаторов. Как правило, природные или рекомбинантные ферменты для биокатализа синтезируются путем ферментации, чаще всего с использованием бактерий, но иногда их также получают из дрожжевых культур. Хотя ферменты можно получать и из более сложных культур клеток млекопитающих, бактерии и дрожжи обычно содержат достаточное количество естественных молекулярных путей для фолдинга и умеренных посттрансляционных модификаций, необходимых для рекомбинантных биокаталитических ферментов. Полученные таким образом ферменты обычно выделяют путем лизиса или другого метода разрушения клеточных структур, пригодного для высвобождения рекомбинантных ферментов, и далее очищают теми же способами, что и другие биологические фармацевтические препараты. Ферментация, сбор материала и последующее выделение целевого продукта представляют собой отдельные задачи, которые решаются с помощью процессно-аналитической технологии (PAT).
Стабилизация и иммобилизация. Иммобилизация ферментов используется для получения более стабильных и активных ферментов, пригодных для повторного использования. Как правило, поперечно сшитые ферментные агрегаты (ПСФА) могут быть образованы на различных твердых субстратах, таких как кремнезем, смолы и полимеры (например, полиэтиленгликоль), и даже на липидных наночастицах (LNP). В некоторых процессах химии непрерывных потоков ПСФА формируются на поверхностях и датчиках, например на таких, которые используются в измерениях поверхностно-усиленными методами для аналитических или каталитических целей. Проблемы синтеза родственных компонентов, адсорбции, конъюгации и других типов ассоциации, а также стабильности продукта и рецептуры решаются способами, применяемыми при производстве вакцин и использовании адъювантов.
Сбор и выделение продукта. По завершении биокаталитического процесса ПСФА отделяются от продукта и остаточных реагентов для повторного использования или хранения. Впоследствии низкомолекулярные продукты могут быть выделены с помощью фильтрации или хроматографии, хотя во многих случаях предпочтение по-прежнему отдается методам кристаллизации. Высокомолекулярные продукты биокатализа выделяются, как правило, с применением обычных технологий.
Технологические параметры, влияющие на биокатализ
Для успешной разработки биокаталитического протокола с использованием любого фермента, как связанного в субстратом или твердой поверхностью, так и свободного, важно учитывать его время полужизни и стабильность. Основные факторы:
Автоматизация для успешной разработки и масштабирования биокаталитических реакций
Разработка и масштабирование биокаталитических реакций зависят от природы используемых биокатализаторов, субстратов, сопутствующих факторов и условий проведения реакции. Как и в случае химического катализа, эту сложную взаимозависимую матрицу переменных легче всего изучать при строгом контроле переменных реакции и данных аналитических измерений в режиме реального времени. Однако большая часть ограничений, связанных с разработкой, масштабированием и плотностью данных, для современных процессов связана с продолжающейся практикой ручного регулирования реакций биокатализа, которая требует времени и ресурсов. Ручное управление подразумевает присутствие персонала у биореактора для почти постоянного обслуживания, регулирования и отбора проб, чтобы выполнить все более строгие нормативные и организационные требования к описанию процесса и передаче технологии.
Биокатализ без ручного управления возможен благодаря применению лабораторных систем автоматизации, которые реагируют на динамические условия реакции, непрерывно измеряемые с помощью встроенных датчиков и средств процессно-аналитической технологии (PAT). Автоматизированные реакторы синтеза упрощают проведение экспериментов, сводят к минимуму участие оператора и риск человеческой ошибки. Если в дополнение к ним использовать модульные средства автоматического отбора проб из реактора для автономного хроматографического анализа, то можно составить общую картину всех критических параметров процесса (CPP) и выявить тенденции. Данные параметрического контроля и анализа процесса автоматически регистрируются в режиме реального времени с последующим структурированием для управления и архивирования. Уменьшение изменчивости параметров в рамках серии экспериментов и повышенная воспроизводимость в реакторах разного объема дополнительно упрощают масштабирование, основанное на фактических данных.