Антихеликобактерные средства (ч. 2)
Схема эрадикации бактерии H. pylori подбирается в индивидуальном порядке в зависимости от чувствительности бактерии и реакции организма на выбранные препараты.
Преферанская Нина Германовна
Доцент кафедры фармакологии института фармации им. А.П. Нелюбина Первого МГМУ им. И.М. Сеченова (Сеченовский университет), к.фарм.н.
Амоксициллин (табл./капс. 250 мг, 500 мг) — полусинтетический антибиотик пенициллинового ряда широкого спектра действия, с умеренной активностью в отношении H. pylori. Биодоступность составляет 70–80%, растворимая лекарственная форма — 90%. В тканях достигается терапевтическая концентрация. Амоксициллин характеризуется широким спектром антимикробного действия, низким уровнем резистентности, хорошей всасываемостью в желудочно–кишечном тракте, высокой биодоступностью и кислотостойкостью. Блокада амоксициллином пенициллиносвязывающих белков приводит к остановке роста и гибели микробной клетки.
Период полувыведения — 1–1,5 ч. Выводится на 50–70% почками в неизмененном виде путем канальцевой секреции (80%) и клубочковой фильтрации (20%), печенью — 10–20%. В небольшом количестве выделяется с грудным молоком.
Противопоказаниями служит повышенная чувствительность к амоксициллину, детский возраст до 3 лет.
Важно! Вызывает аллергические реакции, тошноту, нарушения со стороны крови и лимфатической системы очень редко, диарею, очень редко кристаллурию.
Кларитромицин (табл. 250 мг, 500 мг; капс. 250 мг) — относится к группе полусинтетических макролидов, оказывает дозозависимый бактериостатический эффект за счет блокирования белковых систем микробной клетки, взаимодействует с 50S рибосомальной субъединицей, подавляет синтез белка бактерий. Однако при достижении концентрации, которая в 2–3 раза превышает минимальную ингибирующую концентрацию, оказывает бактерицидное действие. Бактерицидное действие оказывает в отношении H. pylori, данная активность Кларитромицина выше при нейтральном pH, чем при кислом. Кларитромицин по эффективности в отношению к H. pylori превышает все другие активные субстанции этой группы. Обладает широким спектром действия и является одним из наиболее эффективных и распространенных макролидов. При приеме внутрь хорошо всасывается, концентрация его в тканях намного превышает сывороточную. Максимальное накопление также наблюдается в слизистой ЖКТ.
Препарат хорошо проникает внутрь клеток (моноцитов, макрофагов, фагоцитов), создавая высокие внутриклеточные концентрации. Высокие концентрации в очаге воспаления делают его средством выбора при H. pylori — ассоциированной патологии желудка и 12-перстной кишки. Благодаря лиофильности способен проникать в клетки и накапливаться в высоких концентрациях в слизистой оболочке желудка и двенадцатиперстной кишки, что имеет большое значение при эрадикации H. pylori.
Также нельзя не вспомнить позитивный эффект санации, присущий Кларитромицину. Широкий спектр активности данного антибиотика по отношению к грампозитивным и грамнегативным бактериям позволяет элиминировать патогенные и условно–патогенные возбудители из полости ЖКТ, колонизация которых наблюдается в условиях хеликобактер–ассоциированных заболеваний. Препарат обладает собственной противовоспалительной активностью, что обусловлено угнетением продукции провоспалительных цитокинов и стимуляцией синтеза противовоспалительных гуморальных факторов. Однако самым главным его качеством является способность разрушать матрикс биопленки. 99% микроорганизмов, к которым относится и H. pylori, существуют не в виде отдельных микроорганизмов, а в составе сложно организованных сообществ — биопленок, которые представляют собой совокупность бактериальных клеток, которые окружены внеклеточным матриксом, который имеет полисахаридную природу. Матрикс выполняет защитную функцию и часто является причиной устойчивости микроорганизмов к действию антибиотиков, резистентность бактерий в составе биопленки возрастает в 10–1000 раз.
Важно! При применении препарата могут возникать диарея, гиперчувствительность, аллергические реакции, часто сыпь, очень редко может вызвать анафилактоидную реакцию, дерматит, нарушение слуха, звон в ушах (частота неизвестна), а также снижение числа лейкоцитов и тромбоцитов.
Метронидазол (ТН «Трихопол», «Флагил», табл. 250 мг) — противопротозойный препарат, относится к производным 5-нитроимидазола, активен в отношении микроаэрофилов H. pylori. Механизм действия заключается в биохимическом восстановлении 5-нитрогруппы внутриклеточными транспортными протеинами анаэробных микроорганизмов и простейших. Препарат оказывает избирательный бактерицидный эффект в отношении тех микроорганизмов, ферментные системы которых способны восстанавливать нитрогруппу. Восстановленная 5-нитрогруппа взаимодействует с дезоксирибонуклеиновой кислотой (ДНК) клетки микроорганизмов. Возникает ингибирование тканевого дыхание, нарушается репликация ДНК, синтез нуклеиновых кислот и синтез белка, что ведет к гибели бактерий.
Метронидазол быстро проникает в ткани (легкие, почки, печень, кожу, желчь, спинномозговую жидкость, слюну, семенную жидкость, вагинальный секрет), в грудное молоко и проходит через плацентарный барьер. Около 30–60 % метронидазола метаболизируется путем гидроксилирования, окисления и глюкуронирования.
Препарат медленно выводится из организма, период полувыведения 8–10 час., при повторных введениях кумулирует. Проникает в ткани и жидкости организма, обеспечивая терапевтические концентрации.
Важно! Вызывает темное окрашивание мочи, металлический привкус во рту, тошноту, рвоту, диарею, могут возникать аллергические реакции: крапивница, кожная сыпь, нарушения со стороны иммунной системы: ангионевротический отек, анафилактический шок.
КОМПЛЕКСНОЕ ПРИМЕНЕНИЕ ЛС
Успешная схема лечения основана на сочетании препаратов, которые предотвращают возникновение резистентности и настигают бактерию в различных участках желудка. Терапия должна гарантировать, что даже небольшая популяция микроорганизмов не останется жизнеспособной. В схемы терапии обязательно включают препараты висмута, химиотерапевтические препараты и ингибиторы протонной помпы (о последних препаратах мы писали в предыдущей статье).
Существуют стандартные схемы лечения двух-, трех- или четырехкомпонентной терапии в период лечения и обострения гастритов, язвенной болезни12-перстной кишки и желудка.
Используют:
√ БИТЕРАПИЮ: Ранитидин + Висмута цитрат (Пилорид);
Амоксициллин + Метронидазол (Хеликоцин);
√ ТРОЙНУЮ ТЕРАПИЮ:
Кларитромицин + Омепразол + Тинидазол (Пилобакт);
√ КВАДРОТЕРАПИЮ:
ЭРАДИКАЦИОННАЯ ТЕРАПИЯ H. pylori включает комплекс нескольких препаратов. Распространенная ошибка, которая зачастую приводит к непредсказуемым результатам, замена даже одного хорошо изученного препарата из стандартной схемы на другой препарат той же группы. Использование данных схем лечения значительно улучшает состояние больных и предупреждают развитие рецидивов.
Применение комбинированных лекарственных препаратов «Пилобакт», «Пилорид», «Хеликоцин» и др. значительно улучшает состояние больных и предупреждает развитие рецидивов. Как правило, терапия обязательно включает антисекреторные препараты, химиотерапевтические средства, гастропротекторы и препараты коллоидного висмута.
Интенсивную терапию проводят до достижения устойчивой ремиссии и отсутствия рецидивов у больных в течение 1,5–2 лет. При необходимости проводят профилактическую противорецидивную терапию. При применении комбинированной терапии необходимо убедиться в безопасном применении сочетанных препаратов, их переносимости и эффективности. При применении таких препаратов могут наблюдаться нежелательные побочные явления: тошнота, рвота (20%), диарея (10%), псевдомембранозный колит (1%), головокружение (2%), чувство жжения в ротовой полости, глотке, кандидоз (15%). Неэффективность лечения может быть обусловлена нарушением правил приема препаратов или развитием устойчивости бактерии к ним. Но несмотря на применение комбинированных схем лечения, у 10–20% пациентов, инфицированных H. pylori, не удается достичь элиминации возбудителя.
Повышают клиническую эффективность эрадикационной терапии комбинации ингибиторов протонной помпы (ИПП) с противомикробными препаратами.
Предполагается, что антисекреторные препараты из группы ИПП могут способствовать повышению концентрации антимикробных средств (Метронидазола и Кларитромицина) в просвете желудка. ИПП уменьшают объем желудочного сока, вследствие чего вымывание антибиотиков с поверхности слизистой уменьшается, а концентрация антибиотиков, соответственно, увеличивается. Кроме того, снижение объема соляной кислоты поддерживает стабильную терапевтическую концентрацию антимикробных препаратов. При проведении эрадикационной антихеликобактерной терапии совместно с ИПП является одним из необходимых условий.
Успешность комбинированных схем терапии определяется во многом правильным выбором антибактериального средства и обеспечением постоянно высокого уровня эрадикации бактерии. Удлинение курса лечения до 10–14 дней также повышает эффективность эрадикации в среднем на 5%, а назначение высоких (двойных) доз ИПП позволяет дополнительно получить 8% показателей эффективности эрадикации H. pylori.
Именно два антибактериальных агента Амоксициллин и Кларитромицин определяют высокую эффективность в отношении микроорганизмов, которые находятся в фазе деления. Поддержка уровня рН в желудке выше чем 3,0 при помощи антисекреторных препаратов резко тормозит процесс деградации Кларитромицина (при рН 1,0 в желудочном соке Т½ составляет 1 час, а при рН 7,0 205 час.), что обеспечивает полноценную эрадикацию H. pylori. На протяжении последних 20 лет в основных схемах эрадикационной терапии сохраняется стойкая комбинация указанных антибиотиков, что связано с фармакокинетическими и фармакодинамическими особенностями данных препаратов.
Схема эрадикации бактерии H. pylori подбирается в индивидуальном порядке в зависимости от чувствительности бактерии и реакции организма на выбранные препараты. Продолжительность курса лечения определяется лечащим врачом. Самолечение такого опасного заболевания, как хеликобактериоз, категорически противопоказано.
Возможности использования пробиотиков в эрадикации Helicobacter pylori
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Микробиота желудка разнообразна. Инфекция Helicobacter pylori (HP) меняет ее состав в целом, что может способствовать более быстрому прогрессированию хронического гастрита. Пробиотики могут быть эффективны в коррекции микробиома желудка.
Цель исследования: изучить эффективность использования Lactobacillus reuteri DSMZ17648 (Lr) при лечении HP-ассоциированного гастрита у детей и эрадикации HP.
Материал и методы: проведено двойное слепое рандомизированное плацебо-контролируемое исследование эффективности применения убитых Lr как в виде монотерапии, так и на фоне эрадикационной схемы (омепразол + амоксициллин + метронидазол + висмут в течение 10 дней) у 103 HP(+) пациентов от 9 до 17 лет. Курс применения Lr в подгруппах А составил 28 дней, в подгруппах В – 56 дней. Для контроля проводили эндоскопическое, гистологическое исследование, быстрый уреазный тест, дыхательный аммиачный тест (АВТ), подсчитывали количество HP в биоптате, определяли воспалительный и атрофический индексы.
Результаты исследования: при значительной обсемененности HP в желудке отмечалось снижение микробного разнообразия. Это сопровождалось более выраженным воспалением, очаговой атрофией слизистой оболочки. При слабой обсемененности HP окружающая микробиота сохраняла разнообразие, воспаление было выражено минимально. Эрадикация HP была достигнута при монотерапии Lr у 50% детей через 28 и у 60% — через
56 дней, при адъювантном назначении Lr — у 60% через 28 и у 77,8% через 56 дней, в группе плацебо — у 68,8% через
28 и 56 дней.
Заключение: клиническое улучшение на фоне применения Lr было более ранним, снижение показателей АВТ — стабильным, достоверно снизились воспалительные и атрофические изменения слизистой оболочки желудка.
Монотерапия с применением Lr сравнима по эффективности со стандартной схемой, включающей 2 антибиотика. Пробиотики могут быть альтернативой традиционной терапии HP.
Ключевые слова: Helicobacter pylori, HP-ассоциированный гастрит, нехеликобактерная микробиота желудка, рак желудка, пробиотики, Lactobacillus reuteri.
Для цитирования: Корниенко Е.А., Паролова Н.И., Иванов С.В. и др. Возможности использования пробиотиков в эрадикации Helicobacter pylori. РМЖ. Медицинское обозрение. 2018;2(7(II)):51-58.
1 St. Petersburg State Pediatric Medical University
2 Pavlov First St. Petersburg State Medical University
3 St. Petersburg State University
A gastric microbiota is diverse. Helicobacter pylori (HP) infection changes its composition as a whole, which may contribute to the more rapid progression of chronic gastritis. Probiotics can be effective in correcting the gastric microbiome.
Aim: to study the effectiveness of the use of Lactobacillus reuteri DSMZ17648 (Lr) in the treatment of HP-associated gastritis in children and HP eradication.
Patients and Methods: a double-blind, randomized, placebo-controlled study of the effectiveness of treatment with killed Lr both as monotherapy and on the background of the eradication scheme (omeprazole + amoxicillin + metronidazole + bismuth —
10 days) in 103 patients from 9 to 17 years old with HP(+), Lr course in subgroups A was 28 days, in subgroups B — 56 days.
For the control, endoscopic, histological studies, rapid urease test, ammonia breath test (ABT) were performed, the number of HP
in the biopsy, inflammatory and atrophic indices were calculated.
Results: with significant HP contamination in the stomach, there was a decrease in microbial diversity, the suppression of other microbes. This was accompanied by a more pronounced inflammation, focal atrophy of the mucous membrane. With low HP contamination, the surrounding microbiota preserved diversity, inflammation was minimal. HP eradication was achieved with Lr monotherapy in 50% of children after 28 days and 60% — after 56 days, with adjuvant Lr prescribing, in 60% — after 28 days and 77.8% — after 56 days, in the placebo group 68.8% — after 28 days and 56 days.
Conclusion: clinical improvement on the background of Lr was earlier, the decline in ABT indications was stable, inflammatory and atrophic changes in the gastric mucosa decreased significantly. According to the effectiveness, Lr monotherapy
is comparable to the standard dual antibiotic regimen, probiotics can be an alternative to traditional HP therapy.
Key words: Helicobacter pylori, HP-associated gastritis, non-Helicobacter gastric microbiota, gastric cancer, probiotics, Lactobacillus reuteri.
For citation: Kornienko E.A., Parolova N.I., Ivanov S.V. et al. Possibilities of using probiotics in Helicobacter pylori eradication //
RMJ. Medical Review. 2018. № 7(II). P. 51–58.
Статья посвящена возможностям использования пробиотиков в эрадикации Helicobacter pylori. Представлены результаты исследования эффективности использования Lactobacillus reuteri DSMZ17648 (Lr) при лечении Helicobacter pylori-ассоциированного гастрита у детей и эрадикации Helicobacter pylori.

Введение
Материал и методы
Дизайн исследования
Методы исследования
Статистическая обработка результатов исследования
Результаты
Обсуждение
Вывод
Только для зарегистрированных пользователей
Инновационный подход к лечению хеликобактерной инфекции желудка детей и взрослых
Лечение хеликобактер пилори — одна из наиболее частых забот врача-гастроэнтеролога, а Хеликобактер пилори — один из наиболее «популярных» микроорганизмов, широко изучаемых во многих странах с 1983 года. Заражение, бывает, происходит в детском возрасте и многие годы он может никак не проявлять себя. Установлено, что хеликобактер выявляется у 30-35% детей и у 50-85% взрослого населения. Хеликобактер пилори считается причиной заболеваний желудка, таких как, гастрит, язвенная болезнь, онкология желудка.
Неэффективность традиционного лечения
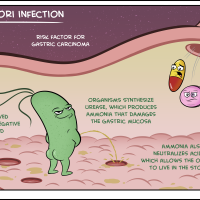
Стандарты лечения регламентируются международными и российскими соглашениями, в основе которых лежит курс лечения с назначением препаратов, снижающих кислотность желудочного сока (антисекреторные препараты – ИПП, например, Омез, Париет и др.), двух антибиотиков (например, Клацид и Амоксициллин).
Лечение хеликобактерной инфекции в любой возрастной категории сопровождается большим количеством побочных, нежелательных реакций на применяемые препараты и то, что их применение не исключает повторения инфекции или повторного заражения препараты-ИПП).
Почему при лечении хеликобактера отказываются от антибиотиков
Нечувствительность хеликобактера к антибиотикам приводит к уменьшению эффективности лечения – отмечено снижение эффективности с 80-90% до 30-60%, что является характерным для многих стран, для различных регионов в России.
Сегодня стоит еще раз напомнить о побочных эффектах применения антисекреторных препаратов и антибиотиков.
Так, при приеме антисекреторных препаратов (ИПП) нарушаются процессы переваривания пищи и всасывания кальция, железа, цинка, лекарственных препаратов при приеме внутрь. При длительном применении ИПП существует риск развития инфекций желудочно-кишечного тракта и легких, т. к. в желудок попадают микроорганизмы из ротовой полости, носоглотки, кишечника. Если они не инактивируются в условиях сниженной желудочной секреции, то некоторые из них могут вырабатывать вещества (канцерогены), которые могут вызывать онкологические заболевания. Длительный прием препаратов, снижающих желудочную секрецию, может привести к
Применение антибиотиков в лечении различных заболеваний и, в том числе, хеликобактериозе, несколько ограничено при наличии заболеваний печени, почек, нарушений микрофлоры кишечника, аллергии на антибиотики
Лечение антибиотиками может привести к развитию антибиотико-ассоциированного поноса, ухудшению пищеварения, вызвать дисепсические жалобы – тошноту, рвоту, изменение вкуса, нередко головную боль. Особенно это характерно для пожилых людей. Кроме того, могут развиваться аллергические реакции, вплоть до формирования поливалентной аллергии. Эти побочные эффекты, знакомые нашим пациентам, заставляют многих отказаться от приема антибиотиков из-за риска их развития.
К сожалению, официальные стандарты-IV Маастрихтского соглашения продолжают рекомендовать применение этих схем, однако…
Лечение хеликобактер пилори по-новому
В последние годы официальные стандарты-IV Маастрихтского соглашения пополнились применением препаратов висмута (Денол), пробиотиком Saccharomyces boulardii (препарат Энтерол) – тропического штамма дрожжевых грибов, выделенных из сока личи и манго.
Наиболее перспективным направлением оптимизации лечения хеликобактериоза желудка являлось использование пробиотиков, в первую очередь, лактобацилл в виде монотерапии. Исследования, проведенные российскими, зарубежными учеными и собственные данные подтверждают эффективность пробиотиков для эрадикации хеликобактер пилори. Опыт показал, что применение молочно-кислых бактерий, лактобацилл ацидофилюс, сочетание нескольких штаммов лактобацилл (Трилакт), позволило получить достаточно высокий процент положительных результатов, (39 — 54%) у детей и взрослых. При таком подходе к лечению встает вопрос, какой пробиотик выбрать, при каких заболеваниях желудка и других ситуациях применить, в каком возрасте, какова продолжительность курса.
Как выбрать пробиотик для лечения хеликобактера
Важным условием применения пробиотика является кислотоустойчивость штамма живых микроорганизмов, которая доказана в отношении группы лактобацилл (L.rbamnosus, L.reuteri, L.plantarum, L.acidophilus, способных оказывать прямое действие на хеликобактер пилори. Эти штаммы лактобацилл вырабатывают вещества (метаболиты), которые подавляют рост, обладают антибактериальным действием, снижают активность ферментов хеликобактерий и других микроорганизмов, уменьшают воспаление слизистой оболочки желудка.
Кому показано лечение пробиотиками
Лечение хеликобактерной инфекции с применением только пробиотиков показано:
Дальнейшие исследования показали, что положительно действуют не только пробиотики на основе живых микроорганизмов, но и продукты их метаболизма (обмена). На основе этого открытия был разработан в 2014 году в России новый препарат с уникальным антихеликобактерным действием.
Хелинорм – инновационное антихеликобактерное средство из группы метаболиков
Принцип действия

Связывание снижает подвижность хеликобактерий — бактерии перестают связываться со слизистой оболочкой желудка и вымываются из желудка, что приводит к уменьшению бактерий в слизистой оболочке и снижают риск развития гастрита, язвенной болезни.
Хелинорм – разумная альтернатива антибиотикотерапии при хеликобактериозе.
Схема лечения
Курс лечения Хелинормом составляет 4 недели, по 1 капсуле во время еды 1 раз в день.

С профилактической целью в дальнейшем возможно использовать закваски Эвиталия или Нарине, которые позволяют готовить лечебный кисломолочный продукт в домашних условиях, в котором оптимальное сочетание и живых бактерий – лактобацилл, и продуктов их жизнедеятельности. Использовать его в натуральном виде, с добавлением растительных компонентов (овощи, фрукты, отруби), заправлять им разнообразные салаты.
Место пробиотиков в антихеликобактерной терапии
В настоящее время инфекция, обусловленная Helicobacter pylori, считается наиболее распространенной хронической бактериальной инфекцией у человека. Предположительно H. pylori встречается у 50% населения земного шара. Инфекция H. pylori связана с ремоделированием кишечной микробиоты. Эрадикация H. pylori позволяет контролировать развитие осложнений заболеваний, ассоциированных с хеликобактерной инфекцией (язва желудка и двенадцатиперстной кишки). Ингибиторы протонной помпы (ИПП) в монорежиме могут влиять на бактериальную композицию желудка. Они способствуют чрезмерному росту микробиоты орофарингеального происхождения в пищеводе, желудке и двенадцатиперстной кишке, а вызванная ИПП гипохлоргидрия позволяет микроорганизмам, входящим в состав микробиоты верхних отделов желудочно-кишечного тракта, распространяться в более дистальные отделы пищеварительного тракта. Антихеликобактерная терапия не только уничтожает H. pylori, но и изменяет микробиоту кишечника. До своего первоначального состояния она восстанавливается только спустя год. Чтобы избежать подобных изменений, к обычному лечению добавляют альтернативные и адъювантные методы, например пробиотики. Линекс® Форте рекомендуется использовать во время приема ИПП, а также в комплексе антихеликобактерной терапии для профилактики и лечения дисбиотических нарушений желудочно-кишечного тракта.
В настоящее время инфекция, обусловленная Helicobacter pylori, считается наиболее распространенной хронической бактериальной инфекцией у человека. Предположительно H. pylori встречается у 50% населения земного шара. Инфекция H. pylori связана с ремоделированием кишечной микробиоты. Эрадикация H. pylori позволяет контролировать развитие осложнений заболеваний, ассоциированных с хеликобактерной инфекцией (язва желудка и двенадцатиперстной кишки). Ингибиторы протонной помпы (ИПП) в монорежиме могут влиять на бактериальную композицию желудка. Они способствуют чрезмерному росту микробиоты орофарингеального происхождения в пищеводе, желудке и двенадцатиперстной кишке, а вызванная ИПП гипохлоргидрия позволяет микроорганизмам, входящим в состав микробиоты верхних отделов желудочно-кишечного тракта, распространяться в более дистальные отделы пищеварительного тракта. Антихеликобактерная терапия не только уничтожает H. pylori, но и изменяет микробиоту кишечника. До своего первоначального состояния она восстанавливается только спустя год. Чтобы избежать подобных изменений, к обычному лечению добавляют альтернативные и адъювантные методы, например пробиотики. Линекс® Форте рекомендуется использовать во время приема ИПП, а также в комплексе антихеликобактерной терапии для профилактики и лечения дисбиотических нарушений желудочно-кишечного тракта.
В мире в 2015 г. насчитывалось 4,4 млрд человек, инфицированных Helicobacter pylori [1]. Как известно, с инфекцией H. pylori в слизистой оболочке желудка связаны острый и хронический гастрит, язвенная болезнь, неязвенная диспепсия, атрофический гастрит, кишечная метаплазия, аденокарцинома желудка, а также MALT-лимфома [2–4]. С H. pylori ассоциировано несколько экстрагастродуоденальных расстройств, таких как железодефицитная анемия, склеродермия, розацеа, атеросклероз и аутоиммунные заболевания щитовидной железы [5].
Инфекция H. pylori может ингибировать секрецию желудочной кислоты, вызывать хроническое воспаление слизистой оболочки желудка и тем самым приводить к изменению микробного сообщества [6, 7]. Кроме того, изменения микробиоты кишечника обусловлены рядом желудочно-кишечных и системных заболеваний [8]. И хотя желудок считается исключительной средой обитания H. pylori [9], эта бактерия была обнаружена посредством секвенирования 16S рРНК в образцах кала, правда с низкой относительной распространенностью [10]. Более того, согласно результатам исследований, H. pylori приводит к отчетливым изменениям микробиоты кишечника в дистальных отделах желудочно-кишечного тракта (ЖКТ) [11]. Аналогично в исследованиях с использованием флуоресцентной гибридизации in situ образцов фекалий у лиц, инфицированных H. pylori, показано снижение количества клостридий, а также общих анаэробов по сравнению с индивидуумами, негативными по H. pylori [12]. Эти наблюдения позволяют предположить, что инфекция H. pylori приводит к широко распространенным изменениям в экстрагастральной микробной структуре хозяина в результате изменений микрофлоры желудка. Между тем потенциал для индукции заболеваний и взаимодействие между H. pylori, кишечной микробиотой и здоровьем хозяина остаются недостаточно изученными. Установлено, что микробиота кишечника у H. pylori-негативных субъектов разнообразнее, чем у H. pylori-позитивных пациентов [13].
Колонизация желудка H. pylori влияет на распределение и количество исходных желудочных бактерий и нарушает микроэкологический баланс, что приводит к развитию патологии. Например, при инфицировании H. pylori уровень Lactobacillus в желудке ниже, чем в отсутствие хеликобактерной инфекции [14]. Вследствие хеликобактерной инфекции развивается микроэкологический дисбаланс, главным образом из-за синтеза антибактериального пептида – цекропина. Этот пептид может вызвать аутогенный аутолиз других бактерий [15]. Из-за отсутствия конкуренции со стороны этих бактерий H. pylori беспрепятственно размножается.
Согласно Киотскому глобальному консенсусу по H. pylori, чтобы минимизировать риск отдаленных последствий, включая язвенную болезнь желудка, аденокарциному желудка и лимфоидную опухоль, ассоциированную со слизистой оболочкой желудка (MALT), пациенты с диагностированной инфекцией H. pylori должны получать эрадикационную терапию [16]. Однако современные данные свидетельствуют о том, что эрадикация H. pylori связана с серьезными нарушениями кишечной микробиоты – уменьшением бактериального разнообразия, а также сокращением числа Bifidobacterium, Lactobacillus и продуцентов бутирата, таких как Faecalibacterium prausnitzii [12]. Подобные изменения могут сохраняться до четырех лет после завершения терапии антибиотиками [17].
Появляется все больше данных, подтверждающих потенциальный вред антибиотиков. Это указывает на необходимость более полного изучения сложных взаимодействий между H. pylori, кишечной микробиотой и хозяином для выявления субъектов, наиболее подверженных риску возникновения отдаленных последствий [18].
ИПП широко используются для эрадикации H. pylori. К потенциальным эффектам анти-H. pylori-препаратов относят:
Следует отметить, что снижение активности уреазы достигается только при введении высоких доз ИПП (омепразол 80 мг/сут).
Известно по крайней мере два механизма, с помощью которых ИПП влияют на бактериальную композицию желудка:
Показано, что орофарингеальная и фекальная флора более широко представлена в микрофлоре желудка после применения ИПП [29]. P.F. Sterbini и соавт. выявили значительное увеличение распространенности стрептококка в ЖКТ у пациентов, принимавших ИПП, независимо от статуса H. pylori. Исследователи пришли к заключению, что стрептококк может служить независимым индикатором изменений микробиома желудка у пациентов с диспепсией на фоне применения ИПП. Этим можно объяснить обострение или персистенцию диспепсии у пациентов, находящихся на терапии ИПП [22].
L. Macke и соавт. провели систематический обзор, посвященный оценке влияния ИПП на кишечную микробиоту [30]. В обзор были включены 12 независимых наблюдений с 4277 участниками и 11 интервенционных групп исследования с 180 участниками (все принимали ИПП). Установлено, что терапия ИПП сопровождается умеренными нарушениями микробиоты верхнего и нижнего отделов ЖКТ. В большинстве исследований подобные изменения ассоциировались не с показателями общего количества и разнообразия, а с изменением численности конкретных таксонов. Исследования микробиоты верхних отделов ЖКТ ограничены небольшим размером выборки и разнородным дизайном, но их результаты аналогичны таковым ранних наблюдений: ИПП способствуют чрезмерному росту микробиоты орофарингеального происхождения в пищеводе, желудке и двенадцатиперстной кишке (рисунок) [30].
Связанные с ИПП изменения профилей микробиоты в образцах фекалий подробно описаны как в интервенционных, так и в крупных наблюдательных исследованиях: использование ИПП связано с увеличением числа таксонов родов Bacillales (например, Staphylococcaceae) и Lactobacillales (в частности, Enterococcaceae, Lactobacillaceae и Streptococcaceae), Actinomycetales (Actinomycetaceae и Micrococcaceae), семейств Pasteurellaceae и Enterobacteriaceae и рода Veillonella. Кроме того, при использовании ИПП наблюдаются таксономическое снижение численности представителей семейств Bifidobacteriaceae, Ruminococcaceae и Lachnospiraceae и класса Mollicutes. Эти данные подтверждают вывод, что гипохлоргидрия, вызванная ИПП, позволяет микроорганизмам, входящим в состав микробиоты верхних отделов ЖКТ, заселять более дистальные отделы пищеварительного тракта.
Наблюдается также значительное увеличение Staphylococcus aureus и его бактериальной инвазии эпителиальных клеток, включая гены антибактериальных пептидов с нарушением целостности эпителия. ИПП играют важную роль в споруляции Clostridium difficile за счет снижения устойчивости к колонизации на фоне изменения микробиоты [31].
Многие врачи, под наблюдением которых находятся пациенты с инфекцией H. pylori и экстраалиментарными расстройствами на фоне гастроэнтерологических симптомов, нередко задаются вопросом: проводить эрадикацию H. pylori или не проводить?
В Маастрихтском соглашении V содержится основанное на фактических данных указание о проведении эрадикации H. pylori [32]. Однако клинические решения не всегда просты. Традиционная антихеликобактерная тройная терапия предполагает применение ИПП, кларитромицина и амоксициллина. В начале 1990-х гг. уровень эрадикации на фоне традиционной тройной терапии составлял 90% [33]. В последние десятилетия эффективность эрадикации H. pylori заметно снизилась из-за увеличения устойчивости к антибиотикам. В ряде стран частота несостоявшейся эрадикации превышает 20%. В районах с высокой распространенностью резистентных H. pylori-штаммов этот показатель может быть еще выше [34, 35]. Маастрихтское соглашение V рекомендует в целях эрадикационной терапии H. pylori дважды в день применять антибиотики и высокие дозы ИПП в течение 14 дней [32]. Как следствие – увеличение во время антихеликобактерной терапии (АХТ) частоты нежелательных побочных эффектов, таких как диарея, тошнота или рвота, и соответственно снижение приверженности лечению [36].
В исследованиях у 10–30% пациентов отмечались изменения частоты дефекации и характера стула [37–39], что могло быть связано с нарушением кишечной микробиоты. В исследовании L. Wu и соавт. диарея во время тройной терапии наблюдалась у 35% пациентов [40]. Таким образом, АХТ, основанная на применении антибиотиков, ассоциируется с изменением кишечной микробиоты [41].
L. Chen и соавт. [18] установили, что применение антихеликобактерной висмутсодержащей четырехкомпонентной схемы способно не только уничтожить H. pylori, но и изменить микробиоту кишечника (исследовано с использованием секвенирования 16S рРНК в образцах кала). Показано, что АХТ-индуцированный энтеральный дисбиоз может сохраняться до восьми недель после начала терапии антибиотиками. Однако следует учитывать, что изменения микробиоты кишечника после эрадикации H. pylori – не только результат действия антибиотиков. Это может быть обусловлено длительными изменениями секреции слюны, кислотности и моторики желудка, иммунологического ответа слизистой оболочки, изменениями в метаболических путях и потерей прямого влияния инфекции H. pylori на другие микроорганизмы, населяющие пищеварительный тракт человека [42]. Побочные эффекты эрадикации H. pylori, продолжительность которых превышает восемь недель, способны потенциально влиять на течение ряда заболеваний, связанных с дисбактериозом кишечника (воспалительные заболевания кишечника, пищевая аллергия и сахарный диабет), а также на усвоение пищи и лекарственных средств [43].
В ряде исследований оценивали долговременные изменения микробиоты кишечника. Альфа- и бета-разнообразие микробиоты и относительная численность всех типов восстанавливались до первоначального состояния только через год [10, 17, 44].
Во избежание изменений микробиоты к обычному лечению как взрослых, так и детей необходимо добавлять альтернативные и адъювантные методы, например пробиотики [45–49]. Хотя вопрос о положительном влиянии пробиотиков на эрадикацию H. pylori остается дискутабельным [50], в нескольких метаанализах и обзорах показано, что на фоне применения пробиотиков скорость эрадикации H. pylori увеличивается приблизительно на 5–10% [51–53]. Иммунная система и нормальная микробиота желудка способны эффективно противодействовать колонизации H. pylori, в то время как нарушение баланса микробиоты желудка повышает восприимчивость к инфекции H. pylori. Эти данные составляют теоретическую основу клинического использования пробиотиков в целях увеличения скорости эрадикации H. pylori.
Особое внимание в Маастрихтском соглашении V уделено гастроинтестинальной микробиоте и пробиотикам [32]:
Метаанализ Z. Lv и соавт. показал, что пробиотические добавки способны улучшить показатели эрадикации и уменьшить побочные эффекты, возникшие на фоне эрадикационной терапии. Кроме того, пробиотики, по-видимому, оказывают повышенное влияние на частоту эрадикации при введении до или после стандартных схем. Длительное лечение пробиотиками может иметь преимущество перед краткосрочным введением. Lactobacillus и пробиотические добавки с несколькими видами положительно влияют на скорость эрадикации инфекции H. pylori [54].
F. Wang и соавт. проанализировали 140 исследований (44 английских и 96 китайских), в которых в общей сложности участвовало 20 215 пациентов. Схема эрадикационной терапии H. pylori включала более десяти пробиотических стратегий. Частота эрадикации и побочных явлений в пробиотической группе составила 84,1 и 14,4%, в контрольной группе – 70,5 и 30,1% соответственно. В целом дополнительное применение пробиотиков повысило эффективность эрадикации H. pylori и снизило частоту нежелательных явлений [49].
X. Shi и соавт. провели метаанализ 40 исследований с участием 8924 пациентов и оценили уровень эрадикации, частоту общих побочных эффектов на фоне лечения, эффективность и безопасность пробиотиков в эрадикации H. pylori, наилучшие сроки и продолжительность приема пробиотиков, использование схем эрадикации, штаммов, локализаций и общие побочные эффекты. По сравнению с контрольной в основной (пробиотической) группе наблюдались более высокая частота эрадикации (р 9 КОЕ живых лиофилизированных молочнокислых бактерий. Показаниями к применению являются:
комплексная терапия и профилактика диареи, метеоризма и других нарушений пищеварения, вызванных вирусными и бактериальными инфекциями ЖКТ (например, ротавирусные инфекции, диарея путешественника), терапией антибиотиками широкого спектра действия и другими противомикробными препаратами, лучевой терапией органов брюшной полости.
В обновленную инструкцию вошло показание – диарейные синдромы различной этиологии.
К преимуществу B. lactis (BB-12) и L. acidophilus (LA-5) относится высокая устойчивость к кислой среде желудка и желчи, благодаря чему их жизнеспособность сохраняется при прохождении через весь ЖКТ [58]. Другим крайне важным свойством данных штаммов бактерий является высокая адгезивная способность, играющая ключевую роль в создании колонии в кишечнике хозяина [59]. Спустя неделю после окончания приема B. lactis (BB-12) и L. acidophilus присутствуют в 87,5 и 37,5% образцов фекалий соответственно [60]. С помощью полимеразной цепной реакции установлено, что свыше 90% BB-12 были живыми [61]. Это означает, что они способны выживать и размножаться в кишечнике и по завершении терапии.
Препарат Линекс® Форте рекомендуется для профилактики побочных эффектов и повышения переносимости АХТ и соответственно повышения эффективности эрадикационной терапии инфекции H. pylori.



