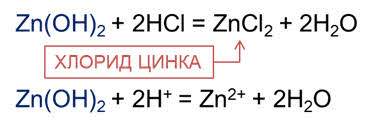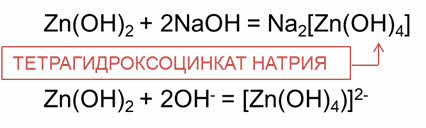Химия, Биология, подготовка к ГИА и ЕГЭ
Амфотерные соединения
Автор статьи — Саид Лутфуллин
Химия – это всегда единство противоположностей.
Посмотрите на периодическую систему.
Некоторые элементы (почти все металлы, проявляющие степени окисления +1 и +2) образуют основные оксиды и гидроксиды. Например, калий образует оксид K2O, и гидроксид KOH. Они проявляют основные свойства, например взаимодействуют с кислотами.
K2O + HCl → KCl + H2O
Некоторые элементы (большинство неметаллов и металлы со степенями окисления +5, +6, +7) образуют кислотные оксиды и гидроксиды. Кислотные гидроксиды – это кислородсодержащие кислоты, их называют гидроксидами, потому что в строении есть гидроксильная группа, например, сера образует кислотный оксид SO3 и кислотный гидроксид H2SO4 (серную кислоту):
Такие соединения проявляют кислотные свойства, например они реагируют с основаниями:
H2SO4 + 2KOH → K2SO4 + 2H2O
А есть элементы, образующие такие оксиды и гидроксиды, которые проявляют и кислотные, и основные свойства. Это явление называется амфотерностью. Таким оксидам и гидроксидам и будет приковано наше внимание в этой статье. Все амфотерные оксиды и гидроксиды — твердые вещества, нерастворимые в воде.
Для начала, как определить является ли оксид или гидроксид амфотерным? Есть правило, немного условное, но все-таки пользоваться им можно:
Амфотерные гидроксиды и оксиды образуются металлами, в степенях окисления +3 и +4, например (Al2O3, Al(OH)3, Fe2O3, Fe(OH)3)
И четыре исключения: металлы Zn, Be, Pb, Sn образуют следующие оксиды и гидроксиды: ZnO, Zn(OH)2, BeO, Be(OH)2, PbO, Pb(OH)2, SnO, Sn(OH)2, в которых проявляют степень окисления +2, но не смотря на это, эти соединения проявляют амфотерные свойства.
Амфотерные органические и неорганические соединения
Урок 44. Химия 11 класс ФГОС
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Амфотерные органические и неорганические соединения»
Амфотэрность с греческого означает и тот, и другой. Их двойственность выражается в том, что они могут проявлять и основные, и кислотные свойства.
Амфотэрными называются соединения, которые в зависимости от условий могут проявлять и кислотные, и основные свойства.
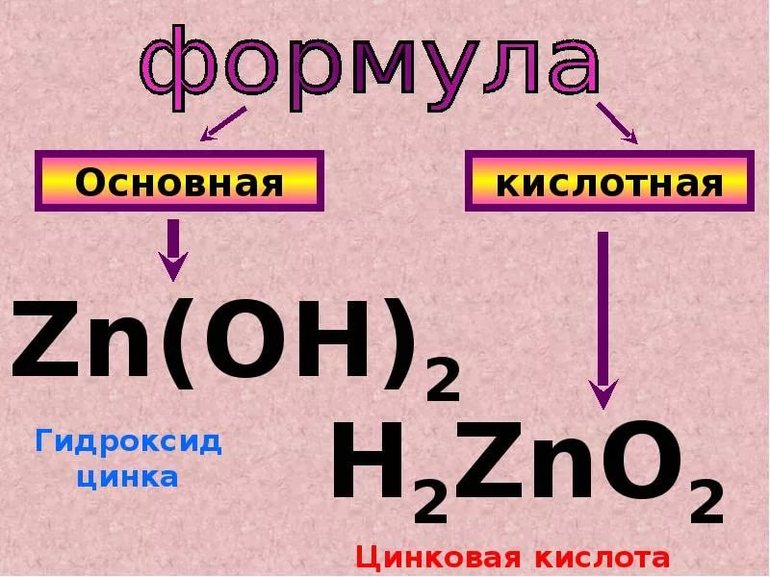
Среди неорганических веществ амфотэрными являются оксиды и гидроксиды пэ-элементов. Например: оксиды и гидроксиды цинка, алюминия, бериллия и других элементов, а также оксиды и гидроксиды некоторых дэ-элементов.
Амфотэрные соединения в реакции с кислотой ведут себя как основания, в реакции с основания выступают в роли кислот.
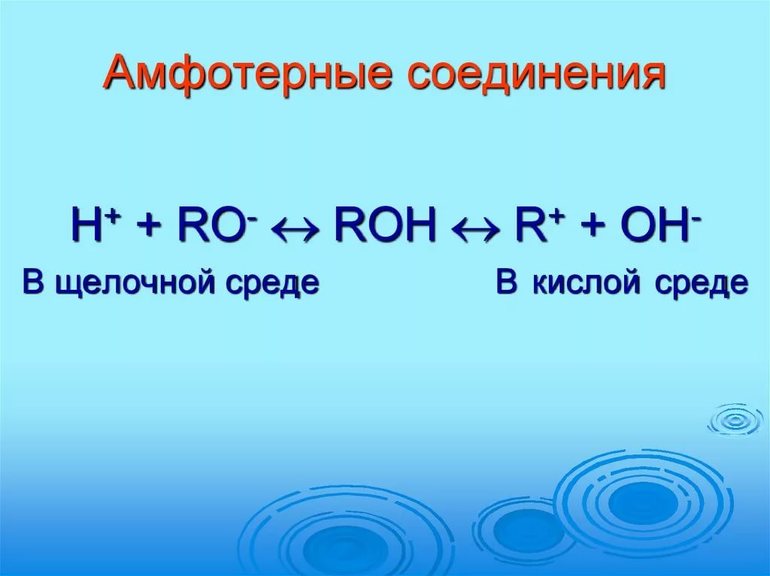
С точки зрения теории электролитической диссоциации кислоты – это электролиты, при диссоциации которых в качестве катионов образуются катионы водорода. Основания – это электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы.
Рассмотрим изменение кислотно-основных свойств гидроксидов.
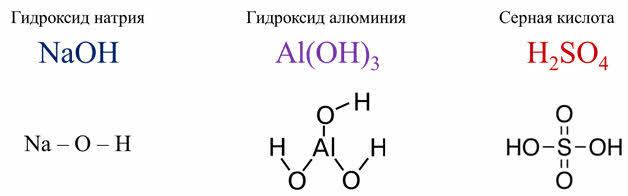
Для примера возьмём строение гидроксида натрия, гидроксида алюминия и серной кислоты.
У этих гидроксидов будет по-разному разрываться связь. В гидроксиде натрия связь натрий-кислород полярнее, чем между кислородом и водородом.
Поэтому гидроксид натрия будет диссоциировать на ионы натрия и гидроксид-ионы. В серной кислоте атомы водорода и кислорода значительно отличаются по электроотрицательности, чем между серой и кислородом. Поэтому серная кислота диссоциирует с образованием катионов водорода и сульфат-ионов.
Таким образом, в периодах с увеличением порядкового номера происходит ослабление основных свойств и усиление кислотных свойств гидроксидов.
Рассмотрим свойства бескислородных соединений.
Вспомним, согласно протолитической теории, кислоты – это вещества, группы атомов или ионы, которые являются в данной реакции донорами катионов, то есть отдают катионы водорода.
Основания – это вещества, группы атомов или ионы, которые являются акцэпторами катионов, то есть принимают протоны водорода.
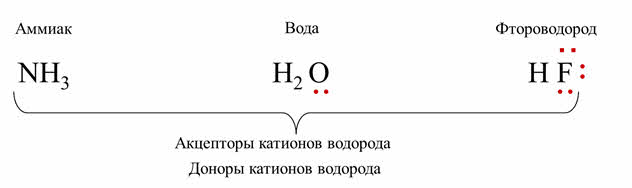
Например, рассмотрим водородные соединения неметаллов: аммиака, воды и фтороводорода.
У атома азота в аммиаке одна неподелённая пара электронов, у кислорода в молекуле воды – две неподелённые пары, а у фтора во фтороводороде – три.
В этих молекулах есть неподелённые пары электронов, что позволяет им быть акцэпторами катионов водорода и проявлять основные свойства. Но в молекулах веществ есть и неметаллы – атомы водорода. При отрыве атомов водорода, соединение может быть донором катионов водорода, то есть проявлять кислотные свойства.
Например, в реакции аммиака с водой, катион водорода отделяется от воды, потому что связь между кислородом и водородом более полярная, чем между азотом и водородом, так как разница в электроорицательности кислорода и водорода больше, чем между азотом и водородом.
Этот катион водорода присоединяется к аммиаку. То есть вода здесь проявляет кислотные свойства, а аммиак – основные.
В реакции фтороводорода с водой от фтороводорода отделяется катион водорода, а вода тем самым является акцэптором катионов водорода, потому что связь между водородом и фтором более полярная, чем между кислородом и водородом, фтороводород является кислотой, а вода – основанием.
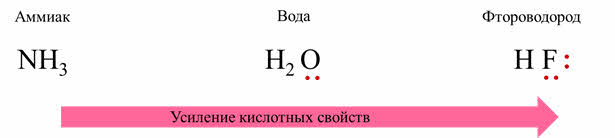
Поэтому в ряду от аммиака до фтороводорода идёт увеличение порядкового номера неметалла, основные свойства ослабевают, а идёт усиление кислотных свойств.
Таким образом, вода является амфотэрным соединением: с аммиаком вода выступает донором катионов водорода, то есть является кислотой, а в реакции с фтороводородом она будет акцэптором катионов водорода, то есть является основанием.
Амфотэрные соединения реагируют с кислотами и щелочами.
Так, в реакции с кислотами амфотэрные оксиды и гидроксиды ведут себя, как основания.
В реакции гидроксида цинка с соляной кислотой образуется соль – хлорид цинка и вода.
В реакции оксида цинка с соляной кислотой образуется соль – хлорид цинка и вода.
В реакциях с основаниями амфотэрные соединения ведут себя, как кислоты. Так, в реакции гидроксида цинка с гидроксидом натрия образуется тэтра-гидроксо-цинкат натрия, в реакции оксида цинка с гидроксидом натрия образуется соль – тэтра-гидроксо-цинкат натрия.
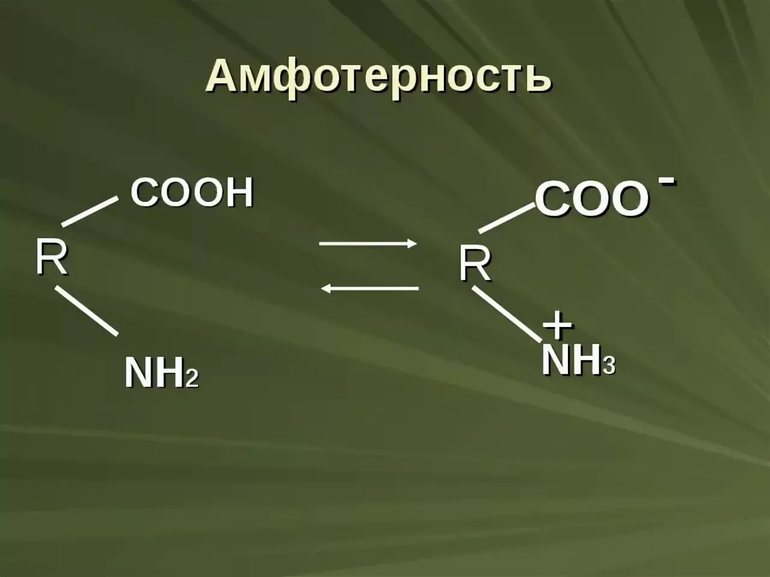
Аминокислоты являются амфотэрными органическими соединениями. В аминокислотах есть две функциональные группы: аминогруппа и карбоксильная группа.
Эти группы отличаются по свойствам. Так, аминогруппа является акцэптором катионов водорода, так как содержит азот, имеющий неподелённую пару электронов. Аминогруппа обуславливает основные свойства. Карбоксильная группа имеет сильно полярную кислород-водородную связь, поэтому является донором катионов водорода. Карбоксильная группа обуславливает кислотные свойства аминокислот.
Амфотэрные свойства аминокислот связаны с тем, что они являются бифункциональными соединениями. Аминокислота присоединяет протон водорода, который образуется при диссоциации кислоты.
При взаимодействии аминокислоты с гидроксидом натрия она проявляет кислотные свойства, так как взаимодействие происходит в карбоксильной группе.
Аминокислоты реагируют со спиртами по реакции этэрификации с образованием сложных эфиров. При чём, от кислоты отщепляется о-аш группа, а от спирта – атом водорода.
В аминокислотах возможно внутримолекулярное взаимодействие из-за наличия двух функциональных групп. Ион водорода, который образуется при диссоциации в карбоксильной группе, присоединяется к аминогруппе и образуется диполярный ион, как бы внутренняя соль, поэтому аминокислоты проявляют амфотэрные свойства.
Аминокислоты также реагируют друг с другом по реакции кондэнсации.
Благодаря этой реакции в рибосомах происходит биосинтез белка. В промышленности таким образом получают синтетические волокна, например, капрон.
Таким образом, к амфотэрным соединениям относятся соединения, которые могут реагировать и с кислотами, и с основаниями. Неорганическими амфотэрными соединениями являются оксиды и гидроксиды некоторых пэ- и дэ-элементов. Органическими амфотэрными соединениями являются аминокислоты.
Это определение было введено при изучении общей теоретической химии в области ведущих и кислотных взаимодействий при наступлении определенных условий.
Отмечается влияние смены растворяющего вещества на дуальные характеристики.
Амфотерные свойства
Гидроксиды элементов и их сцеплений из таблицы Менделеева, которые относятся к амфотерным соединениям:
Чаще всего вещества проявляют одно из взаимодействий, которое изменяет характер при перемене условий. Например, происходят процессы ионизации азотной кислоты, при этом получаются нитрозильные анионы и нитрит-катионы, в качестве амфолита выступает вода.
Амфотерность рассматривается в виде способности проводящего вещества быть донором и акцептировать протоны в рамках протеолитической концепции Бренстеда и Лоури. В этом случае вода проявляет свойства самоионизации в форме обратимой передачи молекул между жидкостями, в результате появляется одинаковое число анионов и катионов.
Амфолитами являются субстанции с содержанием структурных включений органических молекул, которые передают свойственные характеристики разного характера.
Такие вещества представлены пептидами, белками и аминокислотами. Эти группы частично ионизируются при помещении в раствор.
Молекулы и частицы аминокислот имеют равновесные состояния:
В этих случаях вещество представлено кислотой (воспроизводят катионы) и протоны или работает по основному свойству и акцептирует катионы и протоны.
Характеристики гидроксидов
Способность амфотерного элемента проявляется и в форме взаимодействия с кислотами и основаниями.
Так ведут себя оксиды, комплексные соединения, гидроксиды и отдельные р-элементы на средней стадии окисления. Для неорганических связей с присутствием гидроксильной группы ОН такое взаимодействие является общей характеристикой.
Традиционная теория об амфотерности гидроксидов в процессе разложения на ионы по основному и кислотному виду не подтверждается. Амфотерное поведение гидроксидов заключается в реакции обмена частицами среды с молекулами, имеющими связь с акцепторным центром. Гидроксиды обладают особенностью выделять соль и по-разному взаимодействовать в кислотной среде и растворе щелочи.
В первом случае они действуют по типу оснований, а вторая среда заставляет проявлять реакцию кислот.
Амфотерность гидроксидов и оксидов проявляется в продуцировании 2 рядов солей. Двойственность свойств используется при проведении качественного анализа и отделения веществ с подобными характеристиками от других элементов. Интервал появления осадка проявляется узким промежутком, поэтому внимание уделяется тщательности регулировки растворной среды.
Номенклатура и химические особенности
На особом положении в ряду амфотерных элементов находится алюминий, он стоит на границе между кислотами и основаниями. Это ведет к его диссоциации по двум типам поведения.
Амфотерные металлы и неметаллы обладают свойствами:
Гидроксиды с двойственными свойствами имеют физические промежуточные характеристики, доказать амфотерность можно на примере взаимодействия комплексных соединений из списка веществ 3 периода таблицы Менделеева.
В химии свойства однотипных сульфидов и оксидов, а также гидросульфитов и гидроксидов имеют разную реакцию в пределах отличающихся периодов. Свойство оснований проявляют сульфиды типичных металлов, а кислотные характеристики присутствуют в бинарных соединениях неметаллических субстанций. Различие химического происхождения наблюдается при обменной реакции между действующим веществом и растворителем, а также во взаимодействии сульфидов друг с другом.
Амфотерность гидроксидов металлических элементов объясняется тем, что в воде вещество распадается на отдельные ионы водорода по кислотному виду, а образование гидроксильных ионов проходит по типу основы.
Степени окисления
У некоторых веществ наблюдается несколько ступеней окисления, поэтому амфотерные свойства гидроксидов и оксидов подлежат разной классификации. Вещества с низкими окислительными характеристиками тяготеют к группе оснований, а сам элемент обладает свойствами металла, поскольку содержится в категории катионов. Субстанции с высокой степенью окисления являются участниками кислотных групп и проявляют неметаллические показатели, так как представляют собой анионы.
Например, у гидроксида и оксида марганца (2) главными являются основные свойства, а сам элемент входит в категорию катионов. У разновидности марганца (Vil) преобладают показатели кислоты, а само вещество относится к анионовой группы (тип МПО4).
Свойства оксидов и гидроксидов проявляются в зависимости от характеристики металла. Для элементов подвида бора (исключается таллий) типичной является 3-я степень перехода заряженных частиц от донора-восстановителя к окислительному акцептору. В результате свойства основания для элемента ослабляются.
При переходе к 3 группе встречаются вещества, которые образуют кислоты и неорганические кислоты. Последние обладают сочетанием химических и физических показателей, характерных для кислот и являются типовыми для многих элементов, за исключением щелочноземельных и щелочных металлов.
Рост свойств основного вещества происходит при увеличении радиуса движения ионов. Некоторые субстанции имеют почти одинаковую степень диссоциации с получением ионов, а у других аморфные показатели выражаются слабо.
В соединениях развитие основных свойств происходит медленно. Это объясняется тем, что атомы веществ 3 группы представляют собой аналоги с характерным строением внешней оболочки по типу благородных газов. Другие субстанции отличаются наружным слоем атома в форме электронной оболочки с 10 электронами. В таблице после алюминия наблюдается увеличение радиусов ионов, отмечается диагональное сходство, что ведет к постепенному усилению основных характеристик.
Процессы при диссоциации
В некоторых случаях амфотерные характеристики металлических гидроксидов проявляются не только в водной среде, но под действием кислотного и щелочного раствора. Если в случае с кислотой при продуцировании нейтральных частиц выделяется вода и появляется ион металла (свойство основания), то в щелочной среде не происходит отщепление протона.
При тяготении азота к висмуту степень окисления стабилизируется и усиливаются показатели основного характера. Такие соединительные субстанции выполняют одновременно окислительные и восстановительные функции. Двойственный процесс объясняется ионизацией молекулы воды, которая располагается во внутренней сфере, а протон перемещается к иону ОН.
В этом случае затрудняется определение развитости кислотных и основных показателей вещества, так как оно не имеет в составе подвижного водородного атома.
В результате из бокситов получаются другие элементы, что служит показателем использования химических характеристик при разделении. Метод основывается на применении свойства амфотерности алюминия. К этому же разряду относится выделение магния из воды морей и океанов.
Реакции взаимного действия с расплавами щелочей и кислотами ведут к появлению молекул воды и соли, а в результате степень окисления остается неизменной.
Двойственные показатели
Ионный потенциал вещества увеличивается в результате проявления двойственного механизма при диссоциации амфотерных соединений. Например, Мл (0Н) является неуравновешенным основанием, а Мп (0Н)4 представляет собой амфотерный элемент, который в равной степени проявляет кислотные особенности. НМПО4 переходит в категорию усиленных кислот, при этом снижаются свойства основания.
Щелочная среда используется для восстановления элементов с образованием гидросолей, например, гексагидроксоалюминат натрия. Если судить о тетрагидроксиде титана, то название подчеркивает возможность взаимной реакции с кислотами. Эта же субстанция гидроокиси называется ортокислотой при характеристике ее реагирования в условиях щелочной среды.
Активные металлические соединения образовывают сильнополярные ионные связи, поэтому относятся к группе оснований. Уменьшение динамичности характера вещества изменяется в сторону кислотного реагирования: НМпО, КОН, 5с (ОН)3, Са (ОН)2, НУО3 и другие.
Амфотерные оксиды М2О3 и соответствующие им гидроксиды М (ОН)3 (при этом исключается В2О3) плохо растворяются в водном растворе.
Гидроксиды характеризуются неравномерным изменением двойственных характеристик:
Другие вещества
Соединение гидроксида циркония является малорастворимым в воде и проявляет устойчивость к этой среде. Вещество относится к классу полимеров с положительно заряженными частицами, который содержит периодические цепи, расположенные в клеточном порядке. Материал не реагирует на основания, восстановительных и окислительных агентов.
В кислых растворах гидроксид циркония переводит анионы С1, НО3, СГО4, 8Ог на ионы ОН. Увеличение температурных показателей почти не сказывается на скорости обмена. В случае с цирконием не происходит образование определенных гидратов, термогравиметрические измерения показывают осадок полимерных частиц с образованием структурного слоя.
Германий находится ближе к группе металлов и образовывает связи, в которых его степень окисления расценивается по 2 категории. Соединения являются менее прочными, по сравнению с контактами германиевого аналога свинцовой группы, и отличаются восстановительными характеристиками. Амфотерный гидроксид с явно выраженными кислотными свойствами соответствует черному оксиду германия, молекулы которого не растворяются в жидкости. Последний носит название германистой кислоты, а его осадочные соли — германитов.
Если элемент в зависимости от условий образовывает несколько различающихся по составу оснований, то наиболее сильным признается то, которое отличается низкой окислительной степенью.
Качества основания в таких веществах выражаются ярко. Сильной является кислота, анионы которой содержат множество кислородных атомов в случае появления у элемента нескольких кислотосодержащих соединений.