Физиология и нарушения кислотно-основного состояния (методические материалы к практическим и семинарским занятиям)
Информация
Справочное пособие содержит информацию о физиологии кислотно- основного состояния (КОС). Представлена информация о методах лабораторной диагностики нарушений КОС. Перечислены варианты нарушений и методы коррекции. Предназначается для врачей всех специальностей, курсантов ФПК и студентов медвузов.
Физиология кислотно-основного состояния
В норме сильных кислот образуется 50 – 100 ммоль/сутки. При избыточном образовании они вызывают тяжелые нарушения. Это происходит при анаэробном окислении глюкозы.
В норме окисление глюкозы происходит аэробно: С6Н12О2 + 6О2 = 6Н2О + 6СО2 + 38 АТФ
Рис. 1. Доставка 02 к тканям и первые стадии элиминации CO2
Рис. 2. В легких бикарбонат снова превращается в С02 и выводится
Транспорт кислорода из легких к тканям и из тканей к легким обусловлен изменениями, которые воздействуют на сродство кислорода к гемоглобину. На уровне тканей из-за снижения рН это сродство уменьшается (эффект Бора) и вследствие этого улучшается отдача кислорода. В крови легочных капилляров сродство гемоглобина к кислороду увеличивается из-за снижения рС02 и возрастания рН по сравнению с аналогичными показателями венозной крови, что приводит к повышению насыщения артериальной крови кислородом.
Первичные изменения КЩС и компенсаторные реакции
При участии какого фермента в почечных канальцах происходит диссоциация угольной кислоты
Кислотно-основное состояние (КОС) организма является одним из важнейших и наиболее строго стабилизируемых параметров гомеостаза. От соотношения водородных и гидроксильных ионов во внутренней среде организма зависят активность ферментов, гормонов, интенсивность и направленность окислительно-восстановительных реакций, процессы обмена белков, углеводов и жиров, функции различных органов и систем, постоянство водного и электролитного обмена, проницаемость и возбудимость биологических мембран и т.д. Активность реакции среды влияет на способность гемоглобина связывать кислород и отдавать его тканям.
Активную реакцию среды принято оценивать по содержанию в жидкостях ионов водорода.
Величина рН является одним из самых «жестких» параметров крови и колеблется у человека в норме в очень узких пределах – рН артериальной крови составляет 7,35–7,45; венозной – 7,32–7,42. Более значительные изменения рН крови связаны с патологическими нарушениями обмена. В других биологических жидкостях и в клетках рН может отличаться от рН крови.
Сдвиги рН крови за указанные границы приводят к существенным сдвигам окислительно-восстановительных процессов, изменению активности ферментов, прницаемости биологических мембран, обусловливают нарушения со стороны функции сердечно-сосудистой, дыхательной и других систем; сдвиг на 0,3 может вызвать коматозные состояния, а на 0,4 – зачастую несовместим с жизнью.
Кислотно-основное состояние поддерживается мощными гомеостатическими механизмами. В их основе лежат особенности физико-химических свойств буферных систем крови и физиологические процессы, в которых принимают участие системы внешнего дыхания, почки, печень, желудочно-кишечный тракт и др.
Химические буферные системы образуют первую линию защиты против изменений рН жидкости организма, действуют для быстрого их предотвращения.
Буферной системой называют смеси, которые обладают способностью препятствовать изменению рН среды при внесении в нее кислот или оснований. Буферные системы не удаляют H+ из организма, а «связывают» его своим щелочным компонентом до окончательного восстановления КОС. Буферными свойствами обладают смеси, которые состоят из слабой кислоты и ее соли, содержащей сильное основание, или из слабого основания и соли сильной кислоты.
Наиболее емкими буферными системами крови являются бикарбонатный, фосфатный, белковый и гемоглобиновый. Первые три системы особенно важную роль играют в плазме крови, а гемоглобиновый буфер, самый мощный, действует в эритроцитах.
Бикарбонатный буфер является наиболее важной внеклеточной буферной системой и состоит из слабой угольной кислоты Н2СО3 и соли ее аниона – сильного основания 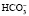
В нормальных условиях (при рН крови около 7,4) в плазме бикарбоната в 20 раз больше, чем углекислоты.
Емкость бикарбонатной системы составляет 53 % всей буферной емкости крови. При этом на бикарбонат плазмы приходится 35 % и на бикарбонат эритроцитов 18 % буферной емкости.
При образовании в плазме избытка кислореагирующих продуктов ионы водорода соединяются с анионами бикарбоната (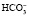
Бикарбонатный буфер способен нейтрализовать и избыток оснований. В этом случае ионы ОНˉ будут связаны углекислотой и вместо самого сильного основания ОНˉ образуется менее сильное 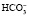
До тех пор, пока количество угольной кислоты и бикарбоната натрия изменяется пропорционально и соотношение между ними сохраняется 1:20, рН крови остается в пределах нормы.
Фосфатный буфер представлен солями одно- и двузамещенных фосфатов. Фосфатная буферная система обеспечивает 5 % буферной емкости крови, является основной буферной системой клеток.
Однозамещенная соль обладает кислыми свойствами, так как при диссоциации дает ион 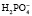
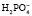
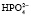
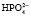
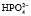
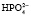
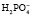
При нормальном рН в плазме соотношение фосфатных солей NаН2РО4: Nа2НРО4 = 1:4. Этот буфер имеет значение в почечной регуляции КОС, а также в регуляции реакции некоторых тканей. В крови же его действие главным образом сводится к поддержанию постоянства и воспроизводства бикарбонатного буфера.
Белковая буферная система является довольно мощным буфером, который способен проявлять свои свойства за счёт амфотерности белков. Белковая буферная система обеспечивает 7 % буферной емкости крови. Белки плазмы крови содержат достаточное количество кислых и основных радикалов, поэтому эта буферная система действует в зависимости от среды, в которой происходит диссоциация белков.
Гемоглобиновый буфер является самой емкой буферной системой. На ее долю приходится до 75 % всей буферной емкости крови. Свойства буферной системы гемоглобину придает главным образом его способность постоянно находиться в виде двух форм – восстановленного (редуцированного) гемоглобина ННb и окисленного (оксигемоглобина) НbО2.
Гемоглобиновый буфер, в отличие от бикарбонатного, в состоянии нейтрализовать как нелетучие, так и летучие кислоты. Окисленный гемоглобин ведёт себя как кислота, увеличивая концентрацию ионов водорода, а восстановленный (дезоксигенированный) – как основание, нейтрализуя H+.
Гемоглобин является классическим примером белкового буфера и эффективность его достаточно высока. Гемоглобин в шесть раз более эффективен как буфер, чем плазменные протеины.
Переход окисленной формы гемоглобина в восстановленную форму предупреждает сдвиг рН в кислую сторону во время контакта крови с тканями, а образование оксигемоглобина в легочных капиллярах предотвращает сдвиг рН в щелочную сторону за счет выхода из эритроцитов СО2 и иона хлора и образования в них бикарбоната.
Система аммиак/ион аммония (NH3/NH4+) – действует преимущественно в моче.
Помимо буферных систем в поддержании постоянства рН активное участие принимают физиологические системы, среди которых основными являются легкие, почки, печень, желудочно-кишечный тракт.
Система дыхания играет значительную роль в поддержании кислотно-щелочного баланса организма, однако для нивелирования сдвига рН крови им требуется 1–3 минуты. Роль легких сводится к поддержанию нормальной концентрации углекислоты, и основным показателем функционального состояния легких является парциальное напряжение углекислого газа в крови. Легочные механизмы обеспечивают временную компенсацию, так как при этом происходит смещение кривой диссоциации оксигемоглобина влево и уменьшается кислородная емкость артериальной крови.
При устойчивом состоянии газообмена легкие выводят углекислого газа около 850 г в сутки. Если напряжение углекислого газа в крови повышается сверх нормы на 10 мм рт. ст., вентиляция увеличивается в 4 раза.
Роль почек в регуляции активной реакции крови не менее важна, чем деятельность дыхательной системы. Почечный механизм компенсации более медленный, чем респираторный. Полноценная почечная компенсация развивается только через несколько дней после изменения pH.
Экскреция кислот при обычной смешанной пище у здорового человека превышает выделение оснований, поэтому моча имеет кислую реакцию (рН 5,3–6,5) и концентрация в ней ионов водорода примерно в 800 раз выше, чем в крови. Почки вырабатывают и выделяют с мочой количество ионов водорода, эквивалентное их количеству, непрерывно поступающему в плазму из клеток организма, совершая при этом замену ионов водорода, секретируемых эпителием канальцев, на ионы натрия первичной мочи. Этот механизм осуществляется с помощью нескольких химических процессов.
Первым из них является процесс реабсорбции натрия при превращении двузамещенных фосфатов в однозамещенные. При истощении фосфатного буфера (при рН мочи ниже 4,5) реабсорбция натрия и бикарбоната осуществляется за счет аммониогенеза.
Второй процесс, который обеспечивает задержку натрия в организме и выведение излишка ионов водорода, – это превращение в просвете канальцев бикарбонатов в угольную кислоту.
Третьим процессом, который способствует сохранению натрия в организме, является синтез в дистальных почечных канальцах аммиака (аммониогенез) и использование его для нейтрализации и выведения кислых эквивалентов с мочой.
Образовавшийся свободный аммиак легко проникает в просвет канальцев, где, соединяясь с ионом водорода, превращается в плохо диффундирующий аммонийный катион 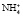
В общем итоге концентрация водородных ионов в моче может превышать концентрацию водородных ионов в крови в несколько сотен раз.
Это свидетельствует об огромной способности почек выводить из организма ионы водорода.
Почечные механизмы регуляции КОС не могут скорректировать рН в течение нескольких минут, как респираторный механизм, но они функционируют в течение нескольких дней, пока рН не вернется к нормальному уровню.
Регуляция КОС с участием печени. Печень окисляет до конечных продуктов недоокисленные вещества крови, оттекающей от кишечника; синтезирует мочевину из азотистых шлаков, в частности из аммиака и из хлорида аммония, поступающих из желудочно-кишечного тракта в кровь портальной вены; печени присуща выделительная функция и поэтому при накоплении в организме избыточного количества кислых или щелочных продуктов метаболизма они могут выделяться с желчью в желудочно-кишечный тракт. При избытке кислот в печени усиливается их нейтрализация и одновременно тормозится образование мочевины. Неиспользованный аммиак нейтрализует кислоты и увеличивает выведение аммонийных солей с мочой. При возрастании количества щелочных валентностей мочекинообразование возрастает, а аммониогенез снижается, что сопровождается уменьшением выведения с мочой аммонийных солей.
Концентрация водородных ионов в крови зависит также от деятельности желудка и кишечника. Клетки слизистой желудка секретируют соляную кислоту в очень высокой концентрации. При этом из крови ионы хлора выделяются в полость желудка в соединении с ионами водорода, образующимися в эпителии желудка с участием карбоангидразы. Взамен хлоридов в плазму в процессе желудочной секреции поступает бикарбонат.
Поджелудочная железа активно участвует в регуляции рН крови, так как она генерирует большое количество бикарбоната. Образование бикарбоната тормозится при избытке кислот и усиливается при их недостатке.
Кожа может в условиях избытка нелетучих кислот и оснований выделять последние с потом. Это имеет особое значение при нарушении функции почек.
Костная ткань. Это наиболее медленно реагирующая система. Механизм ее участия в регуляции рН крови состоит в возможности обмениваться с плазмой крови ионами Са2+ и Na+ в обмен на протоны Н+. Происходит растворение гидроксиапатитных кальциевых солей костного матрикса, освобождение ионов Са2+ и связывание ионов НРО42– с Н+ с образованием дигидрофосфата, который уходит с мочой. Параллельно при снижении рН (закисление) происходит поступление ионов H+ внутрь остеоцитов, а ионов калия – наружу.
Оценка кислотно-основного состояния организма
При изучении кислотно-щелочного баланса наибольшее значение имеет исследование крови. Показатели в капиллярной крови близки к показателям артериальной. В настоящее время показатели КОС определяют эквилибрационным микрометодом Аструпа. Данная методика позволяет, помимо истинного рН крови, получить показатель напряжения СО2 в плазме (рСО2), истинный бикарбонат крови (АВ), стандартный бикарбонат (SB), сумму всех оснований крови (ВВ) и показатель дефицита или избытка оснований (ВЕ).
РОЛЬ ПОЧЕК В ПОДДЕРЖАНИИ КИСЛОТНО-ОСНОВНОГО РАВНОВЕСИЯ
Почки оказывают значительное влияние на кислотно-основное равновесие, но оно сказывается по истечении значительно большего времени, чем влияние буферных систем крови и легких. Влияние буферных систем крови обнаруживается в течение 30 с. Легким требуется примерно 1–3 мин, чтобы сгладить наметившийся сдвиг концентрации водородных ионов в крови, почкам необходимо около 10–20 ч для восстановления нарушенного кислотно-основного равновесия.
Основным механизмом поддержания концентрации водородных ионов в организме, реализуемым в клетках почечных канальцев, являются процессы реабсорбции натрия и секреции ионов водорода. Этот механизм осуществляется с помощью нескольких химических процессов. Первый из них – реабсорбция натрия при превращении двузамещенных фосфатов в одноза-мещенные. Почечный фильтрат, формирующийся в клубочках, содержит достаточное количество солей, в том числе и фосфатов. Однако концентрация двузамещенных фосфатов постепенно убывает по мере продвижения первичной мочи по почечным канальцам. Так, в крови отношение однозаме-щенного фосфата к двузамещенному составляет 1:4, в клубочковом фильтрате – 9:1, в моче, которая проходит через дистальный сегмент нефрона,– 50:1. Это объясняется избирательным всасыванием канальцевыми клетками ионов натрия. Вместо них из канальцевых клеток в просвет почечного канальца выделяются ионы водорода. Таким образом, двузамещенный фосфат Na2HPO4превращается в однозамещенный NaH2PO4и в таком виде выделяется с мочой. В клетках канальцев из угольной кислоты образуется бикарбонат, увеличивая тем самым щелочной резерв крови.
Второй химический процесс, который обеспечивает задержку натрия в организме и выведение излишка водородных ионов,– это превращение в просвете канальцев бикарбонатов в угольную кислоту. В клетках канальцев при взаимодействии воды с углекислым газом под влиянием карбоан-гидразы образуется угольная кислота. Водородные ионы угольной кислоты выделяются в просвет канальца и соединяются там с анионами бикарбоната; эквивалентный этим анионам натрий поступает в клетки почечных канальцев. Образовавшаяся в просвете канальца Н2СО3 легко распадается на СО2 и Н2О и в таком виде покидает организм.
Третьим процессом, который также способствует сохранению натрия в организме, является образование в почках аммиака, который используется вместо других катионов для нейтрализации и выведения кислых эквивалентов с мочой. Основным источником этого служат процессы дезаминиро-вания глутамина, а также окислительного дезаминирования аминокислот, главным образом глутаминовой кислоты.
Распад глутамина происходит при участии фермента глутаминазы, при этом образуются глутаминовая кислота и свободный аммиак (см. главу 12). Глутаминаза обнаружена в различных органах и тканях человека, однако наибольшая ее активность отмечена в тканях почек. В общем итоге соотношение концентрации водородных ионов в моче и крови может составить 800:1 – настолько велика способность почек выводить из организма ионы водорода. Процесс усиливается в тех случаях, когда возникает тенденция к накоплению ионов водорода в организме.
При участии какого фермента в почечных канальцах происходит диссоциация угольной кислоты
а) Секреция протонов и реабсорбция ионов бикарбоната в почечных канальцах. Секреция протонов и реабсорбция ионов бикарбоната происходят практически во всех частях канальцевой системы, за исключением тонкого отдела петли Генле. В целом процесс реабсорбции бикарбоната по ходу тубулярного сегмента нефрона изображен на рисунке ниже.
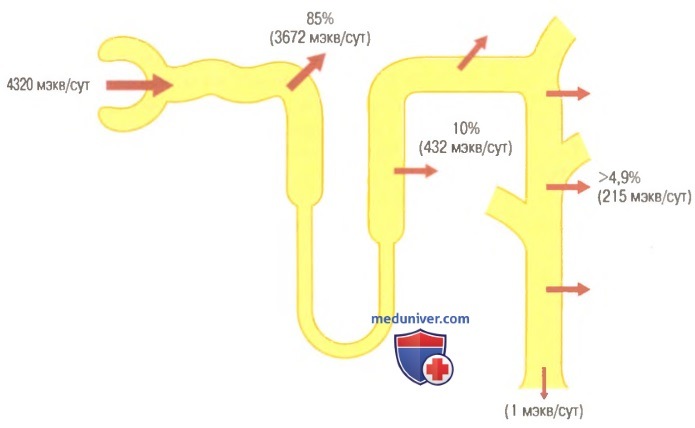
Следует помнить, что для реабсорбции каждого иона бикарбоната в просвет канальца необходимо секретировать один протон.
Около 80-90% реабсорбции ионов бикарбоната (и канальцевой секреции протонов) приходится на проксимальный каналец, поэтому лишь небольшое их количество поступает в дистальные сегменты нефрона. В толстом восходящем отделе петли Генле реабсорбируются другие 10% бикарбоната, прошедшего через почечный фильтр, а остаток поглощается дистальным канальцем и собирательной трубочкой. Как уже обсуждалось ранее, механизм реабсорбции бикарбонатов связан с канальцевой секрецией протонов, однако в различных сегментах канальцевой системы этот процесс протекает по-разному.
б) Секреция ионов водорода в проксимальных сегментах нефрона осуществляется благодаря вторично активному транспорту. Эпителиальные клетки проксимального канальца, толстого восходящего отдела петли Генле, начальных отделов дистальных канальцев секретируют протоны в просвет канальцев благодаря контртранспорту с ионами Na+ (для облегчения понимания просим вас изучить рисунок ниже).
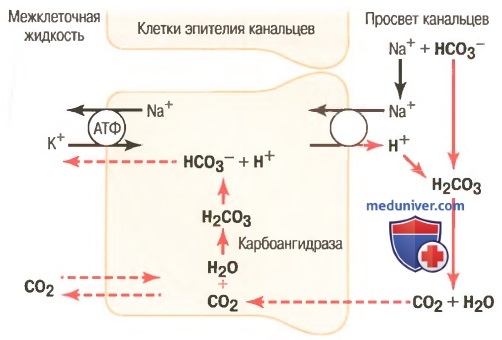
Этот вторично активный механизм секреции связан с переносом ионов Na+ в клетку через апикальную мембрану с помощью белка, обменивающего натрий на протон.
Источником энергии для перемещения ионов Н+ в клетку служит производная градиента концентрации для Na+, который создается работой Na+/K+-насоса (АТФ-азы), расположенной на базолатеральной мембране эпителия канальцев. Таким способом реабсорбируется более 90% бикарбоната, что требует секреции в просвет канальцев ионов Н+ около 3900 мэкв/сут. Тем не менее, этот механизм не обеспечивает создание высокой концентрации ионов Н+ в моче: жидкость в просвете канальцев закисляется лишь в собирательных трубочках и каналах.
Протоны выделяются в просвет канальца с помощью противотранспорта с ионами Na+. Другими словами, перед тем как ионы Na+ переместятся через апикальную мембрану внутрь клетки, они вначале объединяются с мембранным белком-переносчиком. В то же время с другой стороны к белку-переносчику присоединяется ион Н+. Ион Na+ перемещается в клетку по градиенту концентрации, установленному АТФ-азой Na+/K+-насоса, расположенного на базолатеральной поверхности клетки. Энергия, затраченная на создание градиента концентрации, обеспечивает движение ионов Na+ внутрь клетки, а также обусловливает перемещение ионов Н+ в противоположном направлении: из клетки в просвет канальца.
Кислотообразующая функция почки
КИСЛОТООБРАЗУЮЩАЯ ФУНКЦИЯ ПОЧКИ, Минск, 2009
УДК: 616.61:612.461.25 (075.9)
ББК 56.9 я73
В 79
Рекомендовано в качестве издания УМС государственного учреждения образования “Белорусская медицинская академия последипломного образования” (ректор профессор Хулуп Г. Я.)
протокол № 6 от 16 декабря 2008 г.
Рецензенты:
А. Н. Сукало, доктор медицинских наук, профессор
заведующий 1-й кафедрой детских болезней БГМУ.
Н. И. Симченко, доктор медицинских наук,
Могилёвская областная клиническая больница.
Вощула, В. И.
В 79 Кислотообразующая функция почки: учеб.- метод. пособие /
В. И. Вощула, В. С. Пилотович, Н. И. Доста. – Минск: ******, 2009.-
Пособие содержит современные данные о кислотно-основном равновесии, методах его исследования и коррекции. Особое внимание уделено метаболическим нарушениям кислотно-основного равновесия. Описаны буферные системы организма и роль почки в регуляции кислотно-основного баланса организма. Освещены вопросы заболеваний почек, связанных с изменением рН мочи.
Пособие предназначено для урологов, нефрологов, терапевтов, педиатров, врачей общей практики и студентов старших курсов медицинских вузов.
УДК: 616.61:612.461.25 (075.9)
ББК 56.9 я73
СОКРАЩЕНИЯ.. 4
Кислотно-щелочное равновесие.. 5
Исследование кислотно-щелочного равновесия. 6
Нарушения кислотно-щелочного равновесия. 8
Буферные системы. 11
АЦИДИФИКАЦИЯ МОЧИ В НОРМЕ.. 18
Буферные системы в мочи: 21
Почечный канальциевый ацидоз. 21
Проксимальный канальцевый ацидоз (тип II) 22
Дистальный канальцевый ацидоз (тип I) 25
Недостаточность минералокортикоидов (тип IV) 27
Ведение больных при почечном канальцевом ацидозе. 27
НЕФРОЛИТИАЗ ПРИ НАРУШЕНИИ ПУРИНОВОГО ОБМЕНА.. 34
МОЧЕКИСЛЫЙ ДИАТЕЗ. 36
КАМНИ МОЧЕВОЙ КИСЛОТЫ. 36
Лечение и метафилактика. 40
ЛИТЕРАТУРА.. 45
СОКРАЩЕНИЯ
почечный канальцевый ацидоз
Различные заболевания почек сопровождаются нарушением кислотно-щелочного равновесия и изменением уровня мочевого цитрата. Некоторые, как например дистальный почечный канальциевый ацидоз, могут выступать причинными факторами нефролитиаза. Кислотно-основной гомеостаз и уровень рН мочи влияют на диссоциацию мочевой кислоты и фосфатов, а так же ингибирование спонтанной кристаллизации путем комплексообразования с кальцием.
Кислотно-щелочное равновесие
Кислотно-щелочное равновесие (КЩР, кислотно-щелочной баланс, равновесие кислот и оснований) — относительное постоянство концентрации водородных ионов (Н + ) во внутренних средах организма, обеспечивающее полноценность метаболических процессов, протекающих в клетках и тканях.
Обмен веществ и энергии нуждается в непрерывном поступлении кислорода и выведении углекислоты, образующейся в результате метаболических превращений веществ. Кислород в клетки и углекислота из клеток переносятся кровью, которая является важнейшим компонентом внутренней среды организма. Помимо углекислоты кровь содержит и другие кислые продукты, например молочную, β-оксимасляную кислоты, а также основания. Реакция жидкостей организма зависит от соотношения в них кислот и оснований.
Состоянию кислотно-щелочного равновесия соответствует величина водородного показателя (рН) крови в диапазоне от 7,37 до 7,44; в эритроцитах рН составляет 7,19 ± 0,02 и отличается от рН крови на 0,2 единицы рН.
Водородный показатель
Водородный показатель или pH – это отрицательный десятичный логарифм концентрации (активности) ионов водорода (в г-ион/л) в растворе:
Водородный показатель служит количественной характеристикой кислотности растворов, которая оказывает существенное влияние на направление и скорость многих биохимических процессов. При обычной температуре (точнее, при 22 °С) pH = 7 для нейтральных, pH 7 для щелочных растворов.
Нейтральным водным растворам отвечает pH = 7 лишь при комнатных температурах. При повышении температуры диссоциация воды усиливается, KB возрастает, и при 100 °С чистая вода имеет pH ≈ 6. При температурах ниже 22 °С в чистой воде pH > 7.
Исследование кислотно-щелочного равновесия
Исследование КЩР проводят в артериальной, венозной или капиллярной крови. Застой крови при ее взятии должен быть минимальным и как можно менее продолжительным. Параметры, определяющие кислотно-щелочное равновесие, представлены в таблице 1.
Интегральным показателем состояния КЩР служит рН крови. В клинике определяют так называемый актуальный, или истинный, рН, который представляет собой рН цельной крови или плазмы, и метаболический рН, то есть рН крови или плазмы крови после соотнесения его величины с величиной рСО2. У здоровых лиц величина актуального и метаболического рН одинакова. При метаболическом ацидозе величина метаболического рН ниже, чем величина актуального рН, при респираторном ацидозе — выше. При метаболическом алкалозе величина метаболического рН выше величины актуального рН, а при респираторном алкалозе — ниже.
Оценка КЩР осуществляется, как правило, по содержанию компонентов бикарбонатной буферной системы и величине рН. Собственно, достаточно и двух показателей, чтобы с помощью уравнения Гендерсона-Хассельбаха найти третий. Широкую популярность, но не всеобщую доступность завоевал эквилибрационный метод Зиггард-Андерсена, Энгеля, Иоргенсена и Аструпа, выполняемый на аппарате конструкции тех же авторов (Siggard-Andersen O.,Engel K.,1960). Он представляет собой устройство для измерения величины электрического потенциала, cоздаваемого водородными ионами (рН) в микроколичествах крови.
Таблица 1. Параметры кислотно-щелочного равновесия, и их величины в норме [Siggaard-Andersen, 1979]
Показатель и его обозначение
Абсолютная величина в норме
Отрицательный десятичный логарифм концентрации водородных ионов
Парциальное давление углекислого газа в крови (рСО2)
Парциальное давление углекислого газа в газовой смеси, уравновешенной с кровью; отражает концентрацию СО2, растворенного в плазме крови (в т.ч. и гидратированного СО2)
Парциальное давление кислорода в крови (рО2)
Парциальное давление кислорода в газовой смеси, уравновешенной с кровью; отражает концентрацию О2 растворенного в плазме крови
9,6—13,7 (старше 40 лет)
72—104 (старше 40 лет)
Общее содержание СО2 в крови (прежнее название — щелочной резерв)
Концентрация общей углекислоты в крови и плазме, т.е. ее ионизированной фракции (ионы бикарбоната, карбамата и карбоната) и неионизированной фракции, содержащей в основном безводный углекислый газ и угольную кислоту
Стандартный бикарбонат плазмы крови
Концентрация бикарбонатных ионов в пробе крови, уравновешенной при 37° со стандартной газовой смесью при рСО2 — 40 мм рт. ст. и рО2 более 100 мм рт. ст.
Актуальные (истинные) бикарбонаты крови
Концентрация бикарбонатных ионов в плазме крови в физиологических условиях (при 38° в плазме крови, взятой без соприкосновения с воздухом)
Буферные основания (buffer base; ВВ)
Концентрация ионов бикарбоната и анионов белков (буферных оснований) в цельной крови, определяемая путем титрования до изоэлектрической точки белков при рСО2 равном 0
Избыток оснований (base excess; BE)
Разница между концентрацией сильных оснований в крови и в той же крови, оттитрованной сильной кислотой или сильным основанием до рН 7,4 при рСО2 40 мм рт. ст. и 37°. Положительные величины свидетельствуют об относительном дефиците некарбоновых кислот, потере ионов Н + ; отрицательные величины — об относительном избытке некарбоновых кислот и ионов Н +
Нарушения кислотно-щелочного равновесия
В тех случаях, когда компенсаторные механизмы организма не могут предотвратить нарушения кислотно-щелочного равновесия, развиваются два патологических состояния, противоположных по своей направленности: ацидоз и алкалоз. При ацидозе концентрация ионов Н + выше нормы; при этом рН крови ниже нормы. При уменьшении концентрации ионов Н + и соответственном повышении значения рН крови развивается алкалоз. Состояния, при которых рН ниже 6,8 и выше 8,0, не совместимы с жизнью. Однако на практике такие значения рН крови, как 6,8 и 8,0, не наблюдаются.
Ацидоз и алкалоз могут возникнуть вследствие различных причин, но в основном к нарушению кислотно-щелочного равновесия приводят три патологических процесса: нарушение выведения углекислого газа легкими, избыточное образование кислых продуктов в тканях и нарушение выведения из организма оснований с мочой. На практике простые формы расстройства кислотно-щелочного равновесия встречаются реже, чем комбинированные, обусловленные воздействием различных факторов.
По степени выраженности различают компенсированный и декомпенсированный ацидоз и алкалоз.
При компенсированных ацидозах и алкалозах буферные и физиологические системы организма, участвующие в нейтрализации и выведении из организма кислых и щелочных продуктов, несмотря на химические и функциональные сдвиги обеспечивают поддержание рН в пределах нормы. Следовательно, отношение Н2СО3 к NаНСОз приближается к норме (1:20), хотя при этом и происходят сдвиги во всех звеньях компенсации. При истощении и недостаточности защитных механизмов рН смещается за пределы нормы и развиваются декомпенсированные ацидоз и алкалоз.
По механизму развития ацидозы и алкалозы делят дыхательные и метаболические (таблица 2).
Таблица 2. Виды нарушений КЩР.
Патологическое состояние
Респираторный фактор (pCO2)
Метаболический ацидоз — самая частая и очень тяжелая форма нарушения кислотно-щелочного равновесия крови. В основе его лежит накопление в организме нелетучих кислых продуктов (ацетоуксусная, молочная кислоты и др.).
Причинами развития метаболического ацидоза являются:
1) избыточное образование кислых продуктов (кетоновые тела, молочная кислота и др.) при нарушениях обмена веществ (сахарный диабет, гипоксия, голодание и др.);
2) нарушение выведения из организма кислых веществ при недостаточности выделительной функции почек (нефриты, уремия);
3) потеря организмом большого количества оснований со щелочными пищеварительными соками (продолжительные поносы, свищи кишечника);
4) избыточное введение в организм минеральных кислот (отравление уксусной кислотой, введение животным минеральных кислот в эксперименте).
Нейтрализация избытка кислых продуктов происходит отчасти вследствие разбавления их внеклеточными жидкостями (быстро включающийся механизм). Далее эти продукты связываются бикарбонатами. Содержание последних в плазме крови падает, что является характерным показателем метаболического ацидоза. Соответственно уменьшается знаменатель дроби (H2CO3/NaHCO3). Создается относительный избыток угольной кислоты, которая под влиянием фермента карбоангидразы легких разлагается на Н2О и СО2. Последняя удаляется из организма при дыхании. Это — очень важный путь компенсации, однако уменьшение парциального давления СО2 может привести к понижению возбудимости дыхательного и сосудодвигательного центров.
В почках увеличивается выведение кислых продуктов в виде свободных кислот и аммонийных солей, возрастает реабсорбция бикарбонатов.
Пока в результате действия перечисленных механизмов отношение H2CO3/NaHCO3 сохраняется 1:20, ацидоз остается компенсированным, хотя при этом и происходят весьма существенные сдвиги (понижение содержания стандартных бикарбонатов в плазме крови, падение альвеолярного напряжения углекислоты и др.). При истощении и недостаточности регуляторных механизмов развивается декомпенсированный ацидоз со снижением рН.
Смещение активной реакции крови в кислую сторону приводит к тяжелым нарушениям функций организма. Нарушается работа сердца (тахикардия, экстрасистолия, в тяжелых случаях — фибрилляция желудочков), снижается артериальное давление. Понижается сродство гемоглобина к кислороду, в результате чего образование оксигемоглобина в легких и отдача им кислорода в тканях затрудняются. Этот фактор в совокупности с нарушениями сердечной деятельности ведет к развитию гипоксемии и гипоксии.
По происхождению метаболические ацидозы могут быть следующими.
1. Катаболические ацидозы (как правило, гиперкалиемические и гиперхлоремические):
2. Ацидозы задержки (эндогенных кислот) в результате нарушений функции выделительных органов (прежде всего почек). Примером является уремический ацидоз, сопровождающий волемические или гемодинамические сдвиги с нарушением клубочковой фильтрации (“шоковая почка”), острые и хронические поражения клубочкового или канальцевого аппарата.
3. Ацидозы потери (буферных оснований) в результате нарушения реабсорбционной функции выделительных органов (кишечные, желчные, панкреатические свищи; поносы; функциональная недостаточность канальцевого аппарата почек).
5. Перераспределительные ацидозы (неклеточный, гиперка-лиемический или диссоциативный) ацидоз в результате обмена неклеточного калия на клеточный водород с ощелачиванием цитоплазмы (клеточный алкалоз), с блокадой бикарбонат-реабсорбционной функции почек и защелачиванием мочи за счет щелочного резерва плазмы, закислением неклеточной жидкости.
6. Случайные или суицидные ацидозы (отравления кислотами).
7. Ятрогенные ацидозы.
Необходимость выделения ятрогенных ацидозов в отдельную рубрику назрела в связи с чрезвычайной распространенностью неконтролируемых и часто неадекватных вмешательств в водно-электролитное и кислотно-щелочное состояние на разных уровнях (передозировка кислот при коррекции алкалоза; передозировка мочегонных антикарбоангидразного действия или слабительных; злоупотребление монорастворами; неадекватная оксигенация; пренебрежение к своевременной полноценной коррекции анемии, к правилам переливания крови и кровезаменителей и т.д.).
Буферные системы
Для поддержания кислотно-щелочного равновесия в организме существуют эффективные системы, способные обеспечить выведение или нейтрализацию водородных ионов (ионов Н + ) при их избытке или задержку ионов Н + в организме при их дефиците. К таким системам относятся буферные системы крови, дыхательная система (легкие) и выделительная система (почки).
Основные буферные системы организма человека:
— белки (их буферные свойства определяются наличием основных и кислотных групп). Белки крови (прежде всего гемоглобин, обусловливающий около 75% буферной способности крови) обеспечивают относительную устойчивость pH крови. У человека pH крови равен 7,35—7,47 и сохраняется в этих пределах даже при значительных изменениях питания и некоторых других условий.
— гемоглобин (оксигемоглобин/восстановленный гемоглобин).
Такой же механизм действия и другой буферной системы крови — фосфатной, роль кислоты в которой играет однозамещенный фосфат натрия NaH2PO4, а роль соли — двузамещенный фосфат натрия Na2HPO4. Так как фосфатов в крови меньше, чем бикарбонатов, емкость фосфатной буферной системы ниже, чем бикарбонатной.
При прохождении крови через легкие ее буферные системы разгружаются от кислых эквивалентов за счет выделения углекислоты, и буферные резервы крови восстанавливаются в прежнем объеме (чтобы восстановить кислотно-щелочное равновесие буферным системам крови нужно всего 30 с).
Легкие обладают значительным влиянием на КЩР, однако их эффект сказывается по прошествии большего промежутка времени, чем эффект буферных систем крови. Для того, чтобы ликвидировать сдвиг рН крови вправо или влево от нормальной величины, легким требуется примерно 1-3 мин. Однако, увеличивая количество выделяющейся в окружающую среду углекислоты, легкие быстро ликвидируют угрозу ацидоза.
Сказанным далеко не исчерпываются буферные возможности белков. Важнейшим их проявлением является участие в обмене аммиака. Судя по сведениям, приводимым в руководствах, посвященных КЩР, аммониогенез является лишь точкой соприкосновения обменов аммиака и протонов (в почках, где в процессе освобождения аммиака из аминокислот и их амидов (глутамина, аспарагина) с участием карбоангидразы осуществляется регенерация бикарбонатного буфера).
Общеизвестно, что аммиак является продуктом катаболизма аминокислот, обеспечивающих в обычных условиях примерно 10% энергетических нужд организма человека. Его суточная продукция составляет около 120 мг. Известно также, что расщепление аминокислот осуществляется в митохондриях, то есть там же, где генерируются протоны из субстратов углеводного и жирового происхождения. Иными словами, обмен аммиака и протонов сопряжен по месту.
Дезаминирование (освобождение аминогруппы от аминокислот) уже само по себе не что иное, как связывание протонов:
Одновременно из аминокислот образуются субстраты, утилизирующиеся как в цикле Кребса, так и в процессе глюконеогенеза. Аммониогенез всегда сопутствует практически всем состояниям, ведущим к ацидозу (умственная и физическая перегрузка, перегревание, аноксия, гиперкапния). То есть катаболизм аминокислот ситуационно сопряжен с обменом протонов при энергообеспечении организма.
Установлено, что активирующими факторами для ответственных за обмен аммиака ферментов (например, глутаматдегидрогеназы) являются ацидоз и снижение соотношения между АТФ и АДФ. Не случайно, например, аминирование а-кетоглутарата сопровождается регенерацией окисленных форм дегидрогеназ (НАД и НАДФ), необходимых для поддержания гликолиза в условиях тампонады цикла Кребса при гипоксии или гиперкапнии. Образование аммиака в почках в условиях ацидоза возрастает в 4-5 раз и коррелирует с содержанием глутамина в протекающей через них крови. Таким образом, дезаминирование и обмен протонов сопряжены друг с другом и по интенсивности проявления.
За счет этой высокой проникаемости аммиак оказывается более токсичным, чем другие даже более сильные основания. Кроме того, аммиак извращает обмен аминокислот, препятствуя синтезу белка и нуклеиновых кислот. Наконец, образуя при растворении в воде катион аммония, он изменяет активную реакцию среды (то есть рН) и искажает влияния катионов (калия, натрия, кальция, магния) на неспецифические и на специфические функции клеток.
Обезвреживание аммиака осуществляется путем:
— образования аммонийных солей.
Суммарное уравнение цикла мочевины имеет вид:
На каждую образующую молекулу мочевины потребляется один ион бикарбоната, 2 иона аммония и 4 макроэргических фосфатных связи.
Естественно, при интенсификации окислительно-восстановительных процессов при (или) недостаточных обеспечении кислородом и связывании протонов доля мочевинообразования в связывании аммиака резко падает. Решающее значение в этом процессе приобретают кетокислоты: пируват и α-кетоглутарат, аминирование которых сопровождается соответственно образованием аминокислот аланина, глутаматаспартата и фумарата. В таком виде аммиак поступает к почкам и затем покидает организм в виде хлорида аммония.
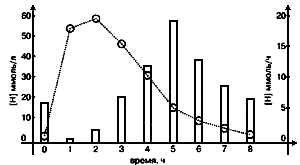
Рисунок 1. Изменения рН мочи на протяжении суток.
АЦИДИФИКАЦИЯ МОЧИ В НОРМЕ
Приблизительно 85 % профильтрованного бикарбоната реабсорбирутся в проксимальных канальцах. У недоношенных детей и здоровых новорожденных реабсорбция транзиторно снижается, и бикарбонаты теряются уже тогда, когда их уровень в сыворотке превышает 20 – 22 ммоль/л. Реабсорбция бикарбонатов в проксимальных канальцах включает в себя секрецию ионов водорода и их просвет в обмен на ион натрия. Ион водорода связывается с профильтрованным ионом бикарбоната с образованием угольной кислоты, которая под влиянием карбоангидразы диссоциирует на углекислый газ и воду. Углекислый газ диффундирует в клетки проксимальных канальцев, в которых под влиянием карбоангидразы вновь превращается в угольную кислоту. Угольная кислота диссоциирует с образованием иона водорода, который вновь секретируется для того, чтобы связать дополнительное количество бикарбоната с образованием ионов, проникающих в околоканальцевые капилляры. Остальные 15 % профильтрованного бикарбоната реабсорбируются в дистальных канальцах. В норме почки реабсорбируют весь профильтровавшийся бикарбонат, но это не делает мочу кислой. Ацидификация мочи происходит за счет секреции ионов водорода в дистальных канальцах (что отчасти зависит от минералокортикоидов) и секреции ионов аммония (при этом образуется ион аммония в кислой моче). Экскреция одного NН4 эквивалентна удалению из организма одного Н + иона. В проксимальных канальцах ангиотензин II и адренергические катехоламины повышают уровень секреции ионов водорода. Допамин и паратгормон ингибируют уровень секреции ионов водорода.
Низкие значения рН
— высокое потребление жиров и белка;
— потеря желудочного содержимого;
— диабет / метаболический синдром;
— идиопатический дефект продукции аммония;
— инсулинорезистентность / метаболический синдром.
По результатам нескольких исследований показано, что многие из пациентов с метаболическим синдромом имеют почечные камни из мочевой кислоты. Около 50% больных с камнями из мочевой кислоты имеют нарушение толерантности к глюкозе или сахарный диабет II типа. Пациенты с инсулинорезистентностью имеют более низкие значения рН мочи. У них снижена продукция аммония (NH4) из аммиака (NH3). Компенсаторным механизмом является повышение зависимой титруемой кислотности (TA), которая снижает рН мочи (рисунок 2).
Рисунок 2. Ацидификация мочи в норме и при инсулинорезистентности.
Отдельным пунктом следует рассмотреть нарушение кислотообразующей функции почки при метаболическом синдроме, причиной которого у мужчин является возрастной андрогенный дефицит. Известно, что у мужчин c возрастом постепенно снижается процесс образования половых гормонов, в первую очередь, тестостерона. Тестостерон является основным мужским половым гормоном, его уровень в крови превышает концентрацию любых других андрогенных соединений. Нарушение обмена пуринов наряду с классическими составляющими метаболического синдрома (артериальная гипертензия, сахарный диабет, нарушение холестеринового обмена и абдоминальное ожирение) обеспечивает повышение уровня мочевой кислоты, а изменения кислотообразующей функции почки из-за нарушения секреции аммония на фоне сахарного диабеты, обеспечивает высокий риск камнеобразования из мочевой кислоты. Эффективная терапия в данном случае имеет место при назначении тестостерона в виде геля “Андрогель”, который наносится на кожу. Суточная доза рассчитывается индивидуально. При использовании Андрогеля отсутствуют супрафизиологические пики концентрации тестостерона и его уровень поддерживается в пределах нормального физиологического диапазона. Нормализация уровня мочевой кислоты и рН мочи происходит в данном случае за счет купирования симптомов, составляющих метаболический синдром и нормализации обмена пуринов.
Высокие значения рН
— потеря содержимого тонкого кишечника;
— почечный канальцевый ацидоз;
Большинство кислых продуктов, образующихся в организме, экскретируется с мочой и связывается буферными системами.
Буферные системы в мочи:
2) HPO4 2- / креатинин
Почечный канальциевый ацидоз
Почечный канальцевый ацидоз (ПКА) – это клиническое состояние, характеризующееся системным гиперхлоремическим ацидозом, связанным с нарушением ацидификации мочи. Существуют три типа заболевания: дистальный (тип I), проксимальный (тип II) ПКА и дефицит минералокортикоидов (тип IV). Предполагавшийся ранее в этой классификации III тип, как выяснилось, относится к типу I (таблица 3).