Закон сохранения и превращения энергии
1. Закон сохранения механической энергии утверждает, что.
2. Какая формула выражает закон сохранения механической энергии?

3. В каком из приведённых случаев происходит превращение механической энергии во внутреннюю энергию?
а) Кусочек Свинца ударами молотка расплющивают в пластинку.
б) Горный поток воды, перетекая с уступа на уступ, попадает наконец в речное русло на равнине.
в) Самолет вдет на посадку и приземляется.
г) Упавший на пол мяч отскакивает от него.
4. В каком из названных здесь примеров внутренняя энергия превращается в механическую?
а) Первобытный человек добывал огонь трением одного куска дерева о другой.
б) Крышка чайника, в котором кипит вода, подпрыгивает.
в) Распиливающая бревно пила нагревается.
г) От вращающегося точильного камня, когда к нему прижимают лезвие ножа, отлетают искры — раскаленные частицы металла.
5. При теплопередаче более холодное тело получает такое количество теплоты, какое.
6. Один из основных законов природы — закон сохранения и превращения энергии выполняется.
7. При забивании молотом в грунт сваи произведена работа 12 кДж. Какая энергия и на сколько изменилась при этом?
а) Внутренняя энергия сваи; на 12 кДж.
б) Внутренняя энергия сваи и молота; на 12 кДж.
в) Механическая энергия молота и сваи; на 6 кДж каждого нз этих тел.
г) Внутренняя энергия сваи, молота и грунта; в сумме на 12 кДж.
Количество теплоты. Уравнение теплового баланса
Урок 36. Физика 10 класс ФГОС
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Количество теплоты. Уравнение теплового баланса»
На прошлых уроках мы говорили о том, что изменить состояние термодинамической системы можно двумя способами. Первый характеризуется передачей энергии в процессе механического взаимодействия тел. Такую форму передачи энергии в термодинамике (как и в механике) называют работой.
Второй способ передачи энергии осуществляется при непосредственном обмене энергией между хаотически движущимися частицами взаимодействующих тел. Если, например, привести в соприкосновение два тела с разными температурами, то частицы более нагретого тела будут передавать часть своей энергии частицам более холодного тела. В результате внутренняя энергия первого тела уменьшается, а второго — увеличивается.
Процесс передачи энергии от одного тела к другому без совершения работы называют теплопередачей.
Ещё в восьмом классе мы говорили о том, что существуют три вида теплопередачи: это теплопроводность, конвекция и излучение.
Давайте вспомним, что теплопроводностью называется процесс теплообмена между телами (или частями тела) при их непосредственном контакте. При теплопроводности не происходит переноса вещества.
Конвекция представляет собой теплопередачу нагретыми потоками жидкости или газа от одних участков занимаемого ими объёма в другие (то есть конвекция сопровождается переносом вещества). Она может протекать только в жидкостях и газах, так как в твёрдом теле вещество не может перемещаться по объёму.
А теплообмен при излучении осуществляется на расстоянии посредством электромагнитных волн. Главной особенностью излучения является то, что оно возможно не только в среде, но и в вакууме.
Количественной мерой энергии, переходящей от одного тела к другому в процессе теплопередачи, является количество теплоты.
Напомним, что обозначается количество теплоты большой латинской буквой Q. А единицей её измерения в СИ является джоуль (Дж). Но иногда для измерения количества теплоты используют и внесистемную единицу — калорию.
Одна калория — это количество теплоты, которое необходимо затратить, чтобы нагреть один грамм воды на один градус Цельсия^ 1 кал = 4,19 Дж.
Основное отличие работы от количества теплоты состоит в том, что работа характеризует процесс изменения внутренней энергии системы, сопровождающийся превращением энергии из одного вида в другой. Количество теплоты же характеризует процесс передачи внутренней энергии от одних тел к другим (от более нагретых к менее нагретым), не сопровождающийся превращениями энергии.
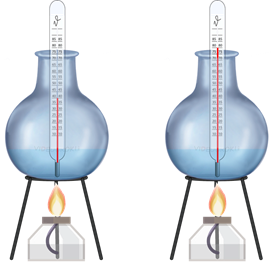
А теперь давайте с вами вспомним от чего зависит количество теплоты. Для этого давайте проведём несколько простых экспериментов. Возьмём два одинаковых сосуда в которых находится разное количество воды, но при одинаковой температуре.
При помощи электроплитки будем подводить тепло к сосудам. Спустя несколько минут после включения плитки мы с вами заметим, что вода в сосуде с меньшим количеством воды нагрелась на большее число градусов, хотя оба сосуда получили одно и тоже количество теплоты. Следовательно, чем больше масса тела, тем большее количество теплоты требуется к нему подвести для нагревания на одно и тоже число градусов.
Продолжим опыты. Опять берём два одинаковых сосуда, но с равным количеством воды при одинаковой температуре. Будем нагревать воду в первом сосуде на 20 о С, а во втором — на 60 о С. Включим секундомер одновременно с плиткой и немного подождём.
На нагревание воды на 20 о С тратится почти в три раза меньше времени, чем на нагревание такой же массы воды, но на 60 о С. Значит, количество теплоты пропорционально изменению температуры тела.
Теперь пусть у нас в одном из сосудов находится вода, а во втором — такое же количество бензина. Через несколько минут после включения нагревателей, проверим температуры обеих жидкостей.
Не трудно заметить, что, получив за одинаковый промежуток времени от нагревателя равное с водой количество теплоты, бензин нагрелся сильнее. Значит, количество теплоты, которое необходимо затратить для увеличения температуры тела, зависит и от рода вещества, из которого это тело сделано:
При остывании тела его конечная температура оказывается меньше начальной, и, поэтому, количество теплоты, отдаваемой телом, отрицательно.
В полученной нами в формуле коэффициент с — это удельная теплоёмкость вещества. Она численно равна количеству теплоты, которую получает или отдаёт вещество массой один килограмм при изменении его температуры на один кельвин (или один градус Цельсия, так изменение температуры в этих шкалах совпадают).
Из определения следует, что единицей удельной теплоёмкости в СИ является:
Значения удельной теплоёмкости веществ определяют экспериментально.
Самую большую удельную теплоёмкость, из представленных в таблице веществ, имеет вода. Для нагревания одного её килограмма всего на один кельвин необходимо затратить 4200 Дж теплоты.
Обратите внимание ещё и на то, что в этой таблице нет удельных теплоёмкостей газов. Дело в том, что их удельная теплоёмкость зависит от того, при каком процессе осуществляется теплопередача. Например, для нагревания газа при постоянном давлении ему нужно передать большее количество теплоты, чем для его нагревания при постоянном объёме, так как в первом случае газ будет расширяться и совершать работу, а во втором — только нагреваться. Но об удельной теплоёмкости газов мы с вами поговорим в одном из следующих уроков.
Следует помнить, что формула, которую мы получили для определения количества теплоты, справедлива только в том случае, если процесс теплопередачи НЕ сопровождается изменением агрегатного состояния вещества. Давайте посмотрим, что же будет происходить при фазовых переходах. Для этого проведём такой опыт. Возьмём два сосуда в которые поместим разное количество льда, находящегося при температуре плавления, и будем их нагревать. Не трудно заметить, что несмотря на постоянное подведение теплоты, температура льда остаётся постоянной. И она не будет изменяться до тех пор, пока весь лёд не перейдёт в жидкое состояние. Только после этого температура образовавшейся изо льда воды начинает повышаться. При этом, обратите внимание, что количество теплоты, которое необходимо затратить на плавление кристаллического вещества, предварительно нагретого до температуры плавления, прямо пропорционально массе этого вещества:
При обратном процессе, то есть в процессе кристаллизации, такое же количество теплоты вещество будет отдавать:
Коэффициент пропорциональности λ, входящий в формулу, называется удельной теплотой плавления. Она численно равна количеству теплоты, необходимому для превращения кристаллического вещества массой один килограмм, взятого при температуре плавления, в жидкость той же температуры:
Из определения следует, что единицей измерения удельной теплоты плавления в СИ является джоуль, делённый на килограмм:
Продолжим наши опыты. Пусть у нас есть сосуд с водой, к которому постоянно подводится теплота. Пока нагреваемая жидкость не кипит, часть сообщаемой ей энергии расходуется на компенсацию потери энергии при испарении, а часть — на увеличение внутренней энергии, о чём свидетельствует увеличение её температуры.
Однако, когда жидкость закипит, её температура перестаёт меняться, хотя теплота продолжает подводится. Очевидно, что теперь вся подводимая теплота расходуется на переход жидкости в газообразное состояние. И так происходит до тех пор, пока вся жидкость не превратится в пар.
Таким образом, чтобы превратить в пар жидкость при температуре кипения, необходимо передать ей определённое количество теплоты, которое прямо пропорционально массе жидкости:
При конденсации пара происходит выделение такого же количества теплоты:
Коэффициент пропорциональности «Эр» (r), входящий в формулу, называется удельной теплотой парообразования. Он численно равен количеству теплоты, которое необходимо передать жидкости массой один килограмм, находящейся при температуре кипения, для превращения её при постоянной температуре в пар:
Из определения следует, что единицей измерения удельной теплоты плавления в СИ является джоуль на килограмм:
В заключение отметим, что при теплообмене двух или нескольких тел абсолютное значение количества теплоты, которое отдало более нагретое тело, равно количеству теплоты, которое было получено более холодным телом.
Учитывая, что отданное количество теплоты считается отрицательным, а полученное — положительным, получается, что при теплообмене между телами, образующими теплоизолированную систему, суммарное количество теплоты, полученное ими, равняется нулю:
Записанное нами равенство называется уравнением теплового баланса и выражает, по сути, закон сохранения энергии.
Удельная теплоемкость вещества
Нагревание и охлаждение
Эти два процесса знакомы каждому. Вот нам захотелось чайку, и мы ставим чайник, чтобы нагреть воду. Или ставим газировку в холодильник, чтобы охладить.
Логично предположить, что нагревание — это увеличение температуры, а охлаждение — ее уменьшение. Все, процесс понятен, едем дальше.
Но не тут-то было: температура меняется не «с потолка». Все завязано на таком понятии, как количество теплоты. При нагревании тело получает количество теплоты, а при нагревании — отдает.
В процессах нагревания и охлаждения формулы для количества теплоты выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
В этих формулах фигурирует и изменение температуры, о котором мы сказали выше, и удельная теплоемкость, речь о которой пойдет дальше.
А вот теперь поговорим о видах теплопередачи.
Виды теплопередачи
Здесь все совсем несложно, их всего три: теплопроводность, конвекция и излучение.
Теплопроводность
Тот вид теплопередачи, который можно охарактеризовать, как способность тел проводить энергию от более нагретого тела к менее нагретому.
Речь о том, чтобы передать тепло с помощью соприкосновения. Признавайтесь, грелись же когда-нибудь возле батареи. Если вы сидели к ней вплотную, то согрелись вы благодаря теплопроводности. Обниматься с котиком, у которого горячее пузо, тоже эффективно.
Порой мы немного перебарщиваем с возможностями этого эффекта, когда на пляже ложимся на горячий песок. Эффект есть, только не очень приятный. Ну а ледяная грелка на лбу дает обратный эффект — ваш лоб отдает тепло грелке.
Конвекция
Когда мы говорили о теплопроводности, мы приводили в пример батарею. Теплопроводность — это когда мы получаем тепло, прикоснувшись к батарее. Но все вещи в комнате к батарее не прикасаются, а комната греется. Здесь вступает конвекция.
Дело в том, что холодный воздух тяжелее горячего (холодный просто плотнее). Когда батарея нагревает некий объем воздуха, он тут же поднимается наверх, проходит вдоль потолка, успевает остыть и спуститься обратно вниз — к батарее, где снова нагревается. Таким образом, вся комната равномерно прогревается, потому что все более горячие потоки сменяют все менее холодные.
Излучение
Пляж мы уже упоминали, но речь шла только о горячем песочке. А вот тепло от солнышка — это излучение. В этом случае тепло передается через волны.
Обоими способами. То тепло, которое мы ощущаем непосредственно от камина (когда лицу горячо, если вы расположились слишком близко к камину) — это излучение. А вот прогревание комнаты в целом — это конвекция.
Удельная теплоемкость: понятие и формула для расчета
Формулы количества теплоты для нагревания и охлаждения мы уже разбирали, но давайте еще раз:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
В этих формулах фигурирует такая величина, как удельная теплоемкость. По сути своей — это способность материала получать или отдавать тепло.
С точки зрения математики удельная теплоемкость вещества — это количество теплоты, которое надо к нему подвести, чтобы изменить температуру 1 кг вещества на 1 градус Цельсия:
Удельная теплоемкость вещества
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Также ее можно рассчитать через теплоемкость вещества:
Удельная теплоемкость вещества
c — удельная теплоемкость вещества [Дж/кг*˚C]
C — теплоемкость вещества [Дж/˚C]
Величины теплоемкость и удельная теплоемкость означают практически одно и то же. Отличие в том, что теплоемкость — это способность всего вещества к передаче тепла. То есть формулу количества теплоты для нагревания тела можно записать в таком виде:
Количество теплоты, необходимое для нагревания тела
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Таблица удельных теплоемкостей
Удельная теплоемкость — табличная величина. Часто ее указывают в условии задачи, но при отсутствии в условии — можно и нужно воспользоваться таблицей. Ниже приведена таблица удельных теплоемкостей для некоторых (многих) веществ.
Тест. Количество теплоты. Уравнение теплового баланса
Список вопросов теста
Вопрос 1
Что такое количество теплоты?
Варианты ответов
Энергия, необходимая для нагревания тела на 1 0 С.
Внутренняя энергия тела при данной температуре.
Часть внутренней энергии, которую теряет или получает тело при теплопередаче.
Правильного ответа нет.
Вопрос 2
Для нагревания двух разных жидкостей одинаковой массы потребовалось одинаковое количество теплоты. Если первую жидкость нагрели на большее количество градусов, значит
Варианты ответов
Вопрос 3
Количество теплоты, требуемое для нагревания вещества на 10 К, составляет 1800 Дж. Найдите удельную теплоёмкость вещества, если его масса равна 0,5 кг. В ответ запишите только число.
Вопрос 4
Количество теплоты зависит от
Варианты ответов
Вопрос 5
Варианты ответов
Количественная мера энергии, переходящей от одного тела к другому в процессе теплопередачи.
Количество теплоты, которое необходимо затратить, чтобы нагреть 1 г воды на 1 о С.
Физическая величина, численно равная количеству теплоты, которую получает или отдаёт вещество массой 1 кг при изменении его температуры на 1 К.
Величина, численно равная количеству теплоты, необходимому для превращения кристаллического вещества массой 1 кг, взятого при температуре плавления, в жидкость той же температуры.
Вопрос 6
Вопрос 7
Укажите верную формулировку уравнения теплового баланса.
Варианты ответов
Вопрос 8
В каких единицах измеряется количество теплоты?
Варианты ответов
Вопрос 9
Вопрос 10
Тест. Повторение темы «Тепловые явления»
Список вопросов теста
Вопрос 1
Энергию движения и взаимодействия частиц, из которых состоит тело, называют.
Варианты ответов
Вопрос 2
Два камня лежали на столе. Первый камень начал падать со стола, а второй взяли и положили на зем лю. Изменилась ли внутренняя энергия камней?
Варианты ответов
Вопрос 3
После того как деталь обработали напильником, деталь нагрелась. Каким способом изменили внут реннюю энергию детали?
Варианты ответов
Вопрос 4
В каком из перечисленных случаев внутренняя энергия чашки не изменилась:
1) чашку переставили из шкафа на стол; 2) чашку передвинули по столу; 3) в чашку налили горячий чай.
Варианты ответов
Вопрос 5
Два железных бруска массами 200 и 300 г, взятых при комнатной температуре, охладили до одинако вой температуры. У какого бруска внутренняя энер гия изменилась больше?
Варианты ответов
Вопрос 6
Вид теплопередачи, при котором энергия передает ся от нагретого конца тела холодному, но само ве щество при этом не перемещается, называют.
Варианты ответов
Вопрос 7
Благодаря какому способу теплопередачи нагрева ется термометр, вывешенный за окно?
Варианты ответов
Вопрос 8
Какой способ теплопередачи помогает птицам с боль шими крыльями держаться на одной высоте, не взмахивая ими?
Варианты ответов
Вопрос 9
Как осуществляется передача энергии глиняной посуде, находящейся в печи?
Варианты ответов
Вопрос 10
Изменится ли температура тела, если оно испуска ет энергии столько же, сколько поглощает?
Варианты ответов
Вопрос 11
Удельной теплоемкостью называют.
Варианты ответов
Вопрос 12
В каких единицах измеряют количество теплоты?
Варианты ответов
Вопрос 13
Четыре шарика одинаковой массы нагрели до од ной и той же температуры. Какому шарику потребовалось для этого меньше энергии?
Варианты ответов
Вопрос 14
Какое количество теплоты выделится при охлаж дении 50 г серебра на 4 °С?
Варианты ответов
Вопрос 15
На сколько градусов нагрелось серебро массой 20 г, если ему сообщили 200 Дж количества теплоты?
Варианты ответов
Вопрос 16
Стальной кубик массой 60 г, нагретый до 285 °С, опустили в воду массой 125 г и температурой 21 °С. Через некоторое время их общая темпера тура стала равна 35 °С. Удельные теплоемкости: воды 4200 Дж/кг о С, стали 500 Дж/кг о С.
Как изменилась внутренняя энергия взаимодейст вующих тел?
Варианты ответов
Вопрос 17
Стальной кубик массой 60 г, нагретый до 285 °С, опустили в воду массой 125 г и температурой 21 °С. Через некоторое время их общая темпера тура стала равна 35 °С. Удельные теплоемкости: воды 4200 Дж/кг о С, стали 500 Дж/кг о С.
Какое количество теплоты отдано сталью?
Варианты ответов
Вопрос 18
Стальной кубик массой 60 г, нагретый до 285 °С, опустили в воду массой 125 г и температурой 21 °С. Через некоторое время их общая темпера тура стала равна 35 °С. Удельные теплоемкости: воды 4200 Дж/кг о С, стали 500 Дж/кг о С. Какое количество теплоты получено водой7?
Варианты ответов
Вопрос 19
Стальной кубик массой 60 г, нагретый до 285 °С, опустили в воду массой 125 г и температурой 21 °С. Через некоторое время их общая темпера тура стала равна 35 °С. Удельные теплоемкости: воды 4200 Дж/кг о С, стали 500 Дж/кг о С. Одинаковое ли количество теплоты отдано сталью и получено водой?
Варианты ответов
Вопрос 20
Стальной кубик массой 60 г, нагретый до 285 °С, опустили в воду массой 125 г и температурой 21 °С. Через некоторое время их общая темпера тура стала равна 35 °С. Удельные теплоемкости: воды 4200 Дж/кг о С, стали 500 Дж/кг о С. Какого результата можно было бы ожидать, если не учесть потери на нагревание (или охлаждение) сосуда, термометра, воздуха?
Варианты ответов
Вопрос 21
К каждой позиции первого столбца таблицы подберите позицию второго столбца так, чтобы получились верные утверждения:
1. При охлаждении тела удельная теплота сгорания вещества, из которого он сделан.
2. Тело принимает количество теплоты без изменения его агрегатного состояния. При этом его температура.
3. При уменьшении массы тела количество теплоты, требуемое для нагревании.
Цифры в ответе не повторяются.
Варианты ответов
Вопрос 22
Прочитайте текст и ответьте на вопрос.
Задавшись целью построить экономичный двигатель, Рудольф Дизель предпринял несколько попыток. В конце 1896г. Был построен окончательный, четвертый вариант опытного двигателя. Этот двигатель расходовал 0,24 кг на 1 л.с. в час керосина, КПД его составил 0,26. Таких показателей не имел еще ни один из существовавших до того времени двигателей. Работа двигателя осуществлялась за четыре такта. За первый ход поршня в цилиндр всасывался воздух, за второй он сжимался приблизительно до 3,5-4 МПа, нагреваясь при этом примерно до 600 о С. В конце второго хода поршня в среду сжатого (разогретого сжатием) воздуха через форсунку начинало вводиться жидкое топливо (при испытаниях использовался жидкий керосин). Попадая в среду разогретого воздуха, топливо воспламенялось и горело почти при постоянном давлении по мере подачи его в цилиндр, продолжавшейся примерно половину третьего хода поршня. На остальной части хода поршня происходило расширение продуктов сгорания. За четвертый ход поршня осуществлялся выпуск отработавших продуктов сгорания в атмосферу. В 897 году в Аугсбурге был создан первый практический дизельный двигатель.
Конструктивным отличием двигателя Дизеля от двигателя внутреннего сгорания (двигателя Отто) является …
Варианты ответов
Вопрос 23
Прочитайте текст и ответьте на вопрос.
Задавшись целью построить экономичный двигатель, Рудольф Дизель предпринял несколько попыток. В конце 1896г. Был построен окончательный, четвертый вариант опытного двигателя. Этот двигатель расходовал 0,24 кг на 1 л.с. в час керосина, КПД его составил 0,26. Таких показателей не имел еще ни один из существовавших до того времени двигателей. Работа двигателя осуществлялась за четыре такта. За первый ход поршня в цилиндр всасывался воздух, за второй он сжимался приблизительно до 3,5-4 МПа, нагреваясь при этом примерно до 600 о С. В конце второго хода поршня в среду сжатого (разогретого сжатием) воздуха через форсунку начинало вводиться жидкое топливо (при испытаниях использовался жидкий керосин). Попадая в среду разогретого воздуха, топливо воспламенялось и горело почти при постоянном давлении по мере подачи его в цилиндр, продолжавшейся примерно половину третьего хода поршня. На остальной части хода поршня происходило расширение продуктов сгорания. За четвертый ход поршня осуществлялся выпуск отработавших продуктов сгорания в атмосферу. В 897 году в Аугсбурге был создан первый практический дизельный двигатель.
В двигателе Дизеля происходят преобразования энергии.