Лечение пиелонефрита
Пиелонефрит – это воспалительное заболевание почек неспецифического характера. Чаще всего от заболевания страдают женщины. Его причина – проникновение в почки бактериальной инфекции, наиболее часто вызывает болезнь кишечная флора (кишечные палочки и энтерококки), реже – протей, золотистый стафилококк, синегнойная палочка и другие микроорганизмы. Иногда в роли возбудителя выступают вирусы или микоплазмы.
Возбудители заболевания могут попасть в почки из воспалительных очагов различной локализации: миндалин при хроническом тонзиллите, кариозных зубов, пазух носа при гайморите и т.д. Кроме этого, большое значение имеет проникновение инфекции из мочевыводящих путей при уретрите или цистите.
Лечение заболевания должно быть комплексным и подбираться индивидуально в соответствии с типом микроорганизма, вызвавшего патологический процесс. Большое значение имеет выявление и санация очагов хронической инфекции, которые могут быть причиной воспаления почек. Лечение пиелонефрита у женщин во время беременности может назначаться даже при отсутствии клинических проявлений, но при наличии бактериальной флоры в анализе мочи. При появлении признаков пиелонефрита ни в коем случае нельзя заниматься самолечением, это может стать причиной перехода инфекции в хроническую форму, которая очень тяжело поддается лечению.
Острый пиелонефрит
Острый пиелонефрит отличается ярко-выраженными симптомами. Температура тела повышается до 39-40°, лихорадка сопровождается ознобом, сильным потоотделением, головными болями, общей интоксикацией организма. Кроме этого, пациент жалуется на боль в поясничной области. Острая форма заболевания является показанием к экстренной госпитализации, особенно, если она сопровождается нарушениями мочеиспускания. На фоне гнойного воспаления почек могут развиться тяжелые осложнения: бактериальный шок, уросепсис, паранефрит. Лечение острого пиелонефрита чаще оперативное, так как необходимо ликвидировать очаги гнойного воспаления и восстановить отток мочи из лоханок. Антибиотики можно назначать только после того, как пассаж мочи возобновиться, иначе повышается риск развития бактериального шока. Если пациент обратился за врачебной помощью при первых признаках воспаления почек, до появления гнойных очагов, тогда в большинстве случаев можно обойтись консервативной терапией. Прогноз при заболевании благоприятный, если лечение начато до развития осложнений. В течение года после выздоровления необходимо регулярно посещать врача, ограничить физические нагрузки, избегать переохлаждения и контакта с нефротоксическими веществами (например, алкоголем).
Хронический пиелонефрит развивается на фоне неизлеченного острого, он может протекать практически бессимптомно или с периодическими обострениями. Пациент жалуется на утомляемость, отсутствие аппетита, сухость кожи, при двустороннем поражении почек могут быть выражены симптомы почечной недостаточности. В области поясницы наблюдаются умеренные тупые боли. Почки при хронической форме заболевания уменьшаются в размере, лоханки могут сильно деформироваться. Лечение хронического пиелонефрита консервативное, продолжается в течение нескольких лет. Анибактериальные препараты применяют курсами по 10 дней раз в месяц, в некоторых случаях показана длительная терапия антибиотиками со сменой препарата каждые 5-7 дней.
Терапия пиелонефрита направлена на:
Основные лекарственные препараты, которые применяются для лечения воспаления почек – это антибактериальные средства, их подбирают после определения типа возбудителя. Чаще всего применяют антибиотики широкого спектра действия, сульфаниламиды, нитрофураны. Лекарственные средства иногда комбинируют между собой или заменяют в процессе лечения. Подбирать препарат должен врач, так как многие антибактериальные препараты оказывают нефротоксическое действие, то есть, действуют на почки разрушающе. При неосложненных острых формах заболевания продолжительность приема антибиотиков – 7-14 дней, при наличии осложнений этот период увеличивается.
Лечение пиелонефрита у взрослых эффективнее при своевременном обращении к врачу. Развитие болезни можно предотвратить, если уделять внимание своему здоровью и лечить воспалительные заболевания других органов, особенно мочеполовой системы. Для их выявления нужно регулярно посещать уролога или гинеколога.
Антибактериальная терапия пиелонефрита
Опубликовано в журнале:
В мире лекарств »» №3 1999 И.Н. ЗАХАРОВА, ДОЦЕНТ КАФЕДРЫ ПЕДИАТРИИ, КАНДИДАТ МЕДИЦИНСКИХ НАУK
ПРОФЕССОР Н.А. КОРОВИНА, ЗАВЕДУЮЩАЯ КАФЕДРОЙ ПЕДИАТРИИ РОССИЙСКОЙ МЕДИЦИНСКОЙ АКАДЕМИИ ПОСЛЕДИПЛОМНОГО ОБРАЗОВАНИЯ, ГЛАВНЫЙ ДЕТСКИЙ НЕФРОЛОГ МЗ РФ
И.Е. ДАНИЛОВА, ЗАВЕДУЮЩАЯ ОТДЕЛЕНИЕМ ТУШИНСКОЙ ДЕТСКОЙ ГОРОДСКОЙ БОЛЬНИЦЫ
Э.Б. МУМЛАДЗЕ, ДОЦЕНТ КАФЕДРЫ ПЕДИАТРИИ, КАНДИДАТ МЕДИЦИНСКИХ НАУК
За последние пять лет частота заболеваний мочевой системы возросла почти в 2 раза [1]. Среди нефро- и уропатий основное место занимают микробно-воспалительные заболевания мочевой системы. В структуре почечной патологии за 1988-1997 годы, по нашим данным, микробно-воспалительные заболевания мочевой системы составляют 75,6%.
По материалам бактериологической лаборатории Тушинской детской больницы (зав. лабораторией М.В. Калинина) за 1995-1997 годы у больных с инфекцией мочевой системы в 88,4 % случаев высевалась грамотрицательная флора, и лишь в 11,4% случаев грамположительные бактерии. Наиболее часто встречалась кишечная палочка (39,3%). Высока частота выделения из мочи клебсиеллы (21,9%) и синегнойной палочки (10,3%) у «госпитальных» больных. Следует отметить, что нередко встречались микробные ассоциации (E.coli+Str.faecalis; E.coli+Staph.saprophyticus; Str.faecalis+Ent.cloacae; Str.faecalis+Staph.epidermitidis) и только в 40,8% случаев определялась монокультура. Положительные результаты бактериологического исследования мочи при пиелонефрите удается получить не всегда. В последние годы наметилась тенденция к снижению процента «высеваемости» микроорганизмов из мочи. Выявить «виновный» микроорганизм при посеве мочи удается у 42,0-75,7% больных пиелонефритом [5, 8, 11].
Быстрое развитие устойчивости микробной флоры к антибактериальным препаратам, изменение спектра микроорганизмов, вызывающих микробно-воспалительный процесс в мочевой системе, продукция многими из них бета-лактамаз, создают трудности при выборе антибактериального препарата и делают традиционную терапию неэффективной [14]. Это приводит к тому, что лечение инфекции мочевой системы становится более сложным и определяет необходимость создания все новых терапевтических средств и внедрения их в педиатрическую практику. Главным фактором, определяющим резистентность бактерий к антибиотикам, является продукция микроорганизмами бета-лактамаз, которые ингибируют активность антибиотиков.
При заболеваниях мочевой системы у детей вопрос о назначении антибиотика, его дозы определяется микрофлорой мочи, спектром действия антибиотика, чувствительностью к нему флоры, характером почечной патологии, функциональным состоянием почек. Известно, что многие антибактериальные препараты лучше действуют при определенных значениях рН мочи, что необходимо учитывать в процессе терапии.
В тяжелых случаях может применяться комбинированная антибактериальная терапия. При этом следует учитывать, что комбинировать необходимо антибактериальные препараты с синергическим действием.
Эффективность антибактериальной терапии зависит от:
Рост устойчивости микрофлоры может быть связан с:
Эмпирическая (стартовая) антибактериальная терапия (в условиях стационара)
У большинства больных с острым течением пиелонефрита до выделения возбудителя «стартовая» антибактериальная терапия назначается эмпирически, то есть основывается на знаниях этиологической характеристики наиболее вероятных возбудителей и их потенциальной чувствительности к данному препарату, поскольку посев мочи и определение чувствительности требуют времени, а начало терапии откладывать недопустимо (табл. 1). При отсутствии клинического и лабораторного (анализ мочи) эффекта через три дня эмпирической терапии проводится ее коррекция со сменой антибиотика.
Таблица 1. Эмпирическая (стартовая) антибактериальная терапия при тяжелой форме
Возможна «ступенчатая терапия»
Цефалоспорины 2 поколения (цефуроксим, цефамандол)
Цефалоспорины 3 поколения (цефотаксим, цефоперазон, цефтазидим, цефтриаксон, цефепим)
Аминогликозиды (гентамицин, нетромицин, амикацин др.)
Цефалоспорины 2 поколения (цефуроксим аксетил, цефаклор)
Цефалоспорины 3 поколения (цефтибутен)
Препараты группы нефторированных хинолонов (пипемидиновой кислоты, налидиксовой кислоты, производные 8-оксихинолина)
«Ступенчатая терапия» предусматривает использование при максимальной активности воспалительного процесса в течение 3-5 дней парентерального введения препаратов одной группы (внутривенно или внутримышечно) с последующей заменой на пероральный путь. При этом возможно применение препаратов одной группы, например, зинацеф в/в или в/м на зиннат per os; аугментин в/в на аугментин per os. Ступенчатая терапия имеет значительные клинические и экономические преимущества. Подобный метод терапии благоприятно сказывается на психоэмоциональном состоянии ребенка. Кроме того, значительно уменьшаются расходы материалов и нагрузка на медицинских работников. При переходе на пероральный прием препарата ребенок может быть выписан домой для амбулаторного долечивания.
При легком течении пиелонефрита может быть использован только пероральный путь введения антибиотика в виде специальных детских форм (сиропа, суспензии), которые отличаются хорошей всасываемостью из желудочно-кишечного тракта, приятными вкусовыми качествами.
Широкий спектр действия, включая большинство грамположительных и грамотрицательных микроорганизмов, позволяет рекомендовать «защищенные» пенициллины в качестве эмпирической терапии до получения результатов бактериологического исследования мочи.
Особенностью этих препаратов является и низкая токсичность. Возможны диспептические явления (рвота, диарея) при пероральном приеме препаратов этой группы за счет изменения кишечной микрофлоры и моторики желудочно-кишечного тракта. Этих симптомов можно избежать при приеме препаратов во время еды.
Таблица 2. Эмпирическая (стартовая) антибактериальная терапия при средне-тяжелой форме
| Манифестное течение пиелонефрита Парентеральный или пероральный (у детей старшего возраста) путь введения антибиотика | «Защищенные» пенициллины (аугментин, амоксиклав, уназин) Цефалоспорины 2 поколения (цефуроксим, цефамандол) Цефалоспорины 3 поколения | ||||||||||||||||||||||||||||||||||
| Период стихания активности Пероральноe применение препаратов | «3ащищенные» пенициллины (аугментин, амоксиклав, уназин) Цефалоспорины 2 поколения (цефуроксим аксетил, цефаклор) Препараты группы нефторированных хинолонов (пипемидиновой кислоты, налидиксовой кислоты, производные 8-оксихинолина) Наиболее часто из препаратов этой группы используется амоксициллин с клавулановой кислотой (аугментин). Рядом клинических испытаний установлено, что аугментин эффективен при лечении 88% больных с инфекциями мочевой системы, в то время как при лечении амоксициллином положительные результаты достигнуты лишь у 40% больных. Достоинством аугментина является, помимо устойчивости к микробным бета-лактамазам, его малая токсичность. Комбинированная антибактериальная терапия при пиелонефрите у детей используется по следующим показаниям: Таблица 3. Этиотропная терапия пиелонефрита (после получения результатов бактериологического исследования мочи)
* Фторхинолоны используются у детей до 14 лет в исключительных случаях [2]. ** Рифампицин назначается в исключительных случаях, ввиду того, что он нефротоксичен и относится к противотуберкулезным препаратам резерва с быстрым развитием резистентности микобактерий туберкулеза. *** Тетрациклины используются у детей старше 8 лет. Антибактериальная терапия пиелонефрита в амбулаторных условиях В ряде случаев при обострении хронического пиелонефрита лечение ребенка может осуществляться амбулаторно с организацией «стационара на дому». В поликлинике под наблюдением нефролога и участкового педиатра после курса непрерывной антибактериальной терапии проводится противорецидивное лечение в течение 4-6 недель в зависимости от характера пиелонефрита (обструктивный, необструктивный). Рекомендуются следующие варианты противорецидивной терапии:
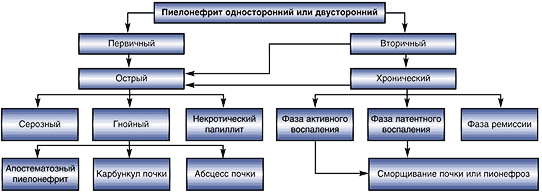
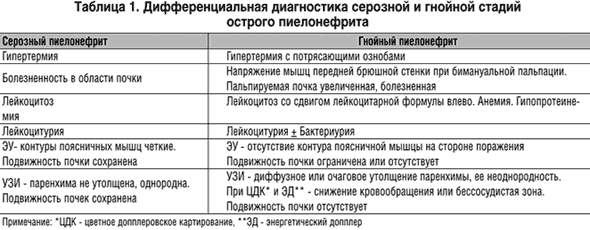
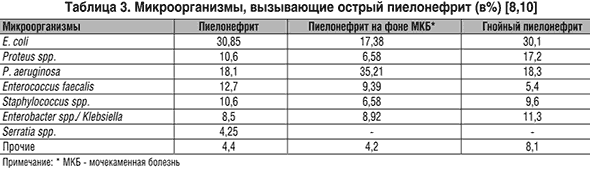
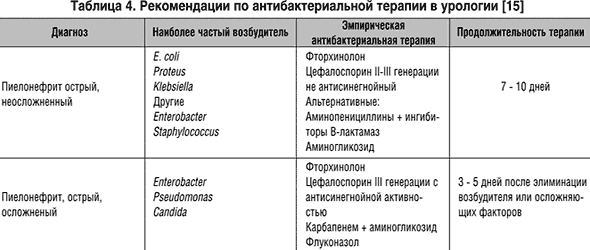
* полусинтетические пенициллины (ампициллин, ампиокс и др.) могут использоваться у амбулаторных больных в случае первой «атаки» заболевания, у ранее не леченных ими больных. Детям раннего возраста принято рассчитывать препараты на кг массы. Им назначаются относительно более высокие дозы. Рассчитывая дозу антибиотика, следует учитывать, что дети раннего возраста имеют более низкий клиренс, эффективный почечный кровоток, «незрелый» тубулярный отдел нефрона; сниженную активность ряда ферментных систем печени, что может приводить к замедлению выведения некоторых лекарственных веществ и кумуляции в организме. У больных с незначительным снижением клубочковой фильтрации дозы природных и полусинтетических пенициллинов, цефуроксима, цефотаксима, цефокситина могут не подвергаться корректировке. При снижении клубочковой фильтрации > 50% по пробе Реберга дозы этих препаратов должны быть уменьшены на 25-75%. С особой осторожностью необходимо подходить к назначению аминогликозидов при нарушении функции почек, они могут быть использованы только в крайних случаях, с мониторингом концентрации вводимого препарата в крови и индивидуальным подбором дозы с учетом снижения клубочковой фильтрации. У больных с хронической почечной недостаточностью, находящихся на гемодиализе, часть антибиотика выводится и требуется его дополнительное введение. От 25 до 50 % пенициллинов, цефаклора, более 50 % сульфаниламидов, аминогликозидов, имипенема, большинство цефалоспоринов удаляется при гемодиализе. Практически не выводятся при гемодиализе макролиды, оксациллин, цефоперазон, цефиксим, цефотетан, амфотерицин В и хинолоны. При перитонеальном диализе не происходит «вымывания» большинства препаратов, за исключением аминогликозидов, цефуроксима (на 15-25%) [9]. Почки могут повреждаться при антибактериальной терапии, так как они являются органом выведения антибиотиков и их метаболитов. В связи с этим, все антибактериальные препараты можно разделить на три основные группы: Таким образом, основной задачей при лечении детей, больных пиелонефритом, является ликвидация или уменьшение микробно-воспалительного процесса в почечной ткани и мочевыводящих путях [4]. Низкая эффективность антибактериальной терапии при лечении пиелонефрита обусловлена в ряде случаев наличием аномалий развития, нарушениями уродинамики, а также постоянно изменяющимися свойствами бактериальной флоры. Это и определяет необходимость постоянного поиска новых антибактериальных препаратов, высоко эффективных при лечении прежде всего грамотрицательных инфекций. В настоящее время фармацевтический рынок располагает большим количеством антибактериальных средств, позволяющим выбрать оптимальный из них. Несмотря на то, что антибиотики являются высокоэффективными препаратами, способными при рациональном их использовании спасти ребенку жизнь, терапия ими всегда является компромиссом между желаемым действием препарата и оценкой возможных побочных эффектов. Для достижения хорошего эффекта при проведении антибактериальной терапии необходимо учитывать следующие рекомендации: Антибактериальная терапия острого пиелонефритаВ статье рассмотрены вопросы эпидемиологии, патогенеза и этиологии инфекций мочевыводящих путей. В соответствии с отечественными и международными рекомендациями даны схемы антибактериального лечения пиелонефрита легкого и тяжелого течения, а также практические рекомендации по ведению пациентов с таким заболеванием. Отмечается, что фторхинолоны, создающие высокие тканевые концентрации, обладающие активностью по отношению к основным возбудителям инфекций мочевых путей, остаются препаратами выбора для лечения острого пиелонефрита. В статье рассмотрены вопросы эпидемиологии, патогенеза и этиологии инфекций мочевыводящих путей. В соответствии с отечественными и международными рекомендациями даны схемы антибактериального лечения пиелонефрита легкого и тяжелого течения, а также практические рекомендации по ведению пациентов с таким заболеванием. Отмечается, что фторхинолоны, создающие высокие тканевые концентрации, обладающие активностью по отношению к основным возбудителям инфекций мочевых путей, остаются препаратами выбора для лечения острого пиелонефрита. Эпидемиология и патогенез инфекций мочевыводящих путей Инфекции мочевыводящих путей относятся к самым распространенным инфекционным заболеваниям, которые требуют значительных финансовых затрат. По поводу инфекций мочевыводящих путей, преимущественно пиелонефрита, ежегодно госпитализируются свыше 100 тыс. человек [1]. На долю инфекций мочевыводящих путей приходится как минимум 40% всех нозокомиальных инфекций, которые в большинстве случаев обусловлены катетеризацией мочевого пузыря [2–4]. У 25% пациентов с установленным на срок более семи дней уретральным катетером развивается бактериурия, при этом частота возникновения бактериурии возрастает ежедневно на 5% [5]. По некоторым оценкам, даже один эпизод нозокомиальной бактериурии значительно увеличивает прямые затраты, связанные с госпитализацией в отделение интенсивной терапии [6]. Возбудители инфекций подвергаются воздействию факторов внутрибольничной среды, в том числе «селективному давлению» антибиотиков и антисептиков. Таким образом, нозокомиальные инфекции мочевыводящих путей составляют самый большой резервуар антибиотикорезистентных микроорганизмов в лечебных учреждениях [5]. Этиология инфекций мочевыводящих путей В работах М.И. Когана [7], а также Ю.Л. Набоки и соавт. [8] убедительно показано, что моча здоровых женщин нестерильна, при посевах на обогащенные питательные среды высевается широкий спектр микроорганизмов, как аэробов, так и анаэробов. Экспериментально, а также клинически доказана роль анаэробов в генезе острого пиелонефрита. Полученные в ходе российского исследования «ДАРМИС» (2011) результаты показали, что основным возбудителем инфекций мочевыводящих путей была Escherichia coli, которая обнаруживалась у 63,5% пациентов. При этом частота ее выделения существенно не зависела от неосложненного (64,6%) или осложненного (62,1%) течения заболевания. Учитывая, что антибактериальная чувствительность уропатогенов, выделенных у пациентов с осложненными и неосложненными инфекциями мочевыводящих путей, несколько отличается, данные по этим формам инфекции мочевыводящих путей для Escherichia coli приведены раздельно (табл. 1) [9]. Следует отметить, что в ряде стран наблюдается рост штаммов Escherichia coli, устойчивых к фторхинолонам, что ограничивает их эмпирическое применение (табл. 2). Лечение пиелонефрита легкого течения Лечение больных острым пиелонефритом должно быть комплексным. На результаты терапии напрямую влияют два фактора: своевременное и адекватное восстановление уродинамики и рациональная стартовая эмпирическая антибактериальная терапия. Выбор метода дренирования мочевых путей зависит от причины нарушения уродинамики, а также от стадии развития острого пиелонефрита. Оценка эффективности проводимой терапии должна осуществляться через 48–72 часа, коррекция – после получения результатов бактериологического исследования. Наиболее эффективной как с клинической, так и экономической точки зрения является ступенчатая антибактериальная терапия. В случае отсутствия факторов риска, способных значительно нарушить всасывание препаратов из желудочно-кишечного тракта, антимикробные препараты назначаются перорально. Антибактериальная терапия проводится длительно. Самые короткие курсы назначаются при первичном остром пиелонефрите в стадии серозного воспаления, их продолжительность составляет семь – десять дней. При остром неосложненном пиелонефрите легкой и средней степени тяжести достаточно проведения пероральной терапии в течение 10–14 дней (уровень доказательности 1b, степень рекомендации B). При уровне резистентности Escherichia coli Антибактериальная терапия острого пиелонефрита*Пятилетний импакт фактор РИНЦ за 2020 г. Читайте в новом номере Пиелонефрит по своей частоте превосходит все почечные болезни вместе взятые [1]. Согласно сборной статистике (более чем 100 авторов), в среднем 1% людей на земле ежегодно заболевает пиелонефритом [2]. Пиелонефрит по своей частоте превосходит все почечные болезни вместе взятые [1]. Согласно сборной статистике (более чем 100 авторов), в среднем 1% людей на земле ежегодно заболевает пиелонефритом [2]. Острый пиелонефрит составляет 14% болезней почек, гнойные его формы развиваются у 1/3 больных [3]. В настоящее время инфекции мочевыводящих путей (ИМВП) разделяют на неосложненные и осложненные [4]. К осложненным ИМВП относят заболевания, объединенные наличием функциональных или анатомических аномалий верхних или нижних мочевых путей или протекающие на фоне заболеваний, снижающих резистентность организма (Falagas M.E.,1995). ИМВП в большинстве стран мира являются одной из наиболее актуальных медицинских проблем. Так, в США ИМВП служат причиной обращения к врачу 7 млн. пациентов в год, из которых 1 млн. требуют госпитализации. Группа осложненных ИМВП представлена крайне разнородными заболеваниями: от тяжелого пиелонефрита с явлениями обструкции и угрозой развития уросепсиса, до катетер–ассоциированных ИМВП, которые могут исчезнуть самостоятельно после извлечения катетера [5]. Некоторые авторы для практических целей придерживаются выделения двух форм пиелонефрита: неосложненный и осложненный [6,7]. Такое условное разделение ни в коей мере не объясняет степень воспалительного процесса в почке, его морфологическую форму (серозный, гнойный). Необходимость выделения осложненного и неосложненного пиелонефрита обусловлена различиями в их этиологии, патогенезе и соответственно – разными подходами к лечению. Наиболее полно отражает различные стадии и формы воспалительного процесса в почке классификация, предложенная в 1974 г. Н.А. Лопаткиным (рис. 1). Рис. 1. Классификация пиелонефрита (Н.А. Лопаткин, 1974) Несмотря на оптимистические предсказания, частота заболеваний пиелонефритом существенно не изменилась в эру антибиотиков и сульфаниламидов. Острый пиелонефрит только у 17,6% больных является первичным, у 82,4% – он вторичен. Поэтому алгоритм диагностики должен ответить на следующие вопросы: функция почек и состояние уродинамики, стадия (серозная или гнойная), форма пиелонефрита (апостематозный, карбункул, абсцесс почки или их сочетание). В алгоритм экстренных исследований включают анализ жалоб больного и сбор анамнеза, клинико–лабораторное обследование, комплексное ультразвуковое исследование с применением допплерографии, рентгенологическое исследование [8]. Наибольшее количество диагностических ошибок допускается на амбулаторном этапе из-за подчас пренебрежительного отношения врачей к сбору анамнеза, недооценки жалоб и тяжести состояния больного, непонимания патогенеза развития острого пиелонефрита. В результате больные госпитализируются в непрофильные отделения в связи с неправильно установленным диагнозом или назначается амбулаторное лечение при обструктивном остром пиелонефрите, что недопустимо. Улучшение качества диагностики острого пиелонефрита и уменьшение количества диагностических ошибок возможно только при использовании комплексного подхода, в основе которого лежат жалобы больного, анамнез заболевания и клинико–лабораторные данные. При установлении диагноза острый пиелонефрит на основании жалоб больного на повышение температуры, боли в поясничной области, наличии лейкоцитурии, бактериурии; необходимо исключить нарушение уродинамики с помощью ультразвукового исследования (УЗИ) с допплерографией, экскреторной урографии (ЭУ). Затем определить стадию пиелонефрита, т.е. провести дифференциальную диагностику между серозной и гнойной стадиями заболевания (табл. 1). При выявлении гнойного пиелонефрита определяется форма заболевания – апостематозный, карбункул почки, абсцесс или их сочетание (табл. 2). При гнойном пиелонефрите – одной из самых тяжелых и опасных для жизни осложненных ИМВП, основными возбудителями являются грамотрицательные условно-патогенные микроорганизмы (76,9%). У пациентов, перенесших открытые оперативные вмешательства на органах мочевой системы или эндоскопические диагностические и лечебные манипуляции и операции, возрастает роль госпитальных штаммов микроорганизмов, в первую очередь это относится к P. aeruginosa. Лечение острого пиелонефрита должно быть комплексным, включающим следующие аспекты: устранение причины, вызывающей нарушение уродинамики, антибактериальная, дезинтоксикационная, иммунокоррегирующая и симптоматическая терапия. Как диагностика, так и выбор метода лечения должны осуществляться в кратчайшие сроки. Лечение острого пиелонефрита преследует цель сохранения почки, профилактики уросепсиса и возникновения рецидивов заболевания. Исключение составляют катетер-ассоциированные инфекции, в большинстве случаев исчезающие после удаления катетера [12]. При любой форме острого обструктивного пиелонефрита в абсолютно неотложном порядке должен быть восстановлен отток мочи от пораженной почки, причем это должно предшествовать всем остальным лечебным мероприятиям. Восстановление или улучшение почечной функции при вторичном (обструктивном) остром пиелонефрите происходит лишь тогда, когда обтурация устранена не позднее, чем через 24 часа после начала острого пиелонефрита. Если же обтурация сохраняется на более длительный срок, это приводит к стойкому нарушению всех показателей функции почек, клинически наблюдается исход в хронический пиелонефрит [1]. Восстановление нормальной уродинамики является краеугольным камнем в лечении любой мочевой инфекции. В тех случаях, когда причина возникновения обструкции не может быть ликвидирована немедленно, следует прибегать к дренированию верхних мочевых путей нефростомическим дренажем, а в случае инфравезикальной обструкции – к дренированию мочевого пузыря цистостомическим дренажем [5]. Обе операции предпочтительнее выполнять под ультразвуковым наведением. Результаты лечения острого пиелонефрита зависят от правильности выбора метода лечения, своевременности дренирования почки и адекватности антибактериальной терапии. Так как при остром пиелонефрите в начале лечения антибактериальная терапия всегда бывает эмпирической, необходимо правильно подобрать антибиотик или рациональную комбинацию препаратов, дозу и способ введения. Стартовая эмпирическая терапия острого пиелонефрита должна быть своевременной, т.е. максимально ранней, также, по мнению Н.В. Белобородовой и соавт. [13], должна преследовать следующие цели: быть клинически и экономически эффективной. При пиелонефрите в первую очередь и в основном поражается межуточная ткань почки, следовательно, необходимо создать высокую концентрацию антибиотика в ткани почки. Для адекватной антибактериальной терапии важно выбрать антибиотик с одной стороны действующий на «проблемные» микроорганизмы, с другой – накапливающийся в почках в необходимой концентрации. Поэтому ошибкой является назначение при остром пиелонефрите таких препаратов, как нитрофурантоин, нефторированные хинолоны, нитроксолин, тетрациклины, хлорамфеникол, концентрация которых в крови и тканях почки обычно ниже значений МПК основных возбудителей заболевания [14]. Не могут быть рекомендованы для эмпирической монотерапии аминопенициллины (ампициллин, амоксициллин), цефалоспорины I поколения (цефалексин, цефазолин), аминогликозиды (гентамицин), так как резистентность основного возбудителя пиелонефрита – кишечной палочки – к этим препаратам превышает 20%. Применяются различные схемы, программы, алгоритмы антибактериальной терапии острого пиелонефрита (табл. 4, 5). Весьма актуальной для больных острым пиелонефритом, особенно при гнойно-деструктивных формах заболевания, является проблема резистентности к антибактериальным препаратам. Невозможно вылечить пациента с обструктивным острым пиелонефритом, если своевременно не восстановить нормальную уродинамику или не создать адекватный отток мочи из почки. При этом далеко не всегда можно удалить все конкременты, на которых формируется биопленка, а наличие дренажей приводит к возникновению «катетер–ассоциированной» инфекции. Таким образом, формируется порочный круг: без дренирования мочевых путей в большинстве случаев невозможно проводить адекватную антибактериальную терапию, а сами дренажи, кроме своей положительной роли, оказывают и отрицательную. Последствиями возросшей резистентности микроорганизмов является увеличение сроков госпитализации, затрат на лечение. Придерживаясь рациональной тактики антибиотикотерапии, можно избежать многих нежелательных последствий, возникающих при неправильном подходе к лечению: распространения антибиотикоустойчивых штаммов возбудителей, проявления токсичности лекарственных средств. Длительное время занимаясь обследованием и лечением больных острым гнойным пиелонефритом, мы установили взаимосвязь возбудителя, пути проникновения инфекции и формы острого пиелонефрита (табл. 6). Выявленная закономерность позволяет подбирать рациональную эмпирическую терапию с учетом наиболее вероятного возбудителя. В лечении больных острым гнойным пиелонефритом нужно использовать препараты с расширенным спектром антибактериальной активности, резистентность к которым основных возбудителей пиелонефрита отсутствует или является достаточно низкой. Препаратами выбора для стартовой эмпирической терапии острого гнойного пиелонефрита являются карбапенемы, цефалоспорины III–IV поколений, фторхинолоны. При отсутствии факторов риска, таких как инвазивные урологические вмешательства, сахарный диабет, возможно проведение комбинированной терапии: цефалоспорины I или II поколений и аминогликозиды. При всех стадиях и формах острого пиелонефрита адекватным является только парентеральный способ введения антибиотиков, предпочтение следует отдавать внутривенному пути введения. Оценка эффективности проводимой терапии при остром пиелонефрите должна осуществляться через 48–72 часа, коррекция – после получения результатов бактериологического исследования. Так как к моменту первичной оценки эффективности терапии (48–72 часа) результаты микробиологического исследования обычно отсутствуют, коррекция антибактериальной терапии при отсутствии эффекта или недо статочной эффективности терапии проводится также эмпирически. Если лечение начиналось с применения цефалоспорина I поколения в сочетании с аминогликозидом, проводится замена первого препарата на цефалоспорин II или III поколения. При отсутствии эффекта от применения цефалоспоринов III поколения в сочетании с аминогликозидами показано назначение фторхинолонов (ципрофлоксацин) или карбапенемов (имипенем). После получения данных микробиологического исследования – переход на этиотропную терапию. При всех стадиях и формах острого пиелонефрита адекватным является только парентеральный способ введения антибиотиков, предпочтение следует отдавать внутривенному пути введения. Оценка эффективности проводимой терапии при остром пиелонефрите должна осуществляться через 48–72 часа, коррекция – после получения результатов бактериологического исследования. Если при остром серозном пиелонефрите антибактериальная терапия проводится в течение 10–14 дней, то при гнойном пиелонефрите длительность проведения антибактериальной терапии увеличивается. Критерием для решения вопроса о прекращении антибактериальной терапии являются нормализация клинической картины, анализов крови и мочи. У пациентов, оперированных по поводу острого гнойного пиелонефрита, антибактериальная терапия продолжается до закрытия нефростомического свища. В дальнейшем амбулаторно проводится назначение антибактериальных препаратов с учетом результатов антибиотикограммы. Острый пиелонефрит – это хирургическая инфекция. В начале заболевания трудно прогнозировать, по какому пути будет развиваться заболевание, при котором в процесс всегда в той или иной степени вовлечены чашечно-лоханочная система и паренхима почки. Достоверно исключить нарушение уродинамики можно только проведя соответствующие исследования: ультразвуковое с применением допплерографии, экскреторную урографию. Поэтому было бы неправильно обсуждать вопросы, касающиеся антибактериальной терапии, в отрыве от алгоритма диагностики острого пиелонефрита, методов восстановления уродинамики. Только объединив усилия клиницистов, микробиологов и химиотерапевтов (создав в каждой крупной многопрофильной больнице соответствующее подразделение), ответив четко и однозначно на предложенные вопросы и поставив во главу угла конкретного больного, а не возбудителей и антибактериальные препараты (схема: Больной – возбудитель – антибиотик), мы сможем улучшить результаты лечения больных острым пиелонефритом. |