Лечение кишечной инфекции: ничего лишнего!
Поделиться:
Летом проблема отравлений становится как никогда актуальной — жара создает благоприятные условия для размножения возбудителей заболевания. Какие же лекарства действительно помогают с минимальными последствиями выйти из неприятного состояния?
Для четкого представления о том, как работают (или не работают) лекарства при отравлениях, нужно понимать, что происходит с отравившимся организмом. В подавляющем большинстве случаев бактерии, а уж тем более паразиты совершенно ни при чем!
В основном кишечная инфекция развивается на фоне заражения вирусами: они несут ответственность за 70 % случаев инфекционной диареи у детей и почти 90 % — у взрослых.
Проникновение в организм возбудителей кишечной инфекции сопровождается выделением большого количества токсинов, которые и вызывают характерные симптомы. При этом воспаляется слизистая оболочка желудка и кишечника — развивается гастроэнтерит.
Однако, несмотря на порой мучительные проявления отравления, его возбудители обречены: все кишечные инфекции являются самоограниченными, т. е. бактерии или вирусы, их вызвавшие, погибают не потому, что на них воздействуют лекарствами, а потому что так задумано природой. В этом отношении почти любая кишечная инфекция сродни ОРВИ — лечи не лечи, а все равно выздоровеешь не раньше, чем достигнет конца своего развития возбудитель. И, к счастью, его век недолог: в течение 1–7 дней после манифестации заболевания, как правило, наступает выздоровление.

Мы привыкли глотать горсти таблеток по поводу и даже иногда без него. При отравлении в том числе. Но далеко не все препараты, которые мы считаем незаменимыми и жизненно необходимыми, действительно нужны. Вспомним всех поименно.
1. Регуляторы водно-электролитного баланса
Препараты этой группы возглавляют короткий перечень лекарств, действительно необходимых при отравлениях. К ним относятся комбинации декстрозы, калия и натрия хлорида, натрия цитрата (Регидрон, Тригидрон, Гидровит).
Диарея и рвота, основные спутники кишечной инфекции, способствуют потерям жидкости и нарушению кислотно-щелочного равновесия в организме. Это главная опасность отравления, которое при неадекватном восполнении образующегося дефицита приводит к обезвоживанию и нарушению электролитного баланса. Поэтому лечение прежде всего должно быть направлено на быстрое восстановление запасов.
Формула успеха проста: сколько жидкости вы потеряли с рвотой и диареей, столько должно поступить в организм с препаратами или, на крайний случай, с лечебной минеральной водой (разумеется, без газа). В случаях, когда прием регидрантов внутрь невозможен, необходимо внутривенное капельное введение жидкости, т. е. капельницы.
2. Антидиарейные препараты
Советская, да и постсоветская медицина зачастую направлена на ожесточенную борьбу с симптомами заболеваний, часто независимо от того, полезна ли для организма эта борьба. Температура? Жаропонижающие, несмотря на то что при этом снижается выработка интерферона и иммунный ответ. Диарея? Противодиарейные, невзирая на выведение с каловыми массами множества токсинов.
Современная тактика ведения больных с острыми кишечными инфекциями нацелена на сознательный подход к купированию симптомов:
Классическим антидиарейным препаратом является лоперамид, замедляющий перистальтику кишечника и увеличивающий время прохождения кишечного содержимого. Кроме того, противодиарейное действие оказывает диоктаэдрический смектит.
3. Адсорбенты
Необходимость в приеме адсорбентов при кишечной инфекции не совсем однозначна. Теоретически адсорбенты (активированный уголь, пектин, диоктаэдрический смектит и др.) связывают токсины, предотвращая их присоединение к мембранам кишечника.
Однако, чтобы препараты работали, они должны поступить в организм прежде, чем токсины прикрепятся к слизистой оболочке, чего достигнуть на практике удается далеко не всегда. И даже если адсорбенты введены вовремя, они, увы, не предотвращают обезвоживание организма, хотя и уменьшают частоту стула.
4. Пробиотики
Применение препаратов, содержащих полезные бактерии, нацелено на восстановление микрофлоры кишечника. Исследования свидетельствуют, что они и в самом деле могут нормализовать ее состав. Однако из всего немалого ассортимента полноценную доказательную базу имеют лишь средства, содержащие Lactobacillus casei GG (входят в состав некоторых БАДов, например, Максилак, Йогулакт) или сахаромицеты Буларди Saccharomyces boulardii (Энтерол). Их назначение помогает снизить интенсивность диареи и улучшить состояние больных.
5. Антибактериальные
Препараты, проявляющие антибактериальный эффект, работают только в случае бактериальной инфекции. При отравлении, вызванном вирусами, они бесполезны, а ведь именно эти возбудители чаще всего и становятся причиной заболевания.
Отличить вирусную и бактериальную инфекцию иногда можно по клиническим проявлениям. Так, первая чаще сопровождается головной, мышечной болью, слабостью и усталостью, а для второй характерно появление крови в стуле. Но чаще всего четко дифференцировать два вида отравления практически невозможно.

Однако даже при инфицировании бактериями целесообразность в приеме антибактериальных средств сомнительна: ведь как мы уже говорили, спустя несколько дней после манифестации болезни наступает самовыздоровление.
Исключение составляют тяжелые инфекции, сопровождаемые высокой температурой, появлением крови в стуле, обезвоживанием, но в подобных ситуациях решение должен принимать доктор. Кстати, в таких случаях может понадобиться и госпитализация.
Таким образом, из длинного списка препаратов, которые мы считаем чуть ли не панацеей при отравлениях, можно ограничиться всего двумя-тремя, а то и вовсе одним лекарством — регидрантом. При этом эффект лечения будет тем же, что и при приме горстей таблеток, а вот побочных эффектов точно гораздо меньше. Какой путь предпочесть — выбирать вам, ведь в конце концов ваше здоровье в ваших руках.
Товары по теме: [product strict=» регидрон»]( регидрон), [product strict=» лоперамид»]( лоперамид), [product strict=» диосмектит»]( диосмектит), [product strict=» смекта»]( смекта), [product strict=» уголь активированный»]( уголь активированный), [product strict=» пектин»]( пектин), [product strict=» энтерол»]( энтерол)
Кишечные инфекции
Роза Исмаиловна Ягудина, д. фарм. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
С наступившим летом тема нашей статьи приобрела особую актуальность. Кишечные инфекции — это целая группа инфекционных заболеваний, поражающих в основном желудочно-кишечный тракт. Острые кишечные инфекции по своей распространенности уступают только острым респираторным заболеваниям. Пик заболеваемости обычно приходится на лето, но и в холодное время года часто встречаются кишечные инфекции, вызываемые преимущественно вирусами. Однако наиболее частая причина возникновения этих заболеваний — попадание возбудителей инфекции с загрязненными продуктами и водой в желудочно-кишечный тракт.
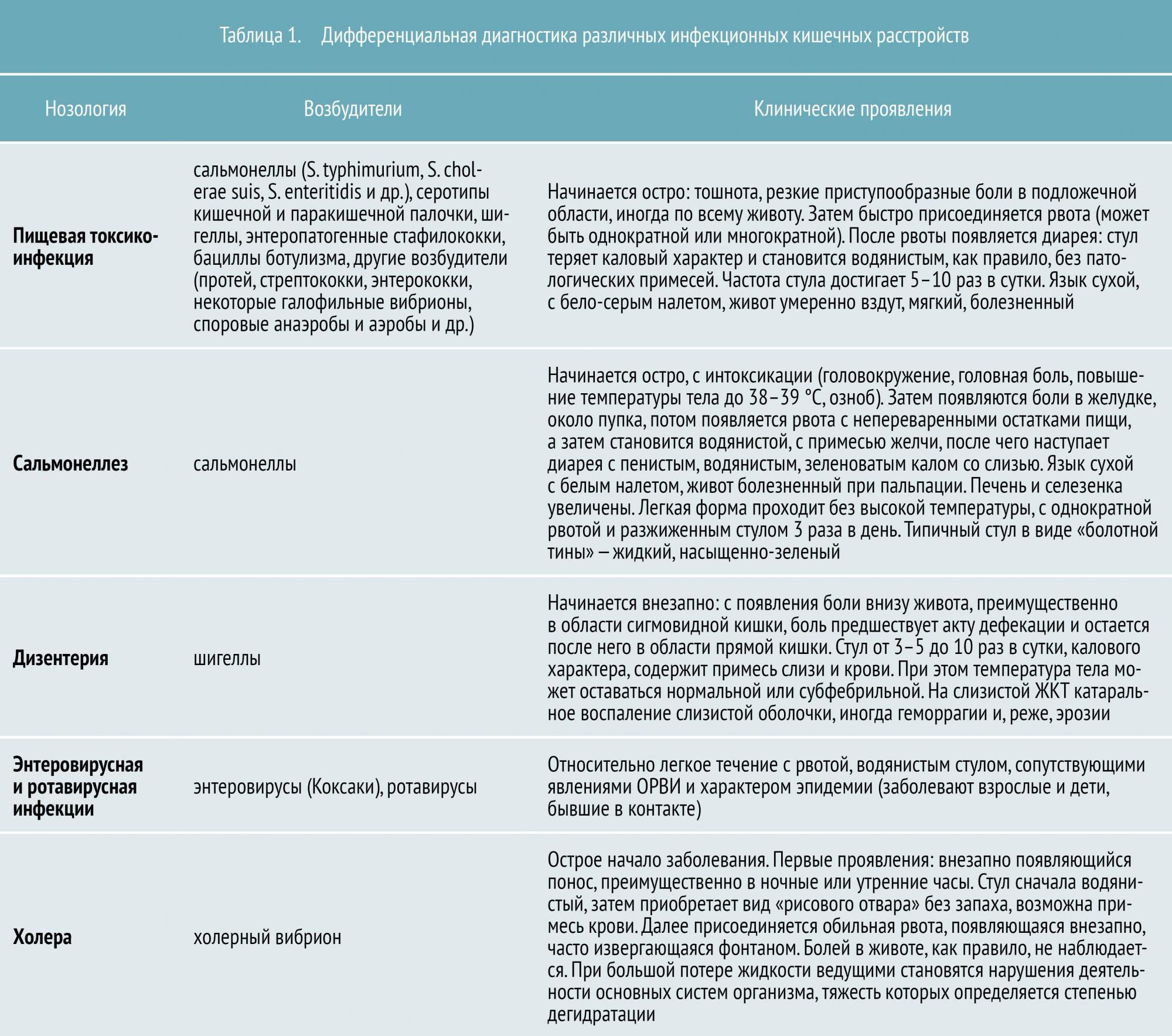
Всего в настоящее время известно около 30 инфекционных кишечных заболеваний. К наиболее распространенным относятся:
По степени опасности их можно условно разделить на неопасные, опасные и особо опасные. Так, к неопасным относят пищевую токсикоинфекцию (ПТИ), а к особо опасным — холеру, брюшной тиф и т. д. Но это не значит, что так называемая «неопасная» ПТИ не наносит серьезного ущерба организму и не приводит к осложнениям.
Осложнения кишечных инфекций:
Возбудители кишечной инфекции
Помимо инфекционных агентов из естественной среды источником заражения может стать уже заболевший человек. Выделяя большое количество патогенных микроорганизмов (микробы выделяются с испражнениями, рвотными массами, иногда с мочой), больной заражает предметы, находящиеся вокруг, и, если не соблюдать меры предосторожности, может возникнуть цепная реакция в распространении инфекции.
Практически все возбудители кишечных инфекций чрезвычайно живучи. Они способы подолгу существовать в почве, воде и на различных предметах (ложках, тарелках, дверных ручках и мебели). Инфекционные микроорганизмы во внешней среде не только не погибают, но и сохраняют способность к размножению, а размножаются они наиболее активно в теплых и влажных условиях. Однако самая благоприятная среда для развития бактерий — это кисломолочные и мясные продукты.
Установлена связь отдельных форм острых кишечных инфекций с видами пищи. Так, дизентерия чаще возникает при употреблении молока и молочных продуктов, а кишечные инфекции, вызванные стафилококком, — при употреблении молочных продуктов и кондитерских изделий с кремом. Иерсиниозы обычно развиваются при употреблении сырых овощей, салатов и другой растительной пищи.
Возбудителями кишечных инфекций могут быть как бактерии (сальмонеллы, шигеллы, иерсинии, энтеропатогенные кишечные палочки, стафилококки), так и их токсины (пищевые токсикоинфекции). Вирусы (ротавирусы, энтеровирусы, астровирусы, парвовирусы) пока на втором месте по частоте встречаемости, однако в последнее время вирусные инфекции получают всё более широкое распространение. И на последнем месте — простейшие (лямблии, амебы, бластоцисты).
После попадания патогенов в организм человека, как правило, проходит бессимптомный инкубационный период, который продолжается от 6 до 48 часов — от попадания микроорганизмов в ротовую полость до момента поступления их в кишечник, где происходит их бурное размножение. После того как патогенные микроорганизмы размножились, начинается стадия клинических проявлений.
Наступает острый период — от 1 до 14 дней, в это время клинические проявления со стороны ЖКТ выражены максимально. Как правило, период заканчивается, когда нормализуется температура и прекращается ведущий симптом (понос или рвота).
Период реконвалесценции — не менее 2 недель, а в некоторых случаях при отсутствии лечения до нескольких лет. В этот период функция желудочно-кишечного тракта, как правило, восстанавливается не полностью — может быть неустойчивый стул.
В основном все кишечные инфекции протекают с достаточно похожими симптомами. Они всегда начинаются внезапно. В самом начале заболевания появляется резкая слабость, вялость, снижение аппетита, головная боль, повышение температуры — неспецифические симптомы, которые могут напоминать симптомы респираторных вирусных инфекций. Однако вскоре возникают тошнота, рвота, схваткообразные боли в животе, понос с примесью слизи, гноя или крови (например, при дизентерии), также могут беспокоить жажда и озноб. Среди клинических проявлений со стороны желудочно-кишечного тракта, как правило, сильнее всего выражены симптомы, связанные с пораженным органом:
Одно из самых неблагоприятных последствий кишечной инфекции — это дегидратация организма из‑за рвоты и/или поноса и, как следствие, нарушение водно-электролитного обмена. Результатом резкой дегидратации может стать даже шок.
Однако иногда кишечные инфекции могут не иметь видимых симптомов, но сопровождаются выделением возбудителей. В плане распространения инфекции такое носительство наиболее опасно: ничего не подозревающий человек становится постоянным источником инфекции, заражая окружающих.
Врачу важно провести дифференциальную диагностику между кишечной инфекцией и соматическими заболеваниями со сходными симптомами: диареей, связанной с приемом лекарственных препаратов, острым аппендицитом, инфарктом миокарда, пневмонией, внематочной беременностью и т. д.
Диагностика и лечение кишечной инфекции
Основные принципы терапии кишечных инфекций:
Во время болезни необходимо соблюдать диету, помогающую замедлить перистальтику кишечника. Рекомендуются продукты с высоким содержанием танина (черника, черемуха, крепкий чай); вещества вязкой консистенции (слизистые супы, протертые каши, кисели); сухари; индифферентные вещества — паровые блюда из нежирного мяса и рыбы. Важный этап в лечении кишечных инфекций — исключение из рациона жареных и жирных блюд, сырых овощей и фруктов.
Главное направление лечебной тактики — нейтрализация экзотоксинов в кишечнике (энтеросорбенты) и регидратация — компенсация патологических потерь жидкости и электролитов специально разработанными глюкозо-солевыми растворами. Объем вводимых растворов зависит от степени обезвоживания и массы тела больного, а скорость введения составляет 1–1,5 л/ч. Дезинтоксикационная и регидратационная терапия в 85–95 % случаев может осуществляться перорально.
Антибиотики может назначить только инфекционист с учетом проведенных лабораторных тестов и выявленного возбудителя инфекции. Однако при выраженной диарее для ускоренной санации обоснованным является назначение антибактериальных ЛС, которые не всасываются или плохо всасываются из кишечника и обладают широким спектром действия (например, энтерофурил или ко-тримоксазол). Эффективными средствами альтернативной этиотропной терапии, в качестве препаратов от острой кишечной инфекции, являются энтеросорбенты и пробиотики. Этиотропное действие пробиотиков связано с выраженной антагонистической активностью в отношении всех возбудителей острых кишечных инфекций (ОКИ) бактериальной этиологии и опосредованным иммуномодулирующим действием на местное звено иммунитета.
Обзор лекарств для лечения кишечных инфекций
Нифуроксазид (энтерофурил)
Безрецептурное противомикробное средство широкого спектра действия, производное 5‑нитрофурана. Антимикробная активность нифуроксазида вызвана наличием в его составе NO2‑группы, которая угнетает активность дегидрогеназы и нарушает синтез белков в патогенных бактериях.
Нифуроксазид не оказывает действия на сапрофитную флору, не нарушает равновесия нормальной кишечной флоры. При острой бактериальной диарее восстанавливает эубиоз кишечника. При инфицировании энтеротропными вирусами препятствует развитию бактериальной суперинфекции. Этот препарат для лечения кишечной инфекции можно назначать беременным и кормящим женщинам, детям начиная с одного месяца. Терапия нифуроксазидом не должна превышать 7 дней, при этом запрещено употреблять алкоголь.
Кипферон
Безрецептурный препарат в форме вагинальных и ректальных суппозиториев. Обладает иммуномодулирующим, противовирусным, антихламидийным действием. Кипферон — комплексная лекарственная форма, содержащая человеческий рекомбинантный интерферон-α2 и комплексный иммуноглобулиновый препарат (КИП). Разрешен к применению у детей на первом году жизни.
Ко-тримоксазол (сульфаметоксазол + триметоприм)
Механизм действия ко-тримоксазол а обусловлен двойным блокированием метаболизма микроорганизмов. Триметоприм обратимо ингибирует дигидрофолатредуктазу микроорганизмов, нарушает образование из дигидрофолиевой кислоты тетрагидрофолиевой, продукцию нуклеиновых кислот, пиримидиновых и пуриновых оснований; подавляет размножение и рост бактерий. Сульфаметоксазол, который по строению схож с парааминобензойной кислотой, захватывается бактерией и препятствует включению парааминобензойной кислоты в дигидрофолиевую кислоту. В связи с тем что ко-тримоксазол угнетает жизнедеятельность кишечной палочки, снижается образование в кишечнике никотиновой кислоты, рибофлавина, тиамина и прочих витаминов B-комплекса. Это лекарство, помогающее от кишечной инфекции, отпускается по рецепту, применяется с 2‑месячного возраста.
Бактисубтил — споры бактерий Bacillus cereus IP. Рецептурный препарат от кишечной инфекции бактисубтил сохраняет и корригирует физиологическое равновесие кишечной флоры. Споры бактерий, содержащиеся в препарате, устойчивы к действию желудочного сока. Прорастание бактерий в вегетативные формы происходит в кишечнике, затем они высвобождают энзимы, которые расщепляют углеводы, жиры, белки. В результате образуется кислая среда, предотвращающая процессы гниения. Препарат препятствует нарушению синтеза витаминов группы В и Р в кишечнике, его нельзя запивать горячим, а также сочетать с алкоголем. Детям его назначают с семилетнего возраста. Бактисубтил резистентен к действию различных антибиотиков и сульфаниламидных препаратов, поэтому может быть назначен одновременно с ними.
Декстроза + калия хлорид + натрия хлорид + натрия цитрат (регидрон)
Регидратирующее средство для перорального приема восстанавливает водно-электролитное равновесие, нарушенное при обезвоживании организма; корректирует ацидоз. Содержимое одного пакетика растворяют в литре свежепрокипяченной охлажденной питьевой воды. Приготовленный раствор нужно хранить в холодильнике и использовать в течение 24 часов. В раствор нельзя добавлять никакие другие компоненты, чтобы не нарушить действие препарата. Отпускается без рецепта.
Смектит диоктаэдрический
Безрецептурное лекарственное средство природного происхождения, обладающее протективным действием в отношении слизистой оболочки кишечника и выраженными адсорбирующими свойствами. Являясь стабилизатором слизистого барьера, образует поливалентные связи с гликопротеинами слизи и увеличивает продолжительность ее жизни, образуя физический барьер, который защищает слизистую оболочку пищеварительного тракта от отрицательного действия ионов Н+, соляной кислоты, желчных солей, микроорганизмов, их токсинов и других раздражителей. Обладает селективными сорбционными свойствами, защищает слизистую оболочку пищеварительного тракта от отрицательного воздействия. В терапевтических дозах не влияет на моторику кишечника.
Профилактика кишечных инфекций, в том числе и острых
Для профилактики кишечных инфекций важно регулярно мыть руки и проводить влажную уборку в квартире. Лучше сразу же выкидывать продукты с истекшим сроком годности, не покупать их в местах с непонятными условиями хранения — как бы ни были привлекательны, скажем, грибочки у бабушки возле метро — а фрукты и овощи есть только тщательно вымытыми.
Избежать распространения болезни поможет ранняя диагностика и изоляция больного с кишечной инфекцией. В очаге инфекции нужно обработать поверхности дезинфицирующими растворами, прокипятить посуду. Выписку пациентов проводят только после отрицательного результата контрольного обследования кала. Всем, кто перенес кишечную инфекцию, в течение месяца необходимо регулярно проходить диспансерное наблюдение в поликлинике.
Простые меры профилактики кишечных инфекций:
Антибиотики нового поколения: за и против
Антибиотики – это вещества биологического или полусинтетического происхождения. Применяются в лечебной практике для борьбы с болезнетворными микробами, вирусами. До появления этих медпрепаратов статус неизлечимых болезней был у брюшного тифа, дизентерии, пневмонии, туберкулеза. Сегодня лечение заболеваний инфекционного характера возможно с применением 1-6 поколения антибиотиков.
На этот момент фармакологическая индустрия выпускает более 2000 разновидностей лекарственных средств подобного типа. Медики описали действие около 600 позиций, а во врачебной практике используются порядка 120-160 препаратов.
Важно! При любом заболевании принимать антибиотики рекомендуется после консультации с врачом. В противном случае может развиться антибиотикорезистентность (снижение чувствительности патогенных микроорганизмов к антибактериальным средствам).
Классификация антибиотиков
Все антибактериальные средства можно разделить на 5 категорий по характеристикам и спектру применения. Рассмотрим эту классификацию подробнее:
Спектр действия
Различают антибактериальные средства:
По составу
Антибактериальные препараты делят на 6 групп:
Поколения препаратов. У передовых антимикробных препаратов насчитывается уже шесть генераций. Например, пенициллин был первым средством природного происхождения, тогда как третья или шестая генерация – это уже улучшенная версия, которая включает в состав сильнейшие ингибиторы. Зависимость прямая: чем новее генерация, тем эффективнее воздействие препаратов на патогенную микрофлору.
По способу приема. Пероральные – принимают через рот. Это различные сиропы, таблетки, растворимые капсулы, суспензии. Парентеральные – вводятся внутривенно или внутримышечно. Они быстрее дают эффект, чем пероральные лекарства. Ректальные препараты вводятся в прямую кишку.
Важно! Принимать антибиотики допускается только после консультации с врачом, иначе разовьется антибиотикорезистентность.
Антибактериальные средства нового поколения
Отличие последних генераций антибиотиков от их ранних версий в более совершенной формуле действующего вещества. Активные компоненты точечно устраняют только патологические реакции в клетке. Например, кишечные антибиотики нового поколения не нарушают микрофлору ЖКТ. При этом они борются с целой «армией» возбудителей инфекций.
Новейшие антибактериальные препараты делятся на пять групп:
Рассмотрим несколько известных противомикробных средств импортного и российского производства.
Амоксициллин – импортный противомикробный препарат из группы пенициллинов. Используется во врачебной практике для лечения бактериальной инфекции. Эффективен при кишечных инфекциях, гайморите, ангине, болезни Лайма, дизентерии, сепсисе.
Авелокс – медпрепарат последней генерации из группы фторхинолонов. Отличается сильнейшим воздействием на бактериальные и атипичные возбудители. Не вредит почкам и ЖКТ. Используется при острых, хронических заболеваниях.
Цефалоспорины – антибиотики третьего поколения. К этой группе относят Цефтибутен, Цефтриаксон и другие. Используются для лечения пиелонефрита, пневмонии. В целом это безопасные средства с малым количеством побочных действий. Однако их нужно принимать только после консультации с врачом. Медпрепаратов много, а какой именно выбрать – порекомендует специалист.
Дорипрекс – импортный противомикробный препарат синтетического происхождения. Показал хорошие результаты при лечении пневмонии, запущенных интраабдоминальных инфекций, пиелонефритах.
Инваз – антибактериальное средство из группы карбапенемов. Выпускается в ампулах для парентерального способа применения. Показывает быстрый эффект при лечении бактериальных расстройств кожи, мягких тканей, инфекциях мочевыводящих путей, пневмонии, септицемиях.
Аугметин – полусинтетический пенициллин третьей генерации с добавлением усиливающих ингибиторов. Педиатрами признается лучшим комплексным медпрепаратом для лечения детских гайморита, бронхита, тонзиллита и других инфекций дыхательных путей.
Цефамандол – антибактериальное средство российского производства. Относится к группе цефалоспоринов третьего поколения. Используется для лечения кишечных инфекций, возбудителей инфекций половых органов. Как противомикробное средство обширного диапазона воздействия применяется при простудных заболеваниях.
Лучшие антибактериальные препараты широкого диапазона действия
Противомикробные средства новой генерации обычно синтезируют из природного сырья и стабилизируют в лабораториях. Это помогает усилить эффект лекарства на патогенную микрофлору.
Какие препараты самые сильные? Врачи относят к таким антибактериальные средства широкого спектра воздействия. Приведем ниже краткий список препаратов по названиям:
Резюме
Мы рассмотрели российские и импортные антибиотики широкого спектра действия, кратко описали классификацию препаратов. Ответим на вопрос: какие антибактериальные средства выбрать?
Важно понимать, противомикробные лекарства для обширного применения обладают токсичностью, поэтому негативно влияют на микрофлору. Кроме того, бактерии мутируют, а значит препараты теряют свою эффективность. Поэтому антибактериальные средства с новейшей структурой будут в приоритете, чем их ранние аналоги.
Самолечение антибиотиками опасно для здоровья. При инфекционном заболевании первым делом нужно обратиться к врачу. Специалист установит причину болезни и назначит эффективные антибактериальные средства. Самолечение «наугад» приводит к развитию антибиотикорезистентности.
Антибактериальная терапия инфекционных диарей у детей
Рассмотрены подходы к терапии острых кишечных инфекциях у детей. Широкий спектр антибактериального действия, практически полное отсутствие влияния на нормальную микрофлору, высокую безопасность, позволяет рекомендовать кишечный антисептик нифуроксазид для
Инфекционные диареи в настоящее время занимают второе место в структуре инфекционной заболеваемости детей, уступая только острым респираторным инфекциям. Уровень заболеваемости острыми кишечными инфекциями (ОКИ) у детей в 2,5–3 раза выше, чем у взрослых, при этом более половины регистрируемых случаев инфекционных диарей приходится на долю детей раннего возраста. По данным Всемирной Организации Здравоохранения (ВОЗ) (2008), в мире ежегодно регистрируется до 2 млрд диарейных заболеваний и около 5 млн детей ежегодно умирают от кишечных инфекций и их осложнений. В Европе ежегодно регистрируется от 0,5 до 1,9 эпизодов инфекционных диарей у каждого ребенка младше 3 лет [1]. У детей инфекционная диарея по-прежнему является одной из основных причин смертности, причем не только в развивающихся странах [2, 3].
В настоящее время в России отсутствуют согласованные подходы к терапии ОКИ у детей, причем частота назначения антимикробных препаратов остается на высоком уровне, особенно у госпитализированных пациентов [4]. По этой причине представляется актуальным освещение вопросов антимикробной терапии ОКИ на современном этапе. Прежде чем начать терапию ОКИ, необходимо установить патогенетический тип диареи (инвазивный, секреторный, осмотический или смешанный), определить синдром поражения желудочно-кишечного тракта (ЖКТ) (гастрит, гастроэнтерит, энтерит, гастроэнтероколит, энтероколит, колит, дистальный колит), кроме этого, необходимо диагностировать развившиеся осложнения ОКИ (синдром дегидратации, инфекционно-токсический шок, гемолитико-уремический синдром и т. д.) и оценить преморбидный фон пациента (есть ли у больного пищевая аллергия, синдром мальабсорбции, иммунодефицитное состояние и т. д.) [5].
Основные принципы терапии ОКИ у детей предполагают целенаправленное воздействие, в первую очередь, на макроорганизм, обуславливающее коррекцию возникших водно-электролитных расстройств, а также и элиминацию возбудителя. При остром гастроэнтерите ВОЗ считает абсолютно доказанной эффективность двух терапевтических мероприятий: регидратации и диетотерапии (2006). При этом не следует забывать, что более 70% всех инфекционных диарей у детей вызываются вирусными агентами [3, 6, 7], а при вирусных инфекциях антибактериальная терапия не только не показана, но и наносит значительный вред макроорганизму [8, 9].
Наиболее дискутабельным остается вопрос о целесообразности использования антимикробных средств в лечении бактериальных ОКИ у детей. Назначая антибиотик в этих случаях, врач ожидает: уменьшения выраженности клинических симптомов; сокращения продолжительности заболевания; снижения частоты развития осложнений; прекращения выделения возбудителя; предупреждения дальнейшего распространения инфекции [10].
В то же время доказано, что использование антибиотиков при бактериальной диарее далеко не всегда эффективно и безопасно. При энтерогеморрагическом эшерихиозе, вызванном как E. coli О157: Н7, так и E. coli O104: H4, применение антибиотиков приводит к массивному высвобождению шигаподобного токсина, следовательно, увеличивает риск развития гемолитико-уремического синдрома (ГУС). При этом включение в терапию фторхинолонов и триметоприм/сульфаметоксазола сопровождалось высоким риском развития ГУС, а наиболее безопасным и эффективным оказалось использование карбапенемов, макролидов и рифаксимина [11].
Назначение антимикробных препаратов при бактериальных диареях в значительном проценте случаев не только не приводит к санации макроорганизма от возбудителя, но и, наоборот, способствует продолжительной персистенции бактериального агента в ЖКТ, вследствие не только подавляющего влияния на нормальную микрофлору кишечника, но и прямого иммуносупрессивного действия [12, 13]. По данным отечественных и зарубежных исследователей, затяжное реконвалесцентное бактериовыделение сальмонелл формируется у значительного числа пациентов, получавших антибиотики в острую фазу инфекции, по сравнению с лицами, получавшими исключительно патогенетическую терапию [14, 15]. По нашим собственным данным, бактериовыделение сальмонелл в периоде реконвалесценции отмечено в среднем у 37% детей, лечившихся системными антимикробными средствами. Влияние антимикробной терапии на иммунный ответ было показано авторами при шигеллезе, причем комбинированная антибактериальная терапия приводила к выраженной супрессии как гуморального иммунного ответа, так и показателей фагоцитоза [16].
Самым серьезным недостатком широкого использования антибактериальных препаратов при лечении инфекционных диарей является быстрое развитие у представителей семейства Enterobacteriaceae резистентности к антимикробным препаратам [17]. Так, отечественными авторами зафиксирован неуклонный рост числа штаммов Salmonella enteritidis, устойчивых к большинству стартовых антимикробных препаратов. Например, к налидиксовой кислоте в настоящее время резистентно до 60% циркулирующих штаммов сальмонелл [14]. Все чаще выявляются штаммы кампилобактерий, обладающие широкой антибиотикорезистентностью, в том числе к макролидам и фторхинолонам [14, 18]. Параллельно с ростом антибиотикорезистентности отмечено снижение клинической эффективности стартовой антибактериальной терапии при назначении налидиксовой кислоты, она уменьшилась к 2009 г. по сравнению с 2000–2005 гг. с 61% до 48,3%, а при использовании амикацина — с 53,9% до 31,7% [14, 15].
Кроме того, применение противомикробных препаратов нередко обуславливает развитие аллергических реакций, вплоть до анафилактического шока, а также назначение антибиотиков может привести к развитию не только идиопатической антибиотикоассоциированой диареи, но и тяжелых антибиотикоассоциированных колитов, обусловленных токсинообразующими штаммами Clostridium difficile [6, 10].
Проведенные в России немногочисленные фармакоэпидемиологические исследования показали, что у детей, болеющих ОКИ, в большинстве случаев в стационаре используется антибактериальная терапия (72–100% госпитализированных), причем минимум у трети больных отсутствуют какие-либо показания к ее назначению, при этом во многих стационарах используются малоэффективные или токсичные препараты (хлорамфеникол, естественные пенициллины, рифампицин) [4, 19, 20].
В практическом здравоохранении отмечаются не только ошибки в выборе антимикробного препарата для лечения инфекционных диарей, но и часто встречаются как недостаточные, так и избыточные дозы назначаемых препаратов, неадекватный способ введения, неправильный выбор интервалов между введениями, необоснованное сочетание двух и более антибактериальных средств [13]. Если доза антибиотика недостаточна и не обеспечивает в крови и тканях концентрации, превышающие минимально подавляющие концентрации основных возбудителей инфекции, то это не только становится одной из причин неэффективности лечения, но и создает предпосылки для формирования антибиотикорезистентности микроорганизмов. В современной ситуации, при наличии высокоэффективных антимикробных препаратов широкого спектра действия для лечения ОКИ, показания к комбинированной антибактериальной терапии практически отсутствуют и приоритет в лечении остается за монотерапией [6, 18, 21].
Кроме этого, до настоящего времени при инфекционных диареях проводится необоснованно длительная антибактериальная терапия со сменой 3–4 лекарственных средств, реже имеет место неоправданно короткая антимикробная терапия [4].
В силу вышесказанного в настоящее время показания к использованию антибиотиков в лечении ОКИ являются строго ограниченными и определяются типом диареи и этиологией заболевания, формой тяжести инфекционного заболевания, возрастом и состоянием преморбидного фона пациента [6, 9, 21].
Антимикробный препарат, предназначенный для лечения инфекционных диарей у детей, должен отвечать следующим критериям: иметь высокую активность в отношении основных циркулирующих возбудителей бактериальных ОКИ; обладать бактерицидным действием; иметь высокую биодоступность действующего вещества и создавать высокую концентрацию в ЖКТ. Необходимо, чтобы уровень штаммов, имеющих резистентность к препарату, был низким. Немаловажную роль в педиатрии играют профиль безопасности (количество и характер токсических эффектов), фармакоэкономические характеристики (соотношение эффективности, безопасности и стоимости) препарата, удобная для детей форма выпуска (суспензия) и режим дозирования лекарственного средства [1, 5–7].
Ю. Б. Белоусовым и С. М. Шатуновым (2001) было предложено разделить антимикробные препараты для лечения кишечных инфекций на две группы. Первая — препараты, которые после перорального приема не абсорбируются (т. е. имеют низкую биодоступность) и обеспечивают антимикробный эффект только в кишечнике, не оказывая системного действия (так называемые кишечные антисептики — нитрофураны, нефторированные хинолоны и хинолины, некоторые сульфаниламиды и др.); вторая — антибиотики, хорошо всасывающиеся в тонкой кишке, которые оказывают системное действие, но одновременно обеспечивают низкие терапевтические концентрации в стенке кишечника (фторхинолоны, хлорамфеникол, тетрациклины, макролиды, нитроимидазолы и др.) [22].
Высокие концентрации препаратов первой группы в пищеварительном тракте являются важной характеристикой для лечения инфекционных диарей, но в случае генерализации инфекции эти антимикробные средства оказываются неэффективными, так как не обеспечивают терапевтических концентраций в крови и паренхиматозных органах [22–24]. В последние годы при лечении бактериальных ОКИ широко применяются невсасывающиеся антимикробные препараты. Их преимуществами по сравнению с системными антибиотиками являются: возможность непосредственного воздействия на бактериальный агент при низком риске развития резистентности штаммов; практически полное отсутствие негативного влияния на нормальную микрофлору; незначительная частота развития системных побочных реакций; отсутствие лекарственного взаимодействия, так как они не оказывают влияния на ферменты системы цитохрома Р450 [25–28].
В соответствии с рекомендациями ВОЗ, антимикробная терапия при инфекционных диареях показана только при следующих нозологических формах: холере, брюшном тифе, шигеллезе и амебиазе [1].
По мнению ведущих отечественных инфекционистов, показаниями к назначению антимикробной терапии у детей с острыми кишечными инфекциями являются развитие (угроза развития) генерализованных форм (тифоподобных, септических) заболеваний; тяжелые формы инвазивных диарей, а также среднетяжелые формы инвазивных ОКИ у детей групп риска. К пациентам групп риска относятся дети с тяжелыми хроническими заболеваниями (первичные иммунодефициты, злокачественные новообразования, воспалительные заболевания кишечника, корригированные оперативным путем врожденные пороки сердца, ювенильные артриты и т. д.) и дети раннего возраста (первые 6–12 месяцев жизни) [6, 7, 21]. Кроме вышеперечисленных лиц, антибактериальная терапия является обязательной для пациентов с иерсиниозами.
Принципы рациональной антибактериальной терапии ОКИ у детей предусматривают своевременное назначение препарата (период разгара болезни); разделение используемых антимикробных препаратов на стартовые, альтернативные и препараты резерва; учет антибиотикочувствительности выделенных штаммов; использование оптимального способа, дозы, кратности введения и курса терапии, а также учет индивидуальных особенностей пациента (возраста, преморбидного фона и т. д.).
Большинство зарубежных источников препаратами выбора для терапии инфекционных диарей у детей, протекающих с клиникой гемоколита, считают цефтриаксон и азитромицин, а у взрослых пациентов — фторхинолоны и азитромицин [1, 18]. Длительность назначения антимикробных препаратов не превышает 5 суток, а во многих случаях ограничивается 24–48 часами. Для терапии шигеллезов сохраняют актуальность ампициллин, налидиксовая кислота, триметоприм/сульфаметоксазол, нитрофураны [18, 29].
Стартовые препараты антибактериальной терапии ОКИ целесообразно использовать в ранние сроки заболевания при среднетяжелых формах инвазивных диарей и отсутствии индивидуальной непереносимости препаратов. Преимущество отдается препаратам с широким спектром действия, которые обладают бактерицидным или бактериостатическим действием, плохо всасываются из кишечника и не оказывают подавляющего влияния на аутохтонную микрофлору. К таким препаратам относятся производные оксихинолина, нитрофураны, аминогликозиды I–II поколения. Так как выбор антибактериального препарата в острый период инфекционной диареи осуществляется эмпирически, то при необходимости следует корригировать терапию в соответствии с антибиотикочувствительностью выделенного возбудителя [13, 22].
Эффективность антибактериальной терапии, основными критериями которой являются нормализация температуры тела, купирование или уменьшение выраженности интоксикации и диарейного синдрома, оценивается в течение 48–72 часов после начала лечения. При отсутствии положительной клинической динамики или прогрессировании симптомов заболевания, а также на поздних сроках заболевания как альтернатива стартовым антибиотикам могут использоваться иные антибиотики: защищенные аминопенициллины, нефторированные хинолоны (налидиксовая кислота), хлорамфеникол, макролиды II поколения, цефалоспорины II–III поколения, аминогликозиды II–III поколения (амикацин, нетилмицин), нитроимидазолы. При тяжелых формах ОКИ целесообразно начинать терапию с парентерального введения антимикробных препаратов, а по достижении клинического эффекта возможен переход на пероральный прием антибиотика до завершения полного курса терапии.
Антибиотики резерва используются исключительно в условиях стационара, обладают широким спектром действия и высокоэффективны в отношении практически всех возбудителей ОКИ, в том числе и устойчивых к антибактериальным препаратам стартовой и альтернативной терапии. Показаниями к назначению таких препаратов являются генерализованные и септические формы ОКИ, тяжелое течение ОКИ у детей с неблагоприятным преморбидным фоном, подозрение на нозокомиальную природу заболевания, а также неэффективность вышеназванных групп антибиотиков. К препаратам резерва относятся цефалоспорины III–IV поколения, карбапенемы, аминогликозиды II–III поколения, фторхинолоны (у детей можно использовать только по жизненным показаниям) [8, 21, 22].
При выборе этиотропной терапии необходимо учитывать не только предполагаемого возбудителя ОКИ, но и быстро формирующуюся резистентность циркулирующих энтеробактерий к традиционно применяемым антибактериальным средствам. В этой связи рекомендации по выбору оптимального антибактериального средства должны обязательно основываться на региональных данных по структуре антибиотикорезистентности.
В детской практике имеются сложности в антимикробной терапии инфекционных диарей, особенно это касается пероральных форм лекарственных средств и связано в первую очередь с возрастными ограничениями по применению препаратов в педиатрии. Так, налидиксовая кислота разрешена к применению с 2-летнего возраста (а по некоторым источникам с 18 лет); рифаксимин с 12-летнего возраста, а Интетрикс в настоящее время вообще не разрешен в педиатрии.
Следовательно, основным стартовым препаратом в детской инфектологии в последние годы является нифуроксазид. Нифуроксазид относится к нитрофурановым препаратам, антибактериальная активность которых обусловлена продукцией нитроанионов. Нитрофурановые препараты являются акцепторами ионов водорода при переносе электронов с флавиновых ферментов на цитохром, тем самым нитрофураны блокируют энергообразование в бактериальной клетке. Кроме этого, нифуроксазид блокирует активность альдолаз, дегидрогеназ, транскетолаз и синтез макробелковых комплексов. В результате этих взаимодействий нитрофуранов с бактериальными агентами нарушаются процессы роста и деления бактериальных клеток. Доказано, что нифуроксазид в среднетерапевтических дозах оказывает бактериостатический, а в высоких дозах — бактерицидный эффект [23, 24, 30].
Нифуроксазид относится к местным антисептикам и практически не всасывается в кровь из ЖКТ, не влияет на эндогенную микрофлору, практически не приводит к формированию антибиотикорезистентных штаммов [30, 31].
В России и за рубежом имеется обширный положительный опыт использования нифуроксазида при шигеллезе, сальмонеллезе, ОКИ, вызванных условно-патогенными возбудителями [15, 31, 32]. В 2013 году в РФ зарегистрирован нифуроксазид под торговым названием Стопдиар, причем у данного препарата есть две лекарственные формы — таблетки, 100 мг, покрытые пленочной оболочкой, разрешены с 6-летнего возраста и форма суспензии для пациентов с 2-месячного возраста. Данная лекарственная форма является комплексной, так как в ее составе кроме нифуроксазида (5 мл = 220 мг) содержится симетикон. Симетикон — это поверхностно-активное пеногасящее средство, уменьшающее газообразование в кишечнике. Содержание симетикона в суспензии Стопдиара особенно актуально для детей раннего возраста, которые страдают от повышенного газообразования на фоне инфекционных диарей.
Таким образом, рост и изменение лекарственной чувствительности штаммов возбудителей инвазивных диарей требует строгих подходов к назначению антимикробных препаратов при ОКИ у детей, целесообразно использовать режим ступенчатой терапии, что определяется высокой клинической эффективностью и уменьшением психотравмирующего влияния на маленького пациента. Учитывая широкий спектр антибактериального действия, практически полное отсутствие влияния на нормальную микрофлору, высокий профиль безопасности и наличие суспензионной лекарственной формы, кишечный антисептик нифуроксазид можно считать стартовым препаратом при лечении инфекционных диарей у детей.
Литература
ФГБУ НИИДИ ФМБА России, Санкт-Петербург