Может ли сахарная вода замерзнуть?
Наличие сахар (или соль, или любое другое растворенное вещество в воды) делает действительно снизить замораживание точка воды, Это делает это за счет снижения давления пара воды (тенденция, описывающая тенденцию вещества превращаться в газ).
Просто так, что может снизить температуру замерзания воды?
Вода быстрее замерзает с солью? Пока чисто вода замерзает при 0 ° C (32 ° F), соленая вода должно быть холоднее перед этим замерзает и поэтому обычно требуется больше времени, чтобы замораживать, Чем больше соль в воды, чем ниже замораживание точка. Часто, соль ставится на дороги, чтобы растопить лед.
Может ли сахарная вода замерзнуть?
Сахар молекулы не упаковываются вместе с воды молекулы, поэтому, когда воды молекулы начинают замораживать, сахар молекулы остаются в жидкости воды.
Что заставляет воду замерзать быстрее?
Как замерзает вода?
Замораживание происходит, когда молекулы жидкости становятся настолько холодными, что замедляются настолько, чтобы зацепиться друг за друга, образуя твердый кристалл. Для чистого воды, это происходит при 32 градусах по Фаренгейту, и, в отличие от большинства других твердых тел, лед расширяется и на самом деле менее плотен, чем воды.
Морозится ли соленая или сахарная вода быстрее?
Мы предполагаем одинаковую массу соль и сахар растворяются в двух одинаковых емкостях воды, затем положите в ту же морозильную камеру, сахарный раствор скорее всего, замораживать первый. Это потому, что соленая вода будем замораживать при более низкой температуре. Это потому, что соленая вода будем замораживать при более низкой температуре.
Снижает ли соль температуру замерзания воды?
Соль тает лед в основном потому, что добавление соль понижает Точка замерзания воды, чистый вода замерзает при 32 ° F (0 ° C). Вода с соль (или любое другое вещество в нем) будет замораживать некоторые более низкая температура.
Что влияет на точку замерзания?
Молекулы с более сильными межмолекулярными силами плотно стягиваются вместе, образуя твердое тело при более высоких температурах, поэтому их Точка замерзания выше. Молекулы с более низкими межмолекулярными силами не затвердеют до тех пор, пока температура опускается дальше.
Что происходит, когда сахар смешивается с водой?
когда сахар растворяется в воды, слабые связи между отдельными молекулами сахарозы разрываются, и эти C12H22O11 молекулы попадают в раствор. Сахар растворяется в воды потому что энергия выделяется, когда слегка полярные молекулы сахарозы образуют межмолекулярные связи с полярными воды молекулы.
При какой температуре замерзает сахарная вода?
Что происходит, когда вы добавляете сахар во лед?
Сахар и все, что может раствориться в воде, растает лед. Сахар расплавы лед понижая температуру плавления и замерзания воды, как соль. Сахар растворился на лед и мешает молекулам воды. Молекулы воды необходимы для связывания лед кристаллы, чтобы он замерз.
Что снижает температуру замерзания воды?
Соль понижается что собой представляет замораживание/ плавление точка воды, поэтому в обоих случаях идея состоит в том, чтобы воспользоваться преимуществом ниже плавления точка. Лед образуется, когда температура воды достигает 32 градусов по Фаренгейту (0 градусов по Цельсию). На проезжей части это означает, что если посыпать лед солью, можно его растопить.
Что влияет на точку замерзания?
Молекулы с более сильными межмолекулярными силами плотно стягиваются вместе, образуя твердое тело при более высоких температурах, поэтому их Точка замерзания выше. Молекулы с более низкими межмолекулярными силами не затвердеют до тех пор, пока температура опускается дальше.
У льда или мороженого более низкая точка замерзания?
Из-за сахара вода закипает быстрее?
Добавление сахар в воды создает истинное решение. Это приводит к снижению давления пара, повышая кипение точка воды.
Из-за сахара вода закипает быстрее?
Добавление сахар в воды создает истинное решение. Это приводит к снижению давления пара, повышая кипение точка воды.
Как замораживание сахара удаляет воду?
Добавьте сахар, чтобы смягчить и подсластить его, и вы уменьшите замораживание точка. Это означает, что он не станет достаточно холодным, чтобы замораживать когда вы кладете его в твердое тело лед, Потому что замораживание точка воды выше, чем у подслащенных крем, лед кристаллы образуются из молекул воды как мороженое смешивать замерзает.
Как замораживание сахара удаляет воду?
Освободи Себя сахар контролирует количество лед образуются при замораживании продукта. Это гарантирует, что мороженое достаточно мягкий, чтобы его можно было зачерпнуть и съесть. Это также придает продукту толщину и делает его устойчивым к тепловому удару (при нахождении в морозильной камере и вне ее). В сахар поможет также высвободить аромат мороженое.
Морозится ли соленая или сахарная вода быстрее?
Мы предполагаем одинаковую массу соль и сахар растворяются в двух одинаковых емкостях воды, затем положите в ту же морозильную камеру, сахарный раствор скорее всего, замораживать первый. Это потому, что соленая вода будем замораживать при более низкой температуре. Это потому, что соленая вода будем замораживать при более низкой температуре.
Что замерзает быстрее: вода или сахарная вода?
Результаты этого эксперимента подтверждают выдвинутую гипотезу и показывают простую вода замерзает сначала, так как он добирается до своего замораживание температура, в то время как сахарная вода и планка воды все еще холодеют. Это также показывает, что замораживание точка соли воды ниже, чем у сахарная вода.
Что я в депрессии точки замерзания?
Замораживание–точечная депрессия это уменьшение Точка замерзания растворителя при добавлении нелетучего растворенного вещества. Примеры включают соль в воде, спирт в воде или смешивание двух твердых веществ, таких как примеси, в тонко измельченном лекарственном средстве.
Что происходит, когда вы добавляете сахар во лед?
Сахар и все, что может раствориться в воде, растает лед. Сахар расплавы лед понижая температуру плавления и замерзания воды, как соль. Сахар растворился на лед и мешает молекулам воды. Молекулы воды необходимы для связывания лед кристаллы, чтобы он замерз.
Почему мороженое такое сладкое?
Для того, чтобы получить текущая вода в замораживать, температура должна быть исключительно низкой. В некотором смысле ледники похожи на замерзшие реки. Затем тонкий слой на поверхности начинает замораживать плавая на более плотном воды ниже. Напротив, в движущаяся вода, весь объем должен остыть до 0C, прежде чем замораживание начинается.
Какая точка замерзания у лимонада?
-0.5 °C. Лимонад сейчас ниже точки замерзания, и ледяные кристаллы покрываются множеством пузырьков, поэтому он замерзает прямо у вас на глазах!
Меняет ли хлор температуру замерзания воды?
Да, хотя их точка замерзания просто немного ниже чем обычно хлорированная вода. Соль воды бассейны замораживать обычно замораживать ближе к 28 градусам вместо 32, но, тем не менее, они все еще замораживать.
Меняет ли хлор температуру замерзания воды?
Вода замерзает из раствора в чистом виде в виде льда. В сахар решение, такое как мороженое, начальный замораживание температура раствора ниже 0 ° C из-за в они растворились сахара (замораживание точечная депрессия), что в основном является функцией сахар содержание смеси.
Вы должны добавить сахар в мороженое?
Так же, как жир, сахар один из тех ингредиентов, из которых мы могли бы исключить мороженое. Или хотя бы уменьшить. Но так же, как толстый, сахар является важным компонентом мороженое. Итак, пока мы может конечно уменьшите, вырезать вообще очень сложно.
Что замерзает быстрее: вода или сахарная вода?
Результаты этого эксперимента подтверждают выдвинутую гипотезу и показывают простую вода замерзает сначала, так как он добирается до своего замораживание температура, в то время как сахарная вода и планка воды все еще холодеют. Это также показывает, что замораживание точка соли воды ниже, чем у сахарная вода.
Какой сахар используется в мороженом?
Лучшее сахар использовать в использование чистый тростник сахар так как это меньше всего влияет на вкус и текстуру. Другой сахара может хорошо работать с точки зрения вкуса, и на самом деле я предпочитаю делать ваниль мороженое с заклинателем сахар так как я нахожу вкус и мягкую текстуру более приятными.
Какая точка замерзания мороженого?
С мороженое это не просто вода, она должна быть немного ниже 32 ° F, чтобы замораживать.
Может ли замерзнуть движущаяся вода?
Результаты этого эксперимента подтверждают выдвинутую гипотезу и показывают простую вода замерзает сначала, так как он добирается до своего замораживание температура, в то время как сахарная вода и планка воды все еще холодеют. Это также показывает, что замораживание точка соли воды ниже, чем у сахарная вода.
Какая точка замерзания у лимонада?
-0.5 ° С. В лимонад сейчас ниже своего Точка замерзания, и есть много пузырей для кристаллов льда, поэтому он замерзает перед твоими глазами!
Как соль влияет на температуру замерзания мороженого?
Для того, чтобы получить текущая вода в замораживать, температура должна быть исключительно низкой. В некотором смысле ледники похожи на замерзшие реки. Затем тонкий слой на поверхности начинает замораживать плавая на более плотном воды ниже. Напротив, в движущаяся вода, весь объем должен остыть до 0C, прежде чем замораживание начинается.
Как происходит замерзание дистиллированной воды, при какой температуре?
Существующая точка зрения о том, что дистиллированная вода не замерзает даже при минусовой температуре, не совсем верна. Процесс замерзания несколько отличается от аналогичного процесса, происходящего с обычной водой.
Замерзание такого состава зависит от ряда факторов. Имеет значение, в каких условиях находится дистиллированная вода. Также важно следовать рекомендациям в ситуациях, когда дистиллят нужно использовать, но он замерз.
Может и должна ли замораживаться?

Если в обычной воде кристаллы льда появляются уже при 0 0 С, то дистиллят замерзает только при твердом минусе.
В неочищенной воде имеются соли с прочими примесями. Из-за них в такой воде много центров кристаллизации. Дистиллированный раствор практически не имеет центров кристаллизации.
В такой среде нет посторонних примесей, за счет которых вода быстрее перейдет в твердую форму. Но при дальнейшем снижении температуры даже идеально очищенная смесь все равно замерзнет.
Почему существует утверждение, что дистиллят не превращается в лед?
Данное мнение основывается на свойствах такого состава. В нем отсутствуют примеси. Именно из-за них простая вода замерзает уже при 0 0 С. Поскольку в очищенных растворах примесей не имеется, то считается, что они могут оставаться в жидком состоянии даже при минусе.
От каких факторов зависит температура кристаллизации?

Играет роль внешнее воздействие на тару с дистиллированной водой. Даже стерильный раствор при добавлении в него небольшого количества посторонних примесей начнет быстро кристаллизоваться даже при слабом минусе.
Отличие в заморозке дистиллята от обычной воды
Замораживание дистиллята отличается от заморозки простой воды более низкой точкой замерзания. Чем состав чище, тем ниже температура потребуется ему для полного превращения в лед. Водопроводная вода превратится в лед уже при 0 0 С.
Отличие также кроется в центрах кристаллизации. В очищенной воде их нет из-за отсутствия в ней примесей. В обычной воде таких центров кристаллизации очень много. По этой причине она быстрее охлаждается.

Очищенный состав кристаллизуется более длительное время. Фрагменты льда в такой воде формируются постепенно.
Обычная вода покрывается льдом по всей поверхности. Замораживание начинается снизу и движется вверх. В дистилляте этот процесс идет сверху вниз.
Температура превращения в лед
Скорость превращения очищенной воды в лед зависит от условий, в которых она находится. Дистиллированная смесь, находящаяся на улице и внутри аккумулятора машины, замерзает при разной температуре. В двух указанных случаях отмечается разная точка замерзания.
На улице
В уличных условиях очищенный состав кристаллизуется довольно быстро. На открытом воздухе нет факторов, препятствующих быстрому переходу раствора в состояние льда.
В аккумуляторе
Поскольку в данном случае очищенная вода находится внутри аккумуляторной батареи, то процесс ее замерзания будет происходить медленнее. Но это касается случаев, если дистиллят заливается в прогретый аккумулятор. Он остывает медленно. При слабом минусе дистиллят внутри него не успеет заморозиться.
Как происходит процесс?
Процесс происходит следующим образом:
В процессе замораживания объем дистиллированной смеси становится больше почти на 10%.
Что делать, при замерзании?
В обычных условиях заморозка дистиллята не создает проблем. Замерзший состав необходимо поставить в отапливаемое помещение и подождать.
Когда он оттает и достигнет комнатной температуры, его можно продолжить использовать по назначению. Свойства такого раствора не изменятся.
Не следует ускорять размораживание дистиллированной воды. Нельзя ее нагревать. При данном процессе раствор перестанет быть чистым. В него попадут посторонние примеси из тары, в которой он нагревается.
Если дистиллят замерз внутри аккумулятора, то необходимо предварительно снять его с автомобиля и положить в теплое помещение. Батарея должна оттаять сама при комнатной температуре.

Дистиллят в состоянии льда из-за своего расширения может повредить их, приведя в негодность весь аккумулятор.
Только после тщательной проверки батареи можно устанавливать ее обратно на автомобиль и продолжать им пользоваться. Часто замерзшая дистиллированная вода в аккумуляторе является причиной его поломки. В таких ситуациях дистиллят сливается, а батарея либо отдается в ремонт, либо заменяется на новую.
Заключение
Дистиллированная вода способна к замораживанию, но при более низких температурных показателях, чем обычная вода. Это обусловлено отсутствием в ней примесей и центров кристаллизации.
При какой температуре замерзает сладкая вода
С уважением Евгений Мультсофт!
Профи (851),закрыт
3 года назад
Дополнен 8 лет назад
Хозяева забыли на даче банки с дистиллированной водой, некрепким сладким чаем и огуречным рассолом и бутылку жидкости для очистки автомобильных стёкол. Концентрации сахара в чае и поваренной соли в рассоле в граммах на 1 литр примерно одинаковы. Наступила зима. В каком порядке будут замерзать жидкости? Ответ обоснуйте.
Дополнен 8 лет назад
Хозяева забыли на даче банки с дистиллированной водой, некрепким сладким чаем и огуречным рассолом и бутылку жидкости для очистки автомобильных стёкол. Концентрации сахара в чае и поваренной соли в рассоле в граммах на 1 литр примерно одинаковы. Наступила зима. В каком порядке будут замерзать жидкости? Ответ обоснуйте.
Дополнен 8 лет назад
Хозяева забыли на даче банки с дистиллированной водой, некрепким сладким чаем и огуречным рассолом и бутылку жидкости для очистки автомобильных стёкол. Концентрации сахара в чае и поваренной соли в рассоле в граммах на 1 литр примерно одинаковы. Наступила зима. В каком порядке будут замерзать жидкости? Ответ обоснуйте.
ДивергентВысший разум(1351298)8 лет назад
RIPvanWINKLEИскусственный Интеллект(156483)8 лет назад
Сергей ЧмелевМастер(2223)8 лет назад
Добрый день. Можете мне объяснить по структуре кристалла льда. Например при замерзании чистой воды, в узлах кристалл решетки находятся молекулы воды. А вот например, если замерзает сладкая вода (вода в которой разбавлен сахар), то в узлах кристалл решетки кристалла находятся молекулы воды и молекулы сахара (вместо сахара, можно использовать любое другое вещество растворяющееся в воде)? Павел Сергеевич, Черновцы
Здравствуйте, уважаемый Павел Сергеевич. Теоретически, большинство молекул белков, жиров и углеводов по своему строению довольно идеально подходят к структуре льда, как бы “вписываясь” в пустоты его кристаллической решетки. Но на практике всё происходит совершенно иначе. Замерзая и превращаясь в лёд вода как бы изгоняет из растущего кристалла все примеси и чужеродные молекулы. Именно на этом принципе и основано очищение воды методом замораживания-оттаивания, когда в результате получается свободная от примесей талая вода.
По другому ведёт себя вода и в отношении молекул, форма которых не подходит в структуре льда: крупные она, замерзая, ломает, а мелкие изгоняет. Достаточно вспомнить лед в Северном Ледовитом океане пресный, потому что вода, замерзая, освобождается от солей.
Вы можете самостоятельно произвести в домашних условиях такой простой эксперимент: В стеклянный стакан с водой налейте немного чернил, акварельной краски или чайной заварки. Укутайте его верхнюю часть слоем теплоизоляции (шерстяной тканью), чтобы слой льда нарастал от дна стакана к поверхности воды, и поставки в морозильную камеру. Теоретически можно предположить, что через несколько часов в стакане окажется кусок окрашенного льда. Были даже советы эти цветные льдинки развешивать на уличных елках. Но разноцветного льда на практике, однако, так получить не удастся.
Ледяной цилиндрик, вынутый из стакана, будет выглядеть очень любопытно. В нижней его части, там, где начиналось замерзание воды, располагается абсолютно прозрачный лед. Верхняя же его часть окрашена, и гораздо более интенсивно, чем сам раствор. Граница между двумя областями бывает настолько резка, что кажется – это два совершенно разных вещества. Если концентрация краски слишком велика, на поверхности льда может даже остаться её раствор. Почему же лед “не хочет” делаться цветным?
Кристалл стремится вырасти как можно более правильным – это “выгодно” с точки зрения его внутренней энергии. А любые посторонние примеси – будь то молекулы или атомы искажают форму решетки. Поэтому растущий кристалл вытесняет любые посторонние атомы и молекулы, стараясь строить идеальную решетку, пока это возможно. И только когда примесям деваться уже некуда, он начинает встраивать их в свою структуру или оставляет в виде капсул с концентрированной жидкостью. Поэтому морской лед пресный, а даже самые грязные лужи покрываются прозрачным и чистым льдом.
На Дону и Кубани, где издавна выращивали виноград и делали сухие вина, зимой готовят крепкие напитки – “выморозки”. Для этого продукт естественного брожения – вино крепостью 10-12 градусов – выставляют на мороз. В растворе в первую очередь замерзает вода, и остается более концентрированный раствор спирта. Его сливают и повторяют операцию до тех пор, пока не добьются нужной крепости. Чем выше концентрация спирта в растворе, тем ниже температура его замерзания.
Водопроводная вода содержит примерно сто частей примесей на миллион частей воды (в основном это хлор, растворенный для дезинфекции, поваренная соль, которая есть везде, и твердые микрочастицы). Дистилляцией в обычных лабораторных условиях их количество нетрудно понизить раз в сто, получив воду с чистотой 99,9999%. Если же сосуд с этой водой медленно охлаждать с одной стороны, получится лед с чистотой уже до шести девяток после запятой. В нем отыщется только одна частица примеси на сто миллионов частиц воды.
В минералогических коллекциях нередко можно видеть, например, прозрачные кристаллы корунда Al2O3, которые заканчиваются рубиновой “шапочкой”. Это растущий кристалл “собрал” со всего объема примесь – ионы хрома Cr3+, которые превращают бесцветный корунд в красный рубин.
Свойство растущего кристалла вытеснять примеси используют в технике для очистки материалов методом зонной плавки. Образец проходит сквозь кольцевую печь; в ней он плавится, а за ней кристаллизуется. Примеси непрерывно переходят из зоны кристаллизации в расплав и постепенно мигрируют вдоль образца в его конец.
Но, оказывается, включить в кристаллическую решётку небольшие атомы, например, благородных газов – гелия, аргона, криптона, всё же возможно. И даже более того, структура некоторых льдов стабилизируется при включении атомов благородных газов в его кристаллическую решётку. Однако, получить такие экзотические льды в обычных природных условиях не возможно, зато возможно их получить, например, в условиях космоса, при очень низких температурах и высоких давлениях.
Наиболее изученным является лёд I-й природной модификации. Лёд встречается в природе в виде льда (материкового, плавающего, подземного и т.д.), а также в виде снега, инея и т.д. Он распространён во всех областях обитания человека. Собираясь в огромных количествах, снег и лед образуют особые структуры с принципиально иными, нежели у отдельных кристаллов или снежинок, свойствами. Ледники, ледяные покровы, вечная мерзлота, сезонный снежный покров существенно влияют на климат больших регионов и планеты в целом: скопившийся на полюсах Земли лёд способен вызывать многолетние колебания уровня Мирового океана. Лед имеет столь большое значение для нашей планеты и обитания на ней живых существ, что ученые отвели для него особую среду — криосферу, которая простирает свои владения высоко в атмосферу и глубоко в земную кору.
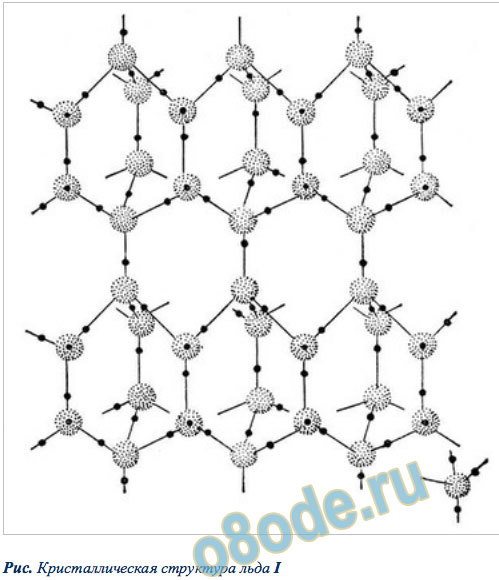
Рис. Кристаллическая структура льда I
Природный лёд I обычно значительно чище, чем вода, т.к. растворимость веществ (кроме NH4F) во льде крайне низкая. А вот лёд II наоборот стабилизуется только в присутствии следовых количеств газов; в чистом виде его никто не получал из-за его нестабильности. Если, например, давление создают с помощью гелия, он обязательно растворится в замерзающей воде. Есть сведения, что аргон — другой инертный газ, пригодный для использования в этой установке, — тоже способен давать со льдом твёрдые растворы. Однако изучением таких клатратных соединений льда с благородными газами специально никто не занимался.
Разгадка структуры льда заключается в строении его молекулы. Кристаллы всех модификаций льда построены из молекул воды H2O, соединённых водородными связями в трёхмерный каркас. Молекулу воды можно упрощенно представить себе в виде тетраэдра (пирамиды с треугольным основанием). В её центре находится атом кислорода, в двух вершинах — по атому водорода, электроны которых задействованы в образовании ковалентной связи с кислородом. Две оставшиеся вершины занимают пары валентных электронов кислорода, которые не участвуют в образовании внутримолекулярных связей, поэтому их называют неподеленными.
Каждая молекула участвует в 4 таких связях, направленных к вершинам тетраэдра. При взаимодействии протона одной молекулы с парой неподеленных электронов кислорода другой молекулы возникает водородная связь, менее сильная, чем связь внутримолекулярная, но достаточно могущественная, чтобы удерживать рядом соседние молекулы воды. Каждая молекула может одновременно образовывать четыре водородные связи с другими молекулами под строго определенными углами, равными 109°28′, направленных к вершинам тетраэдра, которые не позволяют при замерзании создавать плотную структуру. При этом в структурах льда I, Ic, VII и VIII этот тетраэдр правильный. В структурах льда II, III, V и VI тетраэдры заметно искажены. В структурах льда VI, VII и VIII можно выделить 2 взаимоперекрещивающиеся системы водородных связей. Этот невидимый каркас из водородных связей располагает молекулы в виде сетчатой сетки, по структуре напоминающей соты с полыми каналами. Если лед нагреть, сетчатая структура разрушится: молекулы воды начинают проваливаться в пустоты сетки, приводя к более плотной структуре жидкости, — поэтому вода тяжелее льда.
Лед, который образуется при атмосферном давлении и плавится при 0 °С, — самое привычное, но всё же до конца не понятное вещество. Многое в его структуре и свойствах выглядит необычно. В узлах кристаллической решетки льда атомы кислорода выстроены упорядоченно, образуя правильные шестиугольники, а атомы водорода занимают самые разные положения вдоль связей. Поэтому возможны 6 эквивалентных ориентаций молекул воды относительно их соседей. Часть из них исключается, поскольку нахождение одновременно 2 протонов на одной водородной связи маловероятно, но остаётся достаточная неопределённость в ориентации молекул воды.
Другая интересная разновидность льда – лёд II. Расположен лёд II на диаграмме состояния между льдом III и льдом IX. Они различаются между собой упорядочением протонов, кислородный же каркас у них одинаков: спирали из одних молекул воды, как будто нанизанные на оси из других молекул воды. Когда же вероятности протона занять то или иное место равны, лёд будет неупорядоченным.
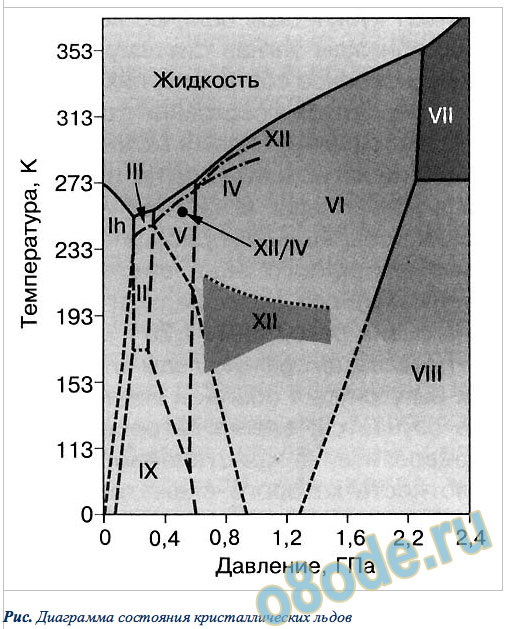
Рис. Диаграмма состояния кристаллических льдов
Лёд III и V-й модификации длительное время сохраняются при атмосферном давлении, если температура не превышает —170°С. При нагревании приблизительно до —150°С лёд превращаются в кубический лёд Ic.
При конденсации паров воды на более холодной подложке образуется аморфный лёд. Эта форма льда может самопроизвольно переходить в гексагональный лёд, причём тем быстрее, чем выше температура.
Лёд IV-й модификации является метастабильной фазой льда. Он образуется гораздо легче и особенно стабилен, если давлению подвергается тяжёлая вода.
Кривая плавления льда V и VII исследована до давления 20 Гн/м2 (200 тыс. кгс/см2). При этом давлении лёд VII плавится при температуре 400°С.
Лёд VIII является низкотемпературной упорядоченной формой льда VII.
Лёд IX — метастабильная фаза, возникающая при переохлаждении льда III и по существу представляющая собой его низкотемпературную форму.
Две самых последние модификации льда — XIII и XIV — открыли ученые из Оксфорда совсем недавно, в 2006 году. Предположение о том, что должны существовать кристаллы льда с моноклинной и ромбической решетками, было трудно подтвердить: вязкость воды при температуре –160°С очень высока, и собраться вместе молекулам чистой переохлажденной воды в таком количестве, чтобы образовался зародыш кристалла, трудно. Этого удалось достичь с помощью катализатора — соляной кислоты, которая повысила подвижность молекул воды при низких температурах. В земной природе подобные модификации льда образовываться не могут, но они могут встречаться на замерзших спутниках других планет.
Однако, все эксперименты с экзотическими льдами, как правило, связаны с их охлаждением до температур сухого льда, жидкого азота, а то и гелия, а также со сжатием до давления в тысячи атмосфер. Общее представление о результатах можно получить, глядя на рисунок выше, где показана диаграмма состояния кристаллических льдов.
Многие льды высокого давления можно сохранить и при нормальном давлении. Для этого их охлаждают в жидком азоте, а затем давление сбрасывают. Именно на таких закалённых льдах и были проведены основные исследования. Они показали, что их строение весьма разнообразно.
Структуру первого льда высокого давления, льда II, определили на заре исследований в этой области, когда появились первые мощные приборы для рентгеноструктурного в 1964 году. Как оказалось, этот лёд состоит из полых колонок, образованных шестизвенными гофрированными циклами. Каждая колонка окружена шестью такими же колонками, сдвинутыми друг относительно друга на треть периода. Структуру этого льда можно получить, если часть сот льда Ih развалить и превратить их в ажурные каркасы, связывающие остальные соты. При этом размер получившихся шестигранных каналов сильно увеличивается — именно у льда II самые широкие каналы, их диаметр составляет 3 Å. В таких каналах могут располагаться атомы гелия, неона и даже молекулы водорода.
Рис. Структура льда II
Включить атомы благородного газа, например, гелия в кристаллическую структуру льда II можно двумя способами. Во-первых, приложить (в атмосфере гелия) к воде давление в 0,28–0,5 ГПа и охладить её до 250–270К. Хотя в этой области диаграммы стабильны льды III и V, получится гидрат на основе льда II. Что интересно, протоны в нём уже упорядочены. (Обычно они упорядочиваются только при сильном охлаждении уже получившегося льда.)
Во-вторых, можно растворить гелий во льду Ih при низкой температуре и давлении 0,3 ГПа. Появление гелия приводит к расширению кристаллической решётки, и затем её нагрев до 180К помогает пройти структурному превращению.
Относительная лёгкость получения твёрдых растворов в льду II, а также его высокий потенциал в качестве хранилища газообразного водорода (одна молекула газа на шесть молекул воды) привлекают к нему внимание учёных-практиков: сейчас активно обсуждается возможность его применения в водородной энергетике.
Но самое удивительное в структуре экзотических льдов заключается в том, что молекулы воды при низких отрицательных температурах и высоких давлениях внутри нанотрубок могут кристаллизоваться в форме двойной спирали, похожей на ДНК. Это было доказано компьютерными экспериментами американских учёных под руководством Сяо Чэн Цзэна в Университете штата Небраска (США).
Рис. Общий вид структуры воды (изображение New Scientist)
Молекулы воды связываются между собой посредством водородных связей, расстояние между атомами кислорода и водорода равно 96 пм, а между двумя водородами – 150 пм. В твёрдом состоянии атом кислорода участвует в образовании двух водородных связей с соседними молекулами воды. При этом отдельные молекулы H2O соприкасаются друг с другом разноимёнными полюсами. Таким образом, образуются слои, в которых каждая молекула связана с тремя молекулами своего слоя и одной из соседнего. В результате, кристаллическая структура льда состоит из шестигранных “трубок” соединенных между собой, как пчелиные соты.
Рис. Внутренняя стенка структуры воды (изображение New Scientist)
Учёные ожидали увидеть, что вода во всех случаях образует тонкую трубчатую структуру. Однако, модель показала, что при диаметре трубки в 1,35 нм и давлении в 40000 атмосфер водородные связи искривились, приведя к образованию спирали с двойной стенкой. Внутренняя стенка этой структуры является скрученной в четверо спиралью, а внешняя состоит из четырёх двойных спиралей, похожих на структуру молекулы ДНК.
Последний факт накладывает отпечаток не только на эволюцию наших представлений о воде, но и эволюцию ранней жизни и самой молекулы ДНК. Если предположить, что в эпоху зарождения жизни криолитные глинистые породы имели форму нанотрубок, возникает вопрос – не могла ли вода, сорбированная в них служить структурной основой (матрицей) для синтеза ДНК и считывания информации? Возможно, поэтому спиральная структура ДНК повторяет спиральную структуру воды в нанотрубках. Как сообщает журнал New Scientist, теперь нашим зарубежным коллегам предстоит подтвердить существование таких макромолекул воды в реальных экспериментальных условиях с использованием инфракрасной спектроскопии и спектроскопии нейтронного рассеяния.