COVID-19: какие мифы могут навредить вашему здоровью?
Чем дальше распространяется инфекция, тем больше в интернете слухов о невероятных способах заражения и еще более неожиданных способах лечения и профилактики. Так, некоторые россияне считают, что коронавирус переносят бананы, а защититься от инфекции можно с помощью щелочных растворов или промывая нос солевым раствором. Роскачество собрало главные опасения и попросило эксперта их прокомментировать.
Содержание
Опасение 1: Правда ли, что если у меня насморк и мокрота при простуде, то я не могу быть носителем коронавирусной инфекции? Коронавирус – это сухой кашель без насморка?
– Действительно, сухой кашель или кашель с небольшим количеством мокроты отмечен в 80% случаев при COVID-19. Это один из клинических симптомов острой респираторной вирусной инфекции наряду с повышением температуры тела, одышкой, утомляемостью.
– Это не совсем так. При чихании, кашле, разговоре вокруг больного образуется «зараженная зона» из слюны, слизи, мокроты с высокой концентрацией возбудителя. Крупные капли такого аэрозоля рассеиваются на расстоянии до 2–3 метров и оседают довольно быстро на различные поверхности. Частицы аэрозоля меньшего размера могут довольно долго находиться во взвешенном состоянии благодаря малейшим движениям воздуха. Естественно, что в помещениях это создает бóльшую угрозу, чем на свежем воздухе. Отсюда и рекомендации находиться на расстоянии друг от друга, использовать средства индивидуальной защиты. Конечно, вирусы и гриппа, и коронавируса во внешней среде не особо устойчивы. Но какое-то время они могут сохранять жизнеспособность не только на холоде, но и при комнатной температуре, а вот на солнце, от воздействия ультрафиолета, они погибают быстрее.
Как защитить себя от вируса в магазине и при заказе еды на дом, читайте здесь.
Опасение 3: Правда ли, что инкубационный период длится 28 дней?
– Такое действительно может быть, но это не правило, а скорее исключение из него. Обычно инкубационный период занимает от 2 до 14 дней, а в среднем 5–7 суток.
Опасение 4: Говорят, что коронавирус схож с ВИЧ. Это правда?
– Нет, это не так. В конце 2002 года появился коронавирус SARS-CoV, а в 2012 году мир столкнулся с новым коронавирусом – MERS (MERS-CoV) – при поиске препаратов для лечения положительный эффект был обнаружен при использовании лекарств для терапии ВИЧ-инфекции. Но это не делает вирусы схожими. Подобные слухи идут от научной публикации, в которой неверно интерпретировали полученный результат. Публикация почти сразу была отозвана.
В сложившихся условиях, когда новый вирус стал экстренно изучаться в различных лабораториях мира, научные публикации часто стали выкладываться нерецензированными, то есть не прошедшими проверку другими специалистами из определенной области. Из-за этого в статьях остается много неточных и ошибочных результатов. По сообщению ТАСС, расчеты молекулярных биологов из Мичиганского университета показали, что SARS-CoV-2 в принципе не мог «унаследовать» участки РНК от любых других вирусов, в том числе и ВИЧ.
Опасение 6: Правда ли, что в коронавирусе содержится 50 штаммов гриппа?
– Это продолжение теории об искусственно выведенном вирусе, и оно не имеет ничего общего с действительностью. Грипп и коронавирус – разные инфекции, и их вызывают разные вирусы.
Опасение 7: Есть версия, что бананы могут быть заражены коронавирусом.
– Такая байка бродила в мессенджерах, но это неправда.
Опасение 8: В интернете пишут, что раствор соды или разведенный в воде лимонный сок можно использовать в качестве профилактических средств от коронавируса. Нужно просто пить эти растворы небольшими порциями 3–4 раза в день. Неужели это так?
– В интернет просочилась очередная псевдопамятка о том, что рН вируса – от 5,5 до 8,5, и одни «эксперты» для нейтрализации вируса предлагают пить щелочные растворы, а другие – кислотные.
Это очередной информационный вброс, взятый с потолка. SARS-CoV-2 устойчив в широком диапазоне кислотности (3–10 pH). Это значит, что на него не подействуют ни кислоты, ни щелочи. Пить содовые растворы, лимонные напитки для защиты от коронавируса – бесполезно.
pH – показатель кислотно-щелочного баланса. Показатель pH меньше 7 относится к кислоте, больше – к щелочи. Сам коэффициент 7 означает нейтральный pH, к нему относится вода.
Опасение 9: Правда ли, что обработка поверхности всего тела этанолом или хлорсодержащими средствами позволяет уничтожить коронавирус?
– Странное и даже опасное для здоровья предложение. Для обработки рук лучше использовать гигиенические, в том числе спиртовые, салфетки. И это если нет возможности помыть руки водой с мылом. Семидесятипроцентный этанол можно использовать как средство дезинфекции. А применение хлорсодержащих веществ для обработки тела просто недопустимо!
Чем можно заменить антисептики. Читайте здесь.
Опасение 10: В интернете есть совет, что настойка мухомора может вылечить от коронавирусной инфекции.
– Нет, конечно, это довольно странная рекомендация. Единственно оправданные меры профилактики всем хорошо известны: личная гигиена (мыть руки, не трогать лицо и так далее), должное санитарное состояние помещений, социальный этикет. По части лекарств ВОЗ сообщает, что медикаментов для лечения и профилактики в настоящий момент нет.
«Инфицированным пациентам должна быть оказана необходимая медицинская помощь для облегчения и снятия симптомов, а лицам с тяжелыми формами заболевания должна обеспечиваться надлежащая поддерживающая терапия. В настоящее время идет работа по созданию специфических лекарственных средств против нового коронавируса, и им предстоит пройти клинические испытания. ВОЗ совместно с рядом партнеров оказывает помощь в целях ускорения работы по созданию новых лекарственных средств», – сообщается на сайте организации.
Недавно в ФМБА России представили препарат для лечения COVID-19. Кроме того, даны подробные рекомендации по лечению этой инфекции Минздравом России с указанием эффективных на данный момент методов и препаратов. Пока что среди них названы препараты Лопинавир/Ритонавир, рекомбинантный интерферон бета-1b, рекомбинантный интерферон альфа, Тоцилизумаб, Хлорохин, Гидроксихлорохин.
Опасение 11: Мама говорит, что, если регулярно промывать нос солевым раствором, это может защитить от заражения. Она права?
– Нет. Научных данных о том, что регулярное промывание носа солевым раствором позволяет защитить от новой коронавирусной инфекции, нет.
По некоторым данным, регулярное промывание носа солевым раствором может ускорить выздоровление при обычной простуде. Однако доказательства эффективности регулярного промывания носа как средства профилактики респираторных инфекций отсутствуют. В памятке Минздрава говорится, что элиминационная терапия, представляющая собой орошение слизистой оболочки полости носа изотоническим раствором хлорида натрия (то есть солевым раствором), обеспечивает снижение числа как вирусных, так и бактериальных возбудителей инфекционных заболеваний и может быть рекомендована для неспецифической профилактики.
Лучше всего, чтобы слизистая носа просто была здорова и увлажнена, в крайнем случае ее можно закрыть маской. Да, обычная медицинская маска не всесильна, но крупные капельки, которые разлетаются в воздухе от чихнувшего человека, она хоть как-то задержать может. По предварительным данным, массовое применение масок в Сингапуре и Гонконге минимизировало распространение инфекции.
В рекомендациях Минздрава также упоминается возможность использовать специальные лор-средства, например на основе целлюлозы, которые, распыляясь, образуют на слизистой тонкую пленку. Полоскать горло мирамистином и хлоргексидином не нужно.
Опасение 12: Правда ли, что для профилактики и лечения коронавирусной инфекции нужны антибиотики?
– Нет, антибиотики против вирусов не действуют. Они позволяют лечить только бактериальные инфекции. Тем не менее пациентам, госпитализированным с COVID-19, могут назначаться антибиотики для лечения сопутствующих бактериальных инфекций.
Следите за новостями, подписывайтесь на рассылку.
При цитировании данного материала активная ссылка на источник обязательна.
При какой температуре умирают кокки
Стрептококковые инфекции – группа заболеваний, включающая инфекции, вызываемые стрептококковой флорой разных видов и проявляющихся в виде поражения дыхательных путей и кожных покровов. К стрептококковым инфекциям относят стрептококковое импетиго, стрептодермию, стрептококковый васкулит, ревматизм, гломерулонефрит, рожу, ангину, скарлатину и другие заболевания. Стрептококковые инфекции опасны склонностью к развитию постинфекционных осложнений со стороны различных органов и систем. Поэтому диагностика включает не только выявление возбудителя, но и инструментальное обследование сердечно-сосудистой, дыхательной и мочевыделительной систем.
Характеристика возбудителя
Клинические формы стрептококковой инфекции
Симптоматика стрептококковых инфекций крайне многообразны ввиду большого количества вероятных локализаций очага инфекции, видов возбудителя. Кроме того, интенсивность клинических проявлений зависит от общего состояния организма инфицированного. Стрептококки группы А склонны к поражению верхних дыхательных путей, слухового аппарата, кожи (стрептодермия), к этой группе относятся возбудители скарлатины и рожи.
Заболевания, развившиеся в результате поражения этими микроорганизмами, можно разделить на первичные и вторичные формы. Первичные формы представляют сбой воспалительные инфекционные заболевания органов, ставших воротами инфекции (фарингит, ларингит, ангина, отит, импетиго и т. д.). Вторичные формы развиваются в результате включения аутоиммунных и токсико-септических механизмов развития воспаления в различных органах и системах. К вторичным формам стрептококковых инфекций с аутоиммунным механизмом развития относятся ревматизм, гломерулонефрит и стрептококковый васкулит. Токсино-инфекционный характер носят некротические поражения мягких тканей, мета- и перитонзиллярный абсцессы, стрептококковый сепсис.
Редкие клинические формы стрептококковых инфекций: некротическое воспаление мышц и фасций, энтерит, синдром токсического шока, очаговые инфекционные поражения органов и тканей (например, абсцесс мягких тканей). Стрептококки группы В в подавляющем большинстве вызывают инфекции у новорожденных, хотя встречаются в любом возрасте. Это связано с преимущественным поражением данным возбудителем мочеполовых путей и заражением новорожденных интранатально.
Стрептококковые инфекции группы В нередко являются причиной послеродовых эндометритов, циститов, аднекситов у родильниц и осложнений в послеоперационном периоде при проведении кесарева сечения. Стрептококковая бактериемия кроме того может отмечаться у лиц с выраженным ослаблением иммунных свойств организма (пожилые люди, больные сахарным диабетом, синдромом иммунодефицита, злокачественными новообразованиями). Нередко на фоне протекающей ОРВИ развивается стрептококковая пневмония. Зеленящий стрептококк может быть причиной развития эндокардитов и последующих клапанных дефектов. Стрептококки группы mutans вызывают кариес.
Осложнения стрептококковых инфекций – это аутоиммунные и токсикосептические вторичные поражения органов и систем (ревматизм, гломерулонефрит, некротические миозиты и фасциты, сепсис и т. д.).
Диагностика стрептококковых инфекций
Этиологическая диагностика стрептококковой инфекции слизистой оболочки глотки и кожных покровов требует бактериологического исследования с выделением и идентификацией возбудителя. Исключением можно считать скарлатину. Поскольку в настоящее время многие виды стрептококковых бактерий приобрели определенную устойчивость к антибиотикам некоторых групп, необходимо тщательное микробиологическое исследование и осуществления теста на чувствительность к антибиотикам. Диагностика, произведенная в достаточном объеме, способствует выбору эффективной тактики лечения.
Экспресс-диагностика стрептококков группы А позволяют установить возбудителя в течение 15-20 минут с момента взятия анализа без выделения чистой культуры. Однако выявление присутствия стрептококков не всегда означает, что именно они являются этиологическим фактором патологического процесса, этот факт может говорить и об обычном носительстве. Ревматизм и гломерулонефрит практически всегда характеризуются повышением титра антител к стрептококкам уже с первые дни обострения. Титр антител к внеклеточным антигенам определяют с помощью реакции нейтрализации. При необходимости проводится обследование пораженных стрептококковой инфекцией органов: осмотр отоларинголога, рентгенография легких, УЗИ мочевого пузыря, ЭКГ и др.
Лечение стрептококковых инфекций
В зависимости от формы стрептококковой инфекции лечение проводит гинеколог, уролог, дерматолог, пульмонолог или другие специалисты. Патогенетическое и симптоматическое лечение зависит от клинической формы заболевания.
Профилактика стрептококковых инфекций
Профилактика заражения стрептококковой инфекцией:
Ангина
Ангина – группа острых инфекционных заболеваний, которые сопровождаются воспалением одной или нескольких миндалин глоточного кольца. Как правило, поражаются нёбные миндалины. Реже воспаление развивается в носоглоточной, гортанной или язычной миндалинах. Возбудители болезни проникают в ткань миндалин извне (экзогенное инфицирование) или изнутри (эндогенное инфицирование). От человека человеку ангина передается воздушно-капельным или алиментарным (пищевым) путем. При эндогенном инфицировании микробы попадают в миндалины из кариозных зубов, придаточных пазух (при синуситах) или носовой полости. При ослаблении иммунитета ангина может вызываться бактериями и вирусами, которые постоянно присутствуют на слизистой рта и глотки.


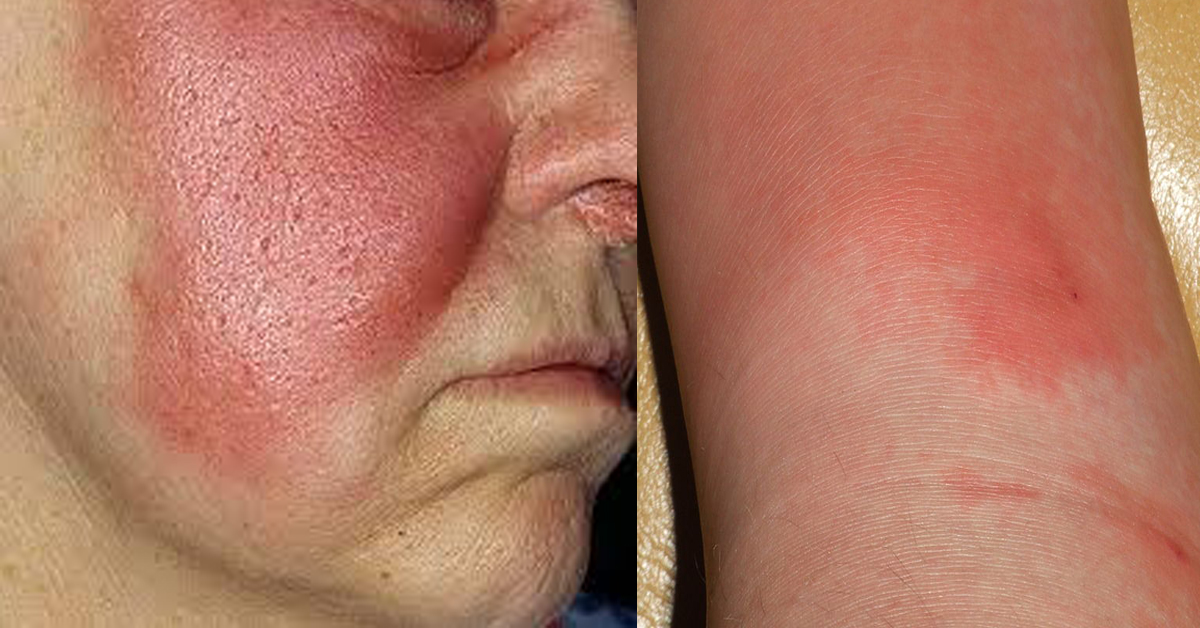
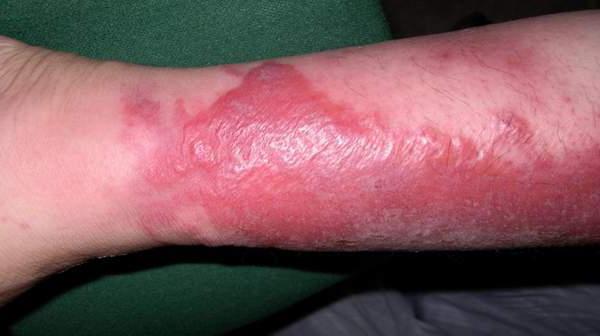
Рожа (рожистое воспаление) представляет собой инфекционное заболевание, вызываемое стрептококком группы А, преимущественно поражающее кожные покровы и слизистые оболочки, характеризующееся возникновением ограниченного серозного или серозно-геморрагического воспаления, сопровождающегося лихорадкой и общей интоксикацией. Рожа входит в число самых распространенных бактериальных инфекций. Характеристика возбудителя
Copyright © 2013-2021, ОГБУЗ «Поликлиника №4 »
Все права защищены
Политика конфиденциальности
Карта сайта
214025, г. Смоленск,
ул. Нормандия-Неман, 37
Стрептококки: чем опасны, как выявлять и лечить
Род бактерий, относящихся к условно патогенной микрофлоре. Носителями различных стрептококков являются практически все люди, включая младенцев. В норме активность микробов подавляет иммунитет. При ослаблении его защиты или получении извне большой заражающей дозы развиваются стрептококковые инфекции: воспалительные заболевания, поражающие слизистые дыхательных путей, ткани внутренних органов, зубы или оболочки мозга. Стрептококки очень устойчивы к факторам внешней среды, способны вырабатывать резистентность к антибактериальным препаратам.
Что такое стрептококки
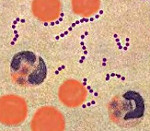
Род Streptococcus объединяет разнообразные грамположительные микроорганизмы, способные размножаться в анаэробных условиях. Бактерии имеют шаровидную форму, их оболочки чрезвычайно устойчивы к агрессии внешней среды. В высушенных образцах биологических материалов стрептококки сохраняются жизнеспособными более года. Погибают при кипячении, химические дезинфицирующие препараты убивают их в течение 20 минут. По этой причине поверхностного антисептирования часто бывает недостаточно.
Источник распространения стрептококков — носители: зараженные или больные люди. В большой концентрации инфекция содержится на поверхности слизистых оболочек, в жидкостных выделениях: гное, экссудате, слюне. Микробы передаются от человека к человеку воздушно-капельным путем при чихании или кашле. В отличие от вирусов стрептококки разлетаются на относительно небольшое расстояние от источника: в радиусе не более трех метров. Высокая устойчивость бактерий во внешней среде определяет также алиментарный путь заражения: через грязные руки, продукты питания. Стрептококки длительное время сохраняются в молоке, мясных и морепродуктах, которые являются для этой группы инфекций питательную среду.
При размножении в организме человека стрептококки провоцируют интенсивные воспалительные реакции:
микробы группы А чаще поражают слизистые носа, ротовой полости, гортани, бронхов и легких, слухового аппарата, кожи, становятся возбудителями синуситов, тонзиллита, кариеса, ангины, пневмонии, дерматитов, рожи, скарлатины, осложнения ран и ожогов;
стрептококки группы В обычно провоцируют воспаления тканей мочевыделительной системы, суставных структур, соединительной ткани, вызывают цистит, адрекситы, инфекционные нефриты, ревматические процессы, послеродовые осложнения у женщин, эти микробы могут передаваться при половых контактах.
Развитию стрептококковых инфекций способствуют различные системные патологии и повреждения тканей. В том числе: сахарный диабет, злокачественные опухоли, иммунодефицитные, послеоперационные состояния, гиповитаминозы, открытые раны.
Признаки инфицирования
Распространенные симптомы стрептококковых инфекций:
повышение местной или общей температуры тела;
зуд, жжение, сухость в области гортани;
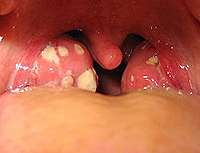
отечность и покраснение миндалин, образование желтого или сероватого налета на слизистых;
заложенность носа с последующими густыми выделениями зеленоватого или желтого цвета;
резкая боль и заложенность слухового прохода, серозные выделения с примесью гноя.
У большинства людей природная высокая склонность к заражению стрептококками. При передаче того или иного вида инфекции воспаляются так называемые входные ворота. Возникают ларингит, фарингит, ангина, отит. При распространении микробов из очагов заражения страдают нижние дыхательные пути, мозг, почки, кишечник и другие органы. К инфекциям вторичной формы можно отнести процессы с включением аутоиммунных механизмов: ревматоидный артрит, стрептококковый васкулит, гломерулонефрит.
Стрептококки — частые провокаторы токсических и некротических осложнений, в том числе тяжелой лихорадки, абсцессов и сепсиса.
Диагностика и лечение стрептококковых инфекций
Специфическая диагностика патогенов требует проведения бактериологического анализа соскобов слизистых, образцов слюны, мочи, мокроты, гнойного отделяемого и других биоматериалов. Кроме того, часто бывает необходимо тестирование крови на антитела к стрептококкам. Лабораторные исследования устанавливают вид возбудителя болезни в течение 20–30 минут.
Кроме этиологических анализов при различных патологиях требуется диагностика общего состояния поражениях органов: обследование у отоларинголога, проведение УЗИ, флюорографии и некоторых других.
Тактику лечения подбирают с учетом выявленных нарушений и устойчивости микробов к медикаментам. Терапию проводят врачи различных профилей: гинекологи, терапевты, пульмонологи, дерматологи. Для подавления активности инфекционной микрофлоры больным назначают курс антибиотиков. Против стрептококков эффективны Азитромицин, Эритромицин,препараты из ряда фторхинолонов: Ципрофлоксацин, Левофлоксацин. Покупать и применять медикаменты важно по назначению врача. Самодеятельность в этом вопросе приводит к развитию суперинфекций. Терапию дополняют также иммуномодулирующими средствами.
Предотвратить развитие стрептококковых заболеваний помогают санитарные меры, закаливание, использование антисептических средств.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Авторизуйтесьчтобы оставлять комментарии
Возрастные ограничения 18+
Лицензия на осуществление фармацевтической деятельности ЛО-77-02-011246 от 17.11.2020 Скачать.
УРОГЕНИТАЛЬНЫЙ ТРИХОМОНИАЗ
В России по-прежнему наблюдается неблагоприятная эпидемиологическая ситуация в отношении инфекций, передаваемых половым путем (ИППП). По данным экспертов Европейского регионального бюро ВОЗ, такое же положение сохраняется во всех новых независимых госуда
В России по-прежнему наблюдается неблагоприятная эпидемиологическая ситуация в отношении инфекций, передаваемых половым путем (ИППП). По данным экспертов Европейского регионального бюро ВОЗ, такое же положение сохраняется во всех новых независимых государствах Восточной Европы. Как и прежде, наибольший удельный вес в структуре всех ИППП занимает трихомониаз (24,7%). Ежегодно в мире заболевают 170 млн человек, при этом распространенность трихомониаза среди сексуально активных женщин достигает 30—50%. Почти одна треть всех визитов к врачу по поводу инфекционного вульвовагинита обусловлена инфицированием трихомонадами. Заболевание встречается повсеместно и с одинаковой частотой возникает у мужчин и женщин. Важность проблемы состоит в том, что наибольшую опасность представляют посттрихомонадные осложнения. Трихомонадная инфекция может служить причиной не только бесплодия, но и различных патологий беременности, родов, послеродового периода, новорожденного, а также детской смертности.
Возбудитель заболевания — Trichomonas vaginalis — микроорганизм, относящийся к отряду паразитических простейших (Protozoa), классу жгутиконосцев (Flagellata Mastigophora), семейству Trichomonadidae, для представителей которого характерно наличие четырех свободных жгутиков и ундулирующей мембраны. Возбудитель трихомониаза был открыт Donne в 1936 г., и некоторое время его ошибочно считали безвредным сапрофитом. Однако влагалищная трихомонада — типичный паразит (свободноживущие формы не обнаружены), представляет собой подвижный одноклеточный организм, приспособившийся в процессе эволюции к жизни в органах мочеполовой системы человека. Влагалищная трихомонада имеет овальную, грушевидную или округлую форму, которая может изменяться в зависимости от условий существования и проводимой терапии, что затрудняет микроскопическую диагностику мочеполового трихомониаза. Размножение ее происходит путем простого поперечного деления, а оптимальным условием развития трихомонад является рН среды 5,5-6,5.
В настоящее время известны более 50 разновидностей трихомонад, различающих по величине, форме клетки, числу жгутиков и т. д. У человека паразитируют только три вида трихомонад: урогенитальные (Tr.vaginalis), ротовые (Tr.tenax) и кишечные (Tr.intestinalis).
Все трихомонады обладают фагоцитарными свойствами, часто с неполным переваривающим циклом. В отдельных случаях трихомонады могут фагоцитировать целые клетки или их фрагменты. В фагосомах обнаруживаются кокки, диплококки, бациллярные формы как грамположительных, так и грамотрицательных микроорганизмов. Объектом фагоцитоза могут быть гонококки. Часто встречается незавершенный фагоцитоз, в результате чего живые клетки выходят из фагосом и продолжают вегетировать и вызывать рецидивы гонореи после ее излечения. Нередко гонококки выявляют в мазках только после излечения мочеполового трихомониаза (Н. М. Овчинников и др., 1987). Обнаруженные явления эндоцитобиоза позволяют рассматривать влагалищную трихомонаду как резерв сохранения гонококковой инфекции.
Большое практическое значение имеет изучение устойчивости влагалищных трихомонад к некоторым условиям внешней среды, действию антисептиков и т. д. Существовавшее ранее мнение, что трихомонады чрезвычайно устойчивы во внешней среде, особенно в воде водоемов, в настоящее время не подтверждается. Влагалищные трихомонады быстро погибают при температуре 45—50°С, а при 60°С гибнут моментально. Они более устойчивы к низким температурам: при замораживании и температуре –10°С Tr.vaginalis остаются жизнеспособными до 45 мин. Влагалищные трихомонады очень чувствительны к изменению осмотического давления и в пресной воде различных водоемов погибают в течение 15—60 мин. Трихомонады плохо переносят высыхание, но во влажной среде могут довольно долго сохранять жизнеспособность, особенно на хлопчатобумажных тканях и губках. Малая устойчивость урогенитальных трихомонад в окружающей среде, вероятно, связана с невозможностью образовывать цисты, что резко ограничивает возможность заражения при непрямом контакте. На гинекологических зеркалах и резиновых перчатках, использованных при обследовании больных, трихомонады могут сохраняться в течение 3—45 мин. Моментально убивают трихомонады антисептические средства, хозяйственное мыло.
В свете современных представлений о урогенитальном трихомониазе возможность инфицирования при купании в водоемах и пользовании баней кажется маловероятной. Заражение происходит, как правило, половым путем и крайне редко — путем непрямого контакта через инфицированное белье, предметы туалета и др. Половой путь заражения как мужчин, так и женщин является не только основным, но и практически единственным. Заражение девушек при сохраненной девственной плеве также чаще возможно при попытке к коитусу или вестибулярном коитусе, что удается установить у большинства из них при тщательном и целенаправленном сборе анамнеза. Изредка встречается контактный путь передачи через перчатки, подкладные клеенки и судна, ночные горшки, сиденья в уборных и др. Возбудитель сохраняет жизнеспособность в течение 24 ч в моче, сперме, а также в воде и может выживать в течение нескольких часов во влажном чистом белье. В редких случаях возможно заражение маленьких девочек внеполовым путем от больных матерей при несоблюдении элементарных правил гигиены. В литературе имеются сообщения о случаях инфицирования новорожденных девочек при прохождении через родовые пути больной матери.
Для урогенитального трихомониаза характерна многоочаговость, при этом поражаются не только влагалище, но и шейка матки, уретра, парауретральные ходы, описаны случаи трихомонадного уретрита и сальпингита. Имеются данные, что трихомонады, как и сперматозоиды, приводят к бактериальному инфицированию внутренних половых органов: стафилококки, стрептококки, гонококки, кишечные палочки и другие микроорганизмы прикрепляются к трихомонадам и проникают вместе с ними за внутренний маточный зев.
Попадая на слизистые оболочки урогенитального тракта, трихомонады могут вызывать развитие воспалительного процесса. Как правило, появление воспалительных изменений слизистой влагалища, сопровождающееся резким увеличением количества полиморфно-ядерных нейтрофилов, связано с наличием трихомонад, которые при прямом клеточном контакте, а также в результате цитотоксического действия разрушают эпителиальные клетки. Выделяемая трихомонадами гиалуронидаза приводит к значительному разрыхлению тканей и более свободному проникновению в межклеточное пространство токсических продуктов метаболизма. Изменения слизистой оболочки влагалища при трихомониазе неспецифичны и мало чем отличаются от обычного воспалительного процесса. Отмечены дистрофические и пролиферативные изменения многослойного плоского эпителия и слущивание поверхностных эпителиальных клеток, а также уменьшение в них содержания гликогена. Таким образом, местом внедрения трихомонад у женщин является слизистая влагалища. Затем постепенно они попадают в уретру, парауретральные ходы и цервикальный канал. Возникают вульвиты, вестибулиты, бартолиниты, эндоцервициты, уретриты. При проникновении трихомонад в маточные трубы развивается трихомонадный сальпингит. Могут иметь место и тубоовариальные образования.
Инкубационный период урогенитального трихомониаза в среднем составляет 10 дней, но иногда он варьирует от двух-трех дней до одного месяца и более. Симптоматика трихомонадных вульвовагинитов разнообразна. Существуют различные клинические классификации мочеполового трихомониаза. В зависимости от длительности заболевания и интенсивности реакции организма на внедрение возбудителя, различают следующие формы трихомониаза:
По характеру влагалищного мазка выделяют свежий трихомониаз, когда в мазке много трихомонад, мало эпителиальных клеток и молочно-кислых палочек; расцвет заболевания, когда в мазке много трихомонад, лейкоцитов, посторонней флоры, отсутствуют молочно-кислые палочки, мало эпителиальных клеток; хронический трихомониаз, когда гнойно-пенистые выделения с пузырьками СО2 сменяются беловатыми выделениями, во влагалищном мазке уровень трихомонад то повышен, то понижен, лейкоцитов мало, эпителиальных клеток, напротив, много, молочно-кислых палочек нет. При скрытом же трихомониазе трихомонад мало, а эпителий и молочно-кислые палочки не определяются вовсе.
Клинический синдром трихомониаза известен уже много лет, а особенно четко он был описан Флеури. Трихомонадный вульвовагинит характеризуется обильными разъедающими пенистыми выделениями из половых путей, сопровождающимися сильным, порой нестерпимым зудом. Жалобы появляются вскоре после начала половой жизни или случайной половой связи.
При осмотре выявляют воспалительные изменения: от умеренной гиперемии слизистой оболочки влагалища и шейки матки до обширных эрозий, петехиальных геморрагий и опрелости в области промежности. Характерный, но не постоянный симптом — это наличие гранулематозных, рыхлых поражений слизистой оболочки шейки матки красного цвета (малиновая шейка матки). В области заднего свода отмечается скопление жидких серовато-желтых, пенистых выделений, которые свободно вытекают из влагалища и раздражают кожу.
При кольпоскопии на слизистой оболочке влагалища и влагалищной части шейки матки обнаруживают точечные кровоизлияния (симптом клубничной шейки). Очаги воспаления при окраске раствором Люголя йоднегативны.
Острые воспалительные явления могут постепенно стихать произвольно или под влиянием неспецифического лечения, и трихомонадный вульвовагинит переходит в подострую, а затем и хроническую стадию, при которой меняется характер выделения из половых путей. Они становятся желтоватыми или белыми, количество их уменьшается. Гиперемия слизистой оболочки влагалища выражена незначительно или вообще отсутствует. Часто наблюдается малосимптомная или асимптомная форма заболевания, при которых субъективные ощущения у больных отсутствуют. Хронический трихомонадный вульвовагинит течет волнообразно, обострения чередуются с ремиссиями. При переходе из острого процесса в хронический больные женщины жалуются на бели и неприятные ощущения во влагалище перед и после менструации.
Трихомонадный эндоцервицит сопровождается отечностью шейки матки, обильными выделениями из цервикального канала и мало чем отличается от клинической картины эндоцервицита гонорейной этиологии.
При вовлечении в воспалительный процесс уретры ее губки отечны и гиперемированы, при массаже можно выдавить небольшое количество гнойных выделений. При пальпации уретры отмечается ее болезненность и пастозность. Трихомонады могут проникать также в мочевой пузырь, почечные лоханки и вызывать поражения мочевыводящих путей, клинически проявляющиеся циститом и пиелонефритом.
При морфологическом исследовании биоптированной ткани в слизистой оболочке влагалища и шейки матки наблюдаются воспалительные изменения различной интенсивности и выраженная васкуляризация в подэпителиальной ткани. В многослойном плоском эпителии отмечаются дистрофические изменения, наиболее выраженные в поверхностных отделах и свидетельствующие о непосредственном воздействии трихомонад на эпителиальные клетки. В связи с воспалительными явлениями эпителиальные клетки приобретают различную величину, появляются клетки с увеличенным ядром, двухъядерные клеточные элементы, выраженный отек клеток многослойного плоского эпителия. Подобные изменения клеток плоского эпителия сохраняются и в цитологических препаратах, которые характеризуются также очаговыми скоплениями лейкоцитов в виде «пушечного ядра» на поверхности клеток плоского эпителия. В связи с наличием воспалительного процесса во влагалище всегда возникают трудности при анализе цитологической картины мазков и требуется проведение повторных исследований после ликвидации воспаления.
Трихомонадная инфекция не приводит к развитию выраженного иммунитета. Выявляемые у больных или переболевших трихомониазом сывороточные или секреторные антитела — лишь признаки существующей или ранее перенесенной инфекции, но они не могут обеспечить иммунитет. Обнаруживаются они в течение года после перенесенного заболевания. Поэтому на основании их определения нельзя судить о том, наступило выздоровление или нет.
Симптомы и клинические проявления заболевания не достаточно специфичны, в связи с чем только на основании этих данных не всегда удается поставить точный диагноз.
Диагноз урогенитального трихомониаза устанавливают на основании клинических признаков заболевания и обнаруживаемых в исследуемом материале трихомонад.
Материал для исследования у женщин берут специальным образом из влагалища, уретры, прямой кишки, у мужчин и из мочеиспускательного канала, а также прямой кишки.
Для лабораторной диагностики трихомониаза наиболее широко применяют следующие методы: микроскопия нативных препаратов; микроскопия мазков, окрашенных по Граму (или другими красителями); культуральная (бактериологическая) диагностика на жидких питательных средах. Относительной информативностью обладают иммунологический метод и метод латекс-агглютинации.
РН влагалища при трихомонадном вульвовагините 4,5-5,5. В нативных препаратах возбудитель обнаруживается по его движению среди клеточных элементов и микроорганизмов. Обнаруживаемые трихомонады по размеру в два раза больше лейкоцитов. Преимуществом микроскопии окрашенных препаратов является возможность их исследования спустя длительное время после взятия материала. Информативность этого метода выше, так как он позволяет определять как подвижные, так и неподвижные формы. Культуральный метод имеет большую ценность при распознавании атипичных форм с целью диагностики трихомониаза и контроля за результатами лечения. Предложенные иммунологические методы (РСК, РИФ, РПГА) не могут быть использованы в качестве основного диагностического теста, так как у части больных выявляется ложноположительные и ложноотрицательные результаты. В некоторых случаях эти методы могут применяться в качестве отборочного теста. Метод латекс-агглютинации выявляет растворимые антигены в концентрации 50 нг/мл и полезен для диагностики хронического трихомониаза и трихомонадоносительства. Однако ни один из вышеперечисленных методов не гарантирует абсолютного выявления трихомонад. Все названные методы диагностики дополняют друг друга.
На сегодняшний день предложено большое количество методов лечения урогенитального трихомониаза. Многие из них имеют только историческое значение и практически не применяются. Современные методы лечения больных трихомониазом основаны на использовании специфических противотрихомонадных препаратов. При этом необходимо соблюдать следующие принципы:
Антибиотики и сульфаниламидные препараты не дают терапевтического эффекта и показаны лишь при наличии смешанной инфекции.
Одним из наиболее распространенных препаратов общего действия при трихомониазе является метронидазол. Полагают, что механизм его действия связан с нарушением структуры ДНК чувствительных микроорганизмов. Метронидазол действует не только на простейших, но и на анаэробную флору.
К метронидазолу устойчивы аэробные микроорганизмы. Кроме того, метронидазол может индуцировать выработку интерферона.
Существуют несколько методик лечения метронидазолом. С целью уменьшения вероятности возможной резистентности трихомонад к метронидазолу рекомендуют следующие схемы лечения метронидазолом:
В последнее время стали появляться сообщения о неэффективности лечения трихомониаза из-за развития резистентности урогенитальных трихомонад к стандартным дозам метронидазола. Неудачи лечения скорее всего обусловлены низкой концентрацией препарата в очагах инфекции, нерегулярным приемом лекарственного средства и низкой его дозировкой. При торпидном и хроническом процессе вследствие нарушений васкуляризации и последующего развития рубцовой ткани в пораженных органах изменяется морфологическая структура слизистой влагалища и снижается концентрация протистоцидных препаратов в очагах поражения. Этой концентрации препарата недостаточно для подавления паразита, что, в свою очередь, приводит к лекарственной устойчивости.
В настоящее время кроме метронидазола применяют ряд других производных нитроимидазола — тинидазол, орнидазол, ниморазол, тенонитрозол.
Лидирующее место среди препаратов данной группы в настоящий момент занимает тиберал (орнидазол). Полагают, что механизм действия связан с нарушением структуры ДНК чувствительных микроорганизмов. Тиберал эффективен в отношении Trichomonas vaginalis, Entamoeba histolytica, Giardia lamlia (Giardia intestinalis), а также анаэробных бактерий, таких, как Bacteroides, Clostridium spp. и анаэробных кокков. После перорального приема орнидазол быстро и почти полностью всасывается. Максимальная концентрация в плазме достигается в течение 3 ч. Связывание тиберала с белками составляет около 13%. Активное вещество очень хорошо проникает в жидкости и ткани организма. Период полувыведения составляет около 13 ч, в связи с чем достаточно двукратного приема препарата — утром и вечером. После однократного приема 85% дозы препарат выводится в течение первых пяти дней, что в ряде случаев, при подозрении на заражение, дает возможность проводить срочную профилактику трихомониаза. Выведение происходит, главным образом, с мочой (63%) и калом (22%), что повышает результативность лечения тибералом циститов, уретритов и проктитов. Назначение орнидазола на раннем сроке беременности и кормящим матерям возможно, однако только по абсолютным показаниям. В отличие от других производных нитроимидазола, тиберал не ингибирует альдегиддегидрогеназу и поэтому совместим с алкоголем. В целом, тиберал хорошо переносится, однако противопоказан больным с поражением ЦНС (так как легко проникает в спинно-мозговую жидкость) или при повышенной чувствительности к препарату в анамнезе. Для лечения трихомониаза рекомендуется орнидазол (тиберал) по одной таблетке два раза в день после еды в течение пяти дней обоим партнерам. Клиническая и бактериологическая эффективность терапии у женщин и мужчин составляет 97% при контрольных исследованиях, проведенных бактериологическими, культуральными и генетическими методами. Клинические проявления в виде жалоб на пенистые выделения и зуд исчезают в течение трех дней лечения орнидазолом у 100% пациенток.
Производные нитроимидазола хотя и очень эффективны при лечении острой фазы трихомониаза, однако они не благоприятствуют долговременной нормализации среды влагалища. Этого можно добиться при помощи вакцинации солкоТриховаком. Данный иммунотерапевтический препарат способствует колонизации лактобацилл и стабилизации рН, создавая тем самым неподходящие условия для размножения T.vaginalis и обеспечивая отсутствие рецидивов. СолкоТриховак — это вакцина, приготовленная из аномальных штаммов лактобацилл, которые обнаруживаются во влагалищном секрете больных трихомониазом женщин. Антитела, индуцированные вакциной, действуют непосредственно против T.vaginalis, благодаря перекрестной антигенной реакции. СолкоТриховак способствует восстановлению нормальной лактофлоры во влагалище и нормализации влагалищного рН. Основная вакцинация — три инъекции по 0,5 мл внутримышечно с интервалом две недели — обеспечивает годичную защиту. Через год проводится повторная ревакцинация — однократно 0,5 мл. После трех инъекций препарата стабилизируется нормальная влагалищная флора, повышается иммунитет, вследствие чего трихомонады и другие патогенные возбудители вытесняются и исчезают.
В последние годы отмечена устойчивость T.vaginalis при использовании стандартных доз метронидазола, лечение нередко бывает более успешным при использовании больших доз метронидазола местно. Сейчас существуют несколько форм метронидазола, применяемых местно (например, метрогил вагинальный гель, метронидазол крем, клион-Д 100 вагинальные таблетки). Метронидазол обладает высокой активностью в отношении анаэробных бактерий (бактероиды, фузобактерии, клостридии, анаэробные кокки) и простейших (Trichomonas vaginalis, Entamoeba histolytica, лямблии). Активен против большинства штаммов микроорганизмов, вызывающих бактериальный вагиноз: Gardnerella vaginalis, Bacteroides spp., Mobiluncus spp., Peptostreptococcus spp. Механизм действия метронидазола заключается в биохимическом восстановлении 5-нитрогруппы метронидазола внутриклеточными транспортными протеинами анаэробных микроорганизмов и простейших. Восстановленная 5-нитрогруппа метронидазола взаимодействует с ДНК клеток микроорганизмов, ингибирует синтез нуклеиновых кислот, что ведет к их гибели.
После однократного внутривлагалищного введения 5 г метрогила вагинального геля, средняя максимальная концентрация препарата в сыворотке крови здоровых женщин достигает 237 нг/мл, что составляет 2% от средней максимальной концентрации метронидазола (12,785 нг/мл) при приеме внутрь дозы в 500 мг. Время достижения максимальной концентрации — 6–12 ч после внутривлагалищного применения однократной дозы в 5 г и 1–3 ч после перорального приема метронидазола в дозе 500 мг. Относительная биодоступность вагинального геля в два раза выше биодоступности одноразовой дозы (500 мг) влагалищных таблеток метронидазола, что обусловлено высокой проникающей способностью препарата во влагалищной жидкости. Поэтому терапевтический эффект вагинального геля достигается уже при низких концентрациях метронидазола. Меньшие дозы вагинального геля ведут к более низким концентрациям метронидазола в сыворотке крови, что приводит к незначительному числу побочных эффектов во время курса лечения.
Для лечения трихомониаза рекомендуемая доза составляет 5 г (один полный аппликатор) дважды в день (утром и вечером) в течение пяти дней.
В последнее время появился ряд публикаций, в которых сообщается об увеличении эффективности лечения урогенитального трихомониаза при сочетанном лечении протистоцидными препаратами системного действия и местного применения метрогила вагинального геля.
Критерии излеченности урогенитального трихомониаза:
Таким образом, назначение адекватной терапии крайне важно для успешного лечения урогенитального трихомониаза, поскольку в противном случае могут отмечаться персистирование инфекции, рецидивы заболевания и посттрихомонадные осложнения.
А. Л. Тихомиров, доктор медицинских наук, профессор
Ч. Г. Олейник, кандидат медицинских наук
МГМСУ, Москва