Мифы об обогревателях: правда ли сжигают кислород и вредят здоровью
Обогреватели какой из них специалисты признают лучшим на данный момент? Когда этих приборов надо опасаться? Может ли привычный зимний прибор воспламениться? И действительно ли он «выжигает кислород»? Программа «Чудо техники» провела несколько тестов и выяснила, что миф, а что правда.
Сжигание обогревателем кислорода это, конечно, миф. Такое может произойти, только если используется открытое пламя: оно действительно забирает из воздуха молекулы кислорода. Откуда же тогда жалобы на плохое самочувствие? Специалисты объясняют: проблема может возникнуть не только с масляным радиатором любой перегрев приводит к уменьшению влажности воздуха отсюда и ухудшение самочувствия. Причем дело не только в пересушивании слизистых. Пыль начинает вести себя и раздражать дыхательные пути.
Так что обогреватель лучше не включать на максимум, а в идеале вообще пользоваться им время от времени. И хорошо, если у вас есть гигрометр прибор для контроля влажности воздуха.
Есть и те, кто боится инфракрасных обогревателей: якобы они излучают опасное. Работу такого обогревателя можно сравнить с солнцем. Греют они оба не воздух, а предметы, на которые направлены их лучи невидимые, в инфракрасном спектре и несут тепло. Опасного в этом ничего нет, хотя правила пользования надо соблюдать если долго находиться рядом с таким обогревателем, может начаться головная боль и появится усталость точно так же, как от продолжительного нахождения на солнце или у открытого огня. Кроме того, злоупотребление инфракрасным спектром может плохо влиять на кожу. Главное расстояние до прибора должно быть не менее двух метров.
Программа «Чудо техники» протестировала самые современные модели тепловентилятор за 27 тысяч рублей, необычный кварцевый обогреватель за 3000 рублей, в котором нагревательный элемент спрятан под толщей кварцевого песка и мраморной крошки, и инфракрасный переносной обогреватель за 5000 рублей.
Как показал тест, инфракрасный самый пожаробезопасный из всех. Главные правила ничего не сушить прямо на обогревателе, не ставить его рядом с занавесками и мебелью и не опрокидывать.
Кислород – рождающий кислоты
Содержание
Кислород при нормальных условиях (температуре и давлении) представляет собой прозрачный газ без запаха, вкуса и цвета. Не относится к горючим газам, но способен активно поддерживать горение.
По химической активности среди неметаллов он занимает второе место после фтора.
Все элементы, кроме благородных металлов (платина, золото, серебро, родий, палладий и др.) и инертных газов (гелий, аргон, ксенон, криптон и неон), вступают в реакцию окисления и образовывают оксиды. Процесс окисления элементов, как правило, носит экзотермический (с выделением теплоты) характер. Также необходимо учитывать тот факт, что при повышении температуры, давления или использовании катализаторов – скорость реакции окисления резко возрастает.
История открытия кислорода
Открытие кислорода приписывают Джозефу Пристли (Joseph Priestley). У него была лаборатория, оборудованная приборами для собирания газов. Он испытывал его физиологическое действие на себе и на мышах. Пристли установил, что после вдыхания газа некоторое время ощущается приятная легкость. Мыши в герметически закрытой банке с воздухом задыхаются быстрей, чем в банке с O2. Поскольку Пристли был приверженцем флогистонной теории он так и не узнал, что оказалось у него в руках. Он только описал этот газ, даже не догадываясь, что он описал. А вот лавры открытия кислорода принадлежат Антуан Лоран Лавуазье (Antoine Laurent de Lavoisier), который и дал ему имя.
Лавуазье, поставил свой знаменитый опыт, продолжавшийся 12 дней. Он нагревал ртуть в реторте. При кипении образовывалась ее красная окись. Когда реторту охладили, оказалось, что воздуха в ней убыло почти на 1/6 его объема, а остаток ртути весил меньше, чем перед нагревом. Но когда разложили окись ртути сильным прокаливанием, все вернулось: и недостача ртути, и «исчезнувший» кислород.
Впоследствии Лавуазье установил, что этот газ входит в состав азотной, серной, фосфорной кислот. Он ошибочно полагал, что O2 обязательно входит в состав кислот, и поэтому назвал его «оксигениум», что значит «рождающий кислоты». Теперь хорошо известны кислоты, лишенные «оксигениума» (например: соляная, сероводородная, синильная и др.).
Способы получения кислорода
В основном кислород получают тремя способами:
Из атмосферного воздуха его получают методом глубокого охлаждения, как побочный продукт при получении азота.
Также O2 добывают путем пропускания электрического тока через воду (электролиз воды) с попутным получением водорода.
Химические способ получения малопроизводителен, а, следовательно, и неэкономичен, он не нашел широкого применения и используются в лабораторной практике.
Наверно многие помнят химический опыт, когда в колбе нагревают марганцовку (перманганат калия KMnO4), а потом выделяющийся в процессе нагрева газ собирают в другую колбу?
Применение кислорода
Помимо того, что все живые существам в природе, за исключением немногих микроорганизмов, при дыхании потребляют кислород, он широко применяется во многих отраслях промышленности: металлургической, химической, машиностроении, авиации, ракетостроении и даже в медицине.
В химической промышленности его применяет:
В металлургии его используют:
В медицинских целях больным, у которых нарушена нормальная деятельность органов дыхания или кровообращения, искусственно увеличивают содержание O2 в воздухе или дают дышать непродолжительное время чистым O2. Медицинский кислород, выпускаемый ГОСТ 5583, особенно тщательно очищают от всех примесей.
Применение кислорода в сварке
Сам по себе O2 является негорючим газом, но из-за свойства активно поддерживать горение и увеличения интенсивности (интенсификации) горения газов и жидкого топлива его используют в ракетных энергетических установках и во всех процессах газопламенной обработки. В таких процессах газопламенной обработки, как газовая сварка, поверхностная закалка высокая температура пламени достигается путем сжигания горючих газов в O2, а при газовой резке благодаря ему происходит окисление и сгорание разрезаемого металла.
При полуавтоматической сварке (MIG/MAG) кислород O2 используют как компонент защитных газовых смесей с аргоном (Ar) или углекислым газом (CO2).
Кислород добавляют в аргон при полуавтоматической сварке легированных сталей для обеспечения устойчивости горения дуги и струйного переноса расплавленного металла в сварочную ванну. Дело в том, что как поверхностно активный элемент он уменьшает поверхностное натяжение жидкого металла, способствуя образованию на конце электрода более мелких капель.
При сварке низколегированных и низкоуглеродистых сталей полуавтоматом O2 добавляют в углекислый газ для обеспечения глубокого проплавления и хорошего формирования сварного шва, а также для уменьшения разбрызгивания.
Чаще всего кислород используют в газообразном виде, а в виде жидкости используют только при его хранении и транспортировке от завода-изготовителя до потребителей.
Вредность и опасность кислорода
За внешней безобидностью скрывается очень опасный газ, но об этом на нашем сайте опубликована статья про маслоопасность и взрывоопасность кислорода и мы не будем здесь дублировать информацию.
Хранение и транспортировка кислорода
Кислород газообразный технический и медицинский выпускают по ГОСТ 5583.
Хранят и транспортируют его в стальных баллонах ГОСТ 949 под давлением 15 МПа. Кислородные баллоны окрашены в синий цвет с надписью черными буквами «КИСЛОРОД».

Жидкий кислород выпускается по ГОСТ 6331. O2 находится в жидком состоянии только при получении, хранении и транспортировке. Для газовой сварки или газовой резки его необходимо снова превратить в газообразное состояние.
Характеристики кислорода
Характеристики O2 представлены в таблицах ниже:
Коэффициент перевода объема и массы O2 при Т=15°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 1,337 | 1 | 1,172 |
| 1,141 | 0,853 | 1 |
| 1 | 0,748 | 0,876 |
Коэффициенты перевода объема и массы O2 при Т=0°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 1,429 | 1 | 1,252 |
| 1,141 | 0,799 | 1 |
| 1 | 0,700 | 0,876 |
Кислород в баллоне
| Наименование | Объем баллона, л | Масса газа в баллоне, кг | Объем газа (м 3 ) при Т=15°С, Р=0,1 МПа |
|---|---|---|---|
| O2 | 40 | 8,42 | 6,3 |
Благодаря этой таблице теперь можно легко дать ответы на вопросы, которые очень часто задают сварщики:
Физические свойства кислорода
Где бы мы ни находились, нас всюду окружает кислород воздуха.
Почему же мы не замечаем и не чувствуем его? Кислород, азот, аргон и другие газы, входящие в состав воздуха, бесцветны и не имеют ни запаха, ни вкуса. Газообразный воздух нельзя ни видеть, ни ощущать.
Воздух из газообразного состояния можно перевести в жидкое. Одновременно с основной массой воздуха — азотом — в жидкое состояние перейдут кислород и большинство других газов, входящих в его состав.
Чтобы газообразный кислород превратить в жидкость, его нужно сжать до 50 атмосфер и охладить до —119°.
Жидкий кислород можно получить и при атмосферном давлении, но для этого нужно газообразный кислород охладить до температуры —183°. При более сильном охлаждении, до температуры —220°, жидкий кислород затвердевает и превращается в снегообразную массу.
Если на некоторое время в жидкий кислород поместить кусочек резины, она потеряет свою эластичность и под ударом разлетится на мелкие части.
Такую же хрупкость приобретает и цинковая пластинка, охлажденная в жидком кислороде до температуры —183°. Жидкая ртуть при такой температуре превращается в твердую массу, которую можно ковать, как свинец, а свинец приобретает способность звенеть, как бронзовый колокольчик.
Жидкий кислород имеет голубоватый цвет. Его можно легко переливать из сосуда в сосуд. При переливании жидкий кислород «парит». Но это не пары кислорода, а пары воды. Жидкий кислород, испаряясь, поглощает много тепла из окружающего воздуха. Воздух сильно охлаждается, и влага, находящаяся в воздухе, конденсируется, образуя туман. Этот туман и создает впечатление пара, исходящего из самой жидкости.
Температура кипения жидкого кислорода равна —183°.
Если фарфоровый стакан с жидким кислородом вынести зимой на мороз 30—40°, он будет кипеть более бурно, чем вода на самом сильном огне газовой плиты.
При комнатной температуре испарение жидкого кислорода идет еще энергичнее, и он быстро переходит в газообразное состояние.
Чтобы использовать жидкий кислород, его необходимо сохранить. Как же заставить эту бурно кипящую жидкость не так быстро испаряться?
Для этого служат специальные сосуды, в которых легко удается «укротить» эту быстро испаряющуюся жидкость.
Стеклянный сосуд для хранения небольшого количества жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — поверхности, посеребренные внутри.
Сосуд для хранения жидкого кислорода представляет собой цилиндр с двойными стенками. Внутренние стороны стенок обычно покрывают тонким слоем серебра. Воздух между стенками сосуда выкачивается.
Разреженные газы плохо проводят тепло, а зеркальная поверхность серебра хорошо отражает его. Таким образом, жидкий кислород, который находится в сосуде, изолирован от внешнего тепла, что обеспечивает сохранение жидкого кислорода в течение одних-двух суток.
При испарении жидкого кислорода объем его увеличивается почти в 800 раз. Из кубического сантиметра жидкого кислорода образуется около 800 кубических сантиметров газообразного.
Хранить жидкий кислород в закрытых сосудах опасно: внутри сосуда может образоваться большое давление, приводящее к взрыву. Поэтому сосуды для хранения жидкого кислорода сверху открыты. Воздух, находящийся над жидкостью, сильно охлаждается и предохраняет кислород от наружного тепла, замедляя дальнейшее испарение.
Для перевозки небольших количеств жидкого кислорода используют металлические емкостью 15—25 литров.
Металлические сосуды состоят из двух шаров или цилиндров, вставленных друг в друга. Внутренний шар или цилиндр имеет высокое и узкое горло, через которое сосуд заполняется жидким кислородом. Горло всегда остается открытым. Из пространства между стенками сосуда воздух выкачан, и создан высокий вакуум, то есть сильное разрежение.
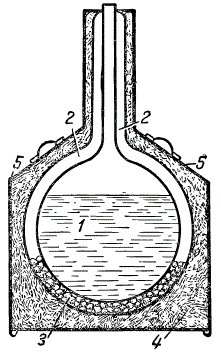
Металлический сосуд для перевозки жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — силикагель; 4 — теплоизоляционный материал; 5 — железный цилиндр.
Чтобы поддержать высокий вакуум, часть пространства между стенками заполняется силикагелем, способным при низкой температуре поглощать количество газа в сотни раз больше своего собственного объема. Если через стенки или через места спайки со временем просочится небольшая часть воздуха, он поглотится силикагелем и разрежение не уменьшится. Высокий вакуум обеспечивает постоянную изоляцию сосуда от внешнего тепла и дает возможность в течение двух и более суток сохранять в нем жидкий кислород. Такие сосуды обычно помещают в железные цилиндры.
Пространство между сосудом и наружным цилиндром заполняют теплоизоляционным материалом. Для переноски на наружном цилиндре имеются ручки.
Большие количества жидкого кислорода перевозятся по железной дороге и автотранспортом в специальных цистернах или танках. Они хорошо изолированы от внешнего тепла. Емкость транспортных танков различна: от 1 тысячи до 10 тысяч литров. Цистерны, в которых жидкий кислород перевозят по железной дороге, вмещают до нескольких десятков тонн.
Жидкий кислород можно получить из жидкого воздуха, который образуется при низких температурах и высоком давлении.
Высокое давление создают в машинах, которые называются компрессорами. Их приводят в движение электродвигатели.
Источник: В. Медведовский. Кислород. Государственное Издательство Детской литературы Министерства Просвещения РСФСР. Ленинград. Москва. 1953
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Температура горения кислорода в воздухе
Взаимодействие кислорода с простыми веществами
Кислороду присуща высокая химическая активность. Многие вещества реагируют с кислородом при комнатной температуре. Так, например, свежий срез яблока довольно быстро приобретает бурую окраску, это происходит вследствие химических реакций между органическими веществами, содержащимися в яблоке, и кислородом, содержащимся в воздухе. С простыми веществами кислород, как правило, реагирует при нагревании. В металлическую ложечку для сжигания веществ поместим уголек, нагреем его в пламени спиртовки докрасна и опустим в сосуд с кислородом. Наблюдаем яркое горение уголька в кислороде. Уголь – простое вещество, образованное элементом углеродом. В реакции кислорода с углеродом образуется углекислый газ:
C + O2 = CO2
Стоит отметить, что многие химические вещества имеют тривиальные названия. Углекислый газ – это тривиальное название вещества. Тривиальные названия веществ используются в повседневной жизни, многие из них имеют давнее происхождение. Например, пищевая сода, бертолетова соль. Однако у каждого химического вещества есть и систематическое химическое название, составление которого регламентируется международными правилами – систематической химической номенклатурой.
Так, углекислый газ имеет систематическое название оксид углерода (IV).
Углекислый газ является сложным веществом, бинарным соединением, в состав которого входит кислород. Поместим в ложечку для сжигания веществ серу и нагреем. Сера плавится, затем загорается. На воздухе сера горит бледным, почти незаметным, синим пламенем. Внесем серу в сосуд с кислородом – сера горит ярким синим пламенем. В реакции серы с кислородом образуется сернистый газ:
S + O2 = SO2
Сернистый газ, как и углекислый газ, относится к группе оксидов. Это оксид серы (IV) – бесцветный газ с резким едким запахом. Теперь внесем в сосуд с кислородом подожженный красный фосфор. Фосфор горит ярким, ослепительным пламенем. Сосуд заполняется белым дымом. Белый дым – это продукт реакции, мелкие твердые частицы оксида фосфора (V):
4P + 5O2 = 2P2O5
В кислороде способны гореть не только неметаллы. Металлы также энергично взаимодействуют с кислородом. Например, магний горит в кислороде и на воздухе ослепительным белым пламенем. Продукт реакции – оксид магния:
2Mg + O2 = 2MgO
Попробуем сжечь в кислороде железо. Раскалим в пламени спиртовки стальную проволоку и быстро опустим в сосуд с кислородом. Железо горит в кислороде с образованием множества искр. Вещество, полученное в результате реакции, называют железной окалиной:
3Fe + 2O2 = Fe3O4.
Снопы искр, образующихся при горении бенгальского огня, объясняются сгоранием порошка железа, входящего в состав этих пиротехнических изделий. После рассмотренных реакций можно сделать важные выводы: кислород реагирует как с металлами, так и неметаллами; часто эти реакции сопровождаются горением веществ. Продуктами реакций кислорода с простыми веществами являются оксиды. Обратите внимание, что при взаимодействии кислорода с простыми веществами – металлами и неметаллами образуются сложные вещества – оксиды. Такой тип химических реакций называют реакциями соединения.
Реакция соединения – реакция, в результате которой из двух или нескольких менее сложных по строению веществ, образуются более сложные по строению вещества
Видео
Обогреватель, не сжигающий кислород: правильный выбор для дома
Сжечь кислород невозможно. Горение – окисление веществ с повышенной скоростью под действием воздуха. Воздух — кислород на 20%. Азот (остальные 80%) не окисляется при нормальных условиях. Кислород не горит, но пыль на спирали нагревательного элемента может сгорать. Этот запах слышится при включении не работавшего прибора. Частички, постоянно витающие в воздухе, станут сгорать при высокой температуре. Обогреватель, не сжигающий кислород, работает по-особому. Посмотрим, что имеется в виду!
Почему «горит» спираль
Не измерялось, при какой температуре в точности начинается горение пыли. Из опыта видно, что подошва утюга неспособна воспламенить пыль, а спираль это делает. Потому при включении стареньких моделей утюгов слышится неприятный запах. Внутри оседает пыль, загорающаяся при включении. Считается, чем ниже температура нагревательного элемента, тем меньше жжет прибор воздух.
Окисляются пыль и материал спирали. Порой прибор перегорает. Это заметили, появились технологии, ограничивающие доступ воздуха к поверхности. К примеру, нашумевшее керамическое покрытие выполняет одновременно две функции:
Температура уменьшается, так как площадь поверхности элемента становится больше. Керамика в качестве покрытия выбрана в силу двух особенностей:
Материал, получаемый при температуре 1200 ºС (порой выше), не боится 300 ºС, встречающихся в типичном обогревателе. Одновременно керамическое покрытие гладкое, мало подвержено оседанию пыли в сравнении с металлом. Обогреватель, не сжигающий кислород, снабжается защитным покрытием из керамического материала.
Найден альтернативный способ защиты — воздушные фильтры. Приспособления уже применяются в керамических обогревателях (ветродувках) и конвекторах. В результате воздух на входе очищается от механических загрязнений, от запахов и микробов. Так функционируют конвекторные обогреватели Электролюкс Air Gate. В созданные Ворота проходит чистый воздух, не оставляющий на нагревательном элементе следа.
Эффект сжигания кислорода
Пользователи замечали, что масляный обогреватель после включения вызывает эффект духоты. Становится трудно дышать. Ситуацию тоже причислили к явлению сжигания кислорода, хотя процесс близко не стоит с химическими реакциями. На деле начинает стремительно понижаться влажность воздуха. Это физиологически чувствуется как удушье. Нормальная влажность в помещении укладывается в диапазон 40 — 60%. В противном случае человеку некомфортно. В случае нагревания влажность опускается ниже 40%.
Вдобавок подобные эффекты вызывают постепенное снижение иммунитета, что приводит к резкому росту заболеваемости. Врачи советуют поддерживать в комнате естественный режим:
Это возвращает человеку нормальное самочувствие, поднимает иммунитет, блокирует размножение большинства грибков и вирусов. Для паразитов создаются неприемлемые условия – слишком холодно. И влажность не подходит. Обогреватель для детской комнаты не ухудшает микроклимат.
Эффект высушивания воздуха получается из-за повышения температуры. Молекулы пара приобретают энергии, чтобы покинуть помещение через бетонные плиты. Стены дышат, слой пароизоляции не блокирует проникновение воды напрочь. Просто процесс обмена пара с окружающей средой сильно замедляется. Придавая молекулам дополнительную энергию, заставляем жидкость стремительно покидать комнату. На этом основывается привычка размещения вещи на батарее для сушки. В последнем случае процесс очевиден.
При повышении температуры концентрация пара снижается. Масляные обогреватели ругают за нежелательный эффект. Чем выше температура и больше площадь, тем сильнее прибор сушит воздух. У масляного обогревателя оба критерия в сумме дают максимум, отсюда и мнение, что жжет кислород. Правдоподобности добавляет запах гари, витающий вокруг. Инфракрасное излучение прогревает стены, потолок, пол. Отсутствие движения воздуха создает благоприятные условия для осаждения паров на поверхность бетона, способствуя проникновению влаги в поры плит, кирпича.
Меры устранения сжигания кислорода нагревателем
Уже назвали косвенно два условия, когда обогреватель жжет кислород:
На указанные два параметра направлено противодействие сжиганию кислорода.
Чтобы избежать осушения воздуха часто в обогреватели добавляют функции увлажнения. Это позволит удержать параметры микроклимата на нормальном уровне. Микробы убиваются ионизатором или ультрафиолетовым излучением. Подобные приборы выпускает шведская фирма Timberk.
Конвекторы
Лучшими считают конвекторы. Добавим, что полезны обогреватели фирмы Электролюкс, снабжённые специальными фильтрами. Timberk выпускает конвекторы с увлажнителями в виде дополнительной опции. Это нормализует микроклимат, больше подходит для юга России, чем для средней полосы, заросшей лесами.
Инфракрасные обогреватели
Хвалят электрические инфракрасные обогреватели потолочного типа. Создаются двух разновидностей:
Первые не отличаются от ламп дневного света. Внутри за решеткой находится длинная стеклянная колба со спиралью. По науке перед работой указанного обогревателя нужно смахнуть пыль с лампы и рефлектора, на практике это делается реже, процесс затрудняется решеткой.
На этом фоне керамические инфракрасные обогреватели смотрятся выгоднее. Напоминают лампы дневного света, вместо решеток защитные панели, но не стекло. Гладкая поверхность представляет сталь, покрытую керамикой. Конструкция ведет себя по свойствам как абсолютно черное тело. Максимум излучения приходится на инфракрасный диапазон. К указанному классу относятся изделия Пион, Билюкс и Иколайн.
Газовые инфракрасные обогреватели для помещений являются неплохим решением. К примеру, камины, работающие по инфракрасному принципу. Внутри за жаропрочным стеклом горит пламя, докрасна разогревая керамическую решетку. Начинается излучение тепла. Газ подводится снаружи, придется пробурить стену под желтую трубу, вдобавок требуется забрать с улицы воздух и выбросить продукты сгорания. Это требует наличия дополнительного отверстия под коаксиал. Это двойная труба – певая внутри второй. Подобный прием позволит обойтись единсвтенной дырой в стене (вместе с желтой трубой получается две).
Подумайте, стоит ли так стараться, только чтобы получить хороший камин. Это дорогое устройство, красивое. Газовый камин называют прибором, обладающим декоративным эффектом и работоспособным в качестве нагревателя.
Для справки. Электрокамины являются устройствами, имитирующими горение очага и не дающими тепла. В лучшем случае внутри спрятана спираль с вентилятором. В наличии маломощная ветродувка. Огромные деньги, уплаченные за оборудование, отдаются за внешнее оформление и спецэффекты.
Имеются газовые конвекторы, не слишком сильно сушат воздух, однако по красоте (и цене) уступают каминам, а дыры в стене все равно делать придется. Если уж задумались о вопросах климата, не стоит брать модели. Обратите внимание, что избранные газовые камины с баллоном забирают воздух из помещения и выкидывают обратно. Такие обогреватели жгут и сушат воздух. Однако! При сгорании газа образуется водяной пар, потери восполняются. Вдобавок образуется четырехвалентный оксид серы, образуя во влажном воздухе серную кислоту. Подобные приборы хороши на даче, на природе, куда выезжает толпа людей повеселиться и отдохнуть.
Кислород воспламеняется?
Нет, кислород по своей природе не воспламеняется. Это окислитель, а это значит, что он помогает гореть другим вещам.
Предположим, вы построите лабораторию, которая будет идеально изолирована от внешнего мира, а это значит, что в нее не смогут попасть никакие примеси или газы. Затем, вы наполните лабораторию чистым кислородом. Если каким-то образом в лабораторию попадет искра, что, по-вашему, произойдет?
Если бы кислород был легковоспламеняющимся газом, искра подожгла бы воздух в лаборатории, но, поскольку кислород негорючий, он не загорается сам по себе.

Однако, если бы в лаборатории был хотя бы небольшой лист бумаги, он бы мгновенно загорелся, так как молекулы на листе бумаги быстро прикрепились бы к окружающему кислороду (то есть к окислителю).
Кислород нужен не всегда, чтобы зажечь огонь; подойдет любой окислитель. Хлор, перекись водорода, серная кислота и азотная кислота являются одними из многих окислителей, которые могут воспламенить вещи при правильных условиях.
Поскольку кислород является наиболее распространенным природным окислителем, принято считать, что все горит только в присутствии кислорода. Другими словами, люди могут предположить, что кислород всегда необходим для того, чтобы что-то сгорело.
Еще один частый вопрос, связанный с огнем и кислородом: как звезды и наше солнце продолжают гореть, если в космосе нет кислорода?
Химические свойства
Кислород является химически активным веществом. Он способен вступать в реакции с множеством других веществ, однако для протекания большинства этих реакций необходима более высокая, чем комнатная, температура. При нагревании кислород реагирует с неметаллами и металлами.
Если стеклянную колбу наполнить кислородом и внести в нее ложечку с горящей серой, то сера вспыхивает с образованием яркого пламени и быстро сгорает (рис. 80).
Химическую реакцию, протекающую в этом случае, можно описать следующим уравнением:
В результате реакции образуется вещество SO2, которое называется сернистым газом. Сернистый газ имеет резкий запах, который вы ощущаете при зажигании обычной спички. Это говорит о том, что в состав головки спички входит сера, при горении которой и образуется сернистый газ.
Подожженный красный фосфор в колбе с кислородом вспыхивает еще ярче и быстро сгорает, образуя густой белый дым (рис. 81).
При этом протекает химическая реакция:
Белый дым состоит из маленьких твердых частиц продукта реакции — P2O5.
Если в колбу с кислородом внести тлеющий уголек, состоящий в основном из углерода, то он также вспыхивает и сгорает ярким пламенем (рис. 82).
Протекающую химическую реакцию можно представить следующим уравнением:
Продуктом реакции является CO2, или углекислый газ, с которым вы уже знакомы. Доказать образование углекислого газа можно, добавив в колбу немного известковой воды. Помутнение свидетельствует о присутствии CO2 в колбе.
Возгорание уголька можно использовать для отличия кислорода от других газов. Если в сосуд (колбу, пробирку) с газом внести тлеющий уголек и он вспыхнет, то это указывает на наличие в сосуде кислорода.
Кроме неметаллов, с кислородом реагируют и многие металлы. Внесем в колбу с кислородом раскаленную стальную проволоку, состоящую в основном из железа. Проволока начинает ярко светиться и разбрасывать в разные стороны раскаленные искры, как при горении бенгальского огня (рис. 83).
При этом протекает следующая химическая реакция:
В результате реакции образуется вещество Fe3O4 (железная окалина). В состав формульной единицы этого вещества входят три атома железа, причем один из них имеет валентность II, а два других атома имеют валентность III. Поэтому формулу этого вещества можно представить в виде FeO * Fe2O3.
На заметку: Реакцию железа с кислородом используют для резки стальных изделий. Для этого определенный участок детали сначала нагревают с помощью кислородногазовой горелки. Затем направляют на нагретое место струю чистого кислорода, для чего перекрывают кран поступления горючего газа в горелку. Нагретое до высокой температуры железо вступает в химическую реакцию с кислородом и превращается в окалину. Так можно разрезать очень толстые железные детали.
Какова максимальная температура огня при горении дерева (любого)?
при нагревании до 105°С из древесины испаряется вода; при нагревании до 150°С из древесины удаляются остатки влаги и начинается разложение и выделение газообразных продуктов; при нагревании 270—280°С начинается экзотермическая реакция с выделением тепла, т. е. созданы условия для самоподдержания необходимой температуры, при • которой идёт разложение древесины с образованием пламени и дальнейшим повышением температуры; при температуре 450°С и более пламенное горение переходит в беспламенное горение угля (тление) с температурой до 900°С.
Думаю градусов 500-600
При температуре 275° на открытом воздухе начинается горение древесины, т. е. соединение ее с кислородом воздуха, сопровождающееся светящимся пламенем. При этом в толстых кусках древесина из-за малой теплопроводности не прогревается; начавшееся горение переходит в тление и прекращается совсем. Поэтому практически точкой воспламенения древесины можно считать (для сосны) 300—330°.
Температура воспламенения для большинства твердых материалов — 300°С. Температура пламени в горящей сигарете — 700-800°С. В спичке температура пламени 750-850 °С, при этом 300°С — температура воспламенения дерева, А ТЕМПЕРАТУРА ГОРЕНИЯ ДЕРЕВА РАВНЯЕТСЯ ПРИМЕРНО 800 — 1000 °С. Температура горения пропан-бутана колеблется от 800 до 1970 °С. Температура горения бензина — 1300-1400 °С. Температура пламени керосина — 1100 °С. Температура пламени спирта не превышает 900 °С. Температура горения магния — 2200 °С.
Ответ зависит от того, что и как греть. Большие температуры за 1000 С для нагрева крупных тел можно получить лишь с подогревом воздуха, в прогретых печах, где тепло не рассеивается в стороны. Хотя верхняя часть пламени имеет выше 1500 С, но никто не расплавит в ней железо.