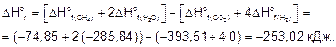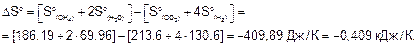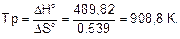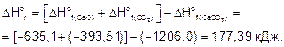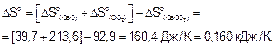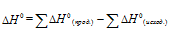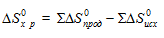При какой температуре самопроизвольно пойдет реакция
Для удобства пользователей и возможности быстрого нахождения решения типовых (и не очень) задач на xим. энергию и термодинамику.
©Для некоммерческого использования. При перепечатке решений обязательна ссылка на источник.
Решение:
1) H2(г)+1/2 O2(г) = Н2О(ж)
Задача 5
Вычислить изменение энергии Гиббса для реакции CaCO3(к.) = СаО(к.)+СО2(г.)
при 25, 500, 1500*С. Зависимостью дельта Н и дельта S от температуры пренебречь.
Для 500С (773К):
ΔGо= 178 – 773 * 0,162 = 52,77 кДж > 0 (реакция невозможна и при 500С)
Подобным образом найдите ответ для остальных реакций.
Задача 13
Константа диссоциации муравьиной кислоты при 298 К равна 1,7 * 10^(-4)
Рассчитайте ΔG298 процесса диссоциации. Какой процесс (диссоциация или моляризация) протекает в системе самопроизвольно, если концентрация Снсoo- =Сн+= Cнсоон= 10^(-2) моль/л
Ответ подтвердите рассчетом ΔG.
Решение:
Температура выражает меру теплового движения частиц и кол-во энергии, необходимой для осуществления какого-либо процесса (энергию ведь, как вы знаете, измерить невозможно).
Между молекулами обоих в-в водородные связи, при плавлении они сохраняются и лишь несколько ослабляются, поэтому для плавления требуется сходное кол-во энергии.
Мера ослабления межмолекулярных связей при плавлении этих веществ сходна (те же связи), потому и темп. плавления сходны.
Не так при кипении. При кипении межмолекулярные связи разрушаются, и энергия, требуемая для их разрушения, находится в прямой зависимости от сил межмолекулярного притяжения.
Между молекулами Н2О2 больше водородных связей, и кроме того, Ван-дер-Ваальсовы силы притяжения тем больше, чем больше электронное облако молекулы, поэтому несомненно для разрушения сил межмолекулярного притяжения требуется намного больше энергии, а значит, темп. кипения будет значительно выше.
Определение энергии Гибсса и константы реакции при заданной ткмпературе
1. Расчет энтальпии реакции получим:
2. Расчет энтропии реакции получим:
Переведем температуру из шкалы Цельсия в шкалу Кельвина: Т = 273 + 200 = 473 К. Для расчета ΔG o 473 воспользуемся уравнением:
ΔG o 473 = ΔH o – TΔS o
ΔG o 473 = –153,6 – 473·(–0,01718) = –145,47 кДж.
Таким образом, ΔG o 473 o С возможно.
Ответ: ΔG o 473 = –145,47 кДж; возможно.
1. Расчет энтропии реакции получим:
2. Расчет энтропии реакции получим:
3. Теперь рассчитаем изменение энергии Гиббса при Т = 298 К для реакции, получим:
Как свидетельствуют результаты расчетов,ΔG 0 х.р. > 0 и, значит, этот процесс самопроизвольно протекать не будет.
Задача 72.
Возможно ли протекание реакции: CaCO3(к) = CaO(к) + CO2(г) при 25 и 1800°C? Найдите приближённое значение температуры, при которой ΔG 0 Т = 0. Зависимостями ΔH 0 и ΔS 0 от температуры пренебречь. Рассчитайте константу равновесия реакции для трёх указанных температур.
Решение.
ΔH 0 CaO(к) = −635,1 кДж/моль;
ΔH 0 CO2(г) = −393,5 кДж/моль;
ΔH 0 CaCO3(к) = −1206,8 кДж/моль;
ΔS 0 CaO(к) = 38,1 Дж/(моль . K);
ΔS0CO2(г) = 213,7 Дж/(моль . K);
ΔS 0 CaCO3(к) = 91,7 Дж/(моль . K).
ΔG 0 T реакции можно определить по формуле:
Вычислим ΔH 0 298 и ΔS 0 298 по формулам:
Так как ΔG 0 298 > 0, то протекание реакции при 25 °C невозможно.
Рассчитаем энергию Гиббса реакции при температуре 1800 °C, получим:
По условию задачи можно считать, что ΔH 0 298 = ΔH 0 2073 и ΔS 0 298 = ΔS 0 2073.
Температуру, при которой ΔGT = 0, находим по формуле:
Константу равновесия реакции для этих трёх температур найдём на основании формулы:
Таким образом, чем меньше значение ΔG 0 Т, тем более полно протекает реакция и тем больше константа равновесия.
Направление химических реакций
Многие химические реакции протекают самопроизвольно, т.е. без затрат энергии извне. Одной из движущих сил самопроизвольного химического процесса является уменьшение энтальпии системы, т.е. экзотермический тепловой эффект реакции. Другой – стремление частиц (молекул, ионов, атомов) к хаотическому движению, беспорядку. Мерой хаотичности, неупорядоченности состояния системы служит термодинамическая функция, называемая энтропией (S).
При переходе системы из более упорядоченного состояния в менее упорядоченное состояние (нагревание, испарение, плавление) энтропия возрастает (DS>0). В случае перехода системы из менее упорядоченного состояния в более упорядоченное (охлаждение, конденсация, кристаллизация) энтропия системы уменьшается (DS 0) – это суть второго закона термодинамики.
Энтропия вещества в стандартном состоянии называется стандартной энтропией (So) и имеет единицу измерения Дж/моль•К (Приложение, табл.1). Изменение энтропии системы в результате протекания химической реакции (DSo) равно сумме энтропий продуктов реакции за вычетом энтропий исходных веществ с учетом стехиометрических коэффициентов:
DSo = SSoпрод — SSoисх.
Энтропия вещества в газообразном состоянии существенно выше, чем в жидком и твердом состояниях, поэтому об изменении энтропии в химической реакции судят по изменению числа молей газообразных веществ. Например, в реакции
из одного моля СО2 образуется 2 моля СО, следовательно энтропия возрастает (DS>0).
В реакции образования аммиака
энтропия уменьшается, т.к. число молей NH3 меньше суммы молей N2 и Н2.
Возможность самопроизвольного протекания химического процесса определяется двумя факторами:
— стремлением к образованию прочных связей между частицами, к возникновению более сложных веществ, что сопровождается понижением энергии системы – энтальпийный фактор (DH 0).
Эти факторы объединяет функция, называемая энергией Гиббса (DG), равная:
Изменение энергии Гиббса служит критерием самопроизвольного протекания химической реакции:
— химическая реакция принципиально возможна, если энергия Гиббса в ходе реакции уменьшается (DG 0), протекает обратная реакция;
— химическая реакция может протекать как в прямом, так и в обратном направлении, т.е. система находится в состоянии равновесия (DG=0).
Из уравнения DG=DH-T•DS следует:
— если DН 0, то всегда DG 0 и DS 0, т.е. реакция с поглощением теплоты и увеличением степени порядка невозможна ни при каких условиях;
— DH>0, DS |DH|. Эти реакции протекают при высокой температуре;
— DH 0. Условие самопроизвольного протекания реакции: |DH|>|T•DS|. Такие реакции идут обычно при низких температурах.
Температуру, при которой происходит смена знака энергии Гиббса реакции, можно определить из условия равновесия:
где Тр – температура, при которой устанавливается равновесие.
Изменение энергии Гиббса системы при образовании 1 моль вещества из простых веществ, устойчивых в стандартных условиях, называется стандартной энергией Гиббса образования вещества (DGof). Стандартная энергия Гиббса образования простых веществ принимается равной нулю.
Стандартную энергию Гиббса химической реакции (DGor) можно рассчитать как сумму стандартных энергий Гиббса образования продуктов реакции за вычетом суммы энергий Гиббса образования исходных веществ с учетом стехиометрических коэффициентов:
DGo = SDGofпрод — SDGofисх.
Пример 1. На основании стандартных энтальпий образования и стандартных энтропий веществ вычислите DG реакции, протекающей по уравнению:
СО2(г) + 4Н2(г) = СН4(г) +2Н2О(ж).
В каком направлении будет протекать данная реакция? Рассчитайте температуру, при которой наступит равновесие.
СО2(г) + 4Н2(г) = СН4(г) +2Н2О(ж).
DSo, Дж/моль•К 213,6 130,6 186,19 69,96
На основании следствия из закона Гесса вычисляем стандартные энтальпию и энтропию реакции:
Стандартная энергия Гиббса
DGo 0, следовательно реакция при Т=298 К невозможна.
Температура, при которой становится возможным восстановление Fe2O3
Ответ. Температура начала восстановления Fe2O3 908,8 К.
Пример 3. Возможна ли реакция разложения карбоната кальция СаСО3 при температурах 900 и 1200 К?
Решение. Уравнение реакции разложения СаСО3
СаСО3(к) = СаО(к) + СО2(г)
DSo, Дж/моль•К 92,9 39,7 213,6
По следствию из закона Гесса вычисляем DHor и DSo реакции.
Энергия Гиббса при температурах 900 и 1200 К
DG900 = 177,39 — 900•0,160 = 33,39 кДж
DG900>0, следовательно реакция разложения СаСО3 при Т=900 К невозможна.
Расчет температуры, при которой наступает равновесие системы. Определение направления реакции
Температура наступления равновесия системы
Задача 10.
Термохимическое уравнение реакции: СО(г) + 2H2(г) = CH3OH(ж) + 128 кДж.
Вычислите, при какой температуре наступает равновесие в этой системе?
Решение:
Так как при реакции выделяется тепло, то это экзотермическая реакция. При экзотермических реакциях энтальпия системы уменьшается и ∆H 0 прод. – ∆S 0 исх.
Так как энтропия растет с повышением температуры, то можно считать, что мера беспорядка (– Т∆S). При Р = const и Т = const общую движущую силу процесса, которую обозначают ∆G, можно найти из соотношения:
Находим ∆S. для данной системы:
Из условия равновесия :
∆H = T∆S находим Т = ∆H/∆S.
Ответ: при 385,7 K наступит равновесие в системе.
Определение направления протекания реакции
Задача 11.
Определить направление протекания реакции:
СН4(г) + СО2(г) ⇔ 2СО(г) + 2Н2(г) при стандартных условиях. Вычислить ∆G 0 298
Решение:
В основе термохимических расчетов лежит закон Гесса (1840 г.): тепловой эффект реакции зависит только от природы и физического состояния исходных веществ и конечных продуктов, но не зависит от пути перехода.
В термохимических расчетах применяют чаще следствие из закона Гесса: тепловой эффект реакции (∆Hх.р.) равен сумме энтальпий образования ∆Hобр продуктов реакции за вычетом суммы энтальпий образования исходных веществ с учетом стехиометрических коэффициентов:
т.к. ∆Н для простых веществ равна 0, то выражение принимает вид:
∆G, можно найти из соотношения:
Необходимо рассчитать возможность самопроизвольного протекания реакции при стандартных условиях (Т = 298 K), получим:
Ответ: ∆G = +170,9 кДж. Так как ∆G > 0, следовательно, при стандартных условиях невозможно протекание прямой реакции. Реакция может протекать в обратном направлении.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ



Задача 1.Рассчитайте стандартную энтальпию и стандартную энтропию химической реакции. Определите в каком направлении при 298°К (прямом или обратном) будет протекать реакция Fe2O3(к) +3H2 =2Fe(к) +3H2O(г). Рассчитайте температуру, при которой равновероятны оба направления реакции.
ΔHр-ции = Σ∆H 0 прод – Σ∆H 0 исх. Используя справочные данные стандартных энтальпий веществ, находим:
ΔHр-ции = (2·ΔH 0 Fe+3·ΔH 0 H2O)— (ΔH 0 Fe2O3+3·ΔH 0 H2) = 2·0 + 3·(- 241,82) – (-822,16) — 3·0 = 96,7 кДж.
ΔSр-ции=ΣS 0 прод – ΣS 0 исх. Используя справочные данные стандартных энтропий веществ, находим:
ΔSр-ции = (2·S 0 Fe + 3·S 0 H2O) — (S 0 Fe2O3 + 3·S 0 H2) = 2·27,15 + 3·188,7 – 89,96 — 3·131 = 137,44 Дж/K = 0,13744 кДж/K.
ΔG = ΔH – TΔS= 96,7 – 298 ·0,13744 = 55,75 кДж.
При Т=298°К, ΔG > 0 – реакция не идет самопроизвольно, т.е. реакция будет протекать в обратном направлении.
Чтобы рассчитать температуру, при которой равновероятны оба направления реакции, надо ΔG приравнять к нулю:
ΔH – TΔS = 0, тогда ΔH = TΔS и T= ΔH/ΔS= 96,7/0,13744 = 703,58 K.
При Т=703,58К реакция будет идти равновероятно как в прямом так и в обратном направлении.
Задача 2.Вычислите энергию Гиббса и определите возможность протекания реакции при температурах 1000 и 3000 К. Cr2O3 (т) + 3C (т) = 2Cr (т) + 3CO (г).
Вычисления энергии Гиббса проводим согласно выражению:
Необходимо рассчитать энтальпию и энтропию химической реакции: ΔHр-ции = Σ∆H 0 прод – Σ∆H 0 исх и ΔSр-ции=Σ∆S 0 кон – Σ∆S 0 исх.
Используя справочные данные стандартных энтальпий веществ, находим:
ΔHр-ции = (2·ΔH 0 Cr + 3·ΔH 0 CO) — (ΔH 0 Cr2O3 + 3·ΔH 0 C) = 2·0 + 3·(- 110,6) – (-1141) — 3·0 = 809,2 кДж.
Аналогично, используя справочные данные стандартных энтропий веществ, находим:
ΔSр-ции= (2·S 0 Cr + 3·S 0 CO) — (S 0 Cr2O3 +3·S 0 C)=23,6+3·197,7– 81,2 — 3·5,7 = 542 Дж/K = 0,542 кДж/К.
Найдем энергию Гиббса при 1000 К:
ΔG1000 = ΔH – TΔS= 809,2 – 1000 · 0,542 = 267,2 кДж
ΔG1000 > 0, следовательно, реакция самопроизвольно не идет.
Найдем энергию Гиббса при 3000 К:
ΔG3000= ΔH – TΔS = 809,2 – 3000 · 0,542 = — 816,8 кДж
ΔG3000 ˂0, следовательно, реакция протекает самопроизвольно.
Задача 3.Чем можно объяснить, что при стандартных условиях, невозможна экзотермическая реакция: СО2(г)+Н2(г) ↔ СО (г)+Н2О (ж)? Рассчитайте ΔG данной реакции. При каких температурах данная реакция становится самопроизвольной?
Рассчитаем ΔG данной реакции:
Для этого сначала определим ΔH и ΔS реакции:
ΔHр-ции = Σ∆H 0 прод – Σ∆H 0 исх и ΔSр-ции=ΣS 0 прод – ΣS 0 исх.
Используя справочные данные стандартных энтальпий и энтропий веществ, находим:
Найдем энергию Гиббса при стандартных условиях
ΔG> 0, следовательно, реакция самопроизвольно не идет.
Задача 4.Рассчитав на основании табличных данных ΔG и ΔS, определите тепловой эффект реакции: 2NO (г) +Cl2(г) ↔ 2NOCl(г). С чем будет более интенсивно взаимодействовать газообразный хлористый водород (в расчете на 1 моль): с алюминием или с оловом? Ответ дайте, рассчитав ΔG 0 обеих реакций. Продуктами реакций являются твердая соль и газообразный водород.
Рассчитаем ΔG 0 для реакции взаимодействия газообразного хлористого водорода (в расчете на 1 моль) с алюминием:
ΔG 0 р-ции = ΣΔG 0 прод — ΣΔG 0 исх
ΔG 0 р-ции1 =(2·ΔG 0 AlCl3 +3·ΔG 0 H2) — (2·ΔG 0 Al + 6·ΔG 0 HCl)
Рассчитаем ΔG 0 для реакции взаимодействия газообразного хлористого водорода (в расчете на 1 моль) с оловом:
ΔG 0 р-ции2 =(ΔG 0 SnCl2(т) + ΔG 0 H2) — (ΔG 0 Sn + ΔG 0 HCl)
Обе реакции имеют ΔG0˂0, поэтому они протекают самопроизвольно в прямом направлении, но более интенсивно взаимодействовать газообразный хлористый водород будет с алюминием, т.к ΔG 0 р-ции1 ˂ ΔG 0 р-ции2

Задача 5.Не прибегая к вычислениям, определите, какие знаки (>0,