Пищевая химия
Пищевая химия (лекция 8)
1. Белки мяса и молока
Наиболее распространенным белком в животном мире является коллаген (кожа, сухожилия, кровеносные сосуды, кости, роговица глаз, хрящи). Он обеспечивает внеклеточную структуру в соединительной животной ткани, существуя не менее чем в пяти различных типах. Коллаген внеклеточный белок, но синтезируется он внутри клетки в виде молекул-предшественников.
Близкий по свойствам к коллагену, в эластичных фибриллах соединительной ткани обнаружен белок эластин, содержащийся в связках и стенках кровеносных сосудов. Этот белок беден пролином.
Мясо, содержащее много соединительной ткани, остается жестким и после тепловой обработки; усвояемость коллагена и эластина в нем очень низкая. Однако при необходимости усилить двигательную функцию кишечника целесообразно использовать продукты, богатые соединительной тканью.
Желатин – продукт неполного гидролиза коллагена. По аминокислотному составу желатин неполноценен, но желеобразные продукты из него перевариваются без напряжения секреции пищеварительных органов. Данное свойство позволяет применять желатин в диетах щадящего режима.
Молоко – это гетерогенная система, в которой в качестве дисперсной фазы выступают эмульгированные жировые глобулы и коллоидные мицеллы казеина, а в роли дисперсионной среды – раствор белков, лактозы, солей и витаминов. Общее содержание белков в молоке колеблется от 2,9 до 3,5 %. Среди них выделяют две основные группы: казеины и сывороточные белки.
В молоке содержится более 20 ферментов, а также гормоны и белки в составе оболочек жировых шариков.
Основными белками молока являются казеины, которые легко перевариваются и являются источниками незаменимых аминокислот, кальция, фосфора и ряда физиологически активных пептидов. Например, при действии в желудке на κ-казеин химозина высвобождаются глико- и фосфопептиды, которые регулируют секрецию желудочного сока, моделируют физико-химические свойства белков, осуществляют защиту от протеолиза и влияют на проницаемость мембран клеток. Важнейшими физиологическими функциями обладают сывороточные белки. Иммуноглобулины выполняют защитную функцию, лактоферрин и лизоцим являются носителями антибактериальных свойств, лактоферрин и β-лактоглобулин выполняют транспортную роль, перенося в кишечник микро- и макроэлементы, витамины и липиды.
Казеин в молоке содержится в виде казеинаткальциевого фосфатного комплекса.
Кальций в составе комплекса выполняет роль структурообразователя, создавая мостик между серинфосфатными группами двух молекул казеина. Казеин молока осаждается при рН 4,6-4,7, когда на его молекулах наступает равенство положительных и отрицательных зарядов. Нерастворимый казеин обладает способностью связывать воду в достаточно больших количествах, что важно для устойчивости частиц белка в сыром, пастеризованном или стерилизованном молоке. Гидрофильные свойства казеина усиливаются при взаимодействии его с β-лактоглобулином, которые наблюдаются в процессе тепловой обработки молока, и от них зависят структурно-механические свойства сгустков, образующихся при кислотном свертывании или получении сырной массы при созревании сыров.
Промышленные казеины получают из обезжиренного молока действием кислот, кисломолочной сыворотки, введением солей кальция, химозина и др. В зависимости от способа получения различают казеинат натрия, казеинат кальция, кислотный, сычужный казеин и копреципитат с разными функциональными свойствами. При производстве новых форм белковой пищи большое значение имеет гелеобразование казеина, его взаимодействие с веществами небелковой природы, образование стойких эмульсий и явление синерезиса.
Белки молока характеризуются высокой биологической ценностью, они содержат в избыточных количествах лизин и триптофан с одновременным недостатком серосодержащих аминокислот. Белки сыворотки содержат незаменимые аминокислоты в значительно больших количествах, чем казеин.
Белковый компонент питания детей первого года жизни
Одним из наиболее важных факторов для развития здорового ребенка является рациональное вскармливание. Во многом физическое и интеллектуальное развитие малыша будет зависеть от характера его вскармливания в раннем возрасте.
Одним из наиболее важных факторов для развития здорового ребенка является рациональное вскармливание. Во многом физическое и интеллектуальное развитие малыша будет зависеть от характера его вскармливания в раннем возрасте. Не вызывает сомнения, что самой лучшей пищей для ребенка грудного возраста является молоко матери. Оно обеспечивает ребенка всеми питательными веществами, которые ему нужны первые 6 мес жизни. В грудном молоке содержатся питательные вещества, которые удовлетворяют все пищевые потребности ребенка: незаменимые полиненасыщенные жирные кислоты, молочные белки и железо в легкоусвояемой форме, гормоны, олигосахариды, факторы роста, нуклеотиды, высокоактивные ферменты, факторы иммунной защиты: иммуноглобулины (Ig) — IgA, IgM, IgG, а также лизоцим, С3-компонент комплемента, лейкоциты. Кроме того, естественное вскармливание способствует формированию собственного иммунитета малыша. Женское молоко полностью приспособлено к возможностям пищеварительного тракта младенца. Состав человеческого грудного молока непостоянен и зависит от срока гестации, на котором произошли роды, меняется на протяжении периода кормления, зависит от времени суток и многих других факторов. Естественно, человеческое грудное молоко превосходит все заменители, в том числе детские питательные смеси промышленного производства. Грудное молоко нельзя воссоздать, но можно максимально приблизить к нему состав адаптированной молочной смеси.
При разработке рецептуры молочных смесей обычно учитываются рекомендации ВОЗ — FAO (Food and Agriculture Organization )/WHO (World Health Organization) Codex Alimentarius Commission, Европейского научного общества педиатров-гастроэнтерологов, гепатологов и нутрициологов (European Society for Pediatric Gastroenterology, Hepatology and Nutrition (ESPGAN)), FDA (Food and Drug Administration) и др. В настоящее время промышленным способом выпускаются молочные смеси для вскармливания детей первых 6 мес, которые отличаются высокой степенью адаптации, и так называемые последующие — для вскармливания детей старше 6-месячного возраста. При создании молочной смеси для искусственного вскармливания здорового ребенка необходимо не только провести качественную и количественную адаптацию белкового, жирового и углеводного компонентов молока, но также обогатить смесь витаминами, минеральными веществами, включая макро- и микроэлементы.
Адаптация молочных смесей на основе коровьего молока для вскармливания грудного ребенка должна включать в себя модификацию белкового компонента в виде снижения содержания белка, обогащения сывороточными белками, коррекции аминокислотного состава, включения нуклеотидов; углеводного компонента — добавление олигосахаридов, коррекция уровня лактозы в зависимости от вида смеси; жирового компонента — обогащение полиненасыщенными жирными кислотами ω-3 и ω-6. Также корригируется уровень витаминов, микроэлементов, соотношение и концентрации кальция и фосфора.
Белок — особый компонент питания ребенка. В первую очередь он является источником азота и аминокислот, которые необходимы для синтеза собственных белков и построения тканей живого организма. Содержание белка в грудном молоке в первые дни лактации высокое, в дальнейшем этот показатель постепенно снижается. В последние годы в большинстве развитых стран по рекомендации ВОЗ принята норма потребности белка для детей грудного и раннего возраста, которая составляет 1,99 г/кг/сут в первый месяц и 0,78 г/кг/сут к концу первого года жизни. Рекомендованная в России потребность в белке для детей грудного возраста в первом полугодии жизни составляет от 2,2 до 2,6 г/кг/сут. В большинстве «стартовых» смесей содержание белка в 100 мл составляет 1,2–1,6 г, тогда как в 100 мл женского молока содержится 1,1 г белка. Снижение уровня белка в смесях позволяет уменьшить в 2 раза избыток поступления азота в организм ребенка и соответственно предотвращает метаболический стресс как дополнительную нагрузку на незрелые почки и печень, снижает риск развития ожирения и сахарного диабета у детей, оптимально приближает белок в смесях по количеству и качеству к белку грудного молока (11 г/л).
Основными белковыми фракциями молока являются казеины (α-казеины, β-казеины) и протеины сыворотки (α-лактальбумин, β-лактоглобулин, γ-глобулины, лактоферрин и др.). Казеины термостабильны и не меняют своей структуры при створаживании молока. Протеины сыворотки относятся к видоспецифичным белкам, термолабильны. Соотношение сывороточных белков и казеина в материнском молоке составляет в среднем 60:40 и в молочных смесях, производимых в Европе для детей первого полугодия жизни, оно выдерживается, что способствует лучшей усвояемости белка и снижению риска кишечных колик. Во втором полугодии жизни ребенка, когда «созревает» желудочно-кишечный тракт, нередко используются «казеиновые смеси» с соотношением сывороточных белков и казеина 35:65 или 20:80. Сывороточные заменители грудного молока более физиологичны, чем казеиновые, так как образуют более нежный сгусток в желудке, быстро эвакуируются из желудка, легко усваиваются, способствуют формированию нормальной микрофлоры кишечника, содержат незаменимые аминокислоты. Наиболее предпочтительным является обогащение смесей a-лактальбумином — основным белком сывороточной фракции грудного молока (25–35% от общего белка); α-лактальбумин поставляет в организм ребенка триптофан, метионин и цистеин, улучшает связывание и ускоряет всасывание кальция и цинка, способствует образованию пептидов с антибактериальными и иммунорегулирующими свойствами, стимулирует рост бифидофлоры в кишечнике ребенка. Состояние иммунной системы и биоценоза кишечника у детей, получающих смесь с добавлением a-лактальбумина, соответствует состоянию детей на грудном вскармливании.
Ранее снижение уровня белка в смесях до его уровня в грудном молоке приводило к дефициту некоторых незаменимых аминокислот. Обеспечение минимального необходимого содержания некоторых эссенциальных аминокислот требовало увеличения количества белка в смеси, что приводило к увеличению содержания других аминокислот и усилению метаболической нагрузки на почки и печень ребенка. На данный момент в смесях, содержащих в своем составе a-лактальбумин («Бэби Cэмп 1» и «Бэби Сэмп 2», «Сэмпер Лемолак», «Сэмпер Бифидус») (Швеция), достигнуто оптимальное соотношение уровня и качества белка для грудного ребенка: содержание белка снижено до 13 г/л, аминокислотный состав максимально приближен к грудному молоку. Кроме того, лучшее усвоение белка в смеси «Лемолак» достигается еще и за счет наличия в ее составе небольшого количества лимонной кислоты. При растворении смеси «Сэмпер Лемолак» водой происходит расщепление нестойкой молекулы лимонной кислоты (в желудок ребенка она не попадает), которая инициирует процесс денатурации белка. В процессе денатурации белковая молекула не разрушается, но происходит трансформация четвертичной структуры белка в третичную, что сопровождается образованием нежных белковых хлопьев, которые хорошо усваиваются в результате облегченного расщепления протеолитическими ферментами.
Смесями, содержащими α-лактальбумин, являются также «НАН ГА 1» и «НАН ГА 2» (Швейцария), ориентированные на детей с высоким риском аллергии. Главной особенностью этих смесей является снижение содержания в них белка до 12 г/л за счет модификации аминокислотного спектра путем удаления из молочной сыворотки казеин-гликомакропептида (белок, характеризующийся дефицитом триптофана и избытком треонина) и обогащения a-лактальбумином. Это позволило, с одной стороны, увеличить уровень триптофана в смеси, а с другой — существенно снизить уровень треонина. α-глобулином также обогащены смеси «Нутрилон Пепти ТСЦ» (Голландия) с уровнем белка 18 г/л и «Алфаре» (Швейцария) с уровнем белка 21 г/л, предназначенные для вскармливания детей с непереносимостью белков коровьего молока, синдромом нарушенного кишечного всасывания, гипотрофией различной степени и другими расстройствами пищеварения.
Кроме того, смеси классифицируются в зависимости от степени расщепления (гидролиза) белка. Смеси на основе гидролизатов белка получают путем ферментативного гидролиза белкового субстрата, что позволяет существенно снизить его антигенность, причем чем выше степень гидролиза, тем ниже антигенная агрессивность смеси. После достижения необходимой степени гидролиза смесь пептидов различной длины и аминокислот очищается от нерасщепленных молекул и их фрагментов ультрафильтрацией, центрифугированием и обработкой на адсорбентах. При этом задаются необходимые степень гидролиза, состав и размер пептидов, состав и процентное соотношение аминокислот, удаляются нежелательные примеси. Смеси могут быть частичного или глубокого гидролиза. По клиническим показаниям гидролизаты подразделяются на профилактические, лечебно-профилактические и лечебные, что определяется глубиной гидролиза и другими особенностями состава. Гидролизу может подвергаться как сывороточная, так и казеиновая часть белкового компонента смеси. К профилактическим смесям относятся смеси «Нутрилон Гипоаллергенный 1» и «Нутрилон Гипоаллергенный 2» (Голландия), «Нутрилон Комфорт 1» и «Нутрилон Комфорт 2» (Голландия), «НАН ГА 1» и «НАН ГА 2» (Швейцария). К лечебно-профилактическим можно отнести такие смеси как «ХиПП ГА 1» и «ХиПП ГА 2» (Германия), «Хумана ГА 1» и «Хумана ГА 2» (Германия). Лечебные смеси на основе гидролизата сывороточных белков — это «Нутрилон Пепти ТСЦ» (Голландия), «Алфаре» (Швейцария), «Фрисопеп» (Голландия); на основе казеина — «Энфамил Нутрамиген» (США), «Фрисопеп АС» (Голландия). Смеси на основе полного гидролиза могут использоваться как для лечения, так и для профилактики непереносимости белков молока, в то время как смеси на основе неполного гидролиза рекомендуются только в качестве профилактики пищевой аллергии. Кроме того, эти смеси, обладающие высокой пищевой ценностью и усвояемостью, могут использоваться не только у детей с пищевой аллергией, но и при гипотрофиях, синдроме нарушенного кишечного всасывания. Следует отметить, что, несмотря на все преимущества лечебных смесей, их большим недостатком является горький вкус, что затрудняет перевод ребенка на данный вид питания.
Все гидролизные смеси обогащены комплексом микроэлементов, витаминов, незаменимых аминокислот и удовлетворяют требованиям ВОЗ по составу нутриентов для вскармливания детей первого года жизни. Таким образом, современные гидролизаты являются адаптированными и полноценными заменителями грудного молока.
В практике питания детей с пищевой аллергией к белкам коровьего молока нашли применение смеси на основе изолята белка сои.
Изолят соевого белка промышленного производства лишен ингибитора трипсина и трудноперевариваемых углеводов (раффинозы, стахиозы), содержащихся в соевых бобах и вызывающих у детей раннего возраста метеоризм и диарею. Во все смеси на основе гидролизата белка сои обязательно вводится метионин, так как его содержание в соевом изоляте снижено. Современные соевые смеси обогащены витаминами, минеральными веществами, микроэлементами, таурином в количествах, удовлетворяющих потребности детей первого года жизни.
К смесям на основе соевого белка относятся «Нутрилон Соя» (Голландия), «Хумана СЛ» (Германия), «Энфамил Соя» (США), «Алсой» (Швейцария), «Симилак-Изомил» (Росс Лабораториз, США), «Фрисосой» (Фризленд Фудс, Голландия), «СМА» (США).
Соевые смеси имеют более низкую стоимость по сравнению с «гидролизатами», однако при применении этих смесей необходимо помнить, что у большого числа детей с непереносимостью белков коровьего молока развивается и непереносимость белков сои. При тяжелом течении пищевой аллергии, как правило, наблюдается поливалентная сенсибилизация к широкому спектру пищевых белков. В связи с этим в настоящее время применение смесей на основе соевого изолята считается нерациональным и может быть лишь крайней мерой при невозможности применить смесь на основе гидролизата белков.
Немаловажен для нормального развития грудного ребенка и аминокислотный состав адаптированной смеси, особенно это касается первых месяцев жизни малыша. Дефицит любой из незаменимых аминокислот в пищевом рационе неизбежно ведет к нарушению синтеза белка. При нарушении сбалансированности аминокислотного состава синтез белков также нарушается, что ведет к задержке роста и развития организма.
Лимитирующей аминокислотой, определяющей во многом адекватность белка в продукте, является триптофан, уровень которого в грудном молоке выше, чем в белках коровьего молока, входящих в состав смесей. Это одна из важнейших природных аминокислот. Триптофан является предшественником серотонина и определяет уровень его синтеза в организме — одного из важнейших нейромедиаторов головного мозга, необходимого для формирования его структур. Он также способствует синтезу мелатонина, влияющего на формирование циркадных ритмов и нормализацию фаз сна и бодрствования ребенка, участвует в процессе вырабатывания ниацина — витамина В3 и никотиновой кислоты (витамин РР). В небольших количествах триптофан входит в состав γ-глобулинов, фибриногена, казеина и других белков, способствует увеличению синтеза гормона роста.
Смеси для детей первого полугодия жизни обязательно должны быть обогащены таурином — серосодержащей аминокислотой, присутствующей в грудном молоке. Эта аминокислота необходима для синтеза новых тканей, она способствует клеточной пролиферации. Таурин стимулирует развитие нервной ткани, рост, дифференцировку сетчатки глаза, надпочечников, эпифиза, гипофиза, слухового нерва. Он принимает участие в защите клеточных мембран от экзогенных токсинов; обладает мембраностабилизирующим и антитоксическим действием. Большую роль таурин играет в процессе конъюгации желчных кислот, повышении иммунного ответа за счет стимулирования фагоцитарной активности нейтрофилов. Отмечено и положительное воздействие таурина на сократительную способность миокарда (влияет на распределение внутриклеточных потоков ионов кальция). Таурин необходим детям первых месяцев жизни, особенно недоношенным, родившимся с признаками морфофункциональной незрелости, детям с постгипоксическим повреждением центральной нервной системы. Метионин служит важнейшим донором лабильных метильных групп, необходимых для построения активного липотропного соединения — холина; синтеза пиримидинового основания — тимина; построения биогенного амина — адреналина; метаболизма никотиновой аминокислоты и гистамина.
Лейцин и изолейцин — предшественники ацетоуксусной кислоты — представителя кетоновых тел. Тирозин — предшественник катехоламинов — адреналина, норадреналина, допамина. Из него также образуются гормон щитовидной железы тироксин и пигментное вещество меланин. Из гистидина синтезируется гистамин — медиатор аллергического воспаления. Включение в состав смеси глутаминовой кислоты и аргинина активизирует процессы созревания слизистой оболочки кишечника и повышает эффективность усвоения пищевых веществ; аргинин дополнительно способствует созреванию иммунной системы.
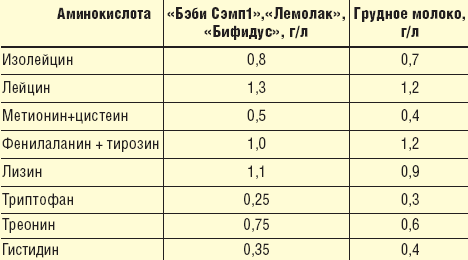
В последнее время на рынке появились смеси, максимально приближенные по аминокислотному составу к «золотому стандарту» — грудному молоку. Примером такого оптимального соотношения количества белка и аминокислотного состава могут служить адаптированные смеси «Сэмпер» (Швеция), в которых при уровне белка 13 г/л содержатся все необходимые аминокислоты в максимально приближенном к грудному молоку количестве. При этом избыток общего количества аминокислот составляет всего 0,65 г/л (табл.). Другим примером сбалансированного аминокислотного состава являются продукты «Нутриция» (Голландия), содержащие в своем составе оптимальный набор аминокислот и других биологически значимых веществ, в том числе таурина, инозитола, L-карнитина L-аргинина (продукты «Нутрилон 1», «Нутрилон 2» и «Нутрилон 3», «Нутрилон Комфорт 1» и «Нутрилон Комфорт 2», «Нутрилон гипоаллергенный 1» и «Нутрилон гипоаллергенный 2», «Нутрилон Пепти ТСЦ» (Голландия).
Еще одним важным составляющим современных адаптированных смесей являются нуклеотиды. Эти соединения играют ключевую роль во многих биохимических внутриклеточных процессах. Они могут синтезироваться в организме из предшественников (пуринов, пиримидинов, некоторых аминокислот) или образовываться в результате деградации одних нуклеотидов и ресинтеза новых. Нуклеотиды являются структурными компонентами ДНК и РНК. Нуклеотиды выполняют роль регуляторов различных процессов биосинтеза, являясь универсальным источником энергии, что важно для быстрорастущего организма ребенка. Кроме того, они способствуют созреванию иммунной системы и формированию иммунного ответа организма, усиливают фагоцитоз, активируют лимфоциты, могут повышать естественную активность клеток-киллеров, улучшают неспецифический иммунитет. Нуклеотиды влияют на созревание клеток кишечного эпителия и ворсинок, формирование благоприятной кишечной микрофлоры. Все это приводит к нормализации и оптимизации процессов усвоения пищевых веществ, в частности, кальция и железа. Кроме того, нуклеотиды входят в состав нуклеиновых кислот, где служат мономерными единицами и являются носителями генетического кода ДНК и РНК. В основном в смесях для вскармливания детей до года нуклеотидный компонент представлен цитидин-монофосфатом, гуанозин-монофосфатом, инозин-монофосфатом, уридин-монофосфатом, аденозин-монофосфатом. Нуклеотиды особенно необходимы в случаях, когда недостаточен их эндогенный запас: при тяжелых инфекциях, у детей с последствиями перинатальной энцефалопатии, при дисфункциях иммунитета, болезнях накопления.
На современном этапе большой выбор адаптированных смесей с различными свойствами для вскармливания грудных детей позволяет педиатру подобрать наиболее адекватное питание, соответствующее потребностям конкретного ребенка. Но необходимо помнить, несмотря на высокую степень адаптации данных смесей: ни одна из них не превосходит по качеству грудное молоко.
По вопросам литературы обращайтесь в редакцию.
Л. А. Анастасевич
С. В. Бельмер, доктор медицинских наук, профессор
РГМУ, Москва
Противоречия эстетической медицины. 6. Методы скинтайтинга: миф о схлопывании коллагеновых волокон
И. Кругликов, доктор физико-математических наук, «Веллкомет ГмбХ», Германия
Статья публикуется с разрешения доктора И. Кругликова и журнала KOSMETICHE MEDIZIN (4/2013), Германия
1 ВВЕДЕНИЕ
Неинвазивные и минимально инвазивные аппаратные методы лечения находят все большее применение в эстетической медицине. Некоторые из этих методов, особенно те, которые предназначены для подтяжки кожи, декларируют долгосрочную модификацию коллагеновой сети как основную цель их применения. Этот эффект может быть достигнут, в частности, за счет конформационных изменений в коллагеновых структурах, вызываемых локальным выделением тепла в ткани-мишени. Одно из таких конформационных изменений – так называемое схлопывание коллагеновых структур – эффект, который практически всеми лазерными и радиочастотными методами подтяжки кожи заявляется в качестве основы их воздействия. Несмотря на то что молекулы коллагена действительно изменяют свою конфигурацию при нагревании и при этом даже могут существенно схлопываться (что было продемонстрировано во многих исследованиях in vitro и in vivo), действительный вклад этого феномена в наблюдаемые клинические результаты после применения различных методов подтяжки кожи остается спорным.
2 МЕХАНИЗМЫ ИЗМЕНЕНИЯ КОЛЛАГЕНОВЫХ СТРУКТУР ПОД ВОЗДЕЙСТВИЕМ ВНЕШНИХ ФАКТОРОВ
Сшитый (зрелый) коллаген – важная составная часть соединительной ткани, а его содержание определяет механические свойства и стабильность этой ткани. Содержание коллагена в ткани сильно зависит от скорости его обновления, которое протекает на разных уровнях – от активирования матричной рибонуклеиновой кислоты и синтеза проколлагена до производства зрелой коллагеновой сетки. Причем первые стадии этого процесса очень неустойчивы и могут чувствительно реагировать на различные физические факторы [1, 2]. Свободные белки проколлагена нестабильны, их внутримолекулярные связи слабы и могут быть ферментативно, а также под воздействием физических факторов расщеплены. Эти белки сами по себе не играют роли в механических свойствах соединительной ткани, поскольку только коллагеновые волокна, образующиеся путем фибриллогенеза, формируют механически ригидные и ферментативно устойчивые структуры (которые связаны также гликозаминогликанами и потому могут эффективно управлять накоплением воды в тканях).
Общепризнанно, что содержание коллагена в соединительной ткани с возрастом непрерывно уменьшается, что может иметь драматические последствия для ее механических свойств. Снижение содержания коллагена, а также деформация коллагеновой сетки ведут к возникновению крупнозернистой и несовершенной пространственной структуры, ригидность которой соответственно уменьшается. Искусственное уплотнение и упрочение этой сетки теоретически должно было бы привести к подтяжке кожи, а значит, и к улучшению ее внешнего вида.
Существуют три основные возможности добиться таких изменений. Некоторые из них могут быть реализованы в долгосрочной перспективе, другие – в среднесрочной или краткосрочной.
Смещение равновесия между формированием и разрушением соединительной ткани
Эта стратегия в долгосрочной перспективе может привести к стабильному обновлению коллагеновой сетки. Смещение в направлении разрушения соединительной ткани развивается в течение длительного времени вследствие разных заболеваний, действия солнечного излучения, а также по мере старения. Обратного развития этого процесса можно добиться путем целевого стимулирования фибробластов при одновременном подавлении матриксных металлопротеиназ, отвечающих за разрушение коллагена. Однако следует учесть, что обновление зрелой коллагеновой сетки в коже протекает в квазифизиологических условиях крайне медленно c периодом полураспада коллагена около 15 лет [3], поэтому такое обновление кожи может произойти только спустя длительное время [1].
Локальное повреждение соединительной ткани, которое приводит к образованию рубцов и соответствующему изменению натяжения кожи Именно такие изменения типичны при проведении минимально инвазивных омолаживающих процедур – лазерных (Fraxel и др.), радиочастотных и других. Эффект подтяжки кожи должен возникнуть при этом в среднесрочной перспективе (от недель до нескольких месяцев) и по времени должен коррелировать с образованием рубцов в соединительной ткани.
Модификация внутри- или межмолекулярных связей в коллагене в целях воздействия на структуры коллагеновой сетки на уровне отдельных коллагеновых молекул, коллагеновых фибрилл и/или коллагеновых волокон
Самым известным примером такой модификации является обратимая или необратимая денатурация коллагена под воздействием тепла, которая терапевтически применяется для укрепления слабой соединительной ткани в нестабильных суставных капсулах с помощью термической капсулорафии, а также в термокератопластике и для подтяжки кожи (Skin Tightening) в эстетической медицине. При массивной денатурации коллагена подтяжка соединительной ткани должна возникнуть сразу или через непродолжительное время после проведения процедуры.
Наиболее важные методы скинтайтинга в эстетической медицине основываются на локальном повышении температуры, причем в связи с этим следует различать следующие виды нагрева: с помощью воды, лазерный, ультразвуковой и радиочастотный. Хотя в основе этих методов лежат разные физические механизмы передачи энергии (а значит, и распределение энергии в тканях происходит по-разному), в конечном итоге все они осуществляют некоторое тепловое воздействие на целевую область.
Практически все эстетические методы коррекции, основанные на выделении тепла, декларируют схлопывание коллагеновых волокон как наиболее важный механизм их действия, не только обеспечивающий надежную теоретическую базу для этих методов, но и обосновывающий получение быстрого и относительно долгосрочного эффекта. Данное объяснение было перенято у достаточно хорошо изученных неинвазивных или минимально инвазивных методов (например, у капсулорафии) без критического анализа различий в распределении энергии и длительности воздействия. При этом часто игнорируется и тот факт, что схлопывание коллагеновых волокон зависит от многих, как правило, плохо контролируемых параметров и при квазифизиологических температурах в живом организме может быть в действительности реализовано лишь очень ограниченно. Так, для большинства применяемых на практике радиочастотных методов
коррекции время местного воздействия составляет менее 10 секунд, а во многих случаях оно лежит даже в миллисекундном диапазоне. В большинстве же исследований in vitro и клинических исследованиях по применению капсулорафии при температуре 60–70° C используется время воздействия в минутном диапазоне. Кроме того, обычно не принимается во внимание и то, что денатурированные молекулы коллагена не могут долго оставаться в ткани и должны быть элиминированы аутогенными желатиназами, что должно достаточно быстро снизить достигнутый эффект, если бы он действительно возникал от схлопывания коллагеновых волокон.
Все это порождает законный вопрос: насколько реально схлопывание коллагеновых волокон при проведении неинвазивных эстетических процедур. Этот вопрос становится особенно актуальным в свете все большей популярности радиочастотных методов эстетической коррекции независимо от используемых технических решений, связанных с моно-, би-, три- или даже мультиполярным расположением электродов.
3 ТЕРМИЧЕСКАЯ СТАБИЛЬНОСТЬ КОЛЛАГЕНА
Молекулы проколлагена состоят из трех полипептидных цепей, которые с помощью слабых внутримолекулярных связей образуют тройную спиральную структуру (три закрученные в левую сторону спирали составляют суперспираль, закрученную в правую сторону). Слабые внутримолекулярные связи (водородные мостики) возникают между глицинами одной спирали и пролинами другой, так что на каждый триплет приходится обычно один водородный «мостик». Такие тройные спиральные структуры могут в дальнейшем организоваться и удерживаться в параллельно расположенных структурах более высокого порядка – микрофибриллах (состоящих из 5 молекул проколлагена) и фибриллах, а также в коллагеновых волокнах, где их связывают уже альдегидные мостики, которые являются существенно более прочными, чем водородные. Только такие зрелые фибриллярные структуры, а не проколлагены могут отвечать за механические свойства соединительной ткани.
Тройные спирали коллагена формируют матриксные структуры различных типов тканей и при нормальных температурах тела остаются термически и механически относительно стабильными. Поэтому длительное время предполагалось, что эти молекулы обладают маргинальной термостабильностью и денатурируют лишь при температурах, на несколько градусов Цельсия превосходящих температуру тела. Однако в настоящее время многое говорит в пользу того, что температура денатурации (TD) тройных спиралей проколлагена на самом деле ниже температуры тела [4]. Если это действительно так, то можно предположить, что молекулы проколлагена уже при температуре тела не существуют в устойчивой для них форме тройной спирали, а должны иметь стохастическую (случайную) структуру. Как только молекулы проколлагена выделяются из клетки, они сразу же начинают распадаться. Предполагается, что это может быть связано с отсутствием стабилизирующих белков теплового шока. Такой быстрый распад объясняет, почему абсолютное большинство вновь синтезированных молекул проколлагена снова спонтанно распадаются и никогда не образуют зрелых фибриллярных структур.
Итак, нагревание при квазифизиологических температурах приводит к тому, что неустойчивые внутримолекулярные связи разрушаются, хотя при этом межмолекулярные сшивки могут сохраняться и дальше. Таким образом происходит денатурация коллагена, часто называемая также схлопыванием коллагеновых волокон, – коллагеновые фибриллы теряют свою внутреннюю спиральную структуру, схлопываются вдоль главной оси и в дальнейшем удерживаются вместе в основном за счет внутримолекулярных связей. Подобное конформационное изменение соответствует переходу коллагена из высокоорганизованной кристаллообразной структуры в гелеобразное (денатурированное) состояние.
Разрушение молекул коллагена по механизму обратной связи приводит к активации фибриллогенеза (образованию коллагеновых фибрилл из отдельных молекул проколлагена), что позволяет вновь стабилизировать коллагеновые структуры. Так из нестабильных молекул проколлагена могут быть образованы стабильные структуры коллагена [5].
Как уже было сказано, квазифизиологическое нагревание ткани может усилить распад молекул проколлагена. Однако этот процесс в первую очередь затронет именно свободные молекулы проколлагена и не должен привести к существенному изменению зрелой коллагеновой сетки, для термической модификации которой потребуются намного более высокие температуры. Зрелый коллаген денатурирует обычно при температуре 60–65° C. Здесь имеется в виду так называемая температура перехода, при которой денатурируют 50% всех молекул коллагена. Поскольку конформационные изменения происходят в температурном диапазоне 10–12° C, первые переходы, как правило, могут наблюдаться уже при температуре на 5–6° C ниже среднего значения TD. Это определяет абсолютный предел минимально эффективной температуры денатурации коллагена в соединительной ткани на уровне 55° C.
Предельная температура, при которой наблюдаются первые признаки денатурации зрелого коллагена во время эстетической процедуры, зависит от различных контролируемых и неконтролируемых параметров – скорости нагрева- ния, гидратации ткани, стресса, предшествующих процедур и т.д. Снижение TD всего на 1° C способно уменьшить длительность распада коллагена с нескольких дней до нескольких часов, вследствие чего может существенно измениться динамический баланс между распадом коллагена и образованием коллагеновых фибрилл.
К этому добавляется еще один важный момент: изменения в структуре коллагена во время нагревания в зависимости от температуры и длительности воздействия могут быть либо обратимыми, либо необратимыми. Умеренное и относительно краткосрочное повышение температуры приводит к локальным изменениям во внутримолекулярной структуре молекул коллагена, которые, однако, регенерируют спустя некоторое время после процедуры (обратимые изменения), если, конечно, прежде эти поврежденные молекулы не были расщеплены ферментативно. При более высоких температурах в молекулах коллагена возникают необратимые структурные изменения, в результате чего они больше не могут спонтанно восстановиться. Такие денатурированные коллагеновые структуры могут быть элиминированы только посредством матриксных металлопротеиназ.
4 УСЛОВИЯ СХЛОПЫВАНИЯ КОЛЛАГЕНОВЫХ МОЛЕКУЛ: ЗАВИСИМОСТЬ ОТ РАЗЛИЧНЫХ ПАРАМЕТРОВ
Результат нагревания коллагена в большой степени зависит от различных параметров.
Наиболее важными из них являются:
– максимальная температура в ткани;
– длительность воздействия;
– механический стресс во время нагревания;
– содержание коллагена и ориентация коллагеновых волокон;
– возраст соединительной ткани;
– значение pH в ткани;
– степень гидратации ткани.
Максимальная температура и длительность нагрева
Чем выше температура, до которой нагреваются коллагеновые структуры, тем короче время, необходимое для получения одинакового модифицирующего эффекта. Так, нагрев in vitro коллагена из плечевого сустава при температуре воды 65° C в течение 10 минут приводит к 10%-ному схлопыванию его волокон, а нагревание до 80° C уже через 1,5 минуты способно вызвать 60%-ную денатурацию коллагена.
Похожий эксперимент по воздействию на такие же коллагеновые пробы радиочастотным током продемонстрировал другие значения: при нагревании пробы до 65° C произошло схлопывание менее 4% коллагеновых волокон, а при ее нагревании до 80° C – 14% [6]. А при исследовании коллагеновых проб из сухожилий крысиных хвостов [7] денатурация коллагена произошла при еще более низкой температуре: через 1,5 минуты нагрева до 58° C денатурировало менее 10% коллагена, а через 9 минут – уже почти 50%.
Исследования in vitro демонстрируют при этом еще один эффект – так называемый эффект плато: при достижении определенной степени денатурации дальнейшего разрушения коллагеновых волокон не происходит, несмотря на последующее повышение температуры.
Если принять во внимание, что повышение температуры всего лишь до 45° C уже существенно влияет на витальность клеток, то представляется совершенно невероятным, что схлопывание коллагена во время неинвазивных радиочастотных процедур (которые, как правило, не вызвают в тканях локальных ожогов) может быть главной причиной часто наблюдаемого на практике эффекта подтяжки кожи.
Механический стресс
Если ткань во время нагревания подвергается механическому стрессу, то температура денатурации коллагена при прочих равных условиях может отчетливо меняться. Если при этом степень нагрева и длительность теплового воздействия демонстрируют качественно схожее воздействие на деградацию коллагена, то влияние механического стресса может проявиться в снижении процентного количества денатурированных коллагеновых волокон при одинаковой длительности нагрева (или в увеличении необходимой длительности нагрева для достижения той же степени денатурации).
Этот эффект может быть объяснен переориентированием коллагеновых волокон под воздействием механического стресса. Действительно, механический стресс может существенно изменить физические свойства ткани и вызвать искусственную анизотропию в направлении натяжения. Этот феномен может играть важную роль при практическом применении некоторых методов подтяжки кожи (например, при комбинации радиочастотного воздействия с вакуумом).
Содержание коллагена и ориентирование коллагеновых волокон
Чем выше содержание коллагена в ткани и чем упорядоченное расположены фибриллы, тем более высокие температуры или более длительное время нагрева будут необходимы, чтобы добиться одной и той же степени модификации коллагена. Это может объяснить, почему результаты температурного воздействия (например, при применении радиочастотного тока) на различных участках тела могут отличаться. Участки с особенно правильно упорядоченными коллагеновыми волокнами в значительной степени анизотропны. Известным примером могут служить так называемые линии Лангера, которые определяют не только предпочтительное направление образования кожных складок или рубцов при повреждении кожи, но и поглощения тканью света [8]. При такой анизотропии выбранное направление прохождения электрического тока или распространения света (параллельно или перпендикулярно локальной ориентации коллагеновых волокон) может оказывать существенное влияние на результаты коррекции.
Возраст и значение pH ткани
Восстанавливаемые ковалентные альдегидные связи с возрастом заменяются на невосстанавливаемые мультивалентные связи. Последние значительно более стабильны и для своего разрушения требуют существенно более высоких температур. Это служит еще одной причиной того, что реакция старческой кожи на температурное воздействие заметно слабее, чем молодой.
Умеренное изменение значения pH ткани в щелочном направлении может привести к существенному повышению температуры денатурации коллагена. Поэтому все дополнительные методы воздействия, которые могут вызвать хотя бы временное снижение pH кожи, должны демонстрировать усиление эффекта от коррекции с применением обсуждаемых здесь методов.
Гидратация ткани
Уже давно известно, что дополнительная гидратация ткани приводит к усилению денатурации коллагена при одинаковых температурах нагрева [9]. Ведущие к этому изменения не до конца понятны, однако можно предположить, что свободные молекулы водорода образуют дополнительные связи с деформированными молекулами коллагена, за счет чего последние больше не в состоянии самопроизвольно восстанавливаться.
Снижение гидратации ткани с возрастом приводит к тому, что реакция старческой кожи на тепловое воздействие протекает значительно хуже, чем молодой. Соответственно дополнительные методы воздействия, ведущие к увеличению содержания воды в ткани перед ее нагревом, должны положительно сказываться на результатах коррекции.
Впрочем, гидратация ткани может и сама изменяться при повышении (в определенных пределах) температуры. Это связано, в частности, с тем, что при температурах выше 42° C в ткани происходит дополнительное производство эндогенной гиалуроновой кислоты [10], которое коррелирует с локальной выработкой белков теплового шока. Добавочное связывание воды новопроизведенной гиалуроновой кислотой ведет к краткосрочному увеличению тургора кожи в районе коррекции, что может повлечь за собой отчетливое, но также относительно краткосрочное улучшение состояния кожи после ее подтяжки радиочастотными токами.
Все это показывает, что денатурация коллагеновых волокон зависит от очень многих параметров и в неодинаковых условиях может протекать совершенно по-разному. Если данный процесс взять за теоретическую основу тепловой трансформации соединительной ткани при применении аппаратных методов подтяжки кожи, то становится очевидно, что результаты лечения разных пациентов должны сильно различаться и, таким образом, будут практически непредсказуемы.
5 МОРФОЛОГИЧЕСКИЕ И МЕХАНИЧЕСКИЕ ИЗМЕНЕНИЯ В ТЕРМИЧЕСКИ ПОВРЕЖДЕННОЙ ТКАНИ
В термически поврежденной ткани в результате денатурации коллагена обычно происходят следующие морфологические изменения:
– размножение и миграция фибробластов (фиброплазия);
– замена нативных бимодальных коллагеновых структур (состоящих из коллагеновых волокон малых и больших диаметров) преимущественно мелкими коллагеновыми волокнами.
Оба этих процесса характерны для заживления ран и образования рубцов, однако они возникают только при настоящем повреждении ткани. Эти же два процесса обеспечивают решающие различия между неинвазивным омоложением кожи и заживлением ран – процессами, которые часто сравнивают друг с другом. Поскольку при продолжительном нагревании ткани при температуре выше 60° C должна происходить не только денатурация коллагеновых волокон, но и массовая гибель клеток, после успешной процедуры радиочастотной коррекции в области обработки теоретически должны наблюдаться как некроз ткани, так и фиброплазия. Впрочем, это скорее исключение, чем правило.
Если бы эффект подтяжки кожи после коррекции радиочастотными токами можно было в основном объяснить денатурацией коллагеновых волокон, то денатурация коллагена должна была бы сочетаться с повышенной упругостью (сопротивлением деформации) кожи. Однако эксперименты показывают совершенно обратное: при подтвержденной денатурации коллагена кожа теряет свою упругость. Более того, известно, что потеря упругости соединительной ткани положительно коррелирует со степенью денатурации коллагеновых волокон (см. обсуждение в [6]). Недавно было также показано, что под влиянием нагрева кожа может по-разному вести себя при растяжении и сжатии: если при растяжении упругость кожи заметно понижается с повышением температуры, то при ее сжатии происходит совершенно обратное [11].
Все это означает, что настоящая термическая денатурация коллагена, хотя и может приводить к краткосрочному увеличению плотности ткани, одновременно должна вызывать ухудшение ее механических свойств, что в капсулорафии даже рассматривается как послеоперационный риск. Такого ухудшения механических свойств кожи после неинвазивного или минимально инвазивного лечения радиочастотным током на практике не наблюдается, что само по себе должно поставить под вопрос всю теорию денатурации коллагеновых волокон как основу тепловых методов подтяжки кожи. Но если существенное механическое ослабление кожи после применения тех или иных неинвазивных методов тепловой коррекции будет действительно установлено, они больше не смогут оцениваться как безопасные из-за возникающих в связи с этим рисков.
6 ВЫВОДЫ
Гипотеза о том, что схлопывание (денатурация) коллагеновых волокон является основной причиной подтяжки кожи при применении различных неинвазивных (прежде всего, связанных с радиочастотным воздействием) методов коррекции должна рассматриваться как крайне сомнительная.
Во-первых, необходимая для этого температура и длительность воздействия находятся далеко за пределами того, что фактически обеспечивают большинство приборов.
Во-вторых, настоящая денатурация коллагеновых волокон должна сопровождаться массовой гибелью клеток в области обработки, чего клинически почти никогда не наблюдается.
В-третьих, существенная зависимость степени денатурации коллагеновых волокон от самых разных параметров сделала бы результаты коррекции очень вариабельными и практически непредсказуемыми.
В-четвертых, массовое схлопывание коллагеновых структур привело бы к значительной потере локальной упругости кожи, которая наблюдалась бы сразу после проведения такой коррекции и привела бы к развитию некоторых побочных явлений.
Хотя феномен денатурации коллагеновых волокон после нагревания действительно существует и во многих исследованиях in vitro и in vivo был надлежащим образом подтвержден, вопрос о том, может ли он быть главной причиной получения клинических результатов, наблюдаемых после применения описанных методов коррекции, все еще остается предметом дискуссии. Даже в капсулорафии нет единого мнения о том, отвечает ли за укрепление сустава непосредственно денатурация коллагеновых волокон или это, скорее, заслуга последующей фиброплазии, заживления ран и образования рубцов [6]. В пользу второго варианта говорит то, что итоговые результаты можно увидеть лишь через несколько месяцев после лечения. Более того, в [12] было показано, что лечение ахиллова сухожилия радиочастотным током не вызывает денатурации коллагеновых волокон, тем не менее существенное укрепление пролеченного сухожилия было достигнуто через 8 недель после выполнения процедур.
В качестве главного механизма, лежащего в основе термических методов подтяжки кожи, происходящей непосредственно во время или вскоре после проведения процедуры, намного более реалистичным представляется не денатурация коллагеновых волокон, а активация местного синтеза гиалуроновой кислоты. Ее выработка ведет к накоплению воды и соответствующему увеличению тургора кожи в области коррекции – быстровозникающему эффекту, почти моментально улучшающему состояние кожи. Несмотря на то что такая быстрая выработка гиалуроновой кислоты относится к неспецифическим реакциям и в большей или меньшей степени должна была бы возникать при всех типах нагревания ткани, она в значительной мере зависит от конкретного типа распределения тепла в ткани, а также от потенциальной способности соединительной ткани к подобному синтезу, которая в стареющей коже, как правило, существенно снижается. Последнее может обусловливать известный возрастной предел эффективности при применении подобных методов коррекции.