Так ли страшен токсокароз, как его малюют?
Даценко Светлана Александровна
Подписаться на email-рассылку
Спасибо за подписку!
Тема паразитарных инфекций вызывает очень живой интерес. Почему-то среди людей очень распространено мнение, что все мы заражены гельминтами, простейшими, и обязательно нужно чиститься. Достаточно много встречается вопросов о токсокарозе. Поэтому сегодня хотелось бы подробно разобрать эту тему, чтобы не оставалось опасений, и не было бесполезного, а иногда и вредного самолечения.
Что это за болезнь
Токсокароз — это паразитарная инфекция, вызванная круглыми червями токсокарами. Вообще это болезнь животных, преимущественно семейства псовых. Человек для токсокар — биологический тупик.
Это значит, что в организме человека токсокары не способны развиться до половозрелой особи и существуют только в форме личинок. Соответственно, размножения паразитов не происходит, яиц они не выделяют и человек не является источником инфекции ни для других людей, ни для окружающей среды.
Токсокароз — достаточно распространённое заболевание среди животных. Заболеваемость людей зависит от числа больных животных и частоты контакта с ними. Так, в европейских странах носителями токсокар являются 2-5% населения, а на Тайване, Карибах, в Колумбии — 50-80% населения. При этом носительство не равно заболеванию.
Заражение собак происходит при:
Токсокара откладывает около 20 0000 яиц в сутки. Они попадают на почву и растения, а оттуда на шерсть собак. Человек заражается при контакте с собакой либо во время работы с почвой, травой. Чаще всего это происходит летом на отдыхе или на даче.
В группе риска находятся охотники, рыбаки, дачники, а также дети, часто играющие в песочницах.
Так выглядят половозрелые токсокары, обитающие в кишечнике собак
Развитие болезни
Яйца после заглатывания попадают в кишечник. Здесь из них выходят личинки и с током крови разносятся по органам. Иммунный ответ организма подавляет активность личинок. Вокруг них образуются капсулы, и личинки токсокар находятся в них в спящем состоянии. Такое бессимптомное носительство может длиться десятки лет, паразит при этом не оказывает никакого негативного действия на организм человека.
При ослаблении иммунной защиты происходит активизация личинок, они начинают мигрировать по разным органам. При этом токсокары вызывают аллергические реакции, а также механическое повреждение тканей и воспалительный процесс.
Проявления болезни
Симптоматика наблюдается только при активизации личинок. При их нахождении в спящем состоянии клиники нет. Соответственно, лечение требуется только при наличии симптомов, так как уничтожить капсулированные личинки невозможно. Это очень важный момент, потому что попытки лечить антитела к токсокарам без клиники приносят только вред.
Симптоматика:
В общем анализе крови наблюдается увеличение эозинофилов от 20 до 85%. В биохимическом анализе крови завышены печёночные трансаминазы, билирубин, снижен уровень белка.
Формы токсокароза
Глазная форма
Личинки находятся в тканях глаза. Редкая форма болезни, проявляется хроническими воспалительными процессами — кератит, неврит, увеит. Активный токсокароз вызывает ухудшение зрения, косоглазие. Чаще поражается один глаз.
Неврологическая форма
Возникает при поражении личинками головного мозга. Еще более редкая форма, развивается преимущественно у людей с иммунодефицитом. Проявляется двигательными расстройствами, судорогами, эпилептическими припадками, нарушениями психики.
Кожная форма
Бывает только активной — это миграция личинок внутри кожи. Встречается редко, проявляется видимым продвижением личинок под кожей.
Висцеральный токсокароз
Личинки находятся во внутренних органах, чаще всего это печень, кишечник, лёгкие. Это самая частая форма заболевания.
Диагностика
Одного анализа на антитела к токсокарам недостаточно, чтобы поставить диагноз. Как и в случае с другими паразитарными инфекциями, распространённость частных лабораторий играет злую шутку.
Не нужно обследоваться на токсокароз, если у вас нет вышеуказанных симптомов. А если вы обследованы и антитела найдены — не нужно бежать в аптеку и просить « что-нибудь от токсокар » . Правильное действие — сходить к инфекционисту.
Прежде всего нужно определить, есть ли вообще риск заражения. Если вы всю жизнь провели в городе, на дачу не ездите и не имеете собаки — риска заражения нет. Токсокары воздушно-капельным путем не передаются. Если же вы входите в одну из групп риска — переходим к следующему этапу.
Это оценка симптоматики. Если у вас есть какие-то из указанных жалоб или симптомов — сдаём анализы.
Необходимые анализы:
Токсокароз — одна из немногих паразитарных инфекций, где сдавать анализ кала не нужно. В просвете кишечника токсокары не живут, яиц не выделяют — искать в кале нечего.
Про изменения в общем и биохимическом анализе мы поговорили выше. Можно еще сдать кровь на общий IgE — он будет завышен в 2-3 раза. Теперь разберём анализ крови на антитела. Диагностический титр — 1:800 и выше. Уточнение — сдавать качественный анализ, то есть где ответ выдают в виде « 0,6 » или « 4,5 » или еще какой-нибудь цифры, не нужно. Этот анализ говорит лишь о том, обнаружены или не обнаружены в вашем организме антитела к токсокарам. Для постановки диагноза нужен именно количественный анализ, то есть титр. Еще одно уточнение — при глазной форме диагностическим будет титр 1:200 и выше.
То есть, если у вас нет никаких жалоб на здоровье, но вы решили сдать кровь на токсокароз и обнаружили титр 1:400 — можно убрать этот результат в сторонку и не беспокоиться. А вот если у вас есть вялотекущее воспаление глаз, ухудшается зрение, и вы при обследовании на токсокароз получили тот же титр 1:400 — нужно шагать к инфекционисту.
Лечение
Расписывать препараты здесь не буду, конечно же. Я не пропагандирую ни самолечение, ни самодиагностику. Расскажу в общих чертах. Лечение проводится обычно амбулаторно. Основные препараты, естественно, антигельминтики. В зависимости от преобладающей симптоматики назначаем антигистаминные, гепатопротекторы, пробиотики. По завершении лечения проводим анализ на антитела. Критерием выздоровления является улучшение самочувствия и снижение уровня антител до 1:400 и ниже, в случае глазного токсокароза до 1:100.
Клинический пример
Глазного токсокароза мне встретить пока не довелось, все-таки форма достаточно редкая. А вот висцеральный полечить пришлось. На консультацию ко мне отправили женщину, 56 лет. Около полугода она лечилась у дерматолога по поводу хронической крапивницы. Периодически возникал дискомфорт в животе, редкие поносы. В общем анализе крови уровень эозинофилов был от 15 до 25 за полгода. Дерматолог назначил пациентке обследование на гельминтозы и был выявлен титр антител к токсокарам 1:1600.
При опросе выяснилось, что у пациентки есть дача, где она проводит все летние месяцы и часть осени. Собак у нее нет, но у соседей по даче есть. Учитывая все эти данные, можно было без сомнений поставить диагноз токсокароза. Пациентка прошла курс лечения, через две недели после его завершения сдала кровь на антитела. На повторном приеме отметила исчезновение высыпаний и зуда. Титр антител снизился до 1:400. Для контроля я назначила ей сдать кровь еще раз через три месяца.
В качестве заключения еще раз напомню — мы живём не в Индии, не в Африке и не в Таиланде. Население России не заражено поголовно гельминтами. У нас нет необходимости профилактического приема антигельминтных препаратов.
Профилактика токсокароза — это лечение домашних животных и тщательное соблюдение личной и пищевой гигиены. Диагностировать и лечить токсокароз может только врач-инфекционист.
ТОКСОКАРОЗ: современный подход
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
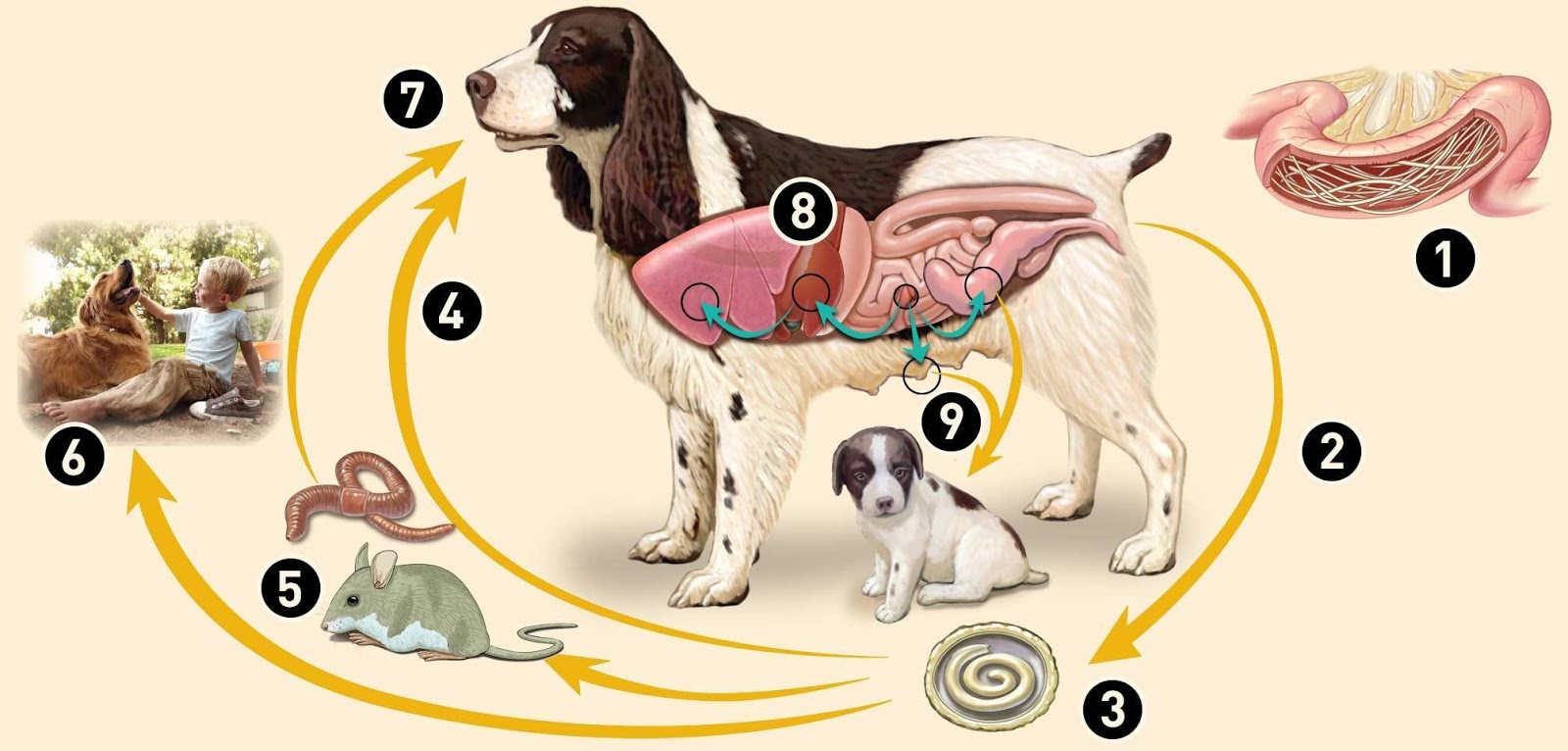
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека. Симптоматика токсокароза малоспецифична и имеет сходство с клиническими симптомами острой фазы других гельминтозов. Заболевание обычно развивается внезапно и остро или после короткой продромы проявляется в виде легкого недомогания. Появляется температура — субфебрильная в легких случаях и высокая до 39°С и выше, иногда с ознобом, — в тяжелых случаях инвазии. Могут наблюдаться кожные высыпания в виде крапивницы или полиморфной сыпи, иногда отеки типа Квинке. В остром периоде наблюдается легочный синдром различной степени тяжести: от легких катаральных явлений до острого бронхита, пневмонии, тяжелых приступов удушья. Особенно тяжело легочный синдром протекает у детей раннего возраста. Рентгенологически выявляется усиление легочного рисунка, «летучие» инфильтраты, картина пневмонии. Наряду с этим у части больных отмечается увеличение печени, иногда и селезенки. Лимфаденопатия более выражена у детей. Иногда имеет место абдоминальный синдром в виде приступов болей в животе, симптомов диспепсии. Возможно развитие миокардита, панкреатита. Известны случаи поражения щитовидной железы, проявляющиеся симптомами опухоли. Возможно поражение мышечной ткани с развитием болезненных инфильтратов по ходу мышц. При миграции личинок в головной мозг развиваются симптомы поражения ЦНС: упорные головные боли, эпилептиформные приступы, парезы, параличи. У детей заболевание сопровождается слабостью, легкой возбудимостью, нарушением сна.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).