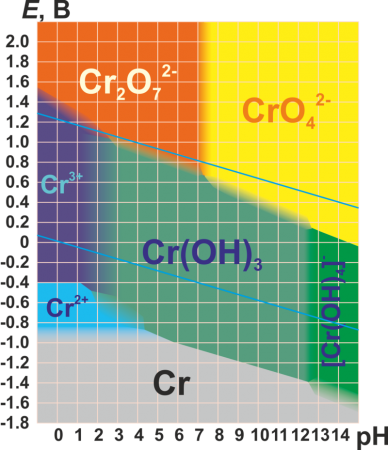
Физические свойства и механические характеристики металла хром и его соединений
Хром – не конструкционный материал, но используется довольно широко за счет того, что обладает превосходными антикоррозийными свойствами. Хромирование защищает любой другой сплав от ржавчины. Кроме того, легирование сталей хромом придает им такую же стойкость к коррозии, которая свойственна и самому металлу.
Итак, давайте обсудим сегодня, каковы технические и окислительные характеристики материала хром, основные амфотерные, восстановительные свойства и получение металла также будут затронуты. А еще мы узнаем, каково влияние хрома на свойства стали.
Особенности металла
Хром – металл 4 периода 6 группы побочной подгруппы. Атомный номер 24, атомная масса – 51, 996. Это твердый металл серебристо-голубоватого цвета. В чистом виде отличается ковкостью и вязкостью, но малейшие примеси азота или углерода придают ему хрупкость и твердость.
Для него характерна объемно-центрированная кубическая решетка. Фазовые переходы отсутствуют. При температуре в 1830 С возможен переход к гранецентрированной решетке.
Однако у хрома есть одна интересная аномалия. При температуре в 37 С некоторые физические свойства металла резко меняются: изменяется электросопротивление, коэффициент линейного расширения, падает до минимума модуль упругости и повышается внутреннее трение. Связано это с прохождением точки Нееля: при этой температуре вещество меняет свои антиферромагнитные свойства на парамагнитные, что представляет собой переход первого уровня и означает резкое увеличение объема.
Химические свойства хрома и его соединений описаны в этом видео:
Химические и физические свойства хрома
Температура плавления и кипения
Физические характеристики металла зависят от примесей до такой степени, что сложным оказалось установить даже температуру плавления.
Ниже будет дана общая характеристика физических и магнитных свойств металла хром.
Общие свойства и характеристики хрома
Физические особенности
Хром относится к наиболее устойчивым из всех тугоплавких металлов.
Далее представлена краткая характеристика теплофизических свойств хрома.
Теплофизические характеристики
Как правило, тугоплавкие металлы имеют высокий уровень теплопроводности и, соответственно, низкий коэффициент теплового расширения. Однако хром заметно отличается по своим качествам.
В точке Нееля коэффициент теплового расширения совершает резкий скачок, а затем с увеличением температуры продолжает заметно расти. При 29 С (до скачка) величина коэффициента составляет 6.2 · 10-6 м/(м•K).
Теплопроводность подчиняется этой же закономерности: в точке Нееля она падает, хотя и не столь резко и уменьшается с возрастанием температуры.
Электрические свойства
Несмотря на нетипичное «поведение» теплопроводности хром является одним из лучших проводников тока, уступая по этому параметру только серебру, меди и золоту.
До точки Нееля – 38 С, вещество является антиферромагнетиком, то есть, под действием магнитного поля и при его отсутствии никаких магнитных свойств не проявляется. Выше 38 С хром становится парамагнетиком: проявляет магнитные свойства под действием внешнего магнитного поля.
Токсичность

Хром – обязательный легирующий элемент при получении нержавеющих и жаропрочных сталей. Его способность противостоять коррозии и передавать это качество сплавам остается самым востребованным качеством металла.
Химические свойства соединений хрома и его окислительно-восстановительные свойства рассмотрены в этом видео:
При какой температуре плавится хром
Кристаллы (99,999%) хрома различной формы, полученные разложением йодида хрома.
Хром — твёрдый металл голубовато-белого цвета. Хром иногда относят к чёрным металлам. Этот металл способен окрашивать соединения в разные цвета, потому и был назван «хром», что означает «краска». Хром – микроэлемент, необходимый для нормального развития и функционирования человеческого организма. Важнейшая его биологическая роль состоит в регуляции углеводного обмена и уровня глюкозы в крови.
СТРУКТУРА
Кристаллическая структура хрома
В зависимости от типов химической связи — как и все металлы хром имеет металлический тип кристаллической решетки, то есть в узлах решетки находятся атому металла.
В зависимости от пространственной симметрии — кубическая, объемно-центрированная а = 0,28839 нм. Особенностью хрома является резкое изменение его физических свойств при температуре около 37°С. Кристаллическая решетка металла состоит из его ионов и подвижных электронов. Аналогично атом хрома в основном состоянии имеет электронную конфигурацию. При 1830 °С возможно превращение в модификацию с гранецентрированной решеткой, а = 3,69Å.
СВОЙСТВА
Хром имеет твердость по шкале Мооса 9, один из самых твердых чистых металлов (уступает только иридию, бериллию, вольфраму и урану). Очень чистый хром достаточно хорошо поддаётся механической обработке. Устойчив на воздухе за счёт пассивирования. По этой же причине не реагирует с серной и азотной кислотами. При 2000 °C сгорает с образованием зелёного оксида хрома(III) Cr2O3, обладающего амфотерными свойствами. При нагревании реагирует со многими неметаллами, часто образуя соединения нестехиометрического состава карбиды, бориды, силициды, нитриды и др. Хром образует многочисленные соединения в различных степенях окисления, в основном +2, +3, +6. Хром обладает всеми характерными для металлов свойствами — хорошо проводит тепло, электрический ток, имеет присущий большинству металлов блеск. Является антиферромагнетиком и парамагнетиком, то есть, при температуре 39 °C переходит из парамагнитного состояния в антиферромагнитное (точка Нееля).
ЗАПАСЫ И ДОБЫЧА
Самые большие месторождения хрома находятся в ЮАР (1 место в мире), Казахстане, России, Зимбабве, Мадагаскаре. Также есть месторождения на территории Турции, Индии, Армении, Бразилии, на Филиппинах.nГлавные месторождения хромовых руд в РФ известны на Урале (Донские и Сарановское). Разведанные запасы в Казахстане составляют свыше 350 миллионов тонн (2 место в мире)Хром встречается в природе в основном в виде хромистого железняка Fe(CrO2)2 (хромит железа). Из него получают феррохром восстановлением в электропечах коксом (углеродом). Чтобы получить чистый хром, реакцию ведут следующим образом:
1) сплавляют хромит железа с карбонатом натрия (кальцинированная сода) на воздухе;
2) растворяют хромат натрия и отделяют его от оксида железа;
3) переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
4) получают чистый оксид хрома восстановлением дихромата натрия углём;
5) с помощью алюминотермии получают металлический хром;
6) с помощью электролиза получают электролитический хром из раствора хромового ангидрида в воде, содержащего добавку серной кислоты.
ПРОИСХОЖДЕНИЕ
ПРИМЕНЕНИЕ
Хром — важный компонент во многих легированных сталях (в частности, нержавеющих), а также и в ряде других сплавов. Добавка хрома существенно повышает твердость и коррозийную стойкость сплавов. Использование Хрома основано на его жаропрочности, твердости и устойчивости против коррозии. Больше всего Хрома применяют для выплавки хромистых сталей. Алюмино- и силикотермический Хром используют для выплавки нихрома, нимоника, других никелевых сплавов и стеллита.
Значительное количество Хрома идет на декоративные коррозионно-стойкие покрытия. Широкое применение получил порошковый Хром в производстве металлокерамических изделий и материалов для сварочных электродов. Хром в виде иона Cr 3+ — примесь в рубине, который используется как драгоценный камень и лазерный материал. Соединениями Хрома протравливают ткани при крашении. Некоторые соли Хрома используются как составная часть дубильных растворов в кожевенной промышленности; PbCrO4, ZnCrO4, SrCrO4 — как художественные краски. Из смеси хромита и магнезита изготовляют хромомагнезитовые огнеупорные изделия.
Используется в качестве износоустойчивых и красивых гальванических покрытий (хромирование).
Хром применяется для производства сплавов: хром-30 и хром-90, незаменимых для производства сопел мощных плазмотронов и в авиакосмической промышленности.
При какой температуре плавится хром
| Название, символ, номер | Хром / Chromium (Cr), 24 |
|---|---|
| Атомная масса (молярная масса) | 51,9961(6) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d 5 4s 1 |
| Радиус атома | 130 пм |
| Ковалентный радиус | 118 пм |
| Радиус иона | (+6e)52 (+3e)63 пм |
| Электроотрицательность | 1,66 (шкала Полинга) |
| Электродный потенциал | −0,74 |
| Степени окисления | 6, 3, 2, 0 |
| Энергия ионизации (первый электрон) | 652,4 (6,76) кДж/моль (эВ) |
| Плотность (при н. у.) | 7,19 г/см³ |
| Температура плавления | 2130 K |
| Температура кипения | 2945 K |
| Уд. теплота плавления | 21 кДж/моль |
| Уд. теплота испарения | 342 кДж/моль |
| Молярная теплоёмкость | 23,3 Дж/(K·моль) |
| Молярный объём | 7,23 см³/моль |
| Структура решётки | кубическая объёмноцентрированая |
| Параметры решётки | 2,885 Å |
| Температура Дебая | 460 K |
| Теплопроводность | (300 K) 93,9 Вт/(м·К) |
| Номер CAS | 7440-47-3 |

Содержание
История
Происхождение названия
Название элемент получил от греч. χρῶμα — цвет, краска — из-за разнообразия окраски своих соединений.
История
Открыт на Среднем Урале, в Березовском золоторудном месторождении. Впервые упоминается в труде М. В. Ломоносова «Первые основания металлургии» (1763 год), как красная свинцовая руда, PbCrO4. Современное название — крокоит. В 1797 году французский химик Л. Н. Воклен выделил из него новый тугоплавкий металл (скорее всего, Воклен получил карбид хрома).
Нахождение в природе
Хром является довольно распространённым элементом в земной коре (0,012 % по массе). Основные соединения хрома — хромистый железняк (хромит) FeO·Cr2O3. Вторым по значимости минералом является крокоит PbCrO4.
Месторождения
Самые большие месторождения хрома находятся в ЮАР (1-е место в мире), Казахстане, России, Зимбабве, Мадагаскаре. Также есть месторождения на территории Турции, Индии, Армении, Бразилии, на Филиппинах.
Главные месторождения хромовых руд в РФ известны на Урале (Донские и Сарановское).
Разведанные запасы в Казахстане составляют свыше 350 миллионов тонн (2-е место в мире).
Геохимия и минералогия
Среднее содержание хрома в различных изверженных породах резко непостоянно. В ультраосновных породах (перидотитах) оно достигает 2 кг/т, в основных породах (базальтах и др.) — 200 г/т, а в гранитах десятки г/т. Кларк хрома в земной коре 83 г/т. Он является типичным литофильным элементом и почти весь заключен в минералах типа хромшпинелидов. Хром вместе с железом, титаном, никелем, ванадием и марганцем составляют одно геохимическое семейство.
Различают три основных минерала хрома: магнохромит (Mg, Fe)Cr2O4, хромпикотит (Mg, Fe)(Cr, Al)2O4 и алюмохромит (Fe, Mg)(Cr, Al)2O4. По внешнему виду они неразличимы, и их неточно называют «хромиты». Состав их изменчив:
Собственно, хромит, то есть FeCr2O4 сравнительно редок. Помимо различных хромитов, хром входит в состав ряда других минералов — хромовой слюды (фуксита), хромового хлорита, хромвезувиана, хромдиопсида, хромтурмалина, хромового граната (уваровита) и др., которые нередко сопровождают руды, но сами промышленного значения не имеют. В экзогенных условиях хром, как и железо, мигрирует в виде взвесей и может накапливаться в глинах. Наиболее подвижной формой являются хроматы.
Получение
Хром встречается в природе в основном в виде хромистого железняка Fe(CrO2)2 (хромит железа). Из него получают феррохром восстановлением в электропечах коксом (углеродом):
Fe(CrO2)2 + 4C → Fe + 2Cr + 4CO
Феррохром применяют для производства легированных сталей.
Чтобы получить чистый хром, реакцию ведут следующим образом:
1) сплавляют хромит железа с карбонатом натрия (кальцинированная сода) на воздухе:
4Fe(CrO2)2 + 8Na2CO3 + 7O2 → 8Na2CrO4 + 2Fe2O3 + 8CO2
2) растворяют хромат натрия и отделяют его от оксида железа;
3) переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
4) получают чистый оксид хрома восстановлением дихромата натрия углём:
Na2Cr27 + 2C → Cr2O3 + Na2CO3 + CO
5) с помощью алюминотермии получают металлический хром:
Cr2O3 + 2Al → Al2O3 + 2Cr + 130kcal
6) с помощью электролиза получают электролитический хром из раствора хромового ангидрида в воде, содержащего добавку серной кислоты. При этом на катодах совершаются в основном 3 процесса:
Физические свойства
В свободном виде — голубовато-белый металл с кубической объёмноцентрированной решёткой, a = 0,28845 нм. Ниже температуры 38 °C является антиферромагнетиком, выше переходит в парамагнитное состояние (точка Нееля).
Хром имеет твёрдость по шкале Мооса 5, один из самых твёрдых чистых металлов (уступает только иридию, бериллию, вольфраму и урану). Очень чистый хром достаточно хорошо поддаётся механической обработке.
Изотопы
Природный хром состоит из четырех стабильных изотопов ( 50 Cr (изотопная распространённость 4,345 %), 52 Cr (83.789 %), 53 Cr (9.501 %), 54 Cr (2.365 %)).
Химические свойства
Характерные степени окисления
Для хрома характерны степени окисления +2, +3 и +6 (см. табл.). Практически все соединения хрома окрашены.
| Степень окисления | Оксид | Гидроксид | Характер | Преобладающие формы в растворах | Примечания |
|---|---|---|---|---|---|
| +2 | CrO (чёрный) | Cr(OH)2 (жёлтый) | Основный | Cr 2+ (соли голубого цвета) | Очень сильный восстановитель |
| +3 | Cr2O3 (зелёный) | Cr(OH)3 (серо-зелёный) | Амфотерный | Cr 3+ (зелёные или лиловые соли) | |
| +4 | CrO2 | не существует | Несолеобразующий | — | Встречается редко, малохарактерна |
| +6 | CrO3 (красный) | H2CrO4 | Кислотный | CrO4 2− (хроматы, желтые) | Переход зависит от рН среды. Сильнейший окислитель, гигроскопичен, очень ядовит. |
Простое вещество
Устойчив на воздухе за счёт пассивирования. По этой же причине не реагирует с серной и азотной кислотами. При 2000 °C сгорает с образованием зелёного оксида хрома(III) Cr2O3, обладающего амфотерными свойствами.
Синтезированы соединения хрома с бором (бориды Cr2B, CrB, Cr3B4, CrB2, CrB4 и Cr5B3), с углеродом (карбиды Cr23C6, Cr7C3 и Cr3C2), c кремнием (силициды Cr3Si, Cr5Si3 и CrSi) и азотом (нитриды CrN и Cr2N).
Соединения Cr(+2)
Степени окисления +2 соответствует основный оксид CrO (чёрный). Соли Cr 2+ (растворы голубого цвета) получаются при восстановлении солей Cr 3+ или дихроматов цинком в кислой среде («водородом в момент выделения»):
Все эти соли Cr 2+ — сильные восстановители вплоть до того, что при стоянии вытесняют водород из воды. Кислородом воздуха, особенно в кислой среде, Cr 2+ окисляется, в результате чего голубой раствор быстро зеленеет.
Коричневый или жёлтый гидроксид Cr(OH)2 осаждается при добавлении щелочей к растворам солей хрома(II).
Синтезированы дигалогениды хрома CrF2, CrCl2, CrBr2 и CrI2
Соединения Cr(+3)
Степени окисления +3 соответствует амфотерный оксид Cr2O3 и гидроксид Cr(OH)3 (оба — зелёного цвета). Это — наиболее устойчивая степень окисления хрома. Соединения хрома в этой степени окисления имеют цвет от грязно-лилового (в водных растворах ион Cr 3+ существует в виде аквакомплексов [Cr(H2O)6] 3+ ) до зелёного (в координационной сфере присутствуют анионы).
Cr 3+ склонен к образованию двойных сульфатов вида M I Cr(SO4)2·12H2O (квасцов)
Гидроксид хрома (III) получают, действуя аммиаком на растворы солей хрома (III):
Можно использовать растворы щелочей, но в их избытке образуется растворимый гидроксокомплекс:
Сплавляя Cr2O3 со щелочами, получают хромиты:
Непрокаленный оксид хрома(III) растворяется в щелочных растворах и в кислотах:
При окислении соединений хрома(III) в щелочной среде образуются соединения хрома(VI):
То же самое происходит при сплавлении оксида хрома (III) со щелочью и окислителями, или со щелочью на воздухе (расплав при этом приобретает жёлтую окраску):
Соединения хрома (+4)
При осторожном разложении оксида хрома(VI) CrO3 в гидротермальных условиях получают оксид хрома(IV) CrO2, который является ферромагнетиком и обладает металлической проводимостью.
Среди тетрагалогенидов хрома устойчив CrF4, тетрахлорид хрома CrCl4 существует только в парах.
Соединения хрома (+6)
Степени окисления +6 соответствует кислотный оксид хрома (VI) CrO3 и целый ряд кислот, между которыми существует равновесие. Простейшие из них — хромовая H2CrO4 и двухромовая H2Cr2O7. Они образуют два ряда солей: желтые хроматы и оранжевые дихроматы соответственно.
Оксид хрома (VI) CrO3 образуется при взаимодействии концентрированной серной кислоты с растворами дихроматов. Типичный кислотный оксид, при взаимодействии с водой он образует сильные неустойчивые хромовые кислоты: хромовую H2CrO4, дихромовую H2Cr2O7 и другие изополикислоты с общей формулой H2CrnO3n+1. Увеличение степени полимеризации происходит с уменьшением рН, то есть увеличением кислотности:
Но если к оранжевому раствору K2Cr2O7 прилить раствор щёлочи, как окраска вновь переходит в жёлтую, так как снова образуется хромат K2CrO4:
До высокой степени полимеризации, как это происходит у вольфрама и молибдена, не доходит, так как полихромовая кислота распадается на оксид хрома(VI) и воду:
Растворимость хроматов примерно соответствует растворимости сульфатов. В частности, жёлтый хромат бария BaCrO4 выпадает при добавлении солей бария как к растворам хроматов, так и к растворам дихроматов:
Образование кроваво-красного малорастворимого хромата серебра используют для обнаружения серебра в сплавах при помощи пробирной кислоты.
Известны пентафторид хрома CrF5 и малоустойчивый гексафторид хрома CrF6. Также получены летучие оксигалогениды хрома CrO2F2 и CrO2Cl2 (хромилхлорид).
Соединения хрома(VI) — сильные окислители, например:
Добавление к дихроматам перекиси водорода, серной кислоты и органического растворителя (эфира) приводит к образованию синего монопероксида хрома(VI) CrO5 (CrO(O2)2), который экстрагируется в органический слой; данная реакция используется как аналитическая.
Применение
Хром — важный компонент во многих легированных сталях (в частности, нержавеющих), а также и в ряде других сплавов. Добавка хрома существенно повышает твердость и коррозийную стойкость сплавов.
Используется в качестве износоустойчивых и красивых гальванических покрытий (хромирование).
Хром применяется для производства сплавов: хром-30 и хром-90, незаменимых для производства сопел мощных плазмотронов и в авиакосмической промышленности.
Биологическая роль и физиологическое действие
Хром — один из биогенных элементов, постоянно входит в состав тканей растений и животных. У животных хром участвует в обмене липидов, белков (входит в состав фермента трипсина), углеводов. Снижение содержания хрома в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови.
В чистом виде хром довольно токсичен, металлическая пыль хрома раздражает ткани лёгких. Соединения хрома(III) вызывают дерматиты.
Соединения хрома в степени окисления +6 особо токсичны. Практически вся хромовая руда обрабатывается через преобразование в дихромат натрия. В 1985 году было произведено примерно 136 000 тонн шестивалентного хрома. Другими источниками шестивалентного хрома являются триоксид хрома и различные соли — хроматы и дихроматы. Шестивалентный хром используется при производстве нержавеющих сталей, текстильных красок, консервантов для дерева, при хромировании и пр.
Шестивалентный хром является признанным канцерогеном при вдыхании. На многих рабочих местах сотрудники подвержены воздействию шестивалентного хрома, например, при гальваническом хромировании или сварке нержавеющих сталей. В Европейском союзе использование шестивалентного хрома существенно ограничено директивой RoHS.
Шестивалентный хром транспортируется в клетки человеческого организма с помощью сульфатного транспортного механизма благодаря своей близости к сульфатам по структуре и заряду. Трёхвалентный хром, более часто встречающийся, не транспортируется в клетки.
Внутри клетки Cr(VI) восстанавливается до метастабильного пятивалентного хрома (Cr(V)), затем до трехвалентного хрома (Cr(III)). Трехвалентный хром, присоединяясь к протеинам, создает гаптены, которые включают иммунную реакцию. После их появления чувствительность к хрому не пропадает. В этом случае даже контакт с текстильными изделиями, окрашенными хромсодержащими красками или с кожей, обработанной хромом, может вызвать раздражение кожи. Витамин C и другие агенты реагируют с хроматами и образуют Cr(III) внутри клетки.
Продукты шестивалентного хрома являются генотоксичными канцерогенами. Хроническое вдыхание соединений шестивалентного хрома увеличивает риск заболеваний носоглотки, риск рака лёгких. (Лёгкие особенно уязвимы из-за большого количества мелких капилляров). Видимо, механизм генотоксичности запускается пяти- и трёхвалентным хромом.
В США предельно допустимая концентрация шестивалентного хрома в воздухе составляет 5 мкг/м³ (0,005 мг/м³). В России предельно допустимая концентрация хрома (VI) существенно ниже — 1,5 мкг/м³ (0,0015 мг/м³).
Одним из общепризнанных методов избежания шестивалентного хрома является переход от технологий гальванического хромирования к газотермическому и вакуумному напылению.
Основанный на реальных событиях фильм «Эрин Брокович» режиссёра Стивена Содерберга рассказывает о крупном судебном процессе, связанном с загрязнением окружающей среды шестивалентным хромом, в результате которого у многих людей развились серьёзные заболевания.
Фото соединений хрома:

Хром окись пигментная

Паста ГОИ (содержит Окись хрома)
Калий хромовокислый (калий хромат)

Хромовой ангидрид (Хрома (VI) окись
Хром (III) окись
Хром азотнокислый
Хромокалиевые квасцы
Соединения двухвалентного хрома.
Оксид хрома (II) CrO
Гидроксид хрома (II) Cr(OH)2
Фторид хрома (II) CrF2
Хлорид хрома (II) CrCl2
Бромид хрома (II) CrBr2
Йодид хрома (II) CrI2
Сульфид хрома (II) CrS
Сульфат хрома (II) CrSO4
Соединения трехвалентного хрома.
Оксид хрома (III) Cr2O3
Гидроксид хрома (III) Cr(OH)3
Фторид хрома (III) CrF3
Хлорид хрома (III) CrCl3
Бромид хрома (III) CrBr3
Иодид хрома (III) CrI3
Оксифторид хрома (III) CrOF
Сульфид хрома (III) Cr2S3
Сульфат хрома (III) Cr2(SO4)3
Ортофосфат хрома (III) CrPO4
Соединения четырехвалентного хрома.
Оксид хрома (IV) CrO2
Фторид хрома (IV) CrF4
Хлорид хрома (IV) CrCl4