Что такое «Оловянная чума», и Действительно ли она погубила великую армию Наполеона
Получайте на почту один раз в сутки одну самую читаемую статью. Присоединяйтесь к нам в Facebook и ВКонтакте.
Однако в средневековье объяснения этому явлению люди не могли найти, да и встречались с ним только жители северных стран, поэтому знали о загадочной «болезни» тогда не все. Только этим можно объяснить то, что на протяжении многих сотен лет олово продолжали массово использовать, хотя это и приводило порой к неприятным ситуациям и даже трагедиям. Так, например, буквально «обратился в прах» огромный груз оловянных слитков, отправленный из Голландии в Россию в конце XIX века. По этому поводу даже проводили полицейское расследование, ведь огромный железнодорожный состав, груженый достаточно дорогим металлом стоил немало, а при вскрытии вагонов там нашли лишь серую пыль.
В 1912 году мужественные полярники покорили свою цель, но оказались не первыми – норвежцы обогнали их на месяц. Экспедиция начала долгий путь домой, но, добираясь до «схронов», измученные люди все чаще обнаруживали канистры с топливом пустыми. Наиболее правдоподобной причиной этого несчастья современные историки считают «оловянную чуму». Пайку швов в то время все еще делали из этого ненадежного металла, и, скорее всего, в условиях полярных морозов канистры дали течь. Кстати, команда Амундсена тоже страдала от этого явления, но их экспедиция была лучше организована, и потеря некоторой части керосина не стала критичной. А вот для англичан все закончилось плохо. Нехватка топлива стала для них настоящей катастрофой, и в марте 1912 года мужественные полярники погибли, не сумев преодолеть обратный путь от покоренного ими полюса.
Понравилась статья? Тогда поддержи нас, жми:
www.toy-soldiers.ru
УРА! ОЛОВЯННЫЕ СОЛДАТИКИ!
Олово и мороз: знатоки, подскажите!
Олово и мороз: знатоки, подскажите!
Сообщение Преподобный Рэй Маккол » Пт дек 07, 2012 12:30 pm
Сообщение ДМБ-84 » Пт дек 07, 2012 2:05 pm
Благословенная Википедия сообщает следующее:
При температуре ниже 13,2 °C происходит увеличение удельного объёма чистого олова на 25,6 %, и оно спонтанно переходит в другое фазовое состояние — серое олово (α-Sn), в кристаллической решётке которого атомы располагаются менее плотно. Одна модификация переходит в другую тем быстрее, чем ниже температура окружающей среды. При −33 °C скорость превращений становится максимальной. Олово трескается и превращается в порошок. Причём соприкосновение серого олова и белого приводит к «заражению» последнего. Совокупность этих явлений называется «оловянной чумой». Начало научного изучения этого фазового перехода было положено в 1870 г. работами петербургского учёного Ю. Фрицше. Установлено, что это есть процесс аллотропического превращения белого олова в серое со структурой типа алмаза. Много ценных наблюдений и мыслей об этом процессе высказано Д. И. Менделеевым в его «Основах химии».
Белое олово — серебристо-белый, блестящий металл со специфической тетрагональной структурой и электронным s2p2-состоянием — β-фазой. Серое олово — ковалентный кристалл со структурой алмаза и электронным sp3-состоянием — α-фазой. Фазовые переходы олова из белого в серое и обратно сопровождаются перестройкой электронной структуры и сильным (26,6 %) объёмным эффектом. Белое олово можно переохладить до гелиевых температур (температура фазового α-β-равновесия около +13,2 °C).
Одним из средств предотвращения «оловянной чумы» является добавление в олово стабилизатора, например висмута.
Любопытные факты:
«Оловянная чума» — одна из причин гибели экспедиции Скотта к Южному полюсу в 1912 г. Она осталась без горючего из-за того, что топливо просочилось через запаянные оловом баки, поражённые «оловянной чумой». Нынешнее название этому процессу в 1911 году дал Г. Коэн.
Некоторые историки[кто?] указывают на «оловянную чуму» как на одно из обстоятельств поражения армии Наполеона в России в 1812 г. — сильные морозы привели к превращению оловянных пуговиц на мундирах солдат в порошок.
«Оловянная чума» погубила многие ценнейшие коллекции оловянных солдатиков. Например, в запасниках петербургского музея Александра Суворова превратились в труху десятки фигурок — в подвале, где они хранились, лопнули зимой батареи отопления.
Сообщение Преподобный Рэй Маккол » Пт дек 07, 2012 2:17 pm
Нестойкий оловянный припой. О чуме, погубившей Роберта Скотта, и о других заразных болезнях
«Моей вдове»
Это знаменитое письмо написал в Антарктиде замерзающий Роберт Скотт в конце марта 1912 года. 17 января 1912 года, в ходе второй антарктической экспедиции под названием «Терра Нова», Скотту и горстке его соратников (Эдгару Эвансу, Лоуренсу Отсу, Эдварду Уилсону и Генри Боуэрсу) удалось достичь Южного Полюса, где они обнаружили норвежский флаг и множество собачьих следов (14 декабря 1911 года к полюсу пришла группа Руаля Амундсена, в которой кроме Амундсена были Оскар Вистинг, Хелмер Хансен, Сверре Хассель, Олаф Бьяланд).
Соперничество Амундсена и Скотта, фамилии которых теперь навечно сцеплены дефисом в названии американской антарктической станции «Амундсен-Скотт» прямо на Южном Полюсе — это редкостной выразительности пример, демонстрирующий сокрушительную победу эффективного менеджера над прекраснодушным героем. Амундсен (которого завистники звали «Рекламундсен») продумал свою экспедицию до таких мелочей как закупка варежек. Его палатки не продувались, так как были оснащены ультрасовременными застежками-молниями (которые, кстати, на антарктическом морозе иногда так замерзали, что из палатки было невозможно выбраться без ножа, либо молнию приходилось отогревать снаружи). Расходуя груз и провиант, Амундсен методично расстреливал ездовых собак, оставляя ровно столько, сколько нужно было, чтобы тащить полегчавшие сани, скармливая убитых собак живым. Он называл ледники в честь своих спонсоров и за всю экспедицию не потерял ни одного человека.
Скотт при движении на юг также оставлял «базовые лагеря» с топливом и провиантом для обратного пути. Были там и запасы керосина в канистрах, запаянных оловом. На свою беду полярники не учли феномена оловянной чумы.
Аллотропия
Для химических элементов характерны так называемые «аллотропные изменения» (модификации). В зависимости от условий окружающей среды физические свойства элемента, а также его наблюдаемое состояние, могут сильно меняться. Это связано с переупорядочиванием атомов и, следовательно, с изменением силы связей между ними.
Рассмотрим три характерных примера аллотропной модификации:
Озон и кислород
Обе этих молекулы состоят из атомов кислорода, но плотность озона в 1,5 раза больше, чем у кислорода, и химическая активность также выше. Например, возможна прямая реакция озона с серебром, которая между кислородом и серебром происходить не будет:
Кислород жизненно необходим для человека, а озон в больших концентрациях вреден, хотя, в малых полезен. Озон обладает сильным приятным запахом, а кислород нет.
Графит и алмаз
Как известно, алмаз имеет максимальную твердость по шкале Мооса (10), а графит минимальную (1). Из иллюстрации понятно, что связи между атомами углерода в горизонтальных слоях графита остаются сильными, а в вертикальном разрезе очень слабые, благодаря чему графит снимается послойно, и им удобно писать.
Белый и красный фосфор

Температура плавления красного фосфора составляет 600 °C, тогда как температура плавления белого – всего 44 °C. При этом красный фосфор не воспламеняется до 250 °C, а белый фосфор воспламеняется уже при 45 °C, а при трении – и при более низких температурах.
Таким образом, поразительные отличия разных аллотропных модификаций у фосфора и углерода связаны с тем, что кристаллическая решетка этих элементов может упорядочиваться принципиально разным образом. Фосфор и углерод находятся в центральной части своих периодов в таблице Менделеева, однако являются полноценными неметаллами, будучи расположены в правом верхнем углу таблицы, где сосредоточены элементы с неметаллическими свойствами:
Здесь желтым цветом обозначены неметаллы, зеленым – переходные металлы, розово-желтым – полуметаллы. И также есть олово, которое, в отличие от сурьмы и германия, правильнее считать полноценным металлом. Но оно находится на три периода ниже углерода, поэтому тоже проявляет ярко выраженные аллотропные свойства.
Оловянная чума
Наиболее опасной чертой такой аллотропной модификации олова является заразность. Серое олово при контакте превращает белое олово в серое, если температура остается достаточно низкой. Так, принесенная с мороза оловянная миска, поставленная в шкаф в неотапливаемом помещении, может заразить всю остальную оловянную посуду.
Очень странно, что Роберт Скотт не учел этого обстоятельства – ведь оловянная чума известна давно; есть даже предположение, что именно из-за оловянной чумы, поразившей пуговицы наполеоновской армии в ходе отступления из Москвы, французы оказались в особенно незавидном положении.
Оказывается, что оловянная чума характерна только для химически чистого олова, для защиты от нее достаточно правильно подобрать сплав на основе олова. Например, в наше время широко известен сплав пьютер, предметы из которого были найдены даже в раскопках древнеегипетского культурного слоя. Наиболее качественный пьютер состоит из 95% олова, 2% меди и 3% сурьмы. Именно из такого сплава выполнена статуэтка «Оскар».
Поразительно, но в недавнем прошлом для оловянной чумы нашлось практическое применение, связанное с очисткой лабораторной и промышленной оптики от капелек олова. Капельки чистейшего олова используются в качестве мишеней для плазмы, которая применяется для получения глубокого ультрафиолета, а глубокий ультрафиолет – для вытравливания микросхем. При этом для сборки ультрафиолета в действующий луч используется тончайшая оптика, которая быстро тускнеет, так как на ней конденсируется олово. Оказалось, что именно обработка оптики серым оловом позволяет полностью очистить стекло, не оставив на нем ни малейших царапин. В результате срок службы такого собирающего зеркала значительно увеличивается.
Но оловянная чума – лишь наиболее известная аллотропная болезнь металла. Есть и значительно более экзотические и не менее опасные метаморфозы, о которых я также хочу здесь рассказать.
Цинковая чума
Это явление во многом подобно оловянной чуме и изучено гораздо хуже. Впервые описано примерно в 1920-е годы в среде мастеров и коллекционеров, увлекающихся миниатюрными моделями машин. В чистом виде цинк в производстве практически не используется, а в промышленности применяется как основа сплава «цамак», содержащего также алюминий, магний и медь. Цамак был разработан в США в 1929 году, в СССР и России более употребительно название «ЦАМ» (цинк, алюминий, медь). Правильное соотношение металлов в ЦАМ: цинк 95%, алюминий 4%, медь 1%.
Чума, подобная оловянной, поражает такой сплав не просто при изменении физических условий, но и, по-видимому, неизбежно, если доли металлов в ЦАМ отмерены неправильно. Цинковая чума начинается с характерных вздутий на поверхности металла.
Затем микроструктурные изменения проникают в глубину металла, и он крошится.
Прямая аналогия таких повреждений с оловянной чумой не доказана, хотя, по данным частных экспериментов, прочность металлических моделей после замораживания действительно падает в разы. Согласно другой версии (изложенной здесь, где показаны фотографии с последовательной деградацией модели), ЦАМ заболевает чумой, если в его составе оказывается хотя бы минимальное количество олова или свинца. Если бы эта версия подтвердилась, то означала бы, что оловянная чума заразна даже для цинка, являющегося переходным металлом.
Чаще цинковую чуму связывают с технологическим браком при производстве. Например, в сплаве может быть слишком велика доля алюминия, как в китайских моделях, либо в него могут попадать примеси никеля или сурьмы. То есть, такой сплав уже нельзя считать ЦАМ.
До недавнего времени цинковая чума считалась неизлечимой. Действительно, вздутия на моделях практически необратимы, но болезнь можно затормозить, заливая микротрещины эпоксидной смолой. До сих пор неизвестно, является ли цинковая чума физико-химическим заболеванием или просто заводским браком, поэтому мне были бы интересны подробные исследования или новости на эту тему, если Хабр их подскажет.
Пурпурная чума
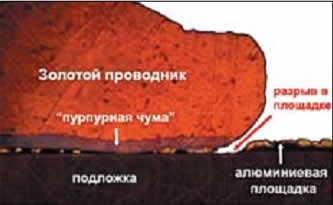
Такое название получила еще одна болезнь металлов, заражение золота алюминием. Проблема была обнаружена в 1970-е годы в США, когда в радиолокационном оборудовании стали применяться СВЧ-транзисторы с алюминиевыми проводниками. При прохождении сильного тока алюминий разогревался, затем, остывая, сжимался, проводник деформировался, транзистор выходил из строя. Чтобы справиться с этой проблемой, проводники стали делать из золота, но подложка транзистора могла по-прежнему содержать алюминий. Тогда оказалось, что при сильном нагревании на стыке золота и алюминия между ними образуется сразу несколько интерметаллических соединений, одно другого пагубнее.
Основной недостаток таких сплавов – хрупкость и низкая прочность. Контакт просто отламывается от транзистора. Наиболее распространенное соединение золота и алюминия – AuAl2, где золото составляет по массе примерно 78,5%, а алюминий – 21,5%. Это соединение имеет яркий фиолетовый цвет, почему и получило название «пурпурная чума».
Пурпурная чума возникает при температурах свыше 1000 °C, то есть, близко к температуре плавления золота (1064 °C). Пурпурная чума образуется неравномерно, поэтому конструкция долго сохраняет механическую плотность, пока не станет слишком поздно. Но уже при остывании до 624 °C пурпурная чума сменяется коричневой, гораздо более хрупким соединением Au2Al. А при температурах 100 °C и ниже начинается диффузия: слои с содержанием алюминия начинают проникать вглубь золота, и пурпурная чума охватывает весь образец, а не только стык (это явление называется «эффект Киркендалла»). При этом уменьшается общий объем вещества, и разрушительное воздействие пурпурной чумы становится фатальным.
Опять же, эта болезнь устраняется достаточно легко: проводник нужно легировать, достаточно 1% платины или палладия.
Интересно, что и пурпурная чума нашла своих ценителей. Соединения золота и алюминия эстетично выглядят, а интерметаллид AuAl2 даже был получен ювелирами в 1930 году и запатентован под названием «аметистовое золото». Уже тогда было замечено, что этот сплав очень хрупкий, поэтому его нельзя ковать или вытягивать, но можно осторожно гранить и оправлять как драгоценные камни. Открыв пурпурную чуму, ювелиры продолжили эксперименты, легируя золото, в частности, галлием и индием. Получались сплавы, близкие по свойствам к золоту, но тяготеющие по цвету к синей части спектра, также очень красивые.
Вместо заключения
Процессы, рассмотренные в статье, можно считать специфическими случаями коррозии. Пример истинной коррозии, напоминающий «металлическую чуму» — это образование дикой патины. В отличие от ровной и плотной благородной патины, которая возникает при медленном окислении меди на воздухе, дикая патина является рыхлой, поэтому не только разрушается вместе с поверхностным слоем медного изделия, но и проникает внутрь него, заражая металл ионами хлора. В Санкт-Петербурге, где атмосфера в конце XX века стала гораздо агрессивнее из-за выхлопных газов, усугубивших высокую влажность, дикая патина серьезно поразила скульптуры «Укрощение коня» на Аничковом Мосту.
Чтобы продлить жизнь этих скульптур, их пришлось искусственно покрывать очень тонким слоем закиси меди, имитирующей благородную патину. Возможно, она позволит продлить жизнь этим красавцам.
При какой температуре олово становится хрупким грузом
Изготовление изделий из металла с высокой точностью возможность только при использовании действительно качественного, надежного и технологичного оборудования.
Одним из первых сооружений, которые воздвигаются на любо земельном участке, является обычный забор. Им огораживают территорию для более удобного зримого разграничения.
Электросварные фитинги предназначаются для обслуживания и строительства трубопроводов ПНД.
Каждый день мы выполняем множество самых разных задач – выполняем работу на производстве, ухаживаем за садом, изготавливаем различные поделки в мастерской и многое.
Дипломы СССР сегодня пользуются большой популярностью среди людей, которые стараются устроиться на работу.
Для выполнения любой работы важно заранее обеспечить себя соответствующими средствами безопасности. Одним из наиболее распространенных вариантов таких средств, которые.
Через зрение человек получает более 80% информации. Поэтому крайне важно, чтобы везде, где он работает, качество освещения было на как можно более высоком уровне.
Использование на работе спецодежды выполняет функцию специальной защиты сотрудника при выполнении трудовых обязанностей.
Основные физические свойства олова
Олово — металл, служивший человеку с незапамятных времен. Физические свойства олова обеспечили его основополагающую роль в истории человечества. Без него невозможно существование бронзы, остававшейся на протяжении многих веков единственным сплавом, из которого человек изготовлял практически все — от орудий труда до ювелирных украшений.
Физические свойства олова
При нормальном давлении и температуре 20°C олово идентифицируется как металл с блеском бело-серебристого цвета. Медленно тускнеет на воздухе вследствие образования оксидной пленки.
Для олова, как и для всех металлов, характерна непрозрачность. Свободные электроны металлической кристаллической решетки заполняют межатомное пространство и отражают световые лучи, не пропуская их. Поэтому находясь в кристаллическом состоянии, металл имеет характерный блеск, а в порошкообразном виде этот блеск утрачивает.
Обладает отличной ковкостью, т. е. легко подвергается обработке с помощью давления. Ковкость олову придает его высокая пластичность в сочетании с низким сопротивлением деформации. Пластичность металла позволяет раскатать его в тонкую фольгу, называемую станиолем или оловянной бумагой. Ее толщина колеблется от 0,008 до 0,12 мм. Ранее станиоль находил применение в качестве подложки при изготовлении зеркал и в электротехнике при производстве конденсаторов, пока не был полностью вытеснен алюминиевой фольгой.
У олова свойства достаточно мягкого металла. Его твердость по шкале Бринелля составляет 3,9–4,2 кгс/мм².
Относится к легкоплавким металлам. Температура плавления олова – 231,9°C – способствует быстрому извлечению его из руды. Олово просто сплавляется с другими металлами, что обеспечивает его обширное применение в промышленности.
Плотность при температуре 20°C составляет 7,29 г/см³. По этому показателю олово в 2,7 раза тяжелее алюминия, но легче серебра, золота, платины и приближено к плотности железа (7,87 г/см³).
Металл закипает при высокой температуре, равной 2620°C, долго оставаясь жидким в расплаве.
Химически чистое олово при обычной температуре обладает незначительной прочностью. При растяжении предел механической прочности составляет всего 1,7 кгс/мм², а относительное удлинение – 80–90%. Эти характеристики говорят о том, что деформировать оловянный прут можно без особых усилий в разных направлениях. При этом смещение слоев кристаллической решетки металла относительно друг друга сопровождается специфичным треском.
Полиморфизм олова
Полиморфизм (аллотропия) — физическое явление, основанное на перестроении атомов или молекул веществ в твердом состоянии, что влечет за собой изменение их свойств. Каждая полиморфная модификация устойчиво существует только в строго определенном интервале значений температур и давлений.
Любой металл обладает специфической кристаллической решеткой. При изменении внешних физических условий кристаллическая решетка может меняться. Полиморфизм металлов используют при их термической обработке в промышленности.
Химические свойства олова определяются его положением в периодической системе элементов Д. И. Менделеева и предусматривают амфотерность, т. е. способность проявлять как основные, так и кислотные свойства. Напрямую зависят от полиморфизма олова физические свойства.
Для металла известны три аллотропные модификации: альфа, бета и гамма. Полиморфная перестройка кристаллических решеток возможна вследствие изменения симметрии электронных оболочек атомов под воздействием разных температур.
Особенности полиморфного перехода β→α
Процесс перехода из одной полиморфной модификации в другую происходит при изменении температуры. При этом наблюдают скачкообразные изменения физико-химических свойств металла.
Выше температуры 161°С бета-олово обратимо превращается в хрупкую гамма-модификацию. Ниже температуры 13°С бета-модификация необратимо переходит в порошкообразное серое олово. Данный полиморфный переход совершается с очень малой скоростью, но стоит только на бета-олово попасть крупинкам альфа-модификации, как плотный металл рассыпается в пыль. Поэтому полиморфный переход β→α иногда называют «оловянной чумой». Обратно альфа-модификация переводится в бета-модификацию только путем переплавки.
Фазовый переход β→α значительно ускоряется при минусовых температурах окружающей среды и сопровождается увеличением удельного объема металла примерно на 25%, что приводит к его рассыпанию в порошок.
В истории есть случаи, когда оловянные изделия на морозе становились серым порошком, обескураживая своих хозяев. «Оловянная чума» встречается редко и характерна лишь для химически чистого вещества. При наличии даже мельчайших примесей переход металла в порошок сильно замедляется.
Интересно предположение некоторых историков, что победу российскому императору Александру I над французской армией под командованием Наполеона Бонапарта помогла одержать «оловянная чума». При сильных морозах пуговицы на шинелях французов просто рассыпались в прах, и солдаты, замерзая, потеряли боеспособность.
Заключение
Олово обладает всеми типичными физическими свойствами металлов, а его полиморфизм по-своему удивителен. Без уникальной тягучести и пластичности этого металла невозможно представить себе современную промышленность. Почти половина от мировой добычи олова используется для производства пищевой жести. Оставшаяся половина расходуется для изготовления сплавов и различных соединений, применяемых во всех хозяйственных отраслях.