Жидкий кислород
Жидкий кислород – это агрегатное состояние кислорода, в котором он представляет собой бледно-синюю жидкость. Он относится к категории веществ, которые одними из первых стали использоваться в разных областях промышленности. Жидкий О2 используется с двумя целями: для усиления процессов горения и для окисления химических процессов. Именно необходимость решения этих задач стала причиной популярности воздухоразделительного оборудования.
Физические свойства жидкого кислорода
В жидком состоянии кислород имеет бледно-голубой оттенок. При переливании из одной емкости в другую жидкий кислород выделяет водяные пары, поглощая тепло из окружающего воздуха. При этом температура воздуха резко снижается, что приводит к образованию тумана.
Этот вид кислорода способен закипать при температуре 183°С. Если в это время поместить его в среду, в которой температура воздуха составляет около 30-40°С, то кипение лишь усилится. При комнатной температуре жидкость быстро испаряется.
Для того чтобы снизить скорость испарения кислорода жидкого, его помещают в специальные баллоны. Баллон для хранения О2 представляет собой двухслойный сосуд. Внутренняя стенка баллона покрыта слоем серебра, а между ней и внешней стенкой полностью выкачан весь воздух. Слой серебра необходим для того, чтобы отражать тепло. В таком баллоне кислород может храниться на протяжении нескольких суток.
К другим физическим свойствам жидкого кислорода можно отнести следующие:
Как получают жидкий кислород?
После этого проводят ректификацию, то есть отделение азота от кислорода. Этого добиваются путем многократного нагревания жидкости, в ходе которого первым делом испаряется азот, а оставшаяся жидкость обогащается О2.
В каких областях используют жидкий кислород?
В настоящее время жидкому кислороду находится применение в разных областях промышленности:
Жидкий О2 служит в качестве сырья для получения других химических соединений, вроде двуокиси титана или окиси этилена. С его помощью также можно повысить производительность большинства окислительных процессов.
В стекольной промышленности кислород применяется для интенсификации процессов горения, необходимых для поддержания работы стеклоплавильных печей. Помимо этого, он помогает снизить выбросы оксида азота и увеличить эффективность стекольного производства.
С этой же целью жидкий О2 используется в металлургии, где он обогащает воздух и повышает эффективность процесса горения.
С жидким кислородом связано ускорение процессов роста клеток, поэтому в фармацевтике его добавляют в ферментеры и биореакторы.
В целлюлозно-бумажной отрасли промышленности с помощью этого вида кислорода осуществляется окислительное экстрагирование, обработка сточных вод и делигнификация (процесс получения целлюлозы).
Помимо этого, кислородом жидким пользуются в автомобилестроении и машиностроении, где он применяется в качестве вспомогательного газа во время лазерной резки. Его также добавляют в состав защитных газовых смесей.
Техника безопасности при работе с жидким кислородом
При работе с жидким кислородом нет угрозы отравления, но все же некоторые требования безопасности необходимо строго соблюдать:
Преимущества сотрудничества с НПК «Грасис»
Научно-производственная компания «Грасис» осуществляет поставки оборудования, которое позволит вам самостоятельно получать газообразный кислород из атмосферного воздуха.
Наша компания более 10 лет занимается разработкой и производством газо- и воздухоразделительного оборудования, а также инжинирингом, проектированием и выполнением комплексных работ «под ключ». Мы поможем вам решить любые задачи, связанные с газо- и воздухоразделением, утилизацией попутного нефтяного газа и подготовкой природного газа.
В процессе производства оборудования мы используем нанотехнологии и высококачественные комплектующие, благодаря которым улучшаются технико-эксплуатационные свойства продукции. Свяжитесь с представителями компании «Грасис», чтобы получить развернутую информацию о заинтересовавшей вас установке!
При какой температуре кислород становится жидким
3. Сжижение газов
Газы отличаются от жидких тел расстоянием между молекулами. Казалось бы поэтому, что для сжижения газа достаточно сблизить его молекулы, т. е. сильно сдавить газ. Однако оказалось, что это не так и что для превращения газа в жидкое состояние должна быть путем охлаждения газа снижена движущая (кинетическая) энергия молекул.
| Название газа | Плотность (воздуха = 1) | Вес 1 литра в г при 0°С и 760 мм | 1 кг газа = литрам газа | Уд. вес жидкого газа при темпер. 15°С вода = 1 (4°) | Давление паров жидкого газа при 150 атм | Точка кипения °С | Точка плавления °С | Критич. температура °С | Критич. давление атм |
| Азот | 0,9701 | 1,2542 | 789 | 0,7914 (-196°) | — | 196° | -211° | -147° | 34 |
| Аммиак | 0,5895 | 0,7621 | 1 312 | 0,6138 | 7,14 | -38,5° | -75° | -132° | 112 |
| Аргон | 1,379 | 1,782 | 561 | 1,212 (-186°) | — | -186° | -190° | -121° | 51 |
| Ацетилен | 0,8988 | 1,620 | 617 | 0,420 (10°) | 37,9 | -84° | -81° | 37° | 68 |
| Водород | 0,0697 | 0,0900 | 11 106 | 0,0763 (-253°) | — | -259° | -253° | -239° | 12 |
| Гелий | 0,1382 | 0,1787 | 5 596 | 0,122 (-269°) | — | -269° | -272° | -268° | 2 |
| Двуокись азота | 3,1812 | 4,1126 | 243 | 1,451 | 0,76 | 26° | 11° | 171° | 100 |
| Двуокись серы | 2,2131 | 2,8611 | 350 | 1,3964 | 2,72 | -10° | -79° | 157° | 78 |
| Двуокись углерода | 1,5201 | 1,9652 | 509 | 0,814 | 52,17 | -78° | -65° | 31,1° | 73 |
| Закись азота | 1,5229 | 1,9688 | 508 | 0,800 | 49,77 | -90° | -115° | 36° | 75 |
| Кислород | 1,1055 | 1,4292 | 700 | 0,106 (-183°) | — | -183° | -218° | -119° | 51 |
| Криптон | 2,868 | 3,654 | 274 | 2,16 (-152°) | — | -152° | -169° | -63° | 54 |
| Ксенон | 4,49 | 5,717 | 175 | 3,52 (107°) | — | -107° | -140° | 15° | 57 |
| Метан | 0,5539 | 0,7160 | 1 396 | 0,466 (-160°) | — | -160° | -184° | -96° | 50 |
| Метиламин | 1,0737 | 1,388 | 720 | 0,699 (-11°) | — | -6° | — | 155° | 72 |
| Неон | 0,695 | 0,9004 | 1 111 | 0,456 (-233°) | — | -233° | -253° | -228° | 27 |
| Окись углерода | 0,9673 | 1,2506 | 800 | 0,7676 (-184°) | — | -190° | -207° | -140° | 36 |
| Фосген | 3,4168 | 4,4172 | 227 | 1,392 | 1,35 | 8,2° | -118° | — | — |
| Хлор | 2,4494 | 3,1666 | 316 | 1,4273 | 5,75 | -33,6° | -102° | 146° | 94 |
| Хлористый метил | 1,7438 | 2,2543 | 443 | 0,917 (17°) | 4,10 | -24° | -104° | 142° | 73 |
| Хлористый этил | 2,2280 | 2,8804 | 347 | 0,921 (0°) | 1,09 | 12,5° | -143° | 182° | 54 |
| Этиламин | 1,558 | 2,0141 | 497 | 0,689 | 0,9 | 18° | -85° | 177° | 66 |
| Этилен | 0,9684 | 1,252 | 798 | 0,310 (6°) | 46 (6°) | -103° | -169° | 10° | 51 |
| Этан | 1,038 | 1,3421 | 746 | 0,466 | 32,3 | -84° | -171° | 35° | 45 |
Сжижение газов является в настоящее время важной отраслью химической промышленности. Так напр., сжижается воздух, и из него при помощи фракционированной дистилляции получается кислород, азот и редкие газы. Сжижается хлор и в жидком виде транспортируется в стальных баллонах на отбельные заводы. Жидкие сернистый ангидрит, аммиак и другие жидкие газы применяются в холодильных установках. Их действие заключается в том, что сильно сжатому компрессором и охлажденному газу представляется возможность сразу расшириться (в пространстве, из которого компрессором отсасывается воздух через так наз. редукционный клапан); в результате этого газ так сильно охлаждается, что превращается в жидкость (явление Джоуля-Томсона). Испарением жидкого газа охлаждается рассол (крепкий солевой раствор), который затем распределяется по помещениям, предназначенным для охлаждения.
Стальные баллоны необходимо оберегать от ударов (при транспортировке) и нельзя подвергать действию высокой температуры (оставлять на солнце или вблизи от отопительной установки или печи). У кислородных баллонов нарезки нужно смазывать не смазочным маслом, а глицерином.
Кислород – рождающий кислоты
Содержание
Кислород при нормальных условиях (температуре и давлении) представляет собой прозрачный газ без запаха, вкуса и цвета. Не относится к горючим газам, но способен активно поддерживать горение.
По химической активности среди неметаллов он занимает второе место после фтора.
Все элементы, кроме благородных металлов (платина, золото, серебро, родий, палладий и др.) и инертных газов (гелий, аргон, ксенон, криптон и неон), вступают в реакцию окисления и образовывают оксиды. Процесс окисления элементов, как правило, носит экзотермический (с выделением теплоты) характер. Также необходимо учитывать тот факт, что при повышении температуры, давления или использовании катализаторов – скорость реакции окисления резко возрастает.
История открытия кислорода
Открытие кислорода приписывают Джозефу Пристли (Joseph Priestley). У него была лаборатория, оборудованная приборами для собирания газов. Он испытывал его физиологическое действие на себе и на мышах. Пристли установил, что после вдыхания газа некоторое время ощущается приятная легкость. Мыши в герметически закрытой банке с воздухом задыхаются быстрей, чем в банке с O2. Поскольку Пристли был приверженцем флогистонной теории он так и не узнал, что оказалось у него в руках. Он только описал этот газ, даже не догадываясь, что он описал. А вот лавры открытия кислорода принадлежат Антуан Лоран Лавуазье (Antoine Laurent de Lavoisier), который и дал ему имя.
Лавуазье, поставил свой знаменитый опыт, продолжавшийся 12 дней. Он нагревал ртуть в реторте. При кипении образовывалась ее красная окись. Когда реторту охладили, оказалось, что воздуха в ней убыло почти на 1/6 его объема, а остаток ртути весил меньше, чем перед нагревом. Но когда разложили окись ртути сильным прокаливанием, все вернулось: и недостача ртути, и «исчезнувший» кислород.
Впоследствии Лавуазье установил, что этот газ входит в состав азотной, серной, фосфорной кислот. Он ошибочно полагал, что O2 обязательно входит в состав кислот, и поэтому назвал его «оксигениум», что значит «рождающий кислоты». Теперь хорошо известны кислоты, лишенные «оксигениума» (например: соляная, сероводородная, синильная и др.).
Способы получения кислорода
В основном кислород получают тремя способами:
Из атмосферного воздуха его получают методом глубокого охлаждения, как побочный продукт при получении азота.
Также O2 добывают путем пропускания электрического тока через воду (электролиз воды) с попутным получением водорода.
Химические способ получения малопроизводителен, а, следовательно, и неэкономичен, он не нашел широкого применения и используются в лабораторной практике.
Наверно многие помнят химический опыт, когда в колбе нагревают марганцовку (перманганат калия KMnO4), а потом выделяющийся в процессе нагрева газ собирают в другую колбу?
Применение кислорода
Помимо того, что все живые существам в природе, за исключением немногих микроорганизмов, при дыхании потребляют кислород, он широко применяется во многих отраслях промышленности: металлургической, химической, машиностроении, авиации, ракетостроении и даже в медицине.
В химической промышленности его применяет:
В металлургии его используют:
В медицинских целях больным, у которых нарушена нормальная деятельность органов дыхания или кровообращения, искусственно увеличивают содержание O2 в воздухе или дают дышать непродолжительное время чистым O2. Медицинский кислород, выпускаемый ГОСТ 5583, особенно тщательно очищают от всех примесей.
Применение кислорода в сварке
Сам по себе O2 является негорючим газом, но из-за свойства активно поддерживать горение и увеличения интенсивности (интенсификации) горения газов и жидкого топлива его используют в ракетных энергетических установках и во всех процессах газопламенной обработки. В таких процессах газопламенной обработки, как газовая сварка, поверхностная закалка высокая температура пламени достигается путем сжигания горючих газов в O2, а при газовой резке благодаря ему происходит окисление и сгорание разрезаемого металла.
При полуавтоматической сварке (MIG/MAG) кислород O2 используют как компонент защитных газовых смесей с аргоном (Ar) или углекислым газом (CO2).
Кислород добавляют в аргон при полуавтоматической сварке легированных сталей для обеспечения устойчивости горения дуги и струйного переноса расплавленного металла в сварочную ванну. Дело в том, что как поверхностно активный элемент он уменьшает поверхностное натяжение жидкого металла, способствуя образованию на конце электрода более мелких капель.
При сварке низколегированных и низкоуглеродистых сталей полуавтоматом O2 добавляют в углекислый газ для обеспечения глубокого проплавления и хорошего формирования сварного шва, а также для уменьшения разбрызгивания.
Чаще всего кислород используют в газообразном виде, а в виде жидкости используют только при его хранении и транспортировке от завода-изготовителя до потребителей.
Вредность и опасность кислорода
За внешней безобидностью скрывается очень опасный газ, но об этом на нашем сайте опубликована статья про маслоопасность и взрывоопасность кислорода и мы не будем здесь дублировать информацию.
Хранение и транспортировка кислорода
Кислород газообразный технический и медицинский выпускают по ГОСТ 5583.
Хранят и транспортируют его в стальных баллонах ГОСТ 949 под давлением 15 МПа. Кислородные баллоны окрашены в синий цвет с надписью черными буквами «КИСЛОРОД».

Жидкий кислород выпускается по ГОСТ 6331. O2 находится в жидком состоянии только при получении, хранении и транспортировке. Для газовой сварки или газовой резки его необходимо снова превратить в газообразное состояние.
Характеристики кислорода
Характеристики O2 представлены в таблицах ниже:
Коэффициент перевода объема и массы O2 при Т=15°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 1,337 | 1 | 1,172 |
| 1,141 | 0,853 | 1 |
| 1 | 0,748 | 0,876 |
Коэффициенты перевода объема и массы O2 при Т=0°С и Р=0,1 МПа
| Масса, кг | Объем | |
|---|---|---|
| Газ, м 3 | Жидкость, л | |
| 1,429 | 1 | 1,252 |
| 1,141 | 0,799 | 1 |
| 1 | 0,700 | 0,876 |
Кислород в баллоне
| Наименование | Объем баллона, л | Масса газа в баллоне, кг | Объем газа (м 3 ) при Т=15°С, Р=0,1 МПа |
|---|---|---|---|
| O2 | 40 | 8,42 | 6,3 |
Благодаря этой таблице теперь можно легко дать ответы на вопросы, которые очень часто задают сварщики:
Жидкий кислород
Жи́дкий кислоро́д (ЖК, англ. Liquid oxygen, LOX ) — жидкость бледно-синего цвета, которая относится к сильным парамагнетикам. Является одним из четырёх агрегатных состояний кислорода. ЖК обладает удельной плотностью 1,141 г/см³ и имеет умеренно криогенные свойства с точкой замерзания 50,5 K (−222,65 °C) и точкой кипения 90,188 K (−182,96 °C). Жидкий кислород активно используется в космической и газовой отраслях, при эксплуатации подводных лодок, широко используется в медицине. Обычно промышленное получение основывается на фракционной перегонке воздуха. Коэффициент расширения (англ. expansion ratio ) кислорода при смене агрегатного состояния на газообразное составляет 860:1 при 20 °C, что иногда используется в системах снабжения кислородом для дыхания в коммерческих и военных самолётах. Основным и практически неисчерпаемым источником получения жидкого кислорода является атмосферный воздух: производится сжижение воздуха и последующее разделение его на кислород и азот.
Из-за своей криогенной природы ЖК может вызвать хрупкость материалов, которые находятся с ним в соприкосновении. Жидкий кислород также является очень мощным окислительным агентом: органическое вещество быстро сгорает в его среде с большим выделением тепла. Более того, некоторые из этих веществ, будучи пропитанными ЖК имеют свойство непредсказуемо взрываться. Нефтепродукты часто демонстрируют такое поведение, включая асфальт.
Жидкий азот имеет более низкую точку кипения 77 K (−196 °C) и устройства, которые содержат жидкий азот могут конденсировать кислород из воздуха: когда большая часть азота испаряется из такого устройства возникает риск того, что остаток жидкого кислорода может сильно прореагировать с органическими материалами. С другой стороны, жидкий азот или жидкий воздух может оказаться насыщенным жидким кислородом, если оставить ёмкость на открытом воздухе — атмосферный кислород будет в ней растворяться, в то время как азот будет испаряться быстрее.
Меры безопасности при работе с жидким кислородом:
4. При перекачке жидкого кислорода производится предварительное «захолаживание» системы малым расходом продукта. Без этого в «горячей» системе образуется интенсивный поток газифицированного кислорода, который при наличии резких поворотов и перепадов давления на элементах системы (вентили и т.п.) может вызвать возгорание металла.
Температура жидкого кислорода по цельсию
Что такое жидкий кислород: общая информация
Кислород – самый распространенный элемент на планете. Он присутствует в воде, земной коре, воздухе и в организмах живых существ, активно участвуя во многих обменных процессах. В природе он обычно существует в виде газа, а в промышленности часто используется в качестве жидкости. Как ведет себя жидкий кислород? Какими свойствами он обладает и где используется?
Газ кислород
Кислород – один из важнейших элементов на планете. Он участвует в процессе дыхания, в метаболизме живых организмов, а также в круговороте веществ в биосфере. Кроме того, он способствует гниению и разложению органических остатков.
В нормальных условиях он является бесцветным газом, который не имеет вкуса и запаха. Он тяжелее воздуха и с трудом растворяется в воде. В химическом плане он очень активен и способен образовывать соединения практически со всеми элементами.
В свободном состоянии в виде молекул О2, состоящих из двух атомов оксигена, он находится в атмосфере. Благодаря такому строению элемент также называется «дикислородом», но он может существовать и в других вариациях. При определенных условиях его атомы могут образовывать «трикислород» с молекулой О3, которая представляет собой голубой газ озон со специфическим запахом.
В атмосфере содержание кислорода составляет примерно 21 % по массе, в земной коре его доля значительно выше и составляет около 47 % по массе. Элемент входит в состав более полутора тысяч разнообразных пород и минералов, большая часть из которых являются силикатами. Там он присутствует в виде соединений. В воде его содержание доходит до 85 %, и это не удивительно, ведь атомы оксигена и образуют воду вместе с элементом гидрогеном.
Жидкий кислород
В жидком состоянии кислород окрашивается в голубой оттенок и усиливает некоторые свойства газообразного вещества. Так, он ведет себя более агрессивно в химических реакциях, а также становится сильным парамагнетиком и может притягиваться магнитом.
Химические свойства
Газообразный кислород является окислителем. Сам по себе он негорюч, но хорошо поддерживает процесс горения, а при значительной концентрации и высоких температурах является взрывоопасным.
С активными веществами (например, щелочными металлами) он может вступать в реакции даже при комнатной температуре и при обыкновенной концентрации в воздухе, образуя с ними соединения оксиды. Результат хорошо виден на многих металлах, на которых он проявляется в виде коррозии.
Жидкий кислород также обладает сильными окислительными свойствами. Многие пропитанные им вещества легко воспламеняются и горят с выделением энергии и тепла. Хлопок, бумага, дерево, уголь и некоторые другие материалы могут взрываться.
Получение
Самым распространенным и легким в получении источником кислорода является воздух. К тому же он неиссякаем и присутствует в нашей жизни повсеместно. Чтобы получить из него необходимые вещества, его сжижают, а затем разделяют на жидкий азот и кислород.
Еще один способ получения жидкости – конденсация ее из газа. Для этого достаточно опустить медный змеевик в контейнер с жидким азотом, а затем пропустить через змеевик газообразный кислород. Температура азота ниже, чем у кислорода, поэтому, проходя по медной трубке, газ будет конденсироваться и превратится в жидкость. При этом на поверхности змеевика образуется небольшой слой снега.
Применение
Сегодня его чаще применяют в медицине, фармацевтике, в металлургии, стекольной, химической, бумажной и других видах промышленности. С его помощью получают различные полезные соединения, например окись титана, которая участвует в производстве лакокрасочных изделий, бумаги и пластмасс. При изготовлении стекла он нужен для поддержания жара в печах, а также для уменьшения количества окиси азота, попадающей в атмосферу. В космической авиации жидкий кислород является одним из компонентов ракетного топлива, где он используется в качестве окислителя, а в роли самого топлива выступает водород или керосин.
В медицине и фармацевтике без него тоже не обходится. Жидкий кислород входит в состав биореакторов, а также используется в качестве добавки к ферментам. В медицине он необходим для анестезии, приготовления кислородных ванн и коктейлей, лечения или облегчения состояния при интоксикации, астме и других недугах. Здесь он чаще всего не используется напрямую в виде жидкости, а является источником газообразного кислорода.
Хранение и меры предосторожности
Жидкий кислород не возгорается и не взрывается сам по себе, он не токсичен для человека и не вреден для окружающей среды. Однако активная реакция в химических процессах, а также криогенный эффект делают его не совсем безопасным веществом.
При работе с ним нужно держать подальше смазочные, горючие и легковоспламеняющиеся материалы, а также всегда использовать перчатки и спецодежду. Кислород очень низкой температуры легко повреждает кожу и может привести к обморожению, травмам и отмиранию живых клеток. Если жидкость покрывает значительную часть тела, все может закончиться даже летальным исходом.
Технический и медицинский жидкий кислород хранят сосудах Дьюара, которые делают преимущественно из стали или алюминия. Это цилиндрические контейнеры с двойными стенками, между стенками которых располагается вакуумная полость, а также теплоизоляционные материалы. Они работают по принципу термосов, хорошо сохраняя жидкости внутри.
Жидкий кислород
Жидкий кислород – это агрегатное состояние кислорода, в котором он представляет собой бледно-синюю жидкость. Он относится к категории веществ, которые одними из первых стали использоваться в разных областях промышленности. Жидкий О2 используется с двумя целями: для усиления процессов горения и для окисления химических процессов. Именно необходимость решения этих задач стала причиной популярности воздухоразделительного оборудования.
Физические свойства жидкого кислорода
В жидком состоянии кислород имеет бледно-голубой оттенок. При переливании из одной емкости в другую жидкий кислород выделяет водяные пары, поглощая тепло из окружающего воздуха. При этом температура воздуха резко снижается, что приводит к образованию тумана.
Этот вид кислорода способен закипать при температуре 183°С. Если в это время поместить его в среду, в которой температура воздуха составляет около 30-40°С, то кипение лишь усилится. При комнатной температуре жидкость быстро испаряется.
Для того чтобы снизить скорость испарения кислорода жидкого, его помещают в специальные баллоны. Баллон для хранения О2 представляет собой двухслойный сосуд. Внутренняя стенка баллона покрыта слоем серебра, а между ней и внешней стенкой полностью выкачан весь воздух. Слой серебра необходим для того, чтобы отражать тепло. В таком баллоне кислород может храниться на протяжении нескольких суток.
К другим физическим свойствам жидкого кислорода можно отнести следующие:
Как получают жидкий кислород?
После этого проводят ректификацию, то есть отделение азота от кислорода. Этого добиваются путем многократного нагревания жидкости, в ходе которого первым делом испаряется азот, а оставшаяся жидкость обогащается О2.
В каких областях используют жидкий кислород?
В настоящее время жидкому кислороду находится применение в разных областях промышленности:
Жидкий О2 служит в качестве сырья для получения других химических соединений, вроде двуокиси титана или окиси этилена. С его помощью также можно повысить производительность большинства окислительных процессов.
В стекольной промышленности кислород применяется для интенсификации процессов горения, необходимых для поддержания работы стеклоплавильных печей. Помимо этого, он помогает снизить выбросы оксида азота и увеличить эффективность стекольного производства.
С этой же целью жидкий О2 используется в металлургии, где он обогащает воздух и повышает эффективность процесса горения.
С жидким кислородом связано ускорение процессов роста клеток, поэтому в фармацевтике его добавляют в ферментеры и биореакторы.
В целлюлозно-бумажной отрасли промышленности с помощью этого вида кислорода осуществляется окислительное экстрагирование, обработка сточных вод и делигнификация (процесс получения целлюлозы).
Помимо этого, кислородом жидким пользуются в автомобилестроении и машиностроении, где он применяется в качестве вспомогательного газа во время лазерной резки. Его также добавляют в состав защитных газовых смесей.
Техника безопасности при работе с жидким кислородом
При работе с жидким кислородом нет угрозы отравления, но все же некоторые требования безопасности необходимо строго соблюдать:
Преимущества сотрудничества с НПК «Грасис»
Научно-производственная компания «Грасис» осуществляет поставки оборудования, которое позволит вам самостоятельно получать газообразный кислород из атмосферного воздуха.
Наша компания более 10 лет занимается разработкой и производством газо- и воздухоразделительного оборудования, а также инжинирингом, проектированием и выполнением комплексных работ «под ключ». Мы поможем вам решить любые задачи, связанные с газо- и воздухоразделением, утилизацией попутного нефтяного газа и подготовкой природного газа.
В процессе производства оборудования мы используем нанотехнологии и высококачественные комплектующие, благодаря которым улучшаются технико-эксплуатационные свойства продукции. Свяжитесь с представителями компании «Грасис», чтобы получить развернутую информацию о заинтересовавшей вас установке!
Физические свойства кислорода
Где бы мы ни находились, нас всюду окружает кислород воздуха.
Почему же мы не замечаем и не чувствуем его? Кислород, азот, аргон и другие газы, входящие в состав воздуха, бесцветны и не имеют ни запаха, ни вкуса. Газообразный воздух нельзя ни видеть, ни ощущать.
Воздух из газообразного состояния можно перевести в жидкое. Одновременно с основной массой воздуха — азотом — в жидкое состояние перейдут кислород и большинство других газов, входящих в его состав.
Чтобы газообразный кислород превратить в жидкость, его нужно сжать до 50 атмосфер и охладить до —119°.
Жидкий кислород можно получить и при атмосферном давлении, но для этого нужно газообразный кислород охладить до температуры —183°. При более сильном охлаждении, до температуры —220°, жидкий кислород затвердевает и превращается в снегообразную массу.
Если на некоторое время в жидкий кислород поместить кусочек резины, она потеряет свою эластичность и под ударом разлетится на мелкие части.
Такую же хрупкость приобретает и цинковая пластинка, охлажденная в жидком кислороде до температуры —183°. Жидкая ртуть при такой температуре превращается в твердую массу, которую можно ковать, как свинец, а свинец приобретает способность звенеть, как бронзовый колокольчик.
Жидкий кислород имеет голубоватый цвет. Его можно легко переливать из сосуда в сосуд. При переливании жидкий кислород «парит». Но это не пары кислорода, а пары воды. Жидкий кислород, испаряясь, поглощает много тепла из окружающего воздуха. Воздух сильно охлаждается, и влага, находящаяся в воздухе, конденсируется, образуя туман. Этот туман и создает впечатление пара, исходящего из самой жидкости.
Температура кипения жидкого кислорода равна —183°.
Если фарфоровый стакан с жидким кислородом вынести зимой на мороз 30—40°, он будет кипеть более бурно, чем вода на самом сильном огне газовой плиты.
При комнатной температуре испарение жидкого кислорода идет еще энергичнее, и он быстро переходит в газообразное состояние.
Чтобы использовать жидкий кислород, его необходимо сохранить. Как же заставить эту бурно кипящую жидкость не так быстро испаряться?
Для этого служат специальные сосуды, в которых легко удается «укротить» эту быстро испаряющуюся жидкость.
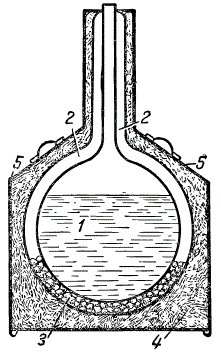
Стеклянный сосуд для хранения небольшого количества жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — поверхности, посеребренные внутри.
Сосуд для хранения жидкого кислорода представляет собой цилиндр с двойными стенками. Внутренние стороны стенок обычно покрывают тонким слоем серебра. Воздух между стенками сосуда выкачивается.
Разреженные газы плохо проводят тепло, а зеркальная поверхность серебра хорошо отражает его. Таким образом, жидкий кислород, который находится в сосуде, изолирован от внешнего тепла, что обеспечивает сохранение жидкого кислорода в течение одних-двух суток.
При испарении жидкого кислорода объем его увеличивается почти в 800 раз. Из кубического сантиметра жидкого кислорода образуется около 800 кубических сантиметров газообразного.
Хранить жидкий кислород в закрытых сосудах опасно: внутри сосуда может образоваться большое давление, приводящее к взрыву. Поэтому сосуды для хранения жидкого кислорода сверху открыты. Воздух, находящийся над жидкостью, сильно охлаждается и предохраняет кислород от наружного тепла, замедляя дальнейшее испарение.
Для перевозки небольших количеств жидкого кислорода используют металлические емкостью 15—25 литров.
Металлические сосуды состоят из двух шаров или цилиндров, вставленных друг в друга. Внутренний шар или цилиндр имеет высокое и узкое горло, через которое сосуд заполняется жидким кислородом. Горло всегда остается открытым. Из пространства между стенками сосуда воздух выкачан, и создан высокий вакуум, то есть сильное разрежение.
Металлический сосуд для перевозки жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — силикагель; 4 — теплоизоляционный материал; 5 — железный цилиндр.
Чтобы поддержать высокий вакуум, часть пространства между стенками заполняется силикагелем, способным при низкой температуре поглощать количество газа в сотни раз больше своего собственного объема. Если через стенки или через места спайки со временем просочится небольшая часть воздуха, он поглотится силикагелем и разрежение не уменьшится. Высокий вакуум обеспечивает постоянную изоляцию сосуда от внешнего тепла и дает возможность в течение двух и более суток сохранять в нем жидкий кислород. Такие сосуды обычно помещают в железные цилиндры.
Пространство между сосудом и наружным цилиндром заполняют теплоизоляционным материалом. Для переноски на наружном цилиндре имеются ручки.
Большие количества жидкого кислорода перевозятся по железной дороге и автотранспортом в специальных цистернах или танках. Они хорошо изолированы от внешнего тепла. Емкость транспортных танков различна: от 1 тысячи до 10 тысяч литров. Цистерны, в которых жидкий кислород перевозят по железной дороге, вмещают до нескольких десятков тонн.
Жидкий кислород можно получить из жидкого воздуха, который образуется при низких температурах и высоком давлении.
Высокое давление создают в машинах, которые называются компрессорами. Их приводят в движение электродвигатели.
Источник: В. Медведовский. Кислород. Государственное Издательство Детской литературы Министерства Просвещения РСФСР. Ленинград. Москва. 1953
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Жидкий кислород, медицинский кислород
Газообразный кислород сегодня в промышленных масштабах получают из атмосферного воздуха. Его производство актуально и востребовано в наши дни. Существует специальное оборудование, которое позволяет получать кислород в необходимых объемах. В условиях лаборатории газообразный (а затем и жидкий) кислород наиболее часто получают, используя возможности электролиза водных растворов щелочей. Также существует еще один способ получения небольшого количество кислорода — взаимодействие подкисленного раствора пероксида водорода и раствора перманганата калия. Газообразный кислород сегодня востребован во множестве профессиональных видов деятельности человека.
Сферы применения кислорода
Основные химические свойства кислорода:
Такие характеристики данного газа обусловили его использование сегодня в самых разнообразных технологических процессах. Любое оборудование для проведения газопламенных работ не может функционировать без кислорода. К газопламенным работам относятся:
В металлургической промышленности использование газообразного кислорода позволяет ощутимо повысить эффективность производства. Кислород технический в работе с металлом востребован в достаточно значительной степени. Без его использования многие виды работ попросту невозможны. Так, кислород технический позволяет повысить температуру горения. Он широко используется в производстве цветных и черных металлов.
Также он широко применяется в химической, нефтехимической и нефтегазовой промышленности. Применение кислорода помогает повысить производительность предприятий, занимающихся выращиванием рыбы и морепродуктов. В стекольной промышленности и при утилизации отходов данный газ также востребован.
Кислород участвует в окислительно-восстановительных реакциях, широко применяется в медицине. Медицинский кислород востребован в медицинских учреждениях. Так, аппараты искусственного дыхания используют медицинский кислород в чистом виде или же в качестве одной из составляющих воздушной смеси. Современное оборудование помогает производить сложнейшие операции и восстанавливать человеческое здоровье, казалось бы, в безнадежных ситуациях.
Жидкий кислород удобен в хранении на складе и транспортировке. Перед использованием его извлекают со склада и посредством специального процесса газификации жидкий кислород переводят в газообразное состояние.
Справка
Кислород — химический элемент с атомным номером 8, обозначающийся символом О, а также вещество (газ при нормальных условиях), молекула которого состоит из двух атомов кислорода (O2). Кислород является самым лёгким элементом из группы халькогенидов (6 группа периодической системы).
История открытия
Официально считается, что кислород был открыт английским химиком Джозефом Пристли 1 августа 1774 путём разложения оксида ртути в герметично закрытом сосуде (Пристли направлял на это соединение солнечные лучи с помощью мощной линзы).
Однако Пристли первоначально не понял, что открыл новое простое вещество, он считал, что выделил одну из составных частей воздуха (и назвал этот газ «дефлогистированным воздухом»). О своём открытии Пристли сообщил выдающемуся французскому химику Антуану Лавуазье.
Несколькими годами ранее (возможно, в 1770-м) кислород получил шведский химик Карл Шееле. Он прокаливал селитру с серной кислотой и затем разлагал получившийся оксид азота. Шееле назвал этот газ «огненным воздухом» и описал своё открытие в изданной в 1777 году книге (именно потому, что книга опубликована позже, чем сообщил о своём открытии Пристли, последний и считается первооткрывателем кислорода). Шееле также сообщил о своём опыте Лавуазье.
Важным этапом, который способствовал открытию кислорода, были работы французского химика Петра Байена, который опубликовал работы по окислению ртути и последующему разложению её оксида.
Наконец, окончательно разобрался в природе полученного газа А. Лавуазье, воспользовавшийся информацией от Пристли и Шееле. Его работа имела громадное значение, потому что благодаря ей была ниспровергнута господствовавшая в то время и тормозившая развитие химии флогистонная теория. [Лавуазье провел опыт по сжиганию различных веществ и опроверг теорию флогистона, опубликовав результаты по весу сожженных элементов. Вес золы превышал первоначальный вес элемента, что дало Лавуазье право утверждать, что при горении происходит химическая реакция (окисление) вещества, в связи с этим масса исходного вещества увеличивается, что опровергает теории флогистона.]
Таким образом, заслугу открытия кислорода фактически делят между собой Пристли, Шееле и Лавуазье.
Происхождение названия
Название oxygenium («кислород») происходит от греческих слов, обозначающих «рождающий кислоту»; это связано с первоначальным значением термина «кислота». Ранее этим термином называли оксиды.
Нахождение в природе
Получение
В настоящее время в промышленности жидкий кислород получают из воздуха. В лабораториях пользуются кислородом промышленного производства, поставляемым в стальных баллонах под давлением около 15 МПа. Важнейшим лабораторным способом его получения служит электролиз водных растворов щелочей. Небольшие количества кислорода можно также получать взаимодействием раствора перманганата калия с подкисленным раствором пероксида водорода.
Физические свойства
Газ без цвета, вкуса и запаха. Растворим в воде, причем растворяется тем лучше, чем ниже ее температура. Поэтому плотность живых организмов в холодных приполярных водах может быть значительно выше, чем в теплых экваториальных.
Химические свойства
Биологическая роль кислорода
Кислород участвует в окислительно-восстановительных реакциях. Живые существа дышат кислородом воздуха. Широко используется кислород в медицине. При сердечнососудистых заболеваниях, для улучшения обменных процессов, в желудок вводят кислородную пену («кислородный коктейль»). Подкожное введение кислорода используют при трофических язвах, слоновости, гангрене. Для обеззараживания и дезодорации воздуха и очистки питьевой воды применяют искусственное обогащение озоном. Радиоактивный изотоп кислорода 15O применяется для исследований скорости кровотока, лёгочной вентиляции.
Токсические производные кислорода
Некоторые производные кислорода (т. н. реактивные формы кислорода), такие как синглетный кислород, перекись водорода, супероксид, озон и гидроксильный радикал, являются высокотоксичными продуктами. Они образуются в процессе активирования или частичного восстановления кислорода. Супероксид (супероксидный радикал), перекись водорода и гидроксильный радикал могут образовываться в клетках и тканях организма человека и животных и вызывают оксидативный стресс.
Компания «СнабТехГаз» предлагает кислород, медицинский и технический, а также его производство и заправку.
Температура жидкого кислорода по цельсию
Жидкий кислород (ЖК, англ. Liquid oxygen, LOX) — жидкость бледно-синего цвета, которая относится к сильным парамагнетикам. Является одним из четырёх агрегатных состояний кислорода. ЖК обладает удельной плотностью 1,141 г/см³ и имеет умеренно криогенные свойства с точкой замерзания 50,5 K (−222,65 °C) и точкой кипения 90,188 K (−182,96 °C).
Жидкий кислород активно используется в космической и газовой отраслях, при эксплуатации подводных лодок, широко используется в медицине. Обычно промышленное получение основывается на фракционной перегонке воздуха. Коэффициент расширения (англ. expansion ratio) кислорода при смене агрегатного состояния на газообразное составляет 860:1 при 20 °C, что иногда используется в системах снабжения кислородом для дыхания в коммерческих и военных самолётах. Основным и практически неисчерпаемым источником получения жидкого кислорода является атмосферный воздух: производится сжижение воздуха и последующее разделение его на кислород и азот.
Общие сведения.
В периодической системе химических элементов Менделеева кислород обозначается символом 0 (от латинского Oxygenium). В нормальных условиях кислород представляет собой очень активный газ, не ощутимый органами чувств человека (т.е. не имеющий запаха, вкуса или цвета). Молекула кислорода обычно двухатомная (формула ее О2), реже трехатомная (О3, такое молекулярное состояние кислорода называют озоном, этот газ обладает весьма специфическим запахом). Кислород является самым распространенным в пределах планеты химическим элементом. Он не только на четверть заполняет атмосферу Земли, но и присутствует во всех внутренних оболочках планеты в составе силикатов (оксиды кремния, из которых состоит вулканическая магма).
История открытия
Существует точная дата экспериментального обнаружения кислорода – 1 августа 1774 года, о чем заявил англичанин Джозеф Пристли. Однако, как часто бывает в химии, всю сущность своего открытия он не осознал, тем самым частично отдав лавры первооткрывателя своим коллегам.
По факту, первым открыл кислород тремя годами ранее шведский естествоиспытатель и фармацевт Карл Шееле (1771 год), когда поставил эксперимент по прокаливанию селитры серной кислотой и последующим разложением оксида азота на составляющие: азот и кислород. Шееле дал новому газу имя «огненный воздух», но опубликовал свои эксперименты только в 1777 году. К этому времени Джозеф Пристли уже провел свои опыты и заявил о своем открытии, хотя и неправильно интерпретировал результаты своего эксперимента. Оба ученых рассказали о своих опытах величайшему химику того времени Антуану Лавуазье. Именно последний в 1775 году установил, что кислород является отдельным химическим элементом, а его двухатомная молекула входит в состав атмосферного воздуха. Труды Лавуазье навсегда опровергли одно из главных заблуждений в химии того времени, теорию флогистона, которой пытались объяснить процессы горения и окисления веществ.
А «официальный» первооткрыватель Джозеф Пристли прославился тем, что в рамках своих многочисленных экспериментов открыл для науки сразу несколько важных химических соединений, среди которых оксиды углерода и серы, аммиак и хлор.
Свойства кислорода
Применение кислорода.
Применение кислорода в промышленном производстве стало возможным с изобретением детандеров в середине прошлого столетия. Детандеры преобразуют потенциальную энергию газа в механическую, при этом газ совершает работу и охлаждается. Таким образом проводят сжижение и разделение воздуха, получая в итоге азот и кислород.
Кислород, будучи сильнейшим окислителем, способствует полному сгоранию топлива, что используется в разных отраслях промышленности. Выплавка металла из руды невозможна без использования кислорода. Жидкий кислород применяется как окислитель для ракетного топлива, особенно в смеси с озоном. Не только космические корабли, но и все современные самолеты не могут обойтись без кислорода во время полета. За один трансокеанический перелет сжигается свыше 10 тонн жидкого кислорода.
В металлургии кислород применяется при конвертерном производстве стали и прокатных изделий. Также он необходим при газопламенной сварке и резке металлов. Используется в качестве реактива-окислителя при синтезе спиртов, альдегидов, аммиака в химической промышленности.
В пищевой промышленности выступает в роли пропеллента (для распыления других веществ), в качестве упаковочного газа и даже как пищевая добавка (Е 948).
В медицине применяется в специальных баллонах в сжиженном состоянии для разных целей: применим в качестве ингалятора, устраняет гипоксию, обогащает дыхательные смеси при наркозе, восстанавливает работу желудочно-кишечного тракта (т.н. кислородные коктейли).
В рыбоводстве кислородом насыщают водную среду для увеличения продуктивности (в теплой воде содержание кислорода ниже, чем в холодной, но большая часть промысловых рыб не способна жить при низких температурах водной среды).
Интересные факты
Содержание кислорода в современной атмосфере — 21% — является необходимым и достаточным для функционирования человека как живого существа. Однако в крупных городах количество кислорода снижено до 17-18%. Это объясняется нехваткой зеленых растений, фотосинтезирующая деятельность которых как раз и восполняет баланс газообразного кислорода в атмосфере. При неблагоприятных метеорологических условиях содержание кислорода в городской черте может опуститься и до 10%, что критично для нашей жизнедеятельности. Ведь при 7%-ном содержании кислорода в воздухе человек погибает. Синдром нехватки кислорода называется гипоксией и проявляется в общей слабости, быстрой утомляемости, бессоннице, снижении внимания, частыми головными болями и повышенной восприимчивости к инфекциям. Считается, что именно нехватка кислорода в мозге обуславливает депрессию.
У человека есть рефлекторный прием кратковременного увеличения количества кислорода в организме – зевота. Считается, что мы зеваем именно в том случае, когда содержание кислорода в головном мозге падает ниже нормального уровня.
В горных местностях воздух более разрежен и содержание в нем кислорода понижено. В ходе эволюции у коренных жителей таких территорий порог чувствительности к нехватке кислорода снизился. Поэтому, жители Непала, Бутана, Боливии, Грузии прекрасно себя чувствуют на высотах свыше 3-4 километров, в то время как представители других национальностей чувствуют усталость, тошноту, а при подъеме выше вынуждены пользоваться кислородными масками.Кислород применяется в самых различных сферах науки, промышленности и сельского хозяйства.
Компания ООО «Спецсервис» осуществляет доставку жидкого кислорода в любой город России.
Исходя из условий поставки и необходимого объема продукции мы сможем предложить Вам оптимальную цену.
Позвоните нам, наши специалисты готовы ответить на любой Ваш вопрос: +7 (8634) 38-38-49.