Уксус
Изготовление уксуса
Такой уксус может быть плодово-ягодным или настоянным на ароматных травах.
Синтетический уксус получают в результате реакции различных химических элементов.
Одним из самых дорогих видов уксуса является бальзамический уксус, который готовят из винограда определенного сорта. Этот виноград собирают перезревшим, отправляют под пресс, варят, процеживают и наливают в бочки, где он хранится от 12 до 50 лет.
Чтобы приготовить винный уксус из винограда в домашних условиях необходимо выжать сок из винограда, полученный жмых поместить в банку из стекла (примерно на половину), добавить воду (в пропорции примерно 1 к 1), и сахар (чем больше сахара, тем концентрированнее получится уксус). банку отправить в теплое темное место для брожения.
Ежедневно необходимо размешивать содержимое деревянной палочкой. Через 14 дней процеживаем, к жидкости добавляем сахар и вновь убираем в теплое темное место для брожения.
Как только содержимое банки посветлеет, перестанет бродить, уксус готов. Переливаем в стеклянные банки и с пользой используем в своих кулинарных шедеврах.
Ароматизированный уксус
В первую очередь уксус – это результат естественного скисания фруктовых соков или плодов. Этот продукт издавна применяли не только для создания кулинарных «шедевров» того времени, но и не меньшим успехом он пользовался в области медицины и косметологии.
В настоящее время разновидность уксуса поражает своим многообразием.
Самым популярным является фруктовый и ароматизированный уксус.
Так же из выше перечисленных видов стоит выделить синтетический уксус. Это уксус, произведенный за счет химически синтезированной кислоты. Так же известна уксусная эссенция, представляющая собой раствор 80% уксусной кислоты.
Ароматизированный уксус чаще относят к продуктам домашнего производства.
Его без труда можно приготовить самостоятельно, ведь формула его приготовления состоит и сочетания синтетического, яблочного или винного уксуса в равных частях, а в качестве ароматической добавки можно использовать любые пряные травы ( мяту, базилик, мелису, тархун и т.д.) или же различные пряности ( перец, кориандр, гвоздику, корицу, имбирь ).
Следует отметить, что технология приготовления различается термической обработкой продуктов. То есть существует холодный и горячий способ приготовления уксуса.
Так же ароматизированный уксус можно купить и в обычном продовольственном магазине, чаще всего встречается можжевеловый и с травой тархуна.
Как правильно хранить уксус?
Уксус – незаменимый ингредиент многих тысяч блюд и салатов, различных соусов и маринадов. Многие продукты современные хозяйки хранят именно в этой приправе. Но мало кто знает, что уксус также надо хранить должным образом.
В первую очередь обратите внимание на тару для хранения. Нельзя хранить уксус в металлических или пластиковых контейнерах.
Потому как металл со временем начнет окисляться и портить данный продукт, а пластик разъедаться и выделять токсичные вещества. Оптимальный вариант – это стеклянная посуда.
Важно, чтобы бутылка была тщательно закрыта. Иначе уксус потеряет все свои полезные свойства и качества, так как будет подвержен испарениям.
Бутылку с этой приправой храните в темном прохладном месте, но не в холодильнике. Если это только не фруктовый и травяной уксус, потому как только там они сохраняют свой аромат и благодатные свойства.
Для остальных сортов уксуса лучше всего подойдет шкаф в кладовке, подальше от различных источников тепла: плиты или отопительных батарей. Под солнечными лучами, в тепле уксус может забродить и придти в негодность.
Если вы заметили, что на дне бутылки образовался осадок, а сверху пена, то без промедления выкидывайте продукт. Он безнадежно испорчен.
Постарайтесь, чтобы уксус хранился в недоступном для детей месте, потому как последствия отравления весьма печальны и неизлечимы.
Сколько уксуса в столовой ложке
Вопрос напрямую связан с размером самой ложки. Только в России используют два вида столовых ложек, разных по размеру. Исходя из базовых показателей, и стоит определять вместимость каждой из них.
Итак, давайте посмотрим классический пример столового прибора:
Обсуждаемый вариант столовой ложки, вмещает от 12 до 18 гр., уксуса. Одна из них, размером 5х3,5 см., вторая 7х4 см.
Ложки Канадского, или Американского происхождения, вмещают 15 гр., уксуса. Если кого-то интересуют другие возможности столовых ложек, для этого имеются специальные таблицы.
Как правило, общепринятая мера столовых приборов, связана со стандартами каждой отдельной страны производителя, но, для точного определения объема, нужно обращаться к эксперту по стандартизации.
Полезен ли яблочный уксус?
Также, уксус имеет в себе пектин и достаточно сильный антиоксидант – провитамин.
Как быстро устранить неприятный запах уксуса
Уксус применяют в домашнем консервировании и для приготовления различных блюд, поскольку именно уксус придает многим блюдам пикантности.
Используя уксус, можно вывести плесень и бактерии со многих поверхностей, а также, обработав уксусом, например разделочные доски или полки в холодильнике, можно быстро избавиться от неприятных ароматов.
Очистка уксусом простой и проверенный временем метод, который поможет очистить помещение без применения токсических веществ.
Уксус имеет довольно специфический и резкий запах, который многим неприятен, или например, если уксус случайно попал на одежду или обувь, но и это не проблема.
Следующие советы помогут вам без проблем избавиться от въедливого на первый взгляд запаха уксуса.
Для начала нужно проветрить помещение. Уксус испаряется, соответственно с парами испарения исчезнет и его запах. Откройте все окна в квартире, так что бы воздух был сквозной. Практически уже через два часа от запаха уксуса не останется и напоминания.
Для удаления плесени, пота или других загрязнений с поверхности одежды, ткань на несколько минут замачивают в растворе уксуса. Избавиться от аромата уксуса поможет обычная стирка в стиральной машинке.
Помимо стирального порошка лучший результат даст применение кондиционера для ткани. Если в стиральной машинке предусмотрен режим дополнительного полоскания, для достижения лучшего эффекта, обязательно примените его.
Обычно с поверхностей запах уксуса исчезает спустя 10-12 часов, но если нужно удалить запах уксуса нужно незамедлительно, тогда поможет обычное моющее средство для посуды.
После чего поверхность тщательно промывают водой и насухо вытирают.
Отличным помощником для удаления запаха уксуса, да и не только, является обычная пищевая сода. Для этого в нескольких местах нужно расставить емкости с насыпанной в них содой. Пищевая сода просто напросто впитывает в себя неприятные запахи.
Избавиться от запаха уксуса с коврового покрытия или другого мягкого и ворсистого материала можно используя мыльный раствор с добавлением нашатырного спирта.
Для этого потребуется соблюдать следующую пропорцию: на 5 литров воды добавить одну столовую ложку порошка и 2 столовые ложки нашатырного спирта.
Полученным раствором тщательно обработать поверхность, а после полного высыхания пропылесосить.
Если случайно при приготовлении блюда вы добавили больше уксуса чем нужно, не стоит переживать.
Просто увеличьте время приготовления блюда и снимите крышку. Уксус в процессе готовки просто испариться уже через полчаса.
Физические свойства уксусной кислоты и ее водного раствора.
Растворение уксусной кислоты в воде сопровождается выделением тепла и, следовательно, повышением температуры раствора. Однако выделение тепла происходит только при определенном соотношений уксусной кислоты и воды. При приготовлении значительно разбавленных растворов происходит поглощение тепла, и температура понижается.
Других соединений уксусной кислоты с водой, по-видимому, не существует, так как кривая имеет только один минимум, отвечающий 62,5% СН3СООН. Впрочем, до концентрации 62,5% кривая имеет некоторую мало заметную выпуклость, а выше 62,5% также мало заметную вогнутость. Это указывает на существование других соединений уксусной кислоты с водой, которые, однако, не являются стабильными и ярко выраженными.
Впервые соединение уксусной кислоты и воды состава С2Н4О2•2Н2О было обнаружено автором и описано им в 1939 г. Образование гидрата СН3СООН•2Н2О подтверждено исследованиями А. А. Глаголевой, а также С.Я. Левитмана и Н.Ф. Ермоленко. Последними авторами по максимуму показателя преломления предположено также существование молекулярного соединения 2СН3СООН•Н2О.
При замораживании растворов, содержащих уксусной кислоты больше 62,5%, вымерзает более концентрированная кислота, а из растворов, содержащих менее 62,5%, вымерзают более разбавленные растворы. Этим свойством иногда пользуются в промышленности для получения более концентрированной уксусной кислоты из разбавленной.
При перегонке водных растворов уксусной кислоты содержание кислоты в парах всегда меньше, чем в растворе. При этом разница между содержанием уксусной кислоты в парах и в жидкости увеличивается по мере того, как содержание кислоты в растворе приближается к величине, соответствующей гидрату С2Н4О2•2Н2О. Эта разница максимальна, когда содержание уксусной кислоты в растворе равно 62,5%.
При высоких давлениях и более высоких концентрациях возможно активное образование азеотропа уксусной кислоты, а также воды. И тогда будет невозможным процесс разделения смеси ректификацией.
Содержание солей в водных растворах уксусной кислоты вызывает повышение содержания уксусной кислоты в парах при перегонке, а при определенной концентрации соли и кислоты возможно даже образование азетропа уксусной кислоты и воды.
Уксусная кислота
Уксусная кислота — органическое соединение, одноосновная карбоновая кислота состава CH 3 COOH. При обычных условиях представляет собой бесцветную жидкость с резким запахом. Температура плавления чистой кислоты несколько ниже комнатной температуры, при замерзании она превращается в бесцветные кристаллы — это дало ей техническое наименование ледяная уксусная кислота.
Название кислоты образована словом уксус, что происходит от лат. Acetum — кислое вино. По номенклатуре IUPAC она систематическую название етанова кислота, которая характеризует соединение как производную этана. Поскольку молекула кислоты имеет в своем составе функциональную группу ацетил CH 3 CO (условное обозначение Ac), ее формула также может записываться как AcOH. В контексте кислотно-основных взаимодействий символом Ac иногда сказывается ацетат-анион CH 3 COO — — в таком случае формула будет иметь запись HAc.
Взаимодействуя с металлами, щелочами и спиртами, уксусная кислота образует ряд солей и эфиров — ацетатов (етаноатив).
Уксусная кислота — один из базовых продуктов промышленного органического синтеза. Более 65% мирового производства уксусной кислоты идет на изготовление полимеров, производных целлюлозы и винилацетата. Поливинилацетат является основой многих ґрунтивних покрытий и красок. С ацетатной целлюлозы изготавливают ацетатного волокна. Уксусная кислота и ее эфиры важные промышленные растворители и экстрагенты.
Общие сведения
Уксусная кислота известна человечеству с древнейших времен. Уксус, 4-12% раствор уксусной кислоты в воде, как продукт ферментации вина получил широкое використування более чем 5000 лет назад, прежде всего как пищевой консервант. Древнегреческий врач Гиппократ использовал растворы кислоты в качестве антисептика, а также в составе настоек от многочисленных заболеваний, включая лихорадку, запоры, желудочные язвы, плеврит.
Уксусная кислота находится в низких концентрациях во многих растительных и животных системах. Она, в частности, синтезируется бактериями рода Acetobacter и Clostridium. Среди рода Acetobacter наиболее эффективно вид Acetobacter aceti.
В 1996 году американскими учеными было сообщено о наблюдении молекул уксусной кислоты в газо-пылевом облаке Стрелец B2. Подобное открытие впервые было осуществлено с применением интерферометрической оборудования.
Физические свойства
Уксусная кислота при стандартном состояния является бесцветной жидкостью с резким запахом. При замерзании при температуре 16,635 ° С, она превращается в прозрачные кристаллы (ледяная уксусная кислота).
| 25 ° C | 50 ° C | 75 ° C | 100 ° C | 110 ° C |
|---|---|---|---|---|
| 1,056 | 0,786 | 0,599 | 0,464 | 0,424 |
Уксусная кислота неограниченно смешивается с водой, образует значительное количество азеотропных смесей с органическими растворителями:
| Второй компонент | Температура кипения, ° C | Содержание кислоты,% | Содержание второго компонента,% |
|---|---|---|---|
| Гексан | 68,3 | 6,0 | 94,0 |
| Октан | 105,7 | 53,7 | 46,3 |
| Циклогексан | 78,8 | 9,6 | 90,4 |
| Бензол | 80,05 | 2,0 | 98,0 |
| Толуол | 100,6 | 28,1 | 71,9 |
| Етилбензен | 114,65 | 66 | 34 |
| Стирен | 116,8 | 85,7 | 14,3 |
| Пиридин | 138,1 | 51,1 | 48,9 |
| Тетрахлорметан | 76 | 98,46 | 1,54 |
| Хлоробензен | 114,7 | 58,5 | 41,5 |
| Нитроэтан | 112,4 | 30 | 70 |
Другие физические свойства:
Получение
Синтез растворов уксусной кислоты (уксуса) проводится в основном методом ферментации, а для получения чистой кислоты, в значительных масштабах применяются методы карбонилирования метанола, окисления бутана и этаналя. Основным методом является получение из метанола.
Карбонилирования метанола
Возможность получения уксусной кислоты из метанола была открыта в немецком концерне BASF в 1913 году:
В 1938 году сотрудник BASF Вальтер Реппе продемонстрировал эффективность использования в качестве катализаторов карбонилов металлов VIIIB группы (группа 9), в частности, карбонила кобальта [Co 2 (CO) 8]. Первое полномасштабное производство с применением кобальтового катализатора было развернуто в 1960 году в Людвигсгафени, Германия.
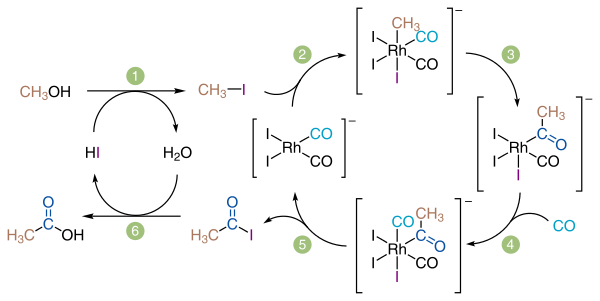
В конце 1960-х в компании «Monsanto» разработали новый тип катализаторов на основе родия, которые имели значительно более высокую активность и селективность по сравнению с кобальтовым: даже при атмосферном давлении выход конечного продукта составлял 90-99%. В 1986 году этот метод приобрел «BP Chemicals» и передал его на совершенствование компании «Celanese».
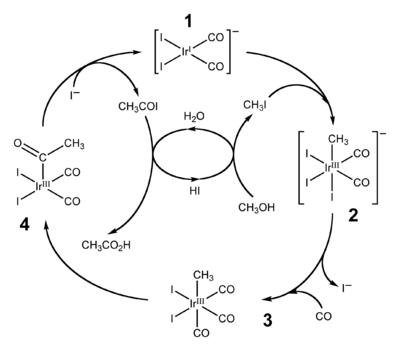
В начале 1990-х «Monsanto» запатентовала использование нового, иридиевого, катализатора. Его преимущество заключалось в большей стабильности и меньшем количестве жидких побочных продуктов. «BP» приобрел права на этот патент и внедрил в производство под названием метод Cativa (англ. Cativa process).
Метод BASF
В производстве по методу BASF катализатором выступает карбонил кобальта [Co 2 (OH) 8], который in situ получают из йодида кобальта (II):

На первой стадии исходный метанол взаимодействует с йодоводнем, который является сопутствующим продуктом синтеза карбонила, с образованием йодометану:
Йодометан реагирует с карбонил:
Впоследствии проводится карбонилирования что ведет к сложному ацилкарбонильного интермедиата:
Под действием йодид-ионов комплекс разлагается, высвобождая катализатор и ацетилйодид, который гидролизуется до уксусной кислоты:

Для реакции карбонилирования метанола чрезвычайно важны парциальные давления исходных веществ. Так, выход конечного продукта достигает 70% в зависимости от подачи монооксида углерода и 90% в зависимости от метанола.
Метод Monsanto
Компания «Celanese» усовершенствовала этот метод, дополнив его циклом оптимизации кислот, когда незначительная дополнительное количество уксусной кислоты в форме ацетат-ионов подавалась на катализатор и повышала его эффективность при низких концентрациях исходных соединений.
Синтез проводится при температуре 150-200 ° C и давлении 3,3-3,6 МПа.
Метод Cativa
Окисления этаналя
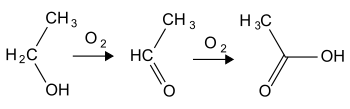
Прекурсором для получения уксусной кислоты служит этаналь, который синтезируют окислением этанола в присутствии солей серебра:
Окисление альдегида происходит по радикальному механизму с использованием инициатору:
Реакция проходит через стадию образования пероксоацетатного радикала:

Полученная пероксоацетатна кислота реагирует с ацетальдегидом с образованием ацетальдегидперацетату, который по механизму перегруппировки Байера — Виллигера разлагается на уксусную кислоту:

Побочным продуктом является метилформиат, который образуется в результате миграции метильной группы.
Катализаторами взаимодействий являются соли кобальта или марганца. Они также играют важную роль в уменьшении количества перацетат-радикалов в реакционной системе, тем самым предотвращая образование взрывоопасных концентраций:

Взаимодействия по этому методу проводятся при температуре 60-80 ° C и давлении 0,3-1,0 МПа. Преобразование альдегида в ацетатную кислоту обычно происходит с выходом более 90% и селективностью по кислотой более 95%.
Окисления углеводородов
Уксусная кислота может быть получена из бутана и легких фракций нефти. Этот метод является одним из самых распространенных благодаря низкой стоимости углеводородного сырья. В присутствии металлических катализаторов типа кобальта, хрома, марганца, бутан окисляется воздухом:
Основными побочными продуктами являются ацетальдегид и бутанон.
Ферментация
Некоторые бактерии, в частности, рода Acetobacter и Clostridium, производят кислоту в процессе своей жизнедеятельности. Использование человеком подобных ферментационных процессов известно еще с давних времен. Таким образом образуется низкоонцентрированных уксусная кислота, которая полностью удовлетворяет бытовые нужды.
К ферментативного производства привлекаются виды бактерий Acetobacter aceti и искусственно выведенные Clostridium thermoaceticum. Для подкормки бактерий используют сахаросодержащую сырье — глюкозу, ксилозу и т.п.:
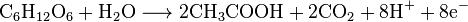
Значительным преимуществом этого метода является полная экологичность производства.
Химические свойства
В газовой фазе между молекулами кислоты возникают водородные связи, поэтому они находятся преимущественно в димерних форме (также известные тетрамеры):
Кроме этого возможно образование гидратированного димера: молекулы сочетаются между собой только одним связью, а к свободным карбоксильной и гидроксильной групп присоединяются водородными связями по одной молекуле воды. Степень превращения в димерные структур увеличивается с повышением концентрации раствора и снижается с повышением температуры.
Уксусная кислота является типичной карбоновой кислотой, она участвует во всех реакциях, характерных для этого ряда соединений. В водном растворе кислота распадается и отдает ион H + молекулам воды, образуя структуру с двумя равными связями C-O:
Проявляя кислотные свойства, уксусная кислота взаимодействует с активными металлами, оксидами и гидридами металлов, металлоорганических соединений, аммиаком, образуя ряд солей — ацетатов.




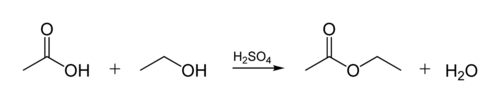
Органические ацетаты является эфирами — продуктами взаимодействия кислоты со спиртами:
Конденсацией кислоты с этен синтезируют винилацетата — промышленно важную соединение, мономер поливинилацетата:
При воздействии сильных обезвоживающих агентов (типа P 2 O 5) образуется уксусный ангидрид. Аналогичным результат при участии некоторых агентов хлорирования (тионилхлорида, фосгена) — тогда синтез ангидрида проходит через стадию получения ацетилхлорида.
Пропуская разогретую пару кислоты над катализатором (оксидами марганца, тория, циркония), можно синтезировать ацетон (с выходом около 80%):
При нагревании до 600 ° C уксусная кислота дегидратируется к Кётене — етенону:
Токсичность
Находясь в состоянии пара в воздухе, кислота повреждает глаза, нос и горло уже при концентрации более 10 мг / м³. Серьезные последствия наблюдаются при десятидневной повторяющейся действия загрязненной кислотой воздуха с содержанием до 26 мг / м³.
Низкоонцентрированных растворы уксусной кислоты (около 5%) могут раздражать слизистые оболочки. Концентрированная кислота в значительной степени повреждает кожу при контакте: в случае ее попадания, необходимо промыть пораженное место большим количеством воды или раствора пищевой соды. При проглатывании уксусной кислоты наблюдается боль в пищеводе и рту, это может привести к появлению тошноты и проблем с дыханием. В этом случае необходимо ополоснуть ротовую полость и обратиться к врачу.
Токсические дозы при потреблении кислоты человеком точно не известны. Полулетальные дозой для крыс является 3310 мг / кг, для кроликов — 1200 мг / кг. Потребление человеком 89-90 г чистой кислоты крайне опасно, а предельной численностью для ежедневного потребления является 2,1 г.
Применение
Применение уксусной кислоты достаточно разнообразное. В химической промышленности из нее производят пластические массы, различные красители, лекарственные вещества, искусственное волокно (ацетатный шелк), невоспламеняющуюся кинопленку и многие другие вещества. Соли уксусной кислоты — ацетаты алюминия, хрома, железа — применяют как протраву при окраске тканей. Уксусная кислота имеет широкое применение и в качестве растворителя.
В пищевой промышленности применяется как консервант, регулятор кислотности и вкусовая приправа; в Европейской системе пищевых добавок уксусная кислота имеет код E260.
Кислота применяется при солянокислотного обработке призабойной зоны пласта в качестве стабилизатора (с целью стабилизации продуктов реакции) от выпадения складновилучуваних гелеобразных соединений железа (осадка). В зависимости от содержания железа в кислотном растворе (от 0,01 до 0,5%) берут 1-3% уксусную кислоту. Для приготовления рабочих растворов используют как синтетическую кислоту, так и лесохимическую техническую очищенную.