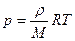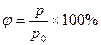§ 6.4. Критическая температура. Критическое состояние
Критическая температура
При достаточно высоких температурах горизонтальный участок изотермы реального газа (см. рис. 6.4) становится совсем коротким и при некоторой температуре обращается в точку (на рис. 6.4 — точка К). Эту температуру называют критической. Критической называется температура, при которой исчезают различия в физических свойствах между жидкостью и паром, находящимся с ней в динамическом равновесии. Каждое вещество имеет свою критическую температуру. Например, критическая температура для углекислоты СO2 равна tK = 31 °С, а для воды — tK = 374 °С.
Критическое состояние
Состояние, соответствующее точке К, в которую обращается горизонтальный участок изотермы при температуре Т = Тк, называют критическим состоянием (критическая точка). Давление и объем в этом состоянии называют критическими. Критическое давление для углекислого газа равно 7,4 • 10 6 Па (73 атм), а для воды 2,2 • 10 7 Па (218 атм). В критическом состоянии жидкость имеет максимальный объем, а насыщенный пар — максимальное давление.
Плотность жидкости и ее насыщенного пара при критической температуре
Мы уже отмечали, что при увеличении температуры возрастает плотность насыщенного пара (см. § 6.3). Плотность жидкости, находящейся в равновесии со своим паром, наоборот, уменьшается вследствие ее расширения при нагревании.
В таблице 2 приведены значения плотности воды и ее насыщенного пара для разных температур.
Таблица 2
Если на одном рисунке начертить кривые зависимости плотности жидкости и ее насыщенного пара от температуры, то для жидкости кривая пойдет вниз, а для пара — вверх (рис. 6.6). При критической температуре обе кривые сливаются, т. е. плотность жидкости становится равной плотности пара. Различие между жидкостью и паром исчезает.
Газ и пар
Мы много раз употребляли слова «газ» и «пар». Эти термины возникли в те времена, когда считалось, что пар может быть превращен в жидкость, а газ нет. После того как все газы были сконденсированы (см. § 6.7), для такой двойственной терминологии не осталось оснований. Пар и газ — это одно и то же, между ними принципиальной разницы нет. Когда говорят о паре какой-нибудь жидкости, то обычно имеют в виду, что его температура меньше критической и сжатием его можно превратить в жидкость. Только по привычке мы говорим о водяном паре, а не о водяном газе, о насыщенном паре, а не о насыщенном газе и т. д.
Экспериментальное исследование критического состояния
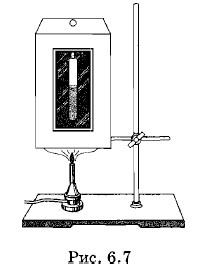
Эксперименты по изучению критического состояния выполнил в 1863 г. русский ученый М. П. Авенариус. Прибор, с помощью которого можно наблюдать критическое состояние (прибор Авенариуса), состоит из воздушной ванны (рис. 6.7) и находящейся внутри ванны запаянной стеклянной трубочки (ампулы) с жидким эфиром. Объем ампулы (ее вместимость) равен критическому объему эфира, налитого в трубочку. Пространство над эфиром в ампуле заполнено насыщенным паром эфира.
При помощи газовой горелки или другого нагревателя воздушную ванну подогревают. За состоянием эфира наблюдают через стеклянное окошко в приборе.
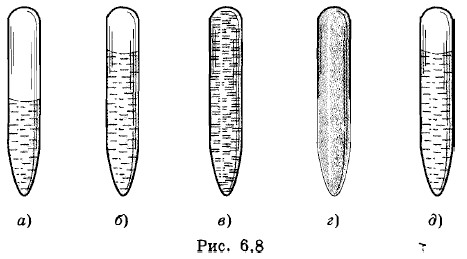
При комнатной температуре можно отчетливо видеть границу между жидкостью и паром (рис. 6.8, а). По мере приближения к критической температуре объем жидкого эфира увеличивается, а граница раздела жидкость — пар становится слабовыраженной, неустойчивой (рис. 6.8, б).
При подходе к критическому состоянию граница между ними исчезает совсем (рис. 6.8, в).
При охлаждении появляется плотный туман, заполняющий всю трубочку (рис. 6.8, г). Это образуются капельки жидкости. Далее они сливаются вместе, и опять возникает граница раздела между жидкостью и паром (рис. 6.8, д).
Для опыта выбран эфир, так как он имеет сравнительно низкое критическое давление (около 36 атм). Критическая температура его тоже невелика: 194 °С.
Если сжимать газ, поддерживая его температуру выше критической (см. рис. 6.4, изотерма Т3), причем, как и раньше, начать с очень больших объемов, то уменьшение объема приведет к возрастанию давления в соответствии с уравнением состояния идеального газа. Однако если при температуре ниже критической при определенном давлении происходила конденсация пара, то теперь образования жидкости в сосуде наблюдаться не будет. При температуре выше критической газ нельзя обратить в жидкость ни при каких давлениях.
В этом и состоит основное значение понятия критической температуры.
Диаграмма равновесных состояний газа и жидкости
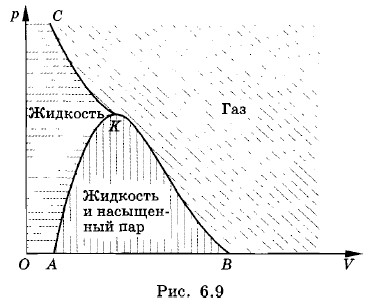
Еще раз вернемся к рисунку 6.4, на котором изображены изотермы реального газа. Соединим все левые концы горизонтальных участков изотерм, т. е. те точки, которые соответствуют окончанию конденсации насыщенного пара и началу сжатия жидкости. Получится плавная кривая, оканчивающаяся в критической точке К. На рисунке 6.9 это кривая ART. Слева от кривой АК, между ней и критической изотермой (участок изотермы СК), расположена область, соответствующая жидкому состоянию вещества (на рис. 6.9 эта область выделена горизонтальной штриховкой). Каждой точке этой области соответствуют параметры р, V и Т, характеризующие жидкость в состоянии теплового равновесия.
Соединим теперь плавной кривой все правые концы горизонтальных участков изотерм. Эта кривая на рисунке 6.9 тоже заканчивается в точке К. Две линии АК и ВК ограничивают область, каждая точка которой соответствует состоянию равновесия между жидкостью и насыщенным паром (на рис. 6.9 эта область выделена вертикальной штриховкой). За исключением области жидкого состояния и области равновесия жидкости с газом вся остальная область соответствует газообразному состоянию вещества. На рисунке 6.9 она выделена косой штриховкой.
В результате получилась диаграмма равновесных состояний газа и жидкости. Каждой точке на этой диаграмме соответствует определенное состояние системы: газ, жидкость или равновесие между жидкостью и газом.
При критической температуре свойства жидкости и насыщенного пара становятся неразличимыми. Выше критической температуры жидкость не может существовать.
Критическая температура — это температура, при которой исчезают различия в физических свойствах между жидкостью и ее насыщенным паром



При критической температуре плотность и давление насыщенного пара становятся максимальными, а плотность жидкости, находящейся в равновесии с паром,— минимальной.
Содержание водяного пара в воздухе, т. е. его влажность, можно характеризовать несколькими величинами.
Ø Парциальное давление водяного пара.
Атмосферный воздух представляет собой смесь различных газов и водяного пара. Каждый из газов вносит свой вклад в суммарное давление, производимое воздухом на находящиеся в нем тела. Давление, которое производил бы водяной пар, если бы все остальные газы отсутствовали, называют парциальным давлением водяного пара.Парциальное давление водяного пара принимают за один из показателей влажности воздуха. Его выражают в единицах давления — Паскалях или в миллиметрах ртутного столба.
Ø Относительная влажность.
Относительной влажностью воздуха 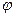
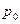
Ø Психрометр.
Влажность воздуха измеряют с помощью специальных приборов, например, психрометр.
Психрометр состоит из двух термометров. Резервуар одного из них остается сухим, и он показывает температуру воздуха. Резервуар другого окружен полоской ткани, конец которой опущен в воду. Вода испаряется, и благодаря этому термометр охлаждается. Чем больше относительная влажность, тем менее интенсивно идет испарение и тем более высокую температуру показывает термометр, окруженный полоской влажной ткани.
При относительной влажности, равной 100%, вода вообще не будет испаряться и показания обоих термометров будут одинаковы. По разности температур этих термометров с помощью специальных таблиц можно определить влажность воздуха.
§ 6.4. Критическая температура. Критическое состояние
Вещество может находиться в жидком состоянии не при любой температуре. Есть предел.
Критическая температура
При достаточно высоких температурах горизонтальный участок изотермы реального газа (см. рис. 6.4) становится совсем коротким и при некоторой температуре обращается в точку (на рис. 6.4 — точка К). Эту температуру называют критической. Критической называется температура, при которой исчезают различия в физических свойствах между жидкостью и паром, находящимся с ней в динамическом равновесии. Каждое вещество имеет свою критическую температуру. Например, критическая температура для углекислоты СO2 равна tK = 31 °С, а для воды — tK = 374 °С.
Критическое состояние
Состояние, соответствующее точке К, в которую обращается горизонтальный участок изотермы при температуре Т = ТK, называют критическим состоянием (критическая точка). Давление и объем в этом состоянии называют критическими. Критическое давление для углекислого газа равно 7,4 • 10 6 Па (73 атм), а для воды 2,2 • 10 7 Па (218 атм). В критическом состоянии жидкость имеет максимальный объем, а насыщенный пар — максимальное давление.
Плотность жидкости и ее насыщенного пара при критической температуре
Мы уже отмечали, что при увеличении температуры возрастает плотность насыщенного пара (см. § 6.3). Плотность жидкости, находящейся в равновесии со своим паром, наоборот, уменьшается вследствие ее расширения при нагревании.
В таблице 2 приведены значения плотности воды и ее насыщенного пара для разных температур.
Если на одном рисунке начертить кривые зависимости плотности жидкости и ее насыщенного пара от температуры, то для жидкости кривая пойдет вниз, а для пара — вверх (рис. 6.6). При критической температуре обе кривые сливаются, т. е. плотность жидкости становится равной плотности пара. Различие между жидкостью и паром исчезает.
Газ и пар
Мы много раз употребляли слова «газ» и «пар». Эти термины возникли в те времена, когда считалось, что пар может быть превращен в жидкость, а газ нет. После того как все газы были сконденсированы (см. § 6.7), для такой двойственной терминологии не осталось оснований. Пар и газ — это одно и то же, между ними принципиальной разницы нет. Когда говорят о паре какой-нибудь жидкости, то обычно имеют в виду, что его температура меньше критической и сжатием его можно превратить в жидкость. Только по привычке мы говорим о водяном паре, а не о водяном газе, о насыщенном паре, а не о насыщенном газе и т. д.
Экспериментальное исследование критического состояния
Эксперименты по изучению критического состояния выполнил в 1863 г. русский ученый М. П. Авенариус. Прибор, с помощью которого можно наблюдать критическое состояние (прибор Авенариуса), состоит из воздушной ванны (рис. 6.7) и находящейся внутри ванны запаянной стеклянной трубочки (ампулы) с жидким эфиром. Объем ампулы (ее вместимость) равен критическому объему эфира, налитого в трубочку. Пространство над эфиром в ампуле заполнено насыщенным паром эфира.
При помощи газовой горелки или другого нагревателя воздушную ванну подогревают. За состоянием эфира наблюдают через стеклянное окошко в приборе.
При комнатной температуре можно отчетливо видеть границу между жидкостью и паром (рис. 6.8, а). По мере приближения к критической температуре объем жидкого эфира увеличивается, а граница раздела жидкость — пар становится слабовыраженной, неустойчивой (рис. 6.8, б).
При подходе к критическому состоянию граница между ними исчезает совсем (рис. 6.8, в).
При охлаждении появляется плотный туман, заполняющий всю трубочку (рис. 6.8, г). Это образуются капельки жидкости. Далее они сливаются вместе, и опять возникает граница раздела между жидкостью и паром (рис. 6.8, д).
Для опыта выбран эфир, так как он имеет сравнительно низкое критическое давление (около 36 атм). Критическая температура его тоже невелика: 194 °С.
Если сжимать газ, поддерживая его температуру выше критической (см. рис. 6.4, изотерма Т3), причем, как и раньше, начать с очень больших объемов, то уменьшение объема приведет к возрастанию давления в соответствии с уравнением состояния идеального газа. Однако если при температуре ниже критической при определенном давлении происходила конденсация пара, то теперь образования жидкости в сосуде наблюдаться не будет. При температуре выше критической газ нельзя обратить в жидкость ни при каких давлениях.
В этом и состоит основное значение понятия критической температуры.
Диаграмма равновесных состояний газа и жидкости
Еще раз вернемся к рисунку 6.4, на котором изображены изотермы реального газа. Соединим все левые концы горизонтальных участков изотерм, т. е. те точки, которые соответствуют окончанию конденсации насыщенного пара и началу сжатия жидкости. Получится плавная кривая, оканчивающаяся в критической точке К. На рисунке 6.9 это кривая АК. Слева от кривой АК, между ней и критической изотермой (участок изотермы СК), расположена область, соответствующая жидкому состоянию вещества (на рис. 6.9 эта область выделена горизонтальной штриховкой). Каждой точке этой области соответствуют параметры р, V и Т, характеризующие жидкость в состоянии теплового равновесия.
Соединим теперь плавной кривой все правые концы горизонтальных участков изотерм. Эта кривая на рисунке 6.9 тоже заканчивается в точке К. Две линии АК и ВК ограничивают область, каждая точка которой соответствует состоянию равновесия между жидкостью и насыщенным паром (на рис. 6.9 эта область выделена вертикальной штриховкой). За исключением области жидкого состояния и области равновесия жидкости с газом вся остальная область соответствует газообразному состоянию вещества. На рисунке 6.9 она выделена косой штриховкой.
В результате получилась диаграмма равновесных состояний газа и жидкости. Каждой точке на этой диаграмме соответствует определенное состояние системы: газ, жидкость или равновесие между жидкостью и газом.
§ 6.4. Критическая температура. Критическое состояние
Критическая температура
При достаточно высоких температурах горизонтальный участок изотермы реального газа (см. рис. 6.4) становится совсем коротким и при некоторой температуре обращается в точку (на рис. 6.4 — точка К). Эту температуру называют критической.
Критической называется температура, при которой исчезают различия в физических свойствах между жидкостью и паром, находящимся с ней в динамическом равновесии. Каждое вещество имеет свою критическую температуру. Например, критическая температура для углекислоты СO2 равна tK = 31 °С, а для воды — tK = 374 °С.
Критическое состояние
Состояние, соответствующее точке К, в которую обращается горизонтальный участок изотермы при температуре Т = Тк, называют критическим состоянием (критическая точка). Давление и объем в этом состоянии называют критическими. Критическое давление для углекислого газа равно 7,4 • 10 6 Па (73 атм), а для воды 2,2 • 10 7 Па (218 атм). В критическом состоянии жидкость имеет максимальный объем, а насыщенный пар — максимальное давление.
Плотность жидкости и ее насыщенного пара при критической температуре
Мы уже отмечали, что при увеличении температуры возрастает плотность насыщенного пара (см. § 6.3). Плотность жидкости, находящейся в равновесии со своим паром, наоборот, уменьшается вследствие ее расширения при нагревании.
В таблице 2 приведены значения плотности воды и ее насыщенного пара для разных температур.
Таблица 2
Если на одном рисунке начертить кривые зависимости плотности жидкости и ее насыщенного пара от температуры, то для жидкости кривая пойдет вниз, а для пара — вверх (рис. 6.6). При критической температуре обе кривые сливаются, т. е. плотность жидкости становится равной плотности пара. Различие между жидкостью и паром исчезает.
Газ и пар
Мы много раз употребляли слова «газ» и «пар». Эти термины возникли в те времена, когда считалось, что пар может быть превращен в жидкость, а газ нет. После того как все газы были сконденсированы (см. § 6.7), для такой двойственной терминологии не осталось оснований. Пар и газ — это одно и то же, между ними принципиальной разницы нет. Когда говорят о паре какой-нибудь жидкости, то обычно имеют в виду, что его температура меньше критической и сжатием его можно превратить в жидкость. Только по привычке мы говорим о водяном паре, а не о водяном газе, о насыщенном паре, а не о насыщенном газе и т. д.
Экспериментальное исследование критического состояния
Эксперименты по изучению критического состояния выполнил в 1863 г. русский ученый М. П. Авенариус. Прибор, с помощью которого можно наблюдать критическое состояние (прибор Авенариуса), состоит из воздушной ванны (рис. 6.7) и находящейся внутри ванны запаянной стеклянной трубочки (ампулы) с жидким эфиром. Объем ампулы (ее вместимость) равен критическому объему эфира, налитого в трубочку. Пространство над эфиром в ампуле заполнено насыщенным паром эфира.
При помощи газовой горелки или другого нагревателя воздушную ванну подогревают. За состоянием эфира наблюдают через стеклянное окошко в приборе.
При комнатной температуре можно отчетливо видеть границу между жидкостью и паром (рис. 6.8, а). По мере приближения к критической температуре объем жидкого эфира увеличивается, а граница раздела жидкость — пар становится слабовыраженной, неустойчивой (рис. 6.8, б).
При подходе к критическому состоянию граница между ними исчезает совсем (рис. 6.8, в).
При охлаждении появляется плотный туман, заполняющий всю трубочку (рис. 6.8, г). Это образуются капельки жидкости. Далее они сливаются вместе, и опять возникает граница раздела между жидкостью и паром (рис. 6.8, д).
Для опыта выбран эфир, так как он имеет сравнительно низкое критическое давление (около 36 атм). Критическая температура его тоже невелика: 194 °С.
Если сжимать газ, поддерживая его температуру выше критической (см. рис. 6.4, изотерма Т3), причем, как и раньше, начать с очень больших объемов, то уменьшение объема приведет к возрастанию давления в соответствии с уравнением состояния идеального газа. Однако если при температуре ниже критической при определенном давлении происходила конденсация пара, то теперь образования жидкости в сосуде наблюдаться не будет. При температуре выше критической газ нельзя обратить в жидкость ни при каких давлениях.
В этом и состоит основное значение понятия критической температуры.
Диаграмма равновесных состояний газа и жидкости
Еще раз вернемся к рисунку 6.4, на котором изображены изотермы реального газа. Соединим все левые концы горизонтальных участков изотерм, т. е. те точки, которые соответствуют окончанию конденсации насыщенного пара и началу сжатия жидкости. Получится плавная кривая, оканчивающаяся в критической точке К. На рисунке 6.9 это кривая ART. Слева от кривой АК, между ней и критической изотермой (участок изотермы СК), расположена область, соответствующая жидкому состоянию вещества (на рис. 6.9 эта область выделена горизонтальной штриховкой). Каждой точке этой области соответствуют параметры р, V и Т, характеризующие жидкость в состоянии теплового равновесия.
Соединим теперь плавной кривой все правые концы горизонтальных участков изотерм. Эта кривая на рисунке 6.9 тоже заканчивается в точке К. Две линии АК и ВК ограничивают область, каждая точка которой соответствует состоянию равновесия между жидкостью и насыщенным паром (на рис. 6.9 эта область выделена вертикальной штриховкой). За исключением области жидкого состояния и области равновесия жидкости с газом вся остальная область соответствует газообразному состоянию вещества. На рисунке 6.9 она выделена косой штриховкой.
В результате получилась диаграмма равновесных состояний газа и жидкости. Каждой точке на этой диаграмме соответствует определенное состояние системы: газ, жидкость или равновесие между жидкостью и газом.
При критической температуре свойства жидкости и насыщенного пара становятся неразличимыми. Выше критической температуры жидкость не может существовать.
При какой температуре исчезают различия в физических свойствах между жидкостью и ее насыщенным паром
Выполнила: Ковалкова А.А.
Цель: Узнать, разобраться и понять суть критического состояния вещества и критической температуры.
Задачи:
-объяснить значение и раскрыть понятия критического состояния вещества и критической температуры;
-показать их зависимость от веществ на графиках;
-рассказать про изменение плотности жидкости и ее насыщенного пара при критической температуре;
-дать информацию об экспериментальном исследовании критического состояния, выполненного русским ученым.
Критическое состояние вещества
Сходство свойств ненасыщенных паров и газов натолкнуло М. Фарадея на предположение: не являются ли газы ненасыщенными парами соответствующих жидкостей? Если предположение верно, то можно попытаться сделать их насыщенными и сконденсировать. Действительно, сжатием удалось сделать насыщенными многие газы, кроме шести, которые М. Фарадей назвал «постоянными»: это азот, водород, воздух, гелий, кислород, оксид углерода CO.
Чтобы понять, в чем здесь дело, изучим подробнее изотермический процесс сжатия (расширения) пара. Мы видели, что изотерма реального газа отличается от изотермы идеального газа наличием горизонтального участка, соответствующего области существования двухфазной системы: насыщенного пара и жидкости.
Если проводить опыты при более высоких температурах (T1 веществ
Критическая температура T кр — это такая температура, при которой плотность жидкости и плотность ее насыщенного пара становятся одинаковыми, т.е. находятся в динамическом равновесии. Каждое вещество имеет свою критическую температуру. Например, критическая температура для углекислоты СО2 равна tк = 31 °С, а для воды —tк= 374 °С.
На изотермах при Т = Tкр горизонтальный участок превращается в точку перегиба К.
Давление насыщенного пара какого-либо вещества при его критической температуре называется критическим давлением pкр. Оно является наибольшим возможным давлением насыщенных паров вещества.
Плотность жидкости и ее насыщенного пара при критической температуре
При увеличении температуры возрастает плотность насыщенного пара. Плотность жидкости, находящейся в равновесии со своим паром, наоборот, уменьшается вследствие ее расширения при нагревании.
Если на одном рисунке начертить кривые зависимости плотности жидкости и ее насыщенного пара от температуры, то для жидкости кривая пойдет вниз, а для пара — вверх. При критической температуре обе кривые сливаются, т. е. плотность жидкости становится равной плотности пара. Различие между жидкостью и паром исчезает.
Существование критической температуры вещества объясняет, почему при обычных температурах одни вещества могут быть как жидкими, так и газообразными, а другие остаются газами.
Выше критической температуры жидкость не образуется даже при очень высоких давлениях.
Таким образом, видно, что принципиальной разницы между газом и паром нет. Обычно газом называют вещество в газообразном состоянии, когда его температура выше критической. Паром называют также вещество в газообразном состоянии, но когда его температура ниже критической. Пар можно перевести в жидкость одним только увеличением давления, а газ нельзя.
Экспериментальное исследование критического состояния
Эксперименты по изучению критического состояния выполнил в 1863 г. русский ученый М. П. Авенариус. Прибор, с помощью которого можно наблюдать критическое состояние (прибор Авенариуса), состоит из воздушной ванны и находящейся внутри ванны запаянной стеклянной трубочки (ампулы) с жидким эфиром. Объем ампулы (ее вместимость) равен критическому объему эфира, налитого в трубочку. Пространство над эфиром в ампуле заполнено насыщенным паром эфира.
Если сжимать газ, поддерживая его температуру выше критической, причем, как и раньше, начать с очень больших объемов, то уменьшение объема приведет к возрастанию давления в соответствии с уравнением состояния идеального газа. Однако если при температуре ниже критической при определенном давлении происходила конденсация пара, то теперь образования жидкости в сосуде наблюдаться не будет. При температуре выше критической газ нельзя обратить в жидкость ни при каких давлениях. В этом и состоит основное значение понятия критической температуры.
Состояние вещества, характеризуемое критическими параметрами ркр (давление), Vкр (удельный объем), Ткр (температура), называется критическим состоянием.
Удельная теплота парообразования, коэффициент поверхностного натяжения при Т=Ткр обращается в нуль.
При температурах Т>Ткр даже при очень больших давлениях невозможно превращение пара в жидкость.
При сверхкритических температурах возможно только парообразное состояние вещества.
Список литературы и источников:
1.Аксенович Л. А. Физика в средней школе: Теория. Задания. Тесты: Учеб. пособие для учреждений, обеспечивающих получение общ. сред, образования / Л. А. Аксенович, Н.Н.Ракина, К. С. Фарино; Под ред. К. С. Фарино. — Мн.: Адукацыя i выхаванне, 2004. — C. 176-178.
Мини-проект по теме «Критическая температура. Критическое состояние».
Выполнила Макарова Анастасия
Задачи:
1) Краткие сведения о критической температуре и критическом состоянии
2) Свойства критической температуры
3) Рассмотреть тройной график
4) Определить, где применяются знания о критической температуре
Краткие сведения о критической температуре и критическом состоянии:
Существование критической температуры было впервые предсказано в 1860г. Д.И.Менделеевым. Исследуя изменение поверхностного натяжения жидкости в зависимости от температуры, Менделеев пришел к выводу, что должна существовать такая температура, при которой на данной жидкости поверхностное натяжение равно нулю и, таким образом, исчезают мениск (искривлённая поверхность жидкости в капиллярной трубке или между близко расположенными твёрдыми стенками) жидкости и различие между жидкостью и ее насыщенным паром. Это и есть критическая температура.
Идеи Менделеева несколько лет спустя были полностью подтверждены опытами Эндрюса.
Первые наиболее обширные и систематические исследования критических параметров ряда веществ были проведены русским физиком М.П.Авенариусом и его учениками в 1873-1895гг.
Свойства вещества в критическом состоянии были также всесторонне исследованы выдающимся русским физиком А.Г.Столеновым.
В 1947-1950гг. понимание критического состояния вещества было уточнено и расширено профессором В.К,Семенченко.
Критическая температура – это температура, при которой исчезают различия в физических свойствах между жидкостью и паром, находящимся с ней в динамическом равновесии.
Критическое состояние – состояние, соответствующее точке К, в которую обращается горизонтальный участок изотермы при температуре Т=Тк.
Свойства критической температуры:
1) Для критического состояния характерно высокое значение теплоемкости и коэффициента теплового расширения
2) Для насыщенного пара давление и температура увеличиваются или убывают совместно
3) Переход из жидкости в пар и из пара в жидкость происходит непрерывно
4) В критическом состоянии жидкость имеет максимальный объем, а насыщенный пар – максимальное давление
5) При критической температуре плотность жидкости становится равной плотности пара, следовательно различие между паром и жидкостью исчезает
Тройной график (диаграмма равновесных состояний газа и жидкости):
При изменении концентрации компонентов в газах и жидкостях, а также в процессе их охлаждения или нагрева (при условии постоянного внешнего давления) происходят существенные фазовые и структурные изменения, которые можно наглядно проследить с помощью диаграмм состояния.
рис. 1 рис. 2
Соединим все левые концы горизонтальных участков изотерм, т. е. те точки, которые соответствуют окончанию конденсации насыщенного пара и началу сжатия жидкости. Получится плавная кривая, оканчивающаяся в критической точке К. На рисунке 2 это кривая АК. Слева от кривой АК, между ней и критической изотермой (участок изотермы СК), расположена область, соответствующая жидкому состоянию вещества (на рис. 2 эта область выделена горизонтальной штриховкой).
Соединим теперь плавной кривой все правые концы горизонтальных участков изотерм. Эта кривая на рисунке 2 тоже заканчивается в точке К. Две линии АК и ВК ограничивают область, каждая точка которой соответствует состоянию равновесия между жидкостью и насыщенным паром (на рис. 2 эта область выделена вертикальной штриховкой). За исключением области жидкого состояния и области равновесия жидкости с газом вся остальная область соответствует газообразному состоянию вещества. На рисунке 2 она выделена косой штриховкой.
В результате получилась диаграмма равновесных состояний газа и жидкости. Каждой точке на этой диаграмме соответствует определенное состояние системы: газ, жидкость или равновесие между жидкостью и газом.
Применение критической температуры:
1) Благодаря эффекту Джоуля-Томсона мы получаем жидкий газ, который находит широкое применение при лабораторных работах и в технике. В лабораториях он применяется для получения высокого вакуума и для других целей. В технике особо широкое применение получают машины, дающие раздельно жидкий кислород и жидкий азот
2) Вата или древесный уголь, пропитанные жидким кислородом, дают весьма сильное взрывчатое вещество, употребляемое при горных работах
3) Метод фракционного испарения используется также для получения из воздуха редких газов: гелия, неона, аргона, криптона и ксенона
4) При выборе материала для производства труб горячего водоснабжения
5) Также знание критической температуры какого-либо вещества применяется и в медицине (критическая температура человека), машиностроении (критическая температура плавления металла), в компьютерах (критическая температура жесткого диска)