Почему вакцину Pfizer приходится хранить при таких низких температурах
11 декабря Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (U.S. Food and Drug Administration, FDA) выдало разрешение на экстренное использование вакцины Pfizer-BioNTech для лиц в возрасте 16 лет и старше. Но фармацевтический гигант сталкивается с огромной проблемой при распространении своей вакцины, которая должна храниться при −70°C, для чего требуются специальные морозильные камеры и транспортные контейнеры.
— Обычно мы не храним вакцины при такой температуре, так что это определённо вызов,
говорит Курт Ситу (Kurt Seetoo), руководитель программы иммунизации в Департаменте общественного здравоохранения штата Мэриленд (Maryland Department of Public Health) в Балтиморе.
Аналогичная вакцина, разработанная компанией Moderna и Национальным институтом аллергии и инфекционных заболеваний США (U.S. National Institute of Allergy and Infectious Diseases), также требует замораживания. Но она сохраняется при температуре −20°C, поэтому её можно хранить в стандартном морозильнике. Большинство вакцин вообще не требуют замораживания, но и вакцины Pfizer, и вакцины Moderna — это новый тип вакцин, для которых низкие температуры необходимы.
С 5 декабря в России тоже началась массовая вакцинация. Российская вакцина сталкивается с похожими проблемами — она должна храниться при температуре −18°C, что затрудняет её транспортировку. Хотя, это, конечно, не пфайзеровские −70°C.
Так почему же вакцина Pfizer должна быть заморожена при субантарктической температуре, а вакцина Moderna — нет, если принцип их работы одинаковый?
Ответ на этот вопрос требует некоторых домыслов. Компании вряд ли раскроют все трюки и коммерческие секреты, которые они использовали для создания вакцин, считает Санджай Мишра (Sanjay Mishra), химик Медицинского центра университета Вандербильта (Vanderbilt University Medical Center) в Нэшвилле.
Но есть, по крайней мере, четыре вещи, способные определять то, насколько хрупка мРНК-вакцина и насколько глубоко она должна быть заморожена, чтобы оставаться свежей и эффективной.
— Урацил — это проблема, потому что он выступает, торчит,
Эти выступающие U могут служить сиганалами специальным протеинам иммунной системы, называющимся толл-подобными рецепторами, которые помогают обнаружить РНК вирусов, в том числе и SARS-CoV-2, и запускают процесс их уничтожения.
Некоторые типы липидов выдерживают нагрев лучше, чем другие. Липиды, которые используют производители, могут сильно повлиять на способность вакцины выдерживать тепло.
— Это как растительное масло и животный жир. Жир ещё твердый при комнатной температуре, в то время как масло жидкое. Для наночастиц то, из чего они сделаны, играет большую роль в том, будут ли они в целом достаточно стабильны, чтобы поддерживать процессы внутри,
Необходимость в ультрахолодном хранении может в конечном итоге ограничить количество людей, получающих вакцину Pfizer.
Компания Pfizer сообщила сотрудникам здравоохранения, что вакцину можно хранить в специальных транспортных контейнерах, заполняемых сухим льдом, что обеспечивает в них температурный режим −70°С±10°С в течение 15 дней, после чего ещё пять дней их можно хранить в холодильнике. Это даёт медицинским работникам 20 дней на то, чтобы применить вакцину после её изготовления. Но вакцины Moderna, Гам-КОВИД-Вак («Спутник V») и другие, которые всё ещё находятся на испытаниях, могут продержаться дольше при более высоких температурах. Если эти вакцины будут столь же или более эффективны, как вакцина компании Pfizer, мир наверняка выберет их.
«Зрада» отменяется: почему Минздрав изменил сроки хранения вакцины Pfizer
Украина изменила сроки хранения вакцины от коронавируса Pfizer. Если изначально препарат можно было держать в обычном холодильнике только пять дней, то теперь на сайте Госреестра лекарственных средств этот срок составляет целый месяц.
Некоторые журналисты обвинили Минздрав в самодеятельности, однако это не так. OBOZREVATEL объясняет, почему в действиях ведомства нет ничего плохого.
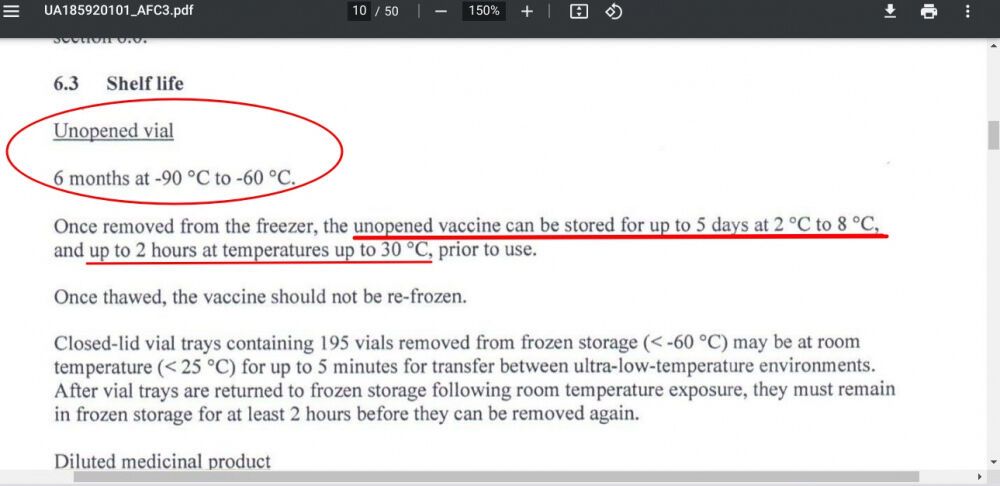
Согласно инструкции производителя, это можно делать в течение пяти дней. То есть за это время препарат нужно доставить в пункт вакцинации и полностью использовать.
Однако журналист Сергей Дибров обратил внимание, что на сайте Госреестра лекарственных средств 28 июня это правило изменилось. Вместо пятидневного дедлайна срок хранения вакцины увеличился до одного месяца.
«Сделали «специальную украинскую», без английской версии, инструкцию, и разрешили держать размороженную вакцину в холодильнике не пять дней, а целый месяц. Учитывая, что регистрационное свидетельство осталось прежним, можно быть уверенным, что состав вакцины от этого не поменялся никак», – отметил он.
Как оказалось, не только Минздрав изменил сроки хранения вакцины. Еще в мае аналогичное решение приняли медицинские регуляторы США и Евросоюза.
«FDA разрешает хранить капсулы с размороженной неразведенной вакциной от коронавируса производства Pfizer-BioNTech при температуре 2–8 градусов Цельсия сроком до одного месяца», — говорилось в заявлении.
Такая мера должна сделать COVID-препарат более доступным для применения в отдаленных регионах и для людей, живущих за пределами городов.
Ее разработкой занимались немецкая биотехнологическая компания BioNTech и американский фармацевтический гигант Pfizer. Этот препарат создан по уникальной технологии: после попадания внутрь человеческой клетки вакцина синтезирует белок антигена S (часть уникального шиповидного белка SARS-CoV-2), а наш организм производит на него иммунный ответ.
По данным производителя, эффективность после первой дозы составляет 90%, после второй – 95%.
Побочные эффекты. Боль в месте инъекции, повышенная температура, усталость, головная боль, озноб, боль в мышцах, диарея – это самые распространенные реакции организма, которые могут продолжаться в течение нескольких дней.
У Pfizer возможен риск развития миокардита и перикардита. Американский регулятор утверждает, что побочные явления намного чаще наблюдаются у мужчин, симптомы проявляются через несколько дней после вакцинации.
Вакцина одобрена для использования в 91 стране мира, в том числе и в Украине. Полный перечень здесь.
Важно: контент, размещенный на данной странице OBOZREVATEL, является результатом творческих исследований автора: он может не иметь медицинского образования или научной степени. Текст не проверяется специалистом в области медицины на предмет точности, сбалансированности, объективности. Некоторые публикации содержат подробности лечения или применения лекарственных препаратов. Данная информация не является руководством к действию и должна быть использована только после обсуждения с вашим лечащим врачом. OBOZREVATEL не призывает применять или распространять какие-либо лекарственные препараты, способы лечения и виды медицинских услуг.
В понедельник, 9 ноября, американская фармацевтическая компания Pfizer и немецкая биотехнологическая компания BioNTech заявили, что эффективность их вакцины против COVID-19 превышает 90%. Компании сообщили, что в ходе испытаний заражение коронавирусом было зафиксировано у 94 добровольцев из 43,5 тыс. проходивших тесты. На фоне этих новостей акции Pfizer выросли на 15%, а ценные бумаги BioNtech – на 24%, сообщает Bloomberg.
Компания планирует использовать для распространения вакцины коробки размером с чемодан, пишет CNBC. Они будут отгружаться в нескольких распределительных центрах в американском городе Каламазу (штат Мичиган) и бельгийском городе Пуурс. Pfizer планирует загружать около двух десятков грузовиков в день, что позволит ежедневно транспортировать 7,6 млн доз вакцины в ближайшие аэропорты.
На прошлой неделе сопредседатель американской программы Operation Warp Speed (OWS) по разработке вакцин от COVID-19 Монсеф Слауи заявил, что Правительство США и Pfizer обсуждали требования к хранению препарата.
«В их случае сыграл роль компромисс между скоростью, с которой вакцина станет доступна, и выбором правильной лекарственной формы, которая была бы стабильной», – отметил Слауи. «Обе [компании Pfizer и Moderna] работают над улучшением стабильности и требований холодовой цепи, по крайней мере, до 2–8 градусов тепла [по Цельсию]… и я уверен, что они найдут решения», – добавил он.
Хотя разработка вакцины от Pfizer не курируется OWS, США предварительно закупили 100 млн доз лекарства, рассматривая также покупку еще 500 млн доз.
США разрешили хранить вакцину Pfizer в обычном холодильнике до месяца
США разрешили хранить вакцину от коронавируса компании Pfizer до одного месяца в обычном холодильнике после разморозки и до разбавления перед инъекцией, говорится в сообщении на сайте медицинского регулятора FDA.
Такая мера должна сделать эту вакцину более доступной для применения в отдаленных регионах и для людей, живущих за пределами городов.
«FDA разрешает хранить капсулы с размороженной неразведенной вакциной от коронавируса производства Pfizer-BioNTech при температуре 2–8 градусов Цельсия сроком до одного месяца», — говорится в заявлении регулятора.
Компания предоставила данные, подтверждающие, что свойства препаратов не меняются при хранении в холодильнике до месяца, пояснили в FDA.
Ранее вакцину Pfizer разрешалось хранить в обычном холодильнике до пяти дней. Транспортировка и долговременное хранение вакцины осуществляются при температуре не выше минус 70 градусов Цельсия.
Еще в ноябре Bloomberg указывал, что поскольку для препарата Pfizer необходимы специальные условия транспортировки и хранения, его распространение требует создания дорогостоящей охлаждающей инфраструктуры, что может стать препятствием для продажи препарата даже в богатые страны. Даже если отдельные страны смогут создать такую инфраструктуру, вакцину будет сложно доставить конкретному пациенту, желающему получить вакцину, особенно в труднодоступные районы, отмечали опрошенные агентством эксперты в области здравоохранения.
Регулятор США одобрил вакцину Pfizer в декабре прошлого года, препарат стал первым разрешенным для использования в стране. По данным разработчиков, эффективность препарата составляет 95%. В мае в США разрешили использовать вакцину Pfizer для подростков 12–15 лет.
По словам гендиректора Pfizer Альберта Бурла, страны с низким и средним уровнем дохода решили не заказывать вакцину, разработанную компаниями Pfizer и BioNTech. Он отметил, что «справедливое и равноправное распределение [вакцины] было путеводной звездой» компании с самого первого дня. Для стран со средним уровнем дохода вакцина стоила в два раза меньше, чем для богатых, а странам с низким уровнем дохода препарат предлагали по себестоимости, пояснил Бурла.
Несмотря на такую политику, большую часть доз вакцин зарезервировали богатые страны, отметил глава Pfizer. Когда компания заметила это, она еще раз предложила «многим главам» стран со средним и низким уровнем доходов им зарезервировать дозы вакцины, однако они, по словам Бурлы, предпочли разместить заказы у других производителей препаратов от коронавируса.
КовиВак (Вакцина коронавирусная инактивированная цельновирионная концентрированная очищенная) (CoviVac (Inactivated whole-virion concentrated, purified coronavirus vaccine)) инструкция по применению
Владелец регистрационного удостоверения:
Лекарственная форма
 | КовиВак (Вакцина коронавирусная инактивированная цельновирионная концентрированная очищенная) |
| 1 доза (0.5 мл) | |
| антиген инактивированного коронавируса SARS-CoV-2* | не менее 3 мкг** |
* получен путем репродукции в перевиваемой культуре клеток линии Vero.
** является величиной расчетной.
Фармакологическое действие
| Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном законодательством порядке. |
Характеристика. Вакцина представляет собой очищенную концентрированную суспензию коронавируса SARS-CoV-2 штамм «AYDAR-1», полученного путем репродукции в перевиваемой культуре клеток линии Vero, инактивированного бета-пропиолактоном.
Фармакологические свойства. Вакцина стимулирует выработку иммунитета в отношении коронавирусной инфекции, вызываемой коронавирусом SARS-CoV-2. Защитный титр антител в настоящее время неизвестен. Продолжительность иммунитета неизвестна. Клинические исследования по изучению протективной эффективности не проводились.
Показания препарата КовиВак (Вакцина коронавирусная инактивированная цельновирионная концентрированная очищенная)
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых в возрасте 18-60 лет.
Режим дозирования
Прививки осуществляют при строгом соблюдении правил асептики и антисептики.
Вакцина предназначена только для внутримышечного введения. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча) двукратно с интервалом 2 недели в дозе 0.5 мл.
Строго запрещено внутривенное введение препарата.
Ампула с вакциной не требует выдерживания при комнатной температуре. Перед инъекцией содержимое ампулы встряхивают, прививку проводят сразу после набора в шприц прививочной дозы.
Не пригоден к применению препарат в ампулах с нарушенной целостностью и маркировкой, при изменении физических свойств (интенсивное окрашивание, наличие механических включений), при истекшем сроке годности, неправильном хранении.
Хранение вскрытой ампулы не допускается.
Отсутствуют доступные данные по взаимозаменяемости вакцины КовиВак (Вакцина коронавирусная инактивированная цельновирионная концентрированная очищенная) с другими вакцинами для профилактики COVID-19 для завершения курса вакцинации. Лица, получившие одну дозу вакцины КовиВак (Вакцина коронавирусная инактивированная цельновирионная концентрированная очищенная), должны получить вторую дозу этой же вакцины для завершения курса вакцинации.
| Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ. |
Побочное действие
В клинических исследованиях вакцины КовиВак и других инактивированных вакцин для профилактики коронавирусной инфекции наиболее частыми были местные реакции: боль (менее 15% от числа вакцинаций) и уплотнение в месте инъекции (до 1%); и общие реакции: головная боль (до 2% вакцинируемых) и кратковременная гипертермия (до 1%). Чаще выявлялись реакции легкой степени тяжести. Тяжелых местных и системных реакций на вакцинацию не было.
Побочные реакции могут появиться в 1-3 сутки после инъекции. Продолжительность реакций обычно не превышает 3 суток. Не исключено также развитие аллергических реакций, синкопальных состояний (реакция на процедуру введения препарата) и увеличение лимфоузлов. Не исключено присоединение острых (например, ОРВИ и т.п.) или обострение хронических инфекционных заболеваний из-за временного напряжения иммунитета на фоне вакцинации. Литературные данные о выявленных нежелательных реакциях при применении инактивированных вакцин для профилактики новой коронавирусной инфекции свидетельствуют о хорошем профиле безопасности.
Противопоказания к применению
1. Серьезная поствакцинальная реакция (температура выше 40°С, гиперемия или отек более 8 см в диаметре) или осложнение (коллапс или шокоподобное состояние, развившиеся в течение 48 ч после вакцинации; судороги, сопровождаемые или не сопровождаемые лихорадочным состоянием) на любую предыдущую вакцинацию в анамнезе.
2. Отягощенный аллергологический анамнез (анафилактический шок, отек Квинке, многоформная экссудативная эритема, гиперчувствительность или аллергические реакции на введение каких-либо вакцин в анамнезе, известные аллергические реакции на компоненты вакцины и др.).
3. Беременность и период грудного вскармливания.
4. Возраст до 18 лет.
1. Острые лихорадочные состояния, острые инфекционные и неинфекционные заболевания, включая период реконвалесценции. Вакцинацию проводят через 2-4 недели после выздоровления. При ОРВИ легкого течения и острых кишечных инфекциях вакцинацию можно проводить после нормализации температуры и/или исчезновения острых симптомов заболевания.
2. Хронические инфекционные заболевания в стадии обострения. Вакцинацию проводят в период ремиссии. Возможность вакцинации лиц, страдающих хроническими заболеваниями, определяет лечащий врач, исходя из состояния пациента.
При хронических заболеваниях печени и почек, выраженных нарушениях нейроэндокринной системы, тяжелых заболеваниях системы кроветворения, заболеваниях ЦНС (эпилепсии, инсультах и др.), сердечно-сосудистой системы (ИБС, миокардитах, эндокардитах, перикардитах), бронхолегочной системы (бронхиальной астме, ХОБЛ, фиброзирующих альвеолитах и др.), желудочно-кишечного тракта (при синдроме мальабсорбции и т.п.), иммунной системы (при аутоиммунных и аллергических заболеваниях). Лечащий врач должен оценивать соотношение польза-риск вакцинации в каждом конкретном случае.
Применение при беременности и кормлении грудью
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.