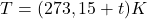Физика. 10 класс
Тепловое движение
Температура. Энергия теплового движения молекул
Необходимо запомнить
Состояние газа описывают с помощью макропараметров – объём, давление и температура.
Температуры тел при соприкосновении уравниваются, между ними устанавливается тепловое равновесие.
Тепловым равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Термометр – это прибор для измерения температуры. Шкала Кельвина имеет точку 0 К – абсолютный нуль – при этой температуре прекращается тепловое движение молекул.
Используют и другую температурную шкалу – шкалу Цельсия, где есть две основные точки: 0 °С и 100 °С.
Цена деления на шкале Кельвина такая же, как и на шкале Цельсия: °С = 1 К. Изменение температуры по шкале Кельвина равно изменению температуры по шкале Цельсия. Абсолютный нуль по шкале Кельвина соответствует отметке – 273 °С.
Температура – мера средней кинетической энергии движения молекул.
Постоянная Больцмана связывает энергетическую температуру с абсолютной температурой.
Давление прямо пропорционально концентрации и средней кинетической энергии молекул.
Температура вещества характеризует интенсивность теплового движения его частиц.
Температура и скорость движения молекул
Что мы знаем о температуре?
Врачи были первыми, кому понадобилась сравнительная и точная шкала теплоты тела. Лекарствам приписывалось охлаждающее или согревающее действие, а степень этого действия определялась градусами (ступенями – по-латыни). Лекарства надо было смешивать, чтобы они могли понизить жар или согреть испытывающего озноб. Умеренность, соразмерность при смешивании, в переводе с латинского, называется tiperatura. В начале XVII века врач Санкторио впервые с помощью ртутного термометра со шкалой, начал измерять температуру человеческого тела.
В науке, лишь в XVII веке стали говорить о температуре в современном смысле. Врачи очень поздно поняли, что здоровые люди имеют практически одну и ту же температуру. Они долго не понимали, что высокая температура (горячка) есть проявление болезни, а не сама болезнь.
Санкторио и Галилея можно считать первыми, кто понял пользу измерения температуры.
Восточных врачей не интересовал термометр. От восточных философов в физику пришли слова цвет и аромат – слова, которые относят к скрытым свойствам элементарных частиц.
Наука развивалась двумя путями, восточным и западным, и только в XX веке эти пути сливаются.
Физика. 10 класс
Тепловое движение
Температура. Энергия теплового движения молекул
Необходимо запомнить
Состояние газа описывают с помощью макропараметров – объём, давление и температура.
Температуры тел при соприкосновении уравниваются, между ними устанавливается тепловое равновесие.
Тепловым равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Термометр – это прибор для измерения температуры. Шкала Кельвина имеет точку 0 К – абсолютный нуль – при этой температуре прекращается тепловое движение молекул.
Используют и другую температурную шкалу – шкалу Цельсия, где есть две основные точки: 0 °С и 100 °С.
Цена деления на шкале Кельвина такая же, как и на шкале Цельсия: °С = 1 К. Изменение температуры по шкале Кельвина равно изменению температуры по шкале Цельсия. Абсолютный нуль по шкале Кельвина соответствует отметке – 273 °С.
Температура – мера средней кинетической энергии движения молекул.
Постоянная Больцмана связывает энергетическую температуру с абсолютной температурой.
Давление прямо пропорционально концентрации и средней кинетической энергии молекул.
Температура вещества характеризует интенсивность теплового движения его частиц.
Температура и скорость движения молекул
Что мы знаем о температуре?
Врачи были первыми, кому понадобилась сравнительная и точная шкала теплоты тела. Лекарствам приписывалось охлаждающее или согревающее действие, а степень этого действия определялась градусами (ступенями – по-латыни). Лекарства надо было смешивать, чтобы они могли понизить жар или согреть испытывающего озноб. Умеренность, соразмерность при смешивании, в переводе с латинского, называется tiperatura. В начале XVII века врач Санкторио впервые с помощью ртутного термометра со шкалой, начал измерять температуру человеческого тела.
В науке, лишь в XVII веке стали говорить о температуре в современном смысле. Врачи очень поздно поняли, что здоровые люди имеют практически одну и ту же температуру. Они долго не понимали, что высокая температура (горячка) есть проявление болезни, а не сама болезнь.
Санкторио и Галилея можно считать первыми, кто понял пользу измерения температуры.
Восточных врачей не интересовал термометр. От восточных философов в физику пришли слова цвет и аромат – слова, которые относят к скрытым свойствам элементарных частиц.
Наука развивалась двумя путями, восточным и западным, и только в XX веке эти пути сливаются.
При какой температуре должно прекратиться движение молекул?
а) 0 градусов Цельсия в) 0 К
Единица концентрации в СИ
Абсолютная температура измеряется в
1) джоулях 2) кельвинах 3) паскалях 4) градусах
4. Какое из приведенных ниже утверждений правильно описывает способность атомов к излучению и поглощению энергии? Атомы могут.
а) излучать любую порцию энергии, а поглощать лишь некоторый дискретный набор значений энергии.
б) поглощать любую порцию энергии, а излучать лишь некоторый дискретный набор значений энергии.
в) излучать и поглощать лишь некоторый дискретный набор значений энергии.
г) излучать и поглощать любую порцию энергии.
5. Формулируется II закон Ньютона так…
а) Тело движется равномерно в инерциальной системе, если воздействие других тел не скомпенсировано
б) Ускорение, приобретаемое телом, прямо пропорционально равнодействующей всех сил, действующих на тело, и обратно пропорционально его массе
в) Направление ускорения тела совпадает с направлением равнодействующей всех сил, действующих на тело
г) Модуль ускорения тела прямо пропорционален модулю равнодействующей всех сил и обратно пропорционален массе тела
Если на тело не действуют никакие другие тела, то тело сохраняет состояние покоя или прямолинейного равномерного движения;
а) это принцип относительности Галилея
б) это обобщение законов Кеплера в) это утверждение неверно.
7. Одним из доказательств того, что электромагнитные волны поперечны, является существование у них свойств:
а) поляризации в) преломления
б) отражения г) интерференции
8. Принципиальное отличие полной цепи от участка цепи в том, что:
а) сопротивление полной цепи всегда больше, нежели у участка цепи
б) полная цепь всегда содержит смешанное соединение проводников
в) полная цепь, в отличие от участка цепи содержит источник электрического тока
9. Сила Лоренса зависит:
а) от скорости движения заряженной частицы
б) от среды, в которой находится частица
в) от массы частицы
г) от рода источника, порождающего магнитное поле
10. Молекулой вещества называют:
а) наименьшую частичку, которая может быть отделена от этого вещества
б) мельчайшую частичку вещества, сохраняющую все физические свойства этого вещества
в) мельчайшую частичку вещества, сохраняющую химические свойства данного вещества
г) мельчайшую частичку вещества, сохраняющую физические и химические свойства этого вещества
11. При кристаллизации температура вещества:
а) увеличивается в) не меняется
б) уменьшается г) становится равной 0
Какое физическое явление доказывает квантовую природу света?
а) Интерференция в) Поляризация
б) Дифракция г) Фотоэффект
Какая величина выражается в Ваттах?
а) Мощность б) Работа в) Сила г) Энергия
а) Радиоволны в) Ультрафиалетовые лучи
б) Инфракрасные лучи г) Рентгеновские лучи д) 
Как называется процесс, при котором давление данной массы идеального газа зависит от объёма ( T- const)?
а) Изотермический б) Изохорный
в) Изобарный г) Адиабатный
Часть В.
( При выполнении заданий части В, необходимо написать правильный ответ)
1.Что является источником электрического поля?
2.В чем измеряется напряжение?
3.Что называется точкой отсчета?
4.Что называется дисперсией?
5.Какие взаимодействия называются магнитными?
6.Что такое кинематика?
7.Какие волны называют когерентными?
8.Сформулируйте закон Ома для участка цепи.
9.Что называют красной границей фотоэффекта?
10.Какой процесс называется адиабатным?
Часть С.
( При выполнении заданий части С, необходимо составить соответствие и решить задачи)
С1. При быстром движении поршня в закрытом цилиндре воздушного насоса объем воздуха увеличился. Установите соответствие между величинами, характеризующими процесс расширения воздуха, перечисленными в первом столбце, и их изменениями во втором столбце.
ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ ИХ ИЗМЕНЕНИЯ
А) Давление 1) Увеличение
Б) Температура 2) Уменьшение
В) Внутренняя энергия 3) Неизменность
III Вариант
Часть А.
( При выполнении заданий части А, выберете один из ниже приведенных ответов)
Термодинамическая шкала температур.
Температура измеряется жидкостными или газовыми термометрами, соответствующим образом градуированными. Высокая температура измеряется оптическими термометрами (по спектру излучения) или электрическими (полупроводниковые термисторы, термопары).
В международной шкале температур за ноль принята температуру таяния льда при нормальном атмосферном давлении, 100 ° С — температуру пара кипящей воды при нормальном атмосферном давлении. 1/100 этого интервала — это 1 ° С (Цельсия). Обозначается t ° С.
В термодинамической шкале температур за ноль принята температура, при которой прекратилось бы тепловое движение частиц, из которых состоит тело.
Эта температура называется абсолютным нулем температур. Единица термодинамической шкалы температур в системе СИ — кельвин (К). Обозначается T (1 К = 1 ° С).
Формула связи термодинамической температуры (T) и температуры по международной шкале температур:
В физике в большинстве случаев пользуются введенной английским ученым У. Кельвином абсолютной шкалой температур (1848 p.), Которая имеет две основные точки.
Первая основная точка — 0 К, или абсолютный ноль.
Вторая основная точка на абсолютной шкале температур — это точка, в которой вода существует во всех трех состояниях (твердом, жидком и газообразном), она названа тройной точкой.
Физический смысл абсолютного нуля: это температура, при которой прекращается тепловое движение молекул.
При абсолютном нуле молекулы поступательно не двигаются, но их колебательный и вращательный движения сохраняются. Тепловое движение молекул непрерывно и бесконечно. Соответственно абсолютный ноль температур при наличии молекул вещества недостижим. Он возможен только при условии отсутствия молекул, которых нет, например, в космосе при большом удалении от звезд и планет. Абсолютный ноль температур — это самая низкая температурная граница, верхней нет.
В быту для измерения температуры используют вторую температурную шкалу — шкалу Цельсия, названную в честь шведского астронома А. Цельсия и введенна им в 1742 году. На шкале Цельсия есть две основные точки: 0 ° С (точка, в которой тает лед) и 100 ° С (точка, в которой кипит вода). Температура, определяемая по шкале Цельсия, сказывается t. Шкала Цельсия имеет как положительные, так и отрицательные значения.
По рисунку можно проследить связь между температурами по шкалам Кельвина и Цельсия.
При какой температуре должно прекратиться движение молекул
Термин «температура» появился во времена, когда ученые-физики думали, что теплые тела состоят из большего количества специфической субстанции – теплорода, – чем такие же тела, но холодные. А температура трактовалась как величина, соответствующая количеству теплорода в теле. С тех пор температуру любых тел измеряют в градусах. Но на самом деле это мера кинетической энергии движущихся молекул, и, исходя из этого, ее следует измерять в Джоулях, в соответствии с Системой единиц Си.
Понятие «абсолютный ноль температуры» исходит из второго начала термодинамики. По нему процесс перехода тепла от холодного тела к горячему невозможен. Это понятие введено английским физиком У. Томсоном. Ему за достижения в физике королевой Англии было даровано дворянское звание «лорд» и титул «барон Кельвин». В 1848 г. У.Томсон (Кельвин) предложил использовать температурную шкалу, в которой за начальную точку принял абсолютный ноль температуры, соответствующий предельному холоду, а ценой деления взял градус Цельсия. Единицей Кельвина является 1/27316 доля температуры тройной точки воды (около 0 град. С), т.е. температуры, при которой чистая вода сразу находится в трех видах: лед, жидкая вода и пар. Абсолютный ноль температуры – это минимально возможная низкая температура, при которой движение молекул останавливается, и из вещества уже невозможно извлечь тепловую энергию. С тех пор шкала абсолютных температур стала называться его именем.
Температура измеряется по разным шкалам
Наиболее употребляемая шкала температуры носит название «шкала Цельсия». Она построена на двух точках: на температуре фазового перехода воды из жидкости в пар и воды в лед. А. Цельсий в 1742 г. предложил расстояние между опорными точками разделить на 100 промежутков, а точку кипения воды принять за ноль, при этом точку замерзания за 100 градусов. Но швед К. Линней предложил сделать наоборот. С тех пор вода замерзает при ноле градусов А. Цельсия. Хотя точно по Цельсию она должна кипеть. Абсолютный ноль по Цельсию соответствует минус 273,16 градусов Цельсия.
Есть еще несколько температурных шкал: Фаренгейта, Реомюра, Ранкина, Ньютона, Рёмера. Они имеют разные опорные точки и цену деления. Например шкала Реомюра тоже построена на реперах кипения и замерзания воды, но она имеет 80 делений. Шкала Фаренгейта, появившаяся в 1724 г., используется в быту только в некоторых странах мира, в т. ч. США; реперные точки: одна – температура смеси водяной лед – нашатырь и другая – человеческого тела. Шкала делится на сто делений. Ноль Цельсия соответствует 32 градусам Фаренгейта. Перевод градусов в фаренгейты можно сделать по формуле: F = 1,8 C + 32. Обратный перевод: С = (F – 32)/1,8, где: F – градусы Фаренгейта, С – градусы Цельсия. Если вам лень считать, сходите в онлайн-сервис по переводу Цельсия в Фаренгейты. В рамочке наберите число градусов Цельсия, нажмите «Рассчитать», выберите «Фаренгейт» и нажмите «Пуск». Результат появится сразу.
Шкала Ранкина названа в честь английского (точнее шотландского) физика Уильяма Дж. Ранкина, бывшего современником Кельвина и одним из создателей технической термодинамики. В его шкале важных точек три: начало – абсолютный ноль, точки замерзания воды 491,67 градус Ранкина и закипания воды 671,67 град. Число делений между замерзанием воды и ее закипанием и у Ранкина, и у Фаренгейта равно 180.
Большинством этих шкал пользуются исключительно физики. А 40% опрошенных в наши дни американских школьников выпускных классов сказали, что они не знают, что такое абсолютный ноль температуры.
Урок №19. Температура. Энергия теплового движения молекул
На уроке рассматриваются понятия: температура и тепловое равновесие; шкалы Цельсия и Кельвина; абсолютная температура как мера средней кинетической энергии теплового движения частиц вещества, зависимость давления от концентрации молекул и температуры.
Макроскопические параметры – величины объём V, давление p и температура t, характеризующие состояние макроскопических тел без учёта их молекулярного строения.
Температура характеризует степень нагретости тела (холодное, тёплое, горячее).
Температура (от лат. temperatura — надлежащее смешение, соразмерность, нормальное состояние) – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
Тепловым равновесием называют – такое состояние тел, при котором температура во всех точках системы одинакова.
Тепловым или термодинамическим равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Термометр — это прибор для измерения температуры путём контакта с исследуемым телом.Различают жидкостные, газовые термометры, термопары, термометры сопротивления.
Абсолютная температура Т прямо пропорциональна температуре Θ (тета), выражаемой в энергетических единицах (Дж).
Абсолютный нуль – предельная температура, при которой давление идеального газа обращается в нуль при фиксированном объёме или объём идеального газа стремится к нулю при неизменном давлении.
Абсолютный нуль – температура, при которой прекращается тепловое движение молекул.
Абсолютная шкала температур (Шкала Кельвина) – здесь нулевая температура соответствует абсолютному нулю, а каждая единица температуры равна градусу по шкале Цельсия.
Кельвин – единица абсолютной температуры в Международной системе измерений (СИ).
Постоянная Больцмана – коэффициент, связывает температуру Θ энергетических единицах (Дж) с абсолютной температурой Т (К).
Абсолютная температура есть мера средней кинетической энергии молекул.
Давление газа прямо пропорционально концентрации его молекул и абсолютной температуре Т.
Закон Авогадро – в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул
Теоретический материал для самостоятельного изучения
Измеряя расположение звёзд на небе, расстояния на земле, время, люди знали, для чего они это делают и изобретали, телескопы, часы, прототипы современных линеек. О температуре такого же сказать было нельзя. О том, что такое тепловое равновесие и что означает степень нагрева тела (температура), существовали разные мнения. Но человек с незапамятных времен точно знал, что, когда два тела плотно соприкасаются, между ними устанавливается, выражаясь современным языком, тепловое равновесие.
Любое макроскопическое тело или группа макроскопических тел при неизменных внешних условиях самопроизвольно переходят в состояние теплового равновесия.
Тепловым равновесием называют такое состояние тел, при котором температура во всех точках системы одинакова.
Температура (от лат. temperatura — надлежащее смешение, соразмерность, нормальное состояние) – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
К числу характеристик состояния макроскопических тел (твёрдых тел, жидкостей, газов) и процессов изменения их состояний, относят объём, давление и температуру. Эти величины описывают в целом тела, состоящие из большого числа молекул, а не отдельные молекулы. При этом микроскопические процессы внутри тела не прекращаются при тепловом равновесии: расположения молекул всё время меняются и меняются их скорости при столкновениях.
Величины объём, давление и температуру, характеризующие состояние макроскопических тел без учёта их молекулярного строения, называют макроскопическими параметрами.
Тепловым или термодинамическим равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Для точной характеристики нагретости тела, необходим прибор, способный измерить температуры тел и дать возможности их сравнения.
Термометр — это прибор для измерения температуры путём контакта с исследуемым телом. Различают жидкостные, газовые термометры, термопары, термометры сопротивления.
В 1597 году Галилей создал термоскоп, в собственных сочинениях учёного нет описания этого прибора, но его ученики засвидетельствовали этот факт. Аппарат представлял собой устройство для поднятия воды при помощи нагревания.
Изобретение термометра, данные которого не зависели бы от перепадов атмосферного давления, произошли благодаря экспериментам физика Э. Торричелли, ученика Галилея.
Во всех приборах, изобретённых в XVIII веке, измерение температуры было относительно расширению столбика воды, спирта или ртути и произвольности выбора начала отсчёта, т.е. нулевой температуры. Наполняющие их вещества замерзали или кипели и этими термометрами нельзя было измерять очень низкие или очень высокие температуры. Необходимо было изобрести такую шкалу, чтобы избавиться от зависимости выбранного вещества, на основе которого формировалось градуирование.
Шкала, предложенная шведским учёным Андерсом Цельсием в 1742 г., точно устанавливала положение двух точек: 0 и 100 градусов. По шкале Цельсия температура обозначается буквой t, измеряется в градусах Цельсия (ºС).
На территории Англии и США используется шкала Фаренгейта. Такая шкала была предложена немецким учёным Даниелем Габриелем Фаренгейтом в 1724 г.: 0 °F — температура смеси снега с нашатырём или поваренною солью, 96 °F —температура здорового человеческого тела, во рту или под мышкой.
Рене Антуан де Реомюр не одобрял применения ртути в термометрах вследствие малого коэффициента расширения ртути. В 1730 году изобрёл водно-спиртовой термометр и предложил шкалу от 0 до 80°.
Шкала Реомюра очень долго использовалась на родине учёного во Франции вплоть до настоящего времени.
Различные жидкости при нагревании расширяются не одинаково. Поэтому расстояния на шкале между нулевой отметкой 0 °C и 100 °C будут разными.
Однако существует способ создать тело, которое приближенно обладает нужными качествами. Это идеальный газ. Было замечено, что в отличие от жидкостей все разряжённые газы – водород, гелий, кислород – расширяются при нагревании одинаково и одинаково меняют своё давление при изменении температуры. Это свойство газов позволяет избавиться в термометрах от одного существенного недостатка шкалы Цельсия – произвольности выбора начала отсчёта, то есть нулевой температуры.
При тепловом равновесии, если давление и объём газа массой m постоянны, то средняя кинетическая энергия молекул газа должна иметь строго определённое значение, как и температура.
Практически такую проверку произвести непосредственно невозможно, но с помощью основного уравнения молекулярно-кинетической теории её можно выразить через макроскопические параметры:
Если кинетическая энергия действительно одинакова для всех газов в состоянии теплового равновесия, то и значение давления р должно быть тоже одинаково для всех газов при постоянном значении отношения объёма к числу молекул. Подтвердить или опровергнуть данное предположение может только опыт.
Возьмём несколько сосудов, заполненных различными газами, например, водородом, гелием и кислородом. Сосуды имеют определённые объёмы и снабжены манометрами, для измерения давления газов в сосудах. Массы газов известны, тем самым известно число молекул в каждом сосуде. Приведём газы в состояние теплового равновесия. Для этого поместим их в тающий лёд и подождём, пока не установится тепловое равновесие и давление газов перестанет меняться.
Здесь устанавливается тепловое равновесие и все газы имеют одинаковую температуру 0 °С. При этом показания манометра показывают разное давление р, объёмы сосудов V изначально были разными и число молекул N различно, так как газы, закаченные в баллоны разные. Найдём отношение для водорода всех параметров для одного моля вещества:
Такое значение отношения произведения давления газа на его объём к числу молекул получается для всех газов при температуре тающего льда. Обозначим это отношение через Θ0 (тета нулевое):
Таким образом, предположение, что средняя кинетическая энергия, а также давление р в состоянии теплового равновесия одинаковы для всех газов, если их объёмы и количества вещества одинаковы или если отношение
Если же сосуды с газами поместить в кипящую воду при нормальном атмосферном давлении, то согласно эксперименту, отношение макроскопических параметров будет также одинаковым для всех газов, но значение будет больше предыдущего
Отсюда следует, что величина Θ растёт с повышением температуры и не зависит от других параметром, кроме температуры. Этот опытный факт позволяет рассматривать величину Θ тета как естественную меру температуры и измерять в энергетических единицах — джоулях.
А теперь вместо энергетической температуры введём температуру, которая будет измеряться в градусах. Будем считать величину тета Θ прямо пропорциональной температуре Т, где k- коэффициент пропорциональности
По этой формуле вводится температура, которая даже теоретически не может быть отрицательной, так как все величины левой части этого равенства больше или равны нулю. Следовательно, наименьшим значением этой температуры является нуль, при любом другом параметре p, V, N равным нулю.
Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объёме или при которой объём идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулём температуры.
Тепловое движение молекул непрерывно и бесконечно, а при абсолютном нуле молекулы поступательно не двигаются. Следовательно, абсолютный нуль температур при наличии молекул вещества не может быть достигнут. Абсолютный нуль температур — это самая низкая температурная граница, верхней не существует, та «наибольшая или последняя степень холода», существование которой предсказывал М.В. Ломоносов.
В 1848 г. английскому физику Вильяму Томсону (лорд Кельвин) удалось построить абсолютную температурную шкалу (её в настоящее время называют шкалой Кельвина), которая имеет две основные точки 0 К (или абсолютный нуль) и 273К, точка в которой вода существует в трёх состояниях (в твёрдом, жидком и газообразном).
Абсолютная температурная шкала — шкала температур, в которой за начало отсчёта принят абсолютный нуль. Температура здесь обозначается буквой T и измеряется в кельвинах (К).
На шкале Цельсия, есть две основные точки: 0°С (точка, в которой тает лёд) и 100°С (кипение воды). Температура, которую определяют по шкале Цельсия, обозначается t. Шкала Цельсия имеет как положительные, так и отрицательные значения.
Из опыта мы определили значения величины Θ (тета) при 0 °С и 100 °С. Обозначим абсолютную температуру при 0 °С через Т1, а при 100 °С через Т2. Тогда согласно формуле:
Отсюда можно вычислить коэффициент k, который связывает температуру в Θ энергетических единицах (Дж) с абсолютной температурой Т (К)
k = 1,38 • 10-23 Дж/К – постоянная Больцмана.
Зная постоянную Больцмана, можно найти значение абсолютного нуля по шкале Цельсия. Для этого найдём сначала значение абсолютной температуры, соответствующее 0°С:
значение абсолютной температуры.
Один кельвин и один градус шкалы Цельсия совпадают. Поэтому любое значение абсолютной температуры Т будет на 273 градуса выше соответствующей температуры t по Цельсию:
Теперь выведем ещё одну зависимость температуры от средней кинетической энергии молекул. Из основного уравнения молекулярно-кинетической теории и уравнения для определения абсолютной температуры
Здесь видно, что левые части этих уравнений равны, значит правые равны тоже.
Средняя кинетическая энергия хаотического поступательного движения молекул газа пропорциональна абсолютной температуре.
Абсолютная температура есть мера средней кинетической энергии движения молекул.
Из выведенных формул мы можем получить выражение, которое показывает зависимость давления газа от концентрации молекул и температуры
Из этой зависимости вытекает, что при одинаковых давлениях и температурах концентрация молекул у всех газов одна и та же. Отсюда следует закон Авогадро, известный нам из курса химии.
Закон Авогадро: в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул.
Рассмотрим задачи тренировочного блока урока.
1. При температуре _______ (370C; 2830C; 270C) средняя кинетическая энергия поступательного движения молекул равна 6,21·10-21Дж.
k = 1,38 • 10-23 Дж/К – постоянная Больцмана
Запишем значение средней кинетической энергии хаотического поступательного движения молекул с зависимостью от абсолютной температуры:
Соотношение между абсолютной температурой и температурой в градусах Цельсия:
Подставим значение абсолютной температуры:
Правильный вариант ответа:
2. При температуре 290 К и давлении 0,8 МПа, средняя кинетическая энергия молекул равна __________ Дж, а концентрация составляет молекул ___________ м-3.
р = 0,8 МПа =0,8·106 Па
k = 1,38 • 10-23 Дж/К – постоянная Больцмана
Значение средней кинетической энергии хаотического поступательного движения молекул:
Подставив значение абсолютной температуры, найдём ответ:
Определим концентрацию газа из соотношения:
Правильный вариант ответа: 6·10-21; 2·1026 м-3.
Урок №19. Температура. Энергия теплового движения молекул
На уроке рассматриваются понятия: температура и тепловое равновесие; шкалы Цельсия и Кельвина; абсолютная температура как мера средней кинетической энергии теплового движения частиц вещества, зависимость давления от концентрации молекул и температуры.
Макроскопические параметры – величины объём V, давление p и температура t, характеризующие состояние макроскопических тел без учёта их молекулярного строения.
Температура характеризует степень нагретости тела (холодное, тёплое, горячее).
Температура (от лат. temperatura — надлежащее смешение, соразмерность, нормальное состояние) – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
Тепловым равновесием называют – такое состояние тел, при котором температура во всех точках системы одинакова.
Тепловым или термодинамическим равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Термометр — это прибор для измерения температуры путём контакта с исследуемым телом.Различают жидкостные, газовые термометры, термопары, термометры сопротивления.
Абсолютная температура Т прямо пропорциональна температуре Θ (тета), выражаемой в энергетических единицах (Дж).
Абсолютный нуль – предельная температура, при которой давление идеального газа обращается в нуль при фиксированном объёме или объём идеального газа стремится к нулю при неизменном давлении.
Абсолютный нуль – температура, при которой прекращается тепловое движение молекул.
Абсолютная шкала температур (Шкала Кельвина) – здесь нулевая температура соответствует абсолютному нулю, а каждая единица температуры равна градусу по шкале Цельсия.
Кельвин – единица абсолютной температуры в Международной системе измерений (СИ).
Постоянная Больцмана – коэффициент, связывает температуру Θ энергетических единицах (Дж) с абсолютной температурой Т (К).
Абсолютная температура есть мера средней кинетической энергии молекул.
Давление газа прямо пропорционально концентрации его молекул и абсолютной температуре Т.
Закон Авогадро – в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул
Теоретический материал для самостоятельного изучения
Измеряя расположение звёзд на небе, расстояния на земле, время, люди знали, для чего они это делают и изобретали, телескопы, часы, прототипы современных линеек. О температуре такого же сказать было нельзя. О том, что такое тепловое равновесие и что означает степень нагрева тела (температура), существовали разные мнения. Но человек с незапамятных времен точно знал, что, когда два тела плотно соприкасаются, между ними устанавливается, выражаясь современным языком, тепловое равновесие.
Любое макроскопическое тело или группа макроскопических тел при неизменных внешних условиях самопроизвольно переходят в состояние теплового равновесия.
Тепловым равновесием называют такое состояние тел, при котором температура во всех точках системы одинакова.
Температура (от лат. temperatura — надлежащее смешение, соразмерность, нормальное состояние) – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
К числу характеристик состояния макроскопических тел (твёрдых тел, жидкостей, газов) и процессов изменения их состояний, относят объём, давление и температуру. Эти величины описывают в целом тела, состоящие из большого числа молекул, а не отдельные молекулы. При этом микроскопические процессы внутри тела не прекращаются при тепловом равновесии: расположения молекул всё время меняются и меняются их скорости при столкновениях.
Величины объём, давление и температуру, характеризующие состояние макроскопических тел без учёта их молекулярного строения, называют макроскопическими параметрами.
Тепловым или термодинамическим равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Для точной характеристики нагретости тела, необходим прибор, способный измерить температуры тел и дать возможности их сравнения.
Термометр — это прибор для измерения температуры путём контакта с исследуемым телом. Различают жидкостные, газовые термометры, термопары, термометры сопротивления.
В 1597 году Галилей создал термоскоп, в собственных сочинениях учёного нет описания этого прибора, но его ученики засвидетельствовали этот факт. Аппарат представлял собой устройство для поднятия воды при помощи нагревания.
Изобретение термометра, данные которого не зависели бы от перепадов атмосферного давления, произошли благодаря экспериментам физика Э. Торричелли, ученика Галилея.
Во всех приборах, изобретённых в XVIII веке, измерение температуры было относительно расширению столбика воды, спирта или ртути и произвольности выбора начала отсчёта, т.е. нулевой температуры. Наполняющие их вещества замерзали или кипели и этими термометрами нельзя было измерять очень низкие или очень высокие температуры. Необходимо было изобрести такую шкалу, чтобы избавиться от зависимости выбранного вещества, на основе которого формировалось градуирование.
Шкала, предложенная шведским учёным Андерсом Цельсием в 1742 г., точно устанавливала положение двух точек: 0 и 100 градусов. По шкале Цельсия температура обозначается буквой t, измеряется в градусах Цельсия (ºС).
На территории Англии и США используется шкала Фаренгейта. Такая шкала была предложена немецким учёным Даниелем Габриелем Фаренгейтом в 1724 г.: 0 °F — температура смеси снега с нашатырём или поваренною солью, 96 °F —температура здорового человеческого тела, во рту или под мышкой.
Рене Антуан де Реомюр не одобрял применения ртути в термометрах вследствие малого коэффициента расширения ртути. В 1730 году изобрёл водно-спиртовой термометр и предложил шкалу от 0 до 80°.
Шкала Реомюра очень долго использовалась на родине учёного во Франции вплоть до настоящего времени.
Различные жидкости при нагревании расширяются не одинаково. Поэтому расстояния на шкале между нулевой отметкой 0 °C и 100 °C будут разными.
Однако существует способ создать тело, которое приближенно обладает нужными качествами. Это идеальный газ. Было замечено, что в отличие от жидкостей все разряжённые газы – водород, гелий, кислород – расширяются при нагревании одинаково и одинаково меняют своё давление при изменении температуры. Это свойство газов позволяет избавиться в термометрах от одного существенного недостатка шкалы Цельсия – произвольности выбора начала отсчёта, то есть нулевой температуры.
При тепловом равновесии, если давление и объём газа массой m постоянны, то средняя кинетическая энергия молекул газа должна иметь строго определённое значение, как и температура.
Практически такую проверку произвести непосредственно невозможно, но с помощью основного уравнения молекулярно-кинетической теории её можно выразить через макроскопические параметры:
Если кинетическая энергия действительно одинакова для всех газов в состоянии теплового равновесия, то и значение давления р должно быть тоже одинаково для всех газов при постоянном значении отношения объёма к числу молекул. Подтвердить или опровергнуть данное предположение может только опыт.
Возьмём несколько сосудов, заполненных различными газами, например, водородом, гелием и кислородом. Сосуды имеют определённые объёмы и снабжены манометрами, для измерения давления газов в сосудах. Массы газов известны, тем самым известно число молекул в каждом сосуде. Приведём газы в состояние теплового равновесия. Для этого поместим их в тающий лёд и подождём, пока не установится тепловое равновесие и давление газов перестанет меняться.
Здесь устанавливается тепловое равновесие и все газы имеют одинаковую температуру 0 °С. При этом показания манометра показывают разное давление р, объёмы сосудов V изначально были разными и число молекул N различно, так как газы, закаченные в баллоны разные. Найдём отношение для водорода всех параметров для одного моля вещества:
Такое значение отношения произведения давления газа на его объём к числу молекул получается для всех газов при температуре тающего льда. Обозначим это отношение через Θ0 (тета нулевое):
Таким образом, предположение, что средняя кинетическая энергия, а также давление р в состоянии теплового равновесия одинаковы для всех газов, если их объёмы и количества вещества одинаковы или если отношение
Если же сосуды с газами поместить в кипящую воду при нормальном атмосферном давлении, то согласно эксперименту, отношение макроскопических параметров будет также одинаковым для всех газов, но значение будет больше предыдущего
Отсюда следует, что величина Θ растёт с повышением температуры и не зависит от других параметром, кроме температуры. Этот опытный факт позволяет рассматривать величину Θ тета как естественную меру температуры и измерять в энергетических единицах — джоулях.
А теперь вместо энергетической температуры введём температуру, которая будет измеряться в градусах. Будем считать величину тета Θ прямо пропорциональной температуре Т, где k- коэффициент пропорциональности
По этой формуле вводится температура, которая даже теоретически не может быть отрицательной, так как все величины левой части этого равенства больше или равны нулю. Следовательно, наименьшим значением этой температуры является нуль, при любом другом параметре p, V, N равным нулю.
Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объёме или при которой объём идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулём температуры.
Тепловое движение молекул непрерывно и бесконечно, а при абсолютном нуле молекулы поступательно не двигаются. Следовательно, абсолютный нуль температур при наличии молекул вещества не может быть достигнут. Абсолютный нуль температур — это самая низкая температурная граница, верхней не существует, та «наибольшая или последняя степень холода», существование которой предсказывал М.В. Ломоносов.
В 1848 г. английскому физику Вильяму Томсону (лорд Кельвин) удалось построить абсолютную температурную шкалу (её в настоящее время называют шкалой Кельвина), которая имеет две основные точки 0 К (или абсолютный нуль) и 273К, точка в которой вода существует в трёх состояниях (в твёрдом, жидком и газообразном).
Абсолютная температурная шкала — шкала температур, в которой за начало отсчёта принят абсолютный нуль. Температура здесь обозначается буквой T и измеряется в кельвинах (К).
На шкале Цельсия, есть две основные точки: 0°С (точка, в которой тает лёд) и 100°С (кипение воды). Температура, которую определяют по шкале Цельсия, обозначается t. Шкала Цельсия имеет как положительные, так и отрицательные значения.
Из опыта мы определили значения величины Θ (тета) при 0 °С и 100 °С. Обозначим абсолютную температуру при 0 °С через Т1, а при 100 °С через Т2. Тогда согласно формуле:
Отсюда можно вычислить коэффициент k, который связывает температуру в Θ энергетических единицах (Дж) с абсолютной температурой Т (К)
k = 1,38 • 10-23 Дж/К – постоянная Больцмана.
Зная постоянную Больцмана, можно найти значение абсолютного нуля по шкале Цельсия. Для этого найдём сначала значение абсолютной температуры, соответствующее 0°С:
значение абсолютной температуры.
Один кельвин и один градус шкалы Цельсия совпадают. Поэтому любое значение абсолютной температуры Т будет на 273 градуса выше соответствующей температуры t по Цельсию:
Теперь выведем ещё одну зависимость температуры от средней кинетической энергии молекул. Из основного уравнения молекулярно-кинетической теории и уравнения для определения абсолютной температуры
Здесь видно, что левые части этих уравнений равны, значит правые равны тоже.
Средняя кинетическая энергия хаотического поступательного движения молекул газа пропорциональна абсолютной температуре.
Абсолютная температура есть мера средней кинетической энергии движения молекул.
Из выведенных формул мы можем получить выражение, которое показывает зависимость давления газа от концентрации молекул и температуры
Из этой зависимости вытекает, что при одинаковых давлениях и температурах концентрация молекул у всех газов одна и та же. Отсюда следует закон Авогадро, известный нам из курса химии.
Закон Авогадро: в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул.
Рассмотрим задачи тренировочного блока урока.
1. При температуре _______ (370C; 2830C; 270C) средняя кинетическая энергия поступательного движения молекул равна 6,21·10-21Дж.
k = 1,38 • 10-23 Дж/К – постоянная Больцмана
Запишем значение средней кинетической энергии хаотического поступательного движения молекул с зависимостью от абсолютной температуры:
Соотношение между абсолютной температурой и температурой в градусах Цельсия:
Подставим значение абсолютной температуры:
Правильный вариант ответа:
2. При температуре 290 К и давлении 0,8 МПа, средняя кинетическая энергия молекул равна __________ Дж, а концентрация составляет молекул ___________ м-3.
р = 0,8 МПа =0,8·106 Па
k = 1,38 • 10-23 Дж/К – постоянная Больцмана
Значение средней кинетической энергии хаотического поступательного движения молекул:
Подставив значение абсолютной температуры, найдём ответ:
Определим концентрацию газа из соотношения:
Правильный вариант ответа: 6·10-21; 2·1026 м-3.