Термодинамические условия электрохимической коррозии металлов
Поскольку электрохимическая коррозия металлов – самопроизвольный процесс, то термодинамическим условием его протекания является уменьшение энергии Гиббса (DrG 0. Поскольку E = jк – jа, то условие самопроизвольного протекания реакции – jа + только в присутствии растворенного в них кислорода.
Электрохимическая коррозия металлов, у которых 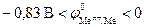
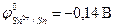
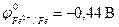
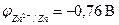
3. Если 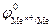
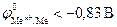

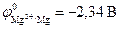
Отметим, что в присутствии в электролите растворенного кислорода большинство металлов корродирует с кислородной деполяризацией, поскольку коррозия с водородной деполяризацией катода менее вероятна. Термодинамическая возможность протекания коррозии часто не реализуется вследствие кинетических факторов.
Дата добавления: 2017-02-20 ; просмотров: 1744 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Электродный потенциал и термодинамическая возможность коррозии
Основная причина коррозии металлов — их термодинамическая неустойчивость в обычных условиях. Металлы (за исключением благородных) в естественных условиях находятся в виде окислов, т.е. в земной коре металлы входят в состав химических соединений (руд).
При неизменности термодинамического потенциала ( Δ G = 0) система находится в равновесии. Это означает, что в процессе самопроизвольного окисления металла (коррозии) скорости реакций окисления и восстановления металла равны. Какое число атомов металла за единицу времени окислилось (потеряло валентные электроны и перешло в виде положительно заряженных катионов в электролит), такое же число ионов металла восстановилось из электролита в кристаллическую решетку металла, получив недостающие электроны от электрода (металла).
Следовательно, при этом не изменяются масса электрода и его заряд. Нарушение равновесия в каком-либо одном из двух направлений приведет к окислению или, наоборот, восстановлению металла.
Это выражение получено из условия равенства работы, произведенной химическими силами (-ΔG) в реакции окисления одного моля металла, работе, производимой электрическими силами при восстановлении одного моля металла (ΔφоzF).
Повышение потенциала электрода выше равновесного (обратимого) приведет к сдвигу равновесия в сторону анодной реакции окисления, снижение потенциала ниже равновесного сдвинет в сторону катодной реакции восстановления.
Если бы при погружении идеального металлического электрода электролит на границе раздела всегда протекал только процесс ионизации — восстановления данного металла, то всегда достигалось бы равновесное (обратимое) состояние, достаточное для сформирования двойного электрического слоя. Однако в большинстве случаев на поверхности реальных электродов одновременно протекают процессы с участием посторонних ионов, что препятствует установлению равновесного состояния и вызывает некомпенсированный перенос массы металла из электрода в электролит, т.е. коррозию. При этом потенциал электрода будет уже неравновесным (необратимым), и что величина будет зависеть не только от обмена электрода с электролитом собственными ионами металла, но и от реакций с участием ионов металла но и от реакций с участием ионов других веществ. При неравновесном состоянии может быть достигнут баланс между электродом и электролитом в обмене электрическими зарядами, но будет нарушен баланс по массе, так как часть восстанавливающихся ионов металла может быть заменена другими ионами и анодный процесс ионизации металла станет превалировать над катодным. Соответствующее значение устанавливающегося необратимого (неравновесного) потенциала называется стационарным потенциалом или потенциалом коррозии металла.
Рассмотрим простейший пример растворения металла в водном растворе кислоты, предполагая, что в процессе участвуют два вида ионов электролита — металла и водорода по реакциям
9.3.2. Термодинамические условия электрохимической коррозии металлов
Поскольку электрохимическая коррозия металлов – самопроизвольный процесс, то термодинамическим условием его протекания
Сравнение электродных потенциалов кислородного и водородного электродов, величина которых зависит от pH электролита, и потенциалов металлов позволяет определить термодинамическую возможность коррозии в различных средах. Для этого можно использовать величины стандартных электродных потенциалов металлов.
1. Если ϕ 0 Me n + /Me больше, чем потенциал кислородного электрода (область III на рис. 8.9), то коррозия металла невозможна. Ес-
=+ 1,50 В. Если + 0,40 В 0
трода, но больше, чем потенциал водородного электрода (область II на рис. 8.9), то коррозия возможна только в присутствии в элек-
что эти металлы растворяются в кислотах, окислителях за счет иона Н + только в присутствии растворенного в них кислорода.
зацией катода в зависимости от величины pH и в отсутствие растворенного кислорода. Это наблюдается, например, для олова:
3. Если ϕ 0 Me n + /Me меньше, чем потенциал водородного электро-
да (область I на рис. 8.9), то коррозия возможна как в присутствии растворенного кислорода с кислородной деполяризацией катода, так и в его отсутствие с водородной деполяризацией. Коррозия ме-
Отметим, что в присутствии в электролите растворенного кислорода большинство металлов корродируют с кислородной деполяризацией, поскольку коррозия с водородной деполяризацией катода менее вероятна. Термодинамическая возможность протекания коррозии часто не реализуется вследствие кинетических факторов.
9.3.3. Факторы, влияющие на скорость электрохимической коррозии
Скорость электрохимической коррозии ( r ), равная количеству окислившегося металла в единицу времени, пропорциональна
плотности коррозионного тока i корр (см. рис. 9.6). Его величина прямо пропорциональна разности равновесных потенциалов элек-
тродов ( ϕ к − ϕ а ) и обратно пропорциональна поляризации анода ( η а ) и катода ( η к ). На рис. 9.11 приведены примеры коррозионных
диаграмм, на которых для простоты поляризационные кривые изображены в виде прямых линий:

φ а
Рис. 9.11. Коррозионные диаграммы: а – два металла с различным значением электродного потенциала; б – кислородная и водородная деполяризация;
в – различные величины поляризации катода
а − увеличение разности равновесных потенциалов электродов приводит к увеличению скорости коррозии. Чем меньше величина электродного потенциала металла, тем больше скорость коррозии при одинаковой реакции деполяризации;
в − чем больше величина поляризации η (больше наклон поляризационной кривой), тем меньше коррозионный ток и, соответственно, скорость коррозии.
Если скорости анодного и катодного процессов сильно различаются по величине, то общая скорость коррозии определяется медленным процессом (лимитирующая или контролирующая ста-
дия). Возможны коррозионные процессы, протекающие с катодным контролем: небольшая скорость реакции восстановления (кинетический контроль) или недостаточная скорость подвода деполяризатора к поверхности катода (диффузионный контроль). Так же для процессов, протекающих с анодным контролем: медленное окисление металла (кинетический контроль) или пассивация металла (диффузионный контроль).
Пассивность металла – резкое уменьшение скорости анодного окисления при наличии в коррозионной среде сильных окислителей – обусловлена образованием на его поверхности защитных пленок. В этом случае на анодной поляризационной кривой выше
потенциала пассивации ( ϕ пасс ) коррозионный ток резко уменьшает-
ϕ а
ϕ пасс Пассивное состояние
Активное состояние 
Рис. 9.12. Анодная поляризационная кривая при пассивации металла; ϕ пасс – потенциал пассивации
Вещества, присутствующие в коррозионной среде, могут как уменьшать, так и увеличивать скорость коррозии, образуя или разрушая защитные пленки на поверхности металлов.
Вещества, снижающие скорость, называются ингибиторами коррозии. Например, железо легко корродирует в разбавленном растворе хлорида натрия. При добавлении в раствор сульфата цинка на катоде образуется малорастворимый дигидроксид цинка, а при добавлении фосфата натрия – на аноде нерастворимый фосфат железа. Это существенно снижает скорости катодного или анодного процессов (катодный и анодный ингибиторы). Такие методы
Общие положения. Термодинамика процессов коррозии
Коррозией металлов называется самопроизвольное их разрушение вследствие химического или электрохимического взаимодействия с окружающей средой.
Химическая коррозия – это процесс, при котором окисление металла и восстановление окислительного компонента среды протекают в одном акте. Типичный пример: окисление железа кислородом воздуха:
Наиболее распространенным и практически важным видом химической коррозии является газовая коррозия – коррозия металлов в газах при высоких температурах. В настоящем курсе лекций, в котором рассматриваются вопросы противокоррозионной защиты металлических сооружений в морской воде, морской атмосфере и других естественных средах, химическая коррозия рассматриваться не будет, как практически мало существенная в данных условиях.
Электрохимическая коррозия – это разрушение металлов вследствие их электрохимического взаимодействия с электролитически проводящей средой, при котором ионизация атомов металла и восстановление окислительного компонента среды протекает не в одном акте и их скорости зависят от величины электродного потенциала металла. Этот вид коррозии наиболее распространен и является превалирующим для интересующих нас условий эксплуатации металлоконструкций.
Первопричиной коррозии металлов является их термодинамическая неустойчивость в различных средах при данных внешних условиях. Термодинамика определяет возможность или невозможность самопроизвольного протекания коррозионного процесса при определенных условиях.
Скорость коррозионного процесса может быть представлена в общем виде с помощью уравнения:
ДСП может быть определена с помощью термодинамики. ТП не может быть определено термодинамически, однако с помощью термодинамики можно оценить условия, уменьшающие или исключающие протекание процесса (применение защитных сред, катодная защита, обескислороживание и др.).
Независимо от механизма коррозии возможность ее протекания определяется знаком изменения термодинамического потенциала. Процессы коррозии наиболее часто описывают изменением изобарно-изотермического потенциала – энергии Гиббса.
Любое изменение энергии системы характеризует переход ее в новое состояние и является мерой стабильности системы:
Очевидно, что при ΔG = 0 система находится в равновесии; при ΔG 0 процесс коррозии невозможен.
Процесс электрохимической коррозии включает в себя пять основных этапов. Например, для случая коррозии углеродистой стали в воде или влажном воздухе процесс протекает следующим образом:
1) ионизация атомов железа с образованием гидратированных ионов в воде и некомпенсированных электронов на анодных участках металла
2) переход электронов на катодные участки и их ассимиляция деполяризаторами (в нейтральных растворах кислородом) с образованием ионов гидроксила
3) образование в растворе гидрата закиси железа
4) доокисление до гидрата окиси железа Fe (ОН)3 и преобразование его в окончательный продукт коррозии Fe2 O3 ∙ mH2 O
Суммарная реакция коррозии стали будет иметь вид:
Коррозия металла представляется как результат работы большого числа коррозионных гальванических элементов, возникающих на отдельных участках поверхности вследствие ее гетерогенности. Электрохимическая гетерогенность поверхности металла, обуславливающая ее дифференциацию на анодные и катодные участки, может быть вызвана различными причинами: макро- и микровключениями примесей, анизотропностью кристаллической решетки, наличием оксидных пленок и других загрязнений, неравномерностью приложения механических нагрузок, наличием пар дифференциальной аэрации и др.
Усредненные значения стационарных потенциалов металлов в морской воде (по водородному электроду, В*) можно расположить в ряд:
Исходя из теории локальных элементов, ток коррозии в общем виде может определяться по закону Ома:
, Rнк + Rna— соответственно поляризационное сопротивление на катоде и аноде;
Rом— сопротивление электролита.
Определяющие скорость коррозии соотношения обычно наглядно представляются в виде коррозионных диаграмме, где потенциалы анода и катода представляются в функции силы тока.
Чаще всего скорость коррозионного процесса определяется следующими факторами:
*Здесь и далее величины потенциалов даны по водородному электроду. На практике обычно применяются хлорсеребряные электроды сравнения, имеющие собственный потенциал +240 мВ по отношению к нормальному водородному электроду, реже медносульфатные +310мВ и цинковые – 800мВ.
ТЕРМОДИНАМИКА ХИМИЧЕСКОЙ КОРРОЗИИ МЕТАЛЛОВ
Первопричиной химической коррозии металлов является их термодинамическая неустойчивость в различных средах при данных внешних условиях, т. е. возможность самопроизвольного перехода металлов в более устойчивое окисленное (ионное) состояние в результате процесса:
Металл + Окислительный компонент среды = Продукт реакции
с соответствующим уменьшением термодинамического потенциала этой системы.
Газовая коррозия — наиболее распространенный вид химической коррозии. Это процесс разрушения металлов и сплавов в результате химического взаимодействия с газами при высоких температурах, когда невозможна конденсация влаги на поверхности металла. Причина газовой коррозии металлов — их термодинамическая неустойчивость в данной газовой среде при определенных внешних условиях (температуре и давлении).
Принципиальная возможность или невозможность самопроизвольного процесса газовой коррозии определяется характером изменения термодинамического потенциала DGT . Если при заданных условиях (температуре и давлении) DGT 0 0 > 0 – коррозионный процесс невозможен (наоборот, возможно восстановление металла из ионного состояния).
При DGT 0 = 0 система находится в термодинамическом равновесии – коррозия невозможна. Формула для расчета DGT :
а) ро2 = рМеО т. е. парциальное давление кислорода ро2 , в газовой смеси и давление диссоциации оксида рМеОравны; реакция находится в равновесии;
Дата добавления: 2015-11-04 ; просмотров: 3369 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ








