Определение рака предстательной железы и его метастаз с помощью современных технологий
» data-image-caption=»» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/03/opredelenie-raka-predstatelnoj-zhelezy-i-ego-metastaz-s-pomoshhju-sovremennyh-tehnologij-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/03/opredelenie-raka-predstatelnoj-zhelezy-i-ego-metastaz-s-pomoshhju-sovremennyh-tehnologij.jpg» title=»Определение рака предстательной железы и его метастаз с помощью современных технологий»>
Александр Попандопуло, студент медицинского института УЛГУ. Редактор А. Герасимова
Сочетание анализов на онкомаркеры, компьютерной томографии и позитронно-эмиссионной томографии позволяет определять параметры опухоли и наличие метастаз с большой точностью.
Современная медицина располагает большим арсеналом методов выявления опухолей предстательной железы. Однако последние исследования показали, что лучшие результаты дает сочетание всех имеющихся технологий.
Это позволяет выявлять опухоль на ранних стадиях и точно определять рецидивы и метастазы в запущенных случаях. К такому выводу пришли австралийские ученые, опубликовавшие статью в журнале «Lancet».
Какие методы диагностики метастазирующего рака простаты существуют в настоящее время
PSMA-PET / CT делает диагностику более точной
Австралийские ученые проанализировали эффективность сочетания PSMA-PET/CT, применив его в 10 клиниках. В исследовании участвовали 302 участника с высоким риском опухоли простаты, которые были разделены на две группы:
В первой группе точность определения диагноза и наличие метастаз составляло 65%, а во второй 92%. Это колоссальная разница, позволяющая назначить максимально верное лечение рака.
Метод также может применяться для диагностики метастаз, возникших после лечения. У многих пациентов они обнаруживаются через несколько месяцев после радикальной простатэктомии (удаления простаты) или лучевой терапии, что значительно ухудшает прогноз.
Каким, по мнению учёных, должен быть алгоритм обнаружения опухолей простаты и их метастаз
Больному делается УЗИ. При обнаружении подозрительных очагов или затемнений назначается дальнейшее исследование.
При высоких показателях онкомаркеров и плохих результатах УЗИ простаты нужно обязательно пройти дополнительную диагностику. Это позволит обнаружить опухоль и назначить адекватное лечение.
Можно сразу сделать больному PSMA-PET/CT, но это исследование достаточно дорогое и сопровождается облучением организма. Поэтому начинать обследоваться нужно с самых простых методов. Более сложные и дорогостоящие процедуры назначаются при обнаружении признаков опухоли.
PSA и его роль в диагностике рака простаты
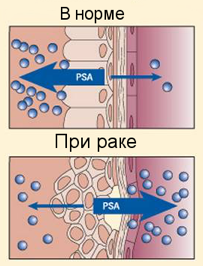
Рис. 1. Модель попадания PSA из эпителиальных клеток в сыворотку крови в норме и при раке предстательной железы.
Специфичность определяемых в сыворотке крови антигенов невелика, и их структурный анализ не дает возможность отличить рак предстательной железы от ее доброкачественной гиперплазии на этапе лабораторной диагностики. В сыворотке крови большая часть PSA находится в комплексе с альфа1-антихимотрипсином, 5-40% обнаруживается в свободном состоянии [2]. При раке предстательной железы по сравнению с ДГПЖ количество связанного PSA выше, а концентрация свободной фракции уменьшается. Определение уровня свободной фракции PSA широко используется для уточнения диагноза рака предстательной железы, однако решающим для дифференциальной диагностики является проведение биопсии органа [5]. Простат-специфический антиген в сыворотке крови образует комплексы и с другими ингибиторами протеаз, и определение уровня содержания этих комплексов может в дальнейшем исключить возможность получения ложноположительных результатов тестов на PSA [2].
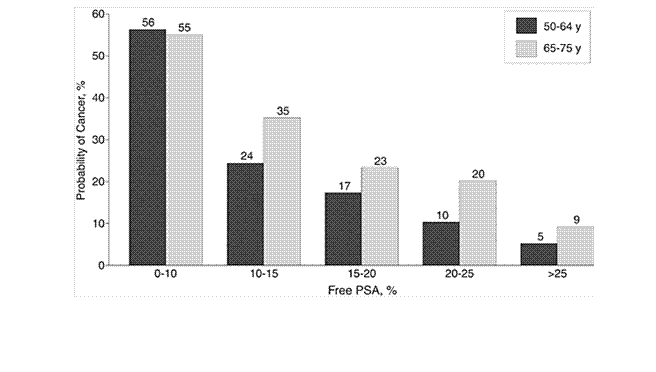
Рис. 2. Доля свободного PSA в сыворотке крови у мужчин с доброкачественной гиперплазией предстательной железы и раком предстательной железы [5].
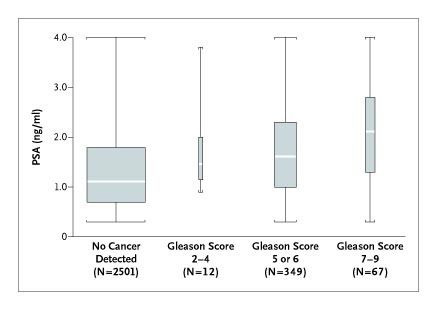
Рис. 3. Наибольшее число наблюдений пациентов с высоким уровнем сывороточного PSA соответствует ДГПЖ. У больных с раком предстательной железы наиболее высокие значения PSA соответствуют высоким градациям по шкале Глисона (5-9) [9].
Роль высокочувствительных проб на PSA, позволяющих выявить сывороточные концентрации этого антигена с уровня в 0.001 нг/мл, в настоящее время представляется двоякой. С одной стороны, высокочувствительные тесты позволяют выявить рецидив рака предстательной железы на ранних этапах, но специфичность выявляемых антигенов при этом по-прежнему невелика. Кроме того, существует категория пациентов, прошедших успешное радикальное лечение рака предстательной железы и демонстрирующих регулярные подъемы уровня сывороточного антигена, не связанные с рецидивированием опухоли. Все это в значительной мере усложняет диагностику рецидивов [10].
В свое время открытие PSA стало революцией в диагностике рака предстательной железы у мужчин. Несмотря на пересмотр роли этого антигена, его значение в улучшении качества жизни больных с аденокарциномой простаты невозможно переоценить. В настоящее время необходимо увеличение специфичности анализов и повышение точности распознавания молекулярных форм свободного и связанного антигенов, что, без сомнений, приведет к снижению уровня ложноположительных результатов [11].
Источники:
Диагностика ПСА-негативного рака предстательной железы, осложненного метастазированием в кости (клинический случай)
М.М. Бобринев, А.А. Аксенов, А.А. Сафронов, А.М. Берщанская
ГБУЗ «Диагностический клинический центр № 1 ДЗМ» (г. Москва)
Рак предстательной железы (РПЖ) — одно из самых распространенных и социально значимых заболеваний в структуре злокачественных новообразований. В Российской Федерации в последние годы отмечен беспрецедентный рост числа выявляемых ежегодно больных, количество, которых в 2009 г. составило 25 215 человек. Темпы прироста за последние 10 лет составили 130,57 %, а смертности — 40,72 %.
На начальных стадиях заболевания РПЖ не имеет самостоятельных клинических проявлений. Клинические проявления при локализованном РПЖ чаще всего связаны с сопутствующей доброкачественной гиперплазией предстательной железы. На более поздних стадиях симптомы заболевания обусловлены проявлением метастатического процесса, что вынуждает пациентов обращаться к врачам-специалистам неурологического профиля. Отсутствие повышения простатоспецифического антигена (ПСА) при РПЖ, вероятнее всего, связано с определенными видами злокачественных образований предстательной железы, при которых уровень ПСА не повышается выше нормальных значений. Такими опухолями предстательной железы чаще всего являются мелкоклеточная карцинома или высокодифференцированная нейроэндокринная карцинома и уротелиальная карцинома.
Учитывая выявленные изменения предстательной железы у пациента, амбулаторно в условиях дневного стационара выполнена промежностная биопсия предстательной железы под местной анестезией с внутривенным потенцированием и взяты 14 локусов биопсийного материала на морфологическое исследование с иммуногистохимической оценкой. При гистологическом исследовании выявлены в двух из 14 столбиков из левой доли предстательной железы локусы высокодифференцированной аденокарциномы G3, индекс Глисона 6. При дальнейшем обследовании у онколога метастатическое поражение костной ткани (позвонки) было подтверждено.
Таким образом, пациенты обращаются впервые, как правило, к специалистам неурологического профиля, и впоследствии рак предстательной железы выявляется на поздней стадии. Регулярный профилактический осмотр урологом мужчин старше 40 лет с назначением необходимых диагностических процедур (пальцевое ректальное исследование, ПСА, трансректальное ультразвуковое исследование) позволяет выявить рак предстательной железы на ранней стадии, улучшить качество жизни и снизить смертность от данной патологии.
Материалы 2-й научно-практической конференции урологов Северо-Западного федерального округа Российской Федерации
21–22 апреля 2016 года, г. Cанкт-Петербург
Урологические ведомости Спецвыпуск 2016 года
Метастазы при раке предстательной железы
Рак предстательной железы прогрессирует медленно. На ранних стадиях заболевание не имеет ярких симптомов, которые могли бы стать стимулом для обращения к врачу, анализа на ПСА (простатспецифический антиген) или комплексного обследования. Само по себе это уже фактор риска.
Что такое метастазы рака простаты
Метастазы (от др.-греч. «перемещение») — отдалённые вторичные очаги злокачественной опухоли, сформировавшийся при перемещении опухолевых клеток из первичного очага в тканях простаты. О начале процесса метастазирования можно говорить, когда опухоль выходит за пределы капсулы простаты.
Основные пути разрастания метастазов
Наиболее уязвимы печень, лёгкие, головной мозг, костный мозг, кости осевого скелета.
Основные органы-мишени – тазовые и забрюшинные лимфатические узлы, подвздошные лимфоузлы, реже органы ЦНС.
Оценка риска метастатического поражения лимфоузлов
Симптомы, которые должны вызвать настороженность
Отдалённые метастазы: куда метастазирует рак простаты
Кости осевого скелета
Особенности строения венозно-вертебрального сплетения, в которое поступает кровь из полости таза, делают костную систему человека наиболее уязвимой при миграции злокачественных клеток из первичного очага опухоли в простате. С током крови атипичные клетки беспрепятственно достигают сосудов костного мозга и костей осевого скелета. Метастазы РПЖ часто выявляются в позвоночнике, костях таза, рёбрах и др. Типичные симптомы метастазов в костях при раке простаты – боль, которую не удается снять анальгетиками, аномально долго заживающие переломы, деформация пораженной кости.
Печень
Злокачественные клетки попадают в печень преимущественно по кровеносным сосудам. Вторичные очаги опухоли могут долго развиваться без симптомов. При значительном поражении наблюдаются слабость, снижение аппетита, тупая боль в правом боку, давящая боль в области желудка.
Лёгкие
Лёгкие – один из самых уязвимых органов для гематогенного метастазирования. Как и при поражении других органов, метастазы развиваются без явной симптоматики. На поздних стадиях возможно появление хронического кашля, одышки, ощущение «тяжести» в груди.
Органы ЦНС
Злокачественные клетки могут достигать органов ЦНС как с кровью, так и с лимфой. Наиболее ранним из симптомов метастатического процесса обычно становятся интенсивные головные боли, иногда они могут сопровождаться тошнотой и головокружением.
Лечение рака простаты с метастазами часто осложняется тем, что злокачественные клетки образуют вторичные очаги опухоли сразу в нескольких органах. До 95 % пациентов, у которых диагностируются метастазы в мозге, имеют метастатические поражения костей. Мозг, кости и лёгкие затрагиваются в 31 % случаев; мозг, кости лёгкие и печень – в 19 % случаев.
Методы диагностики и оценки распространённости рака предстательной железы
УЗИ малого таза / ТРУЗИ
Это базовые исследования, благодаря которым врач может оценить объём простаты, состояние семенных пузырьков, рассмотреть лимфоузлы таза и забрюшинного пространства, печени и т.д. Методы ультразвуковой диагностики позволяют с достаточно точно визуализировать саму простату, но не дают возможности судить о злокачественности опухоли и с высокой достоверностью выявлять метастазы размером меньше 5 мм. Как уточняющее исследование рекомендуется МРТ.
Онкомаркеры
Антиген стволовых клеток предстательной железы (PSCA) – повышенная концентрация PSCA выявляется при злокачественных опухолях простаты и коррелирует с поздними стадиями заболевания.
Трансректальная биопсия под контролем УЗИ
МРТ
Уточняющий метод исследования, позволяющий получить серию поперечных и продольных срезов предстательной железы и окружающих тканей. Как правило, оценка местной распространенности опухоли производится врачом именно на основании МРТ. Исследование позволяет с высокой достоверностью определить, вышла ли опухоль за пределы капсулы простаты, затронуты ли органы, расположенные рядом, в каком состоянии находятся лимфоузлы таза (их увеличение может быть признаком начала метастатического процесса).
КТ
Компьютерная томография используется для оценки состояния лимфоузлов таза и определения полей облучения при лучевой терапии.
ПЭТ с холином
Метод применяется для выявления отдалённых метастазов при высоких уровнях ПСА, а также для оценки состояния лимфоузлов в спорных случаях, когда необходимо отличить воспалительные изменения в лимфоузле от метастазов опухоли.
Тазовая лимфаденэктомия
Наиболее точный метод оценки состояния регионарных лимфоузлов при РПЖ, позволяющий выявлять метастазы размером менее 5 мм.
Остеосцинтиграфия
Наиболее информативный метод выявления метастазов в костях. Радиоизотопное сканирование костей может быть рекомендовано всем пациентам с дифференцировкой опухоли по Глисону ≥ 8 или ПСА превышающим 10.
Рентгенография или КТ органов грудной клетки
Выполняется для проверки лёгких на наличие метастазов.
КТ живота и таза
Исследование назначается при подозрении на висцеральные метастазы. В некоторых случаях для выявления отдалённых метастазов может быть рекомендовано МРТ или ПЭТ-КТ всего тела.
Лечение распространенного рака предстательной железы
Большинство пациентов выбирают радикальные методы лечения в ситуациях, когда рак потенциально излечим, а операция дает надежду на сохранение привычного качества жизни. Если речь идет об опухоли, которая уже вышла за пределы капсулы простаты, радикальная простатэктомия может быть выполнена как один из этапов комплексного (мультимодального) лечения. Хирурги Европейского Центра Простаты в Гронау придерживаются этой тактики во всех случаях, когда состояние здоровья пациента позволяет провести операцию и продлить продолжительность жизни.
Радикальная простатэктомия + лимфаденэктомия
При наличии онкологического процесса, распространившегося на окружающие простату органы, пациентам, относящимся к группе высокого риска (стадия ≥T3a, сумма по шкале Глисона 8-10, ПСА >20 нг/мл), может быть предложена робот-ассистированная радикальная простатэктомия (РПЭ) совмещенная с лимфаденэктомией (удалением пораженных лимфатических узлов). В Европейском Центре Простаты в Гронау обе операции выполняются одновременно с применением роботизированной системы Да Винчи.
Особенности операции на стадии T3a:
Даже при увеличенном объёме вмешательства точность робот-ассистированной простатэктомии Да Винчи позволяет свести к минимуму травмы проксимального отдела и сфинктера уретры, а также шейки мочевого пузыря. Для пациента это означает, что процесс реабилитации будет легче, а естественная функция удержания мочи восстановится быстрее.
Лучевая терапия
Показаниями к лучевой терапии после операции РПЭ считаются:
Как и радикальная простатэктомия, лучевая терапия применяется в качестве одного из компонентов комбинированного лечения. Вариант совмещения лучевой и гормональной терапии считается более эффективным, чем каждая из них по отдельности. Комбинированное лечение достоверно улучшает качество и продолжительность жизни на третьей и четвертой стадиях простаты при наличии метастазов.
Паллиативная лучевая терапия при метастазах в кости
Метод применяется для обезболивания. При одиночных (солитарных) метастазах облучение направляется на пораженную зону, в которой локализован болевой синдром. При множественном поражении костей практикуется применение радионуклидов стронция-89 и самария-153.
Гормональная терапия
Для пациентов со стадией заболевания T3a гормональная терапия служит дополнением радикального лечения (хирургического или лучевого). Но в ситуациях, когда рак простаты уже дал отдалённые метастазы, это метод первого выбора.
Когда оправдано назначение самостоятельной гормональной терапии:
Блокада андрогенов, которые стимулируют рост опухолевых клеток, замедляет рост опухоли и снижает риск болезненных осложнений из-за распространения метастазов. Онколог индивидуально подбирает режим терапии (постоянный или прерывистый), исходя из стадии заболевания, течения болезни, скорости прироста ПСА, риска прогрессии и других факторов.
Химиотерапия
Метод применяется, когда рак с метастазами не отвечает на гормональное лечение. При метастазах в кости наряду с противораковыми препаратами (доцетаксел и др.) используются бисфосфонаты, моноклональные антитела IgG2 и препараты кальция для снижения риска осложнений. При выраженном болевом синдроме назначается паллиативная лучевая терапия.
На сегодняшний день Хирурги Европейского Центра Простаты в Гронау выполнили более 13 000 робот-ассистированных операций по удалению опухолей простаты и пораженных лимфоузлов. Это уникальный опыт в масштабах Европы. Мы добиваемся хороших функциональных результатов, работая с пациентами с 3 стадией рака простаты, с установленными стентами, водителями ритма, в возрасте старше 65 лет – словом, с теми, кому по каким-то причинам не смогли помочь в других клиниках. Проконсультируйтесь с онкологом Центра, чтобы узнать о перспективах хирургического лечения в вашем случае.
Прогностические факторы выживаемости больных при раке предстательной железы
В Российской Федерации рак предстательной железы (РПЖ) является одним из наиболее распространенных онкологических заболеваний у мужчин, занимая второе место после опухолей легких. Доля РПЖ в структуре онкозаболеваний составляет 14,4%. Стандартизированный показатель заболеваемости в 2015 году составил 40 на 100 000 мужчин. В РФ число мужчин, заболевших РПЖ в 2015 г., составило 38 812, тогда как в 2005 г. было зафиксировано 16 861 больных, прирост заболеваемости за последние 10 лет составил +105,7%. Важно отметить, что при общем снижении смертности от всех онкозаболеваний, смертность от РПЖ растет: в 2005 г. было 8192 летальных исходов, в 2015 г. – уже 11987. Несмотря на значительное увеличение числа больных с ранними формами заболевания, 45% пациентов при выявлении заболевания имеют местно-распространенные и метастатические формы [1].
Зная неагрессивный характер большинства типов РПЖ, а также тот простой факт, что это заболевание скорее связано с возрастом, чем с другими факторами, большой клинической проблемой является определение абсолютных показаний для назначения адекватного лечения. Риск чрезмерной диагностики и чрезмерного лечения во многих случаев РПЖ является реальным и вызывает много вопросов. В последние годы сформировалась устойчивая тенденция к изучению выбора наиболее подходящей стратегии и наиболее подходящего вида лечения РПЖ. Учитывая медленные темпы развития и прогрессирования РПЖ и возраст больных, риск смерти от сопутствующих заболеваний часто превышает риск смерти от РПЖ. В то же время лечебные вмешательства, которые проводят при РПЖ, обладают выраженными побочными эффектами и существенно влияют на качество жизни больных. В связи с этим при планировании тактики необходимо тщательно проанализировать факторы риска, связанные с одной стороны с потенциалом прогрессирования рака и с другой стороны – с состоянием соматического здоровья и ожидаемой продолжительностью жизни 6. Настоящая работа предполагает изучение прогностических факторов выживаемости для понимания адекватного клинического подхода в стратегии лечения РПЖ.
Цель исследования: улучшение результатов лечения больных РПЖ на основании выделенных факторов прогноза выживаемости в зависимости от клинико-морфологической характеристики опухоли, соматических данных, тяжести интеркуррентных заболеваний, вида лечения и осложнений.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включены данные 1127 больных с морфологически подтвержденным диагнозом РПЖ. Был проведен ретроспективный анализ лечения больных локализованным(Т0-Т2сNх-0М0),местнораспространенным(Т3а-Т4Nх/0М0) и метастатическим (ТлюбоеNх/1М1а-1c) РПЖ. Больные наблюдались и проходили лечение в ФГБУ «Институт хирургии им. А.В. Вишневского» г. Москвы, ГБУЗ «ГКБ им. Д.Д. Плетнева (ГКБ №57)» г. Москвы, ГБУЗ «ГП №218» г. Москвы, ГБУЗ «Клинический онкологический диспансер №1» г. Краснодара с 1995 по декабрь 2016 гг. включительно.
Возраст больных на момент включения в исследование колебался от 41 до 89 лет, средний возраст – 65,4±5,2 года. В группу хирургического лечения (радикальная простатэктомия – РПЭ) включено 495 больных, в группу лучевых (гормонолучевых) методов лечения – 256 больных, в группу андрогенной депривации – 305 больных и в группу отсроченного лечения (активное наблюдение/выжидательная тактика) – 71 больной. У 447 (39,7%) больных был локализованный РПЖ, у 399 (35,4%) – местно-распространенный и у 281 (24,9%) больного – метастатический РПЖ. У 435(38,6%) больных сумма баллов по шкале Глисона (индекс Глисона) был ≤ 6 баллов, у 478 (42,4%) – 7 баллов и у 198 (17,6%) – 8-10 баллов. Из 478 больных с индексом Глисона равным 7, у 238 (21,1%) больных сумма складывалась как 3+4, и у 240 (21,3%) – как 4+3. У 16 (1,4%) больных после РПЭ при тотальном морфологическом исследовании опухоли не было обнаружено (рТ0).
При сравнении всех групп лечения по ряду клинико-морфологических и соматических признаков имели место статистически значимые отличия, связанные с селекцией больных для различных видов специального лечения из-за степени распространенности опухолевого процесса и сопутствующей патологии.
Общие сроки наблюдения за больными составили 1–213 месяцев, средний период – 43,5±10,5 месяцев. При медиане наблюдения 49 месяцев (ИКР: 31-77 месяцев) из 1127 больных 704 (62,5%) были живы. В процессе специального лечения находился 251 (22,3%) больной. За время наблюдения всего погибло 423 (37,5%) больных: 189 (16,8%) – от прогрессирования кастрат резистентного РПЖ (КРРПЖ), 228 (20,2%) – от причин, не связанных с РПЖ. От осложнений лечебных мероприятий умерло 6 (0,5%) больных: 4 (0,3%) – из группы радикальной простатэктомии и 2 (0,2%) – из группы дистанционного лучевого лечения (ДЛТ).
Для решения поставленных в исследовании задач проведен подгрупповой анализ результатов лечения локализованного, местно-распространенного и метастатического РПЖ с многофакторным анализом влияния на выживаемость больных клинико-морфологических и соматических прогностических факторов.
РЕЗУЛЬТАТЫ
Группа хирургического лечения
РПЖ был причиной смерти у 11 (2,2%) из 495 оперированных больных (21,6% от всех смертей после операции). Независимыми прогностическими факторами ОСВ явились:
За время наблюдения в группе хирургического лечения умер 51 (10,3%) больной: 11 (2,2%) – от прогрессирования КРРПЖ, 36 (7,3%) – от причин, не связанных с РПЖ. От осложнений простатэктомии умерло 4 (0,8%) больных: ОИМ (один больной; 0,2%), ТЭЛА (3 больных; 0,6%). Причины смерти приведены в таблице 1
Таблица 1. Характеристика летальности у больных после простатэктомии
| Причина смерти | n=51 | |
|---|---|---|
| n | % | |
| Осложнения простатэктомии | 4 | 7,8 |
| Прогрессирующий КРРПЖ | 11 | 21,7 |
| Второе онкологическое заболевание | 9 | 17,6 |
| Сердечно-сосудистая патология | 23 | 45,1 |
| Другие причины: болезни, травмы | 4 | 7,8 |
Независимыми прогностическими факторами общей выживаемости (ОВ) являлись:
Группа гормонолучевого лечения
В исследование включены пациенты в стадии сТ1а-Т4N0/1М0. Больные, исходя из задач, были распределены на 4 группы:
Средний возраст больных составил 69,8±7,1 года, медиана – 70 лет (ИКР: 66-74 года, вариация 50-88). В группу лучевого лечения включено 43 (16,8%) больных с локализованным РПЖ, 198 (77,3%) – местно-распространенным РПЖ и 15 (5,9%) больных метастатическим (N +) РПЖ. Подавляющее большинство больных (n=202; 78,9%) относились к группе высокого риска прогрессирования и 39 (15,8%) – к группе промежуточного и низкого риска. У 15 (5,9%) больных была категория N+, индекс Чарльсона составил 0,82±0,91.
Из 256 больных, включенных в исследование, 110 (42,9%) живы (68 пациентов – без признаков болезни). В процессе специального лечения находились 42 (16,4%) больных: 17 (6,6%) имели ПСА-рецидив, 12 (4,7%) – местный рецидив, 13 (5,1%) – метастазирование. За время наблюдения в группе ДЛТ умерли 146 (57,1%) больных: 52 (20,4%) – от прогрессирования КРРПЖ, 94 (36,7%) от причин, не связанных с РПЖ. От осложнений ДЛТ умерло 2 (0,8%) больных: язвенно-некротический ректит (флегмона малого таза) (n=1; 0,4%), язвенный цистит, микроцист (кровотечение) (n=1; 0,4%).
Преимущество длительной андрогенной депривационной терапии выявлено при сравнении 10летней безрецидивной выживаемости (БРВ) с группами ДЛТ в монорежиме, ДЛТ +3-х и 6-ти месячной АДТ: 38,7% и 23,4%, 29,7%, 30,9%, соответственно (р=0,018). Медиана до клинического рецидива в группе длительной АДТ достоверно отличалась при сравнении с группой ДЛТ в монорежиме: 46 против 29 месяцев. Достоверно отличалась 5ти и 10-летняя выживаемость без клинического прогрессированиямежду длительной АДТ (82,9%, 63,4% соответственно) и остальными группами:группаДЛТ (65,3%, 45,8%),группа ДЛТ+3-х месячная АДТ (71,5%, 55,7%) и группа ДЛТ+6-ти месячная АДТ (70,2%, 58,9%) (р=0,005).
Были изучены независимые прогностические факторы риска биохимического рецидива (БХР) у мужчин с длительной гормонолучевой терапией. Сильное влияние на риск рецидива оказывал надир ПСА≥0,5 нг/мл (ОР 1,13, ДИ 1,02-1,25; р=0,011) и индекс Глисона ≥8 (ОР 3,90; ДИ 1,16-15,54; р=0,003). Менее значимым был возраст мужчин моложе 70 лет (р=0,042), стадия N+ (р=0,021) и наличие местно-распространенного РПЖ (р=0,015). На границе статистической значимости было влияние уровня ПСА >20 нг/мл (р=0,048) и наличия ожирение (индекс массы тела – ИМТ ≥30) (р=0,051).
За время наблюдения в группе ДЛТ умерли 146 (57,1%) больных: 52 (20,4%) – от прогрессирования КРРПЖ, 94 (36,7%) – от причин, не связанных с РПЖ. Лучшая 5-ти и 10-ти летняя ОСВ отмечена у больных без метастазов в ЛУ – 98,4%, 76,3% и в группе длительного гормонолучевого лечения – 86,2% и 81,6%, соответственно.
Независимыми факторами прогноза ОСВ являлась:
При анализе ОВ отмечено достоверное улучшение выживаемости больных в группе ДЛТ+длительное АДТ лечение и вгруппе ДЛТ в монорежиме (р=0,010). Показатели ОВ в группах монорежима ДЛТ и 3х и 6-ти месячной АДТ не имеют отличий. На увеличение ОВ положительно влияла длительность АДТ (ОР 0,81, ДИ 0,68-0,96, р=0,038), стадия N0 (ОР 2,19, ДИ 1,42-3,60, р=0,039), возраст мужчин моложе 70 лет (ОР 0,85, ДИ 0,72-0,96, р=0,018). Из конституциональных факторов положительно влияло благополучное соматическое состояние больного (р=0,016). Отсутствие ожирения (ИМТ 0,05).
Группа андрогенной депривации
В группу АДТ вошли больные с локализованной формой РПЖ (n=23; 7,5%), местно-распространеннойформой (n=92; 30,2%) и генерализованным раком (n=190; 62,3%). Отдаленныеметастазы(M1а-с) выявленыу 180 больных (94,7%). Клинически изолированные регионарные метастазы (N1) определялись у 10 (5,3%) больных, только юкстарегионарные – у 17 (8,9%). Регионарные и отдаленные метастазы имелись у 86 (45,3%) пациентов, только отдаленные – у 94 (49,4%). Висцеральные метастазы преимущественно в легких и печени встречались у 15 (7,9%) больных. Подавляющее большинство пациентов имели поражение осевого скелета костнымиметастазами (n=122; 82,4%). Очаги, поражающие грудную клетку, череп и трубчатые кости, отмечены у 63 (42,6%) больных. У 25 (8,2%) пациентов выявлены опухоли с дифференцировкой 4-6 балла по шкале Глисона, у 207 (67,9%) – 7 баллов и у 73 (23,9%) – 8-10 баллов. Средняя концентрация ПСА составила 224,5± 395,1 нг/мл. Медиана составила 202,5 нг/мл (ИКР: 108,5 – 436,5, вариация 6,1-3025). Индекс Чарльсона был равен 0,89±0,95. Наиболее распространенными клинически значимыми интеркуррентными заболеваниями, выявленными у 305 больных, являлись артериальная гипертензия (37,7%) и ишемическая болезнь сердца (51,1%). Индекс массы тела составил 27,2±3,4, ожирение (ИМТ>30) имело место у 108 (35,4%) больных.
При медиане наблюдения 37 месяцев (ИКР: 19-58 месяцев) из 305 больных, включенных в исследование, 126 (41,3%) живы (все с признаками болезни). За время наблюдения 179 (58,7%) больных погибли: 121 (67,6%) – от КРРПЖ, 58 (32,4%) – от причин, не связанных с РПЖ. Без кастрационной рефрактерности живых больных – 45 (14,8%). До десяти лет дожили больные только с локализованными формами РПЖ. Таким образом всего больных, доживших до КРРПЖ было 211 (69,2%).
5-ти и 10-летняя выживаемость 305 больных без резистентности к АДТ составила 36,4% и 2,3%.
Независимыми факторами выживаемости без КРРПЖ являлись:
5-ти, 10-летняя ОСВ 305 больных в группе АДТ составила 41,8% и 4,9%. В многофакторном анализе было подтверждено влияние пяти факторов:
За время наблюдения в группе АДТ умерли 179 (58,7%) больных: 121 (39,7%) – от прогрессирования РПЖ, 58 (19%) от причин, не связанных с РПЖ.
Медиана времени до смерти составила 35 месяцев (ИКИ: 29-41; диапазон от 7 до 145 мес.). 5-ти, 10летняя ОВ была равна 28,6% и 1,3%, соответственно. В многофакторном анализе было подтверждено влияние только трех факторов:
Группа отсроченного лечения
Больные этой группы были подходящими кандидатами для специального лечения: хирургического, лучевого или гормонального. В силу различных обстоятельств: самостоятельный отказ или временное воздержание от лечения, выбор стратегии наблюдения, предложенной онкологом, урологом, больные не получали никакого специального онкологического лечения. В данную группу наблюдения включено 56 (78,9%) больных с локализованным РПЖ и 15 (21,1%) больных местнораспространенным РПЖ. У большей половины больных (67,6%) в группе наблюдения определялись умеренно-высоко дифференцированные опухоли (индекс Глисона ≤6). Средний уровень ПСА составил 10,8±7,4 нг/мл, медиана – 8,6 нг/мл (ИКР: 5,1–14,1, вариация 1,2-56). Индекс Чарльсона составил 1,04±0,97. Наиболее распространенными клинически значимыми интеркуррентными заболеваниями, выявленными у 71 больного, являлись артериальная гипертензия (45,1%) и ишемическая болезнь сердца (69,1%). Индекс массы тела составил 28,5±4,1, ожирение (ИМТ>30) имело место у 28 (39,4%) больных.
За весь период наблюдения 37 (52,1%) больных в связи с прогрессированием стали получать специальное лечение: 6 (8,5%) больных – ДЛТ, 3 (4,2%) – выполнена РПЭ и 28 (39,4%) – получали АДТ. Из 37 больных четверо самостоятельно обратились для радикального специального лечения (РПЭ и ДЛТ). Все 9 больных, получивших местное специальное лечение, были из группы соматически здоровых мужчин (ИКЧ =0). ДЛТ и РПЭ была выполнена в течение первых двух лет наблюдения (вариация 7-24 месяца). Гормонотерапию получали преимущественно больные (n=25) с отягощенным соматическим статусом (ИКЧ ≥1).
Из 71 больного, включенного в исследование, 24 (33,8%) живы. В процессе специального лечения (АДТ) находится 9 (12,7%) больных. За время наблюдения умерли 47 (66,2%) больных: 5 (10,67%) – от прогрессирования КРРПЖ, 42 (89,4%) – от причин, не связанных с РПЖ. От осложнений РПЭ и ДЛТ летальности не было (табл. 2).
Таблица 2. Характеристика летальности в группе наблюдения
| Причина смерти | n=51 | |
|---|---|---|
| n | % | |
| Осложнения простатэктомии/ДЛТ | — | — |
| Прогрессирующий КРРПЖ | 5 | 10,6 |
| Второе онкологическое заболевание | 3 | 6,4 |
| Сердечно-сосудистая патология | 31 | 65,9 |
| Другие причины: болезни, травмы | 8 | 17,1 |
5-ти и 10-летняя общая выживаемость в группе 71 больного составила 67,3%, 36,7%; опухолевоспецифическая – 91,2%, 84,1%, соответственно. Медианы данных показателей выживаемости достигнуты не были. Всего из умерших от других причин погибло 42 (89,4%) больных. Доля неспецифической летальности прямо пропорциональна ухудшению соматического статуса: от 76,9% у соматически здоровых мужчин, до 95,7% больных с ИКЧ ≥2. За весь период наблюдения погибло 25 (89,3%) больных из 28 страдавших ожирением (ИМТ >30). РПЖ был причиной смерти у 5 (7%) больных наблюдавшихся больных (10,6% от всех смертей).
По данным однофакторного анализа достоверно на ОСВ влияет:
Статистически достоверного влияния других анализируемых клинико-морфологических показателей (уровень ПСА, степень дифференцировки опухоли, соматический статус и наличие ожирения) на ОСВ получено не было (р>0,05). Отсутствие подтвержденной статистической значимости других клиникоморфологических факторов объясняется либо небольшим количеством смертельных исходов или преобладанием значений других характеристик.
Многовариантный анализ также не подтвердил статистическую значимость клинико-морфологических факторов на ОСВ (р>0,05). Очевидно, это можно объяснить небольшим количеством наблюдений смерти от РПЖ.
За время наблюдения умерли 47 (66,2%) больных: 5 (7%) – от прогрессирования КРРПЖ, 42 (59,2%) – от причин, не связанных с РПЖ. Медиана времени до гибели больных от всех причин – 40 месяцев (ИКР: 25-72, вариация 4-137 месяцев). 5-ти и 10-летняя общая выживаемость в группе 71 больного составила 67,3% и 36,7%, соответственно. Основной причиной смерти больных явились сердечно-сосудистые заболевания (n=31; 65,9%) (табл. 2).
Независимыми прогностическими факторами являлись:
В настоящее время уделяется внимание изучению зависимости выживаемости от ожидаемой продолжительности жизни и коморбидности. При локализованном РПЖ оценка продолжительности жизни более 10 лет является обязательной для определения выгоды в выживаемости от проведенного местного радикального лечения. Однако коморбидный фон является у мужчин более важной прогностической категорией при анализе общей выживаемости при лечении локализованного РПЖ [20].
В нашей серии наблюдений возраст значительно снижал ОВ, особенно на отрезке 5-10 летнего периода наблюдения: с 87,5% до 72,9%. Влияние определялось, как независимая переменная в многофакторном анализе (ОР 1,29, ДИ 1,15-1,54; р=0,045). Полученные данные сопоставимыс литературными источниками при длительных наблюдениях [21,22].
В последнее время в литературе при прогнозировании выживаемости придается важное значение активности мужчин, нарушению питания и когнитивным расстройством. Коморбидность является основным предиктором смерти от других причин после РПЭ [23]. Это отмечено P. Albertsen и соавт., в работе которых больные не получали активногоместного лечения [20]. Через 10 лет большинство мужчин с индексомкоморбидностиЧарльсона >2 умерли от других причин, независимо от возраста и агрессивности рака.Агрессивность рака имела малое влияние на ОВ. Мужчины с ИКЧ ≤2 имеют низкий риск специфической смерти в течение 10 лет, особенно при высокодифференцированных раках. В последнее время для оценки рисков ранней смерти от других причин у больных при радикальных методахлечения все чаще пользуются Шкалой кумулятивного гериатрического риска (CISR-G) [24]. В нашей ретроспективной работе не было возможности пользоваться данным прогностическим инструментом изза дефицита полной коморбидной информации: показателей эндокринного, метаболического статуса, мышечно-скелетные физиометрические критериев и т.д.
В нашей серии наблюдений отягощенный соматический статус (Индекс Чарльсона ≥2) снижал 5-ти и 10-летнюю ОВ с 96,2% и 90,2% до 91,4% и 84,2%, соответственно. В многофакторном прогнозе этот показатель являлся независимым прогностическим признаком (ОР 1,16, ДИ 1,02-1,35; р=0,025). На другие виды выживаемости коморбидность не оказывала влияния ни в однофакторном, ни мультивариантном анализе (р>0,05).
ЗАКЛЮЧЕНИЕ
Ретроспективный анализ подтверждает эффективность хирургического, гормонолучевого, гормонального метода, а также целесообразность применения отсроченного лечения у определенных групп больных. Длительная АДТ после ДЛТ увеличивает выживаемость без ПСАрецидива и общую выживаемость. Длительная АДТ, по-видимому, обладает широким спектром отрицательного влияния на метаболический статус мужчин с повышенным риском кардиоваскулярных осложнений. Однако таких достоверных данных в нашей работе получено не было. Выбор длительной гормонолучевой терапии целесообразен у больных с неблагоприятным прогнозом течения болезни.
Планируется провести в дальнейшем для всех групп лечения общий многофакторный анализ влияния на выживаемость больных клинико-морфологических и соматических прогностических факторов, а также вида проводимого лечения. Полученные данные, возможно, позволят говорить об определенной селекции больных для наиболее подходящего вида лечения и возможность прогнозирования дальнейшего течения заболевания.
ЛИТЕРАТУРА
1. Злокачественные новообразования в России в 2015 году (заболеваемость и смертность). [Под редакцией А.Д. Каприна, В.В. Старинского, Г.В. Петровой]. М.: 2017. С.12-36.
2. Buhmeida A, Pyrhönen S, Laato M, Collan Y. Prognostic factors in prostate cancer. Diagn Pathol 2006;1–4. doi: 10.1186/1746-1596-1-4
3. Albertsen PC. Observational studies and the natural history of screen-detected prostate cancer. Curr Opin Urol 2015;25(3):232-7. doi: 10.1097/MOU.0000000000000157.
4. Welty CJ, Cooperberg MR, Carroll PR. Meaningful end points and outcomes in men on active surveillance for early-stage prostate cancer. Curr Opin Urol 2014;24(3):288-92. doi: 10.1097/MOU.0000000000000039.
5. Hamdy FC, Donovan JL, Lane JA, Mason M, Metcalfe C, Holding P, et al. 10-Year Outcomes after Monitoring, Surgery, or Radiotherapy for Localized Prostate Cancer. N Engl J Med 2016;375(15):1415-1424. doi: 10.1056/NEJMoa1606220 6. Klotz L, Vesprini D, Sethukavalan P, Jethava V, Zhang L, Jain S, et al. Long-term follow-up of a large active surveillance cohort of patients with prostate cancer. J Clin Oncol 2015;33(3):272-7. doi: 10.1200/JCO.2014.55.1192.
7. Pound CR, Partin AW, Eisenberger MA, Chan DW, Pearson JD, Walsh PC. Natural history of progression after PSA elevation following radical prostatectomy. JAMA 1999;281(17):1591-7.
8. Boorjian SA, Thompson RH, Tollefson MK, Rangel LJ, Bergstralh EJ, Blute ML, et al. Long-term risk of clinical progression after biochemical recurrence following radical prostatectomy: the impact of time from surgery to recurrence. Eur Urol 2011;59(6):893-9. doi: 10.1016/j.eururo.2011.02.026.
9. Antonarakis ES, Feng Z, Trock BJ, Humphreys EB, Carducci MA, Partin AW, et al. The natural history of metastatic progression in men with prostatespecific antigen recurrence after radical prostatectomy: long-term follow-up. BJU Int 2012;109(1):32-9. doi: 10.1111/j.1464-410X.2011.10422.x.
10. Brockman JA, Alanee S, Vickers AJ, Scardino PT, Wood DP, Kibel AS, et al. Nomogram Predicting Prostate Cancer-specific Mortality for Men with Biochemical Recurrence After Radical Prostatectomy. Eur Urol 2015;67(6):1160-1167. doi: 10.1016/j.eururo.2014.09.019
11. Briganti A, Karnes RJ, Joniau S, Boorjian SA, Cozzarini C, Gandaglia G, et al. Prediction of outcome following early salvage radiotherapy among patientswith biochemicalrecurrence after radical prostatectomy. Eur Urol 2014;66(3):479-86. doi: 10.1016/j.eururo.2013.11.045.
12. Trock BJ, Han M, Freedland SJ, Humphreys EB, DeWeese TL, Partin AW, et al. Prostate cancer-specific survival following salvage radiotherapy vs observation in men with biochemical recurrence afterradical prostatectomy.JAMA2008;299(23):2760-9. doi: 10.1001/jama.299.23.2760.
13. Gerber GS, isted RA, Chodak GW, Schroder FH, Frohmuller HG, Scardino PT, et al. Results of radical prostatectomy in men with locally advanced prostate cancer: multi-institutional pooled analysis. Eur Urol 1997;32(4):385-90.
14. Ward JF, Slezak JM, Blute ML, Bergstralh EJ, Zincke H. Radical prostatectomy for clinically advanced (cT3) prostate cancer since the advent of prostate-specific antigen testing: 15-year outcome. BJU Int 2005;95(6):751-6.
15. Hsu CY, Joniau S, Oyen R, Roskams T, Van Poppel H. Outcome of surgery for clinical unilateral T3a prostate cancer: a single-institution experience. Eur Urol 2007;51(1):121-8
16. Joniau S, Spahn M, Briganti A, Gandaglia G, Tombal B, Tosco L, et al. Pretreatment tables predicting pathologic stage of locally advanced prostate cancer. Eur Urol 2015;67(2):319-25. doi: 10.1016/j.eururo.2014.03.013.
17. Freedland SJ, Partin AW, Humphreys EB, Mangold LA, Walsh PC. Radical prostatectomy for clinical stage T3a disease. Cancer 2007;109(7):1273-8. DOI:10.1002/cncr.22544
18. Joniau S, Hsu CY, Gontero P, Spahn M, Van Poppel H. Radical prostatectomy in very high-risk localized prostate cancer: long-term outcomes and outcome predictors. Scand J Urol Nephrol 2012;46(3):164-71. doi: 10.3109/00365599.2011.637956.
19. Moltzahn F, Karnes J, Gontero P, Kneitz B, Tombal B, Bader P, et al. Predicting prostate cancer-specific outcome after radical prostatectomy among men with very high-risk cT3b/4 PCa: a multi-institutional outcome study of 266 patients. Prostate Cancer Prostatic Dis 2015;18(1):31-7. doi: 10.1038/pcan.2014.41
20. Albertsen PC, Moore DF, Shih W, Lin Y, Li H, Lu-Yao GL. Impact of comorbidity on survival among men with localized prostate cancer. J Clin Oncol 2011;29(10):1335-41. doi: 10.1200/JCO.2010.31.2330.
21. Richstone L, Bianco FJ, Shah HH,Kattan MW, Eastham JA, Scardino PT, et al. Radical prostatectomy in men aged >or=70 years: effect of age on upgrading, upstaging, and the accuracy of a preoperative nomogram. BJU Int 2008;101(5):541-6. doi: 10.1111/j.1464-410X.2007.07410.x..
22. Sun L, Caire AA, Robertson CN, George DJ, Polascik TJ, Maloney KE, et al. Men older than 70 years have higher risk prostate cancer and poorer survival in the early and late prostate specific antigen eras. J Urol 2009;182(5):2242-8. doi:10.1016/j.juro.2009.07.034. 23.
Tewari A, Johnson CC, Divine G, Crawford ED, Gamito EJ, Demers R, et al. Longterm survival probability in menwith clinically localized prostate cancer: a case-control, propensity modeling study stratified by race, age, treatment and comorbidities. J Urol 2004;171(4):1513-9. doi: 10.1097/01.ju.0000117975.40782.95
24. Groome PA, Rohland SL, Siemens DR, Brundage MD, Heaton J, Mackillop WJ. Assessing the impact of comorbid illnesses on deathwithin 10 yearsin prostate cancertreatment candidates. Cancer 2011;117(17):3943-52. doi: 10.1002/cncr.25984.