Механизм формирования филадельфийской хромосомы и ее роль в развитии хронического миелоидного лейкоза
Дата публикации: 19.06.2018 2018-06-19
Статья просмотрена: 8432 раза
Библиографическое описание:
Печенкина, А. А. Механизм формирования филадельфийской хромосомы и ее роль в развитии хронического миелоидного лейкоза / А. А. Печенкина. — Текст : непосредственный // Молодой ученый. — 2018. — № 25 (211). — С. 183-187. — URL: https://moluch.ru/archive/211/51560/ (дата обращения: 03.11.2021).
Филадельфийская хромосома (Ph-chromosome) является наиболее частой цитогенетической аномалией, обнаруживающейся в зрелых В-клетках пациентов с хроническим миелоидным лейкозом (ХМЛ), причем встречаемость этой мутации растет с возрастом, у детей выявляясь в 5 %, а у взрослых — в 50–90 %, достигая максимума у больных в возрасте 35–50 лет [1].
В данном обзоре обобщены результаты работ, опубликованных в системе PubMed и посвященных механизму формирования данной генетической аномалии, а также кратко приведены последствия ее возникновения.
Ключевые слова: филадельфийская хромосома, транслокация, хронический миелолейкоз
Филадельфийская хромосома была открыта в 1960 г учеными из Университета Пенсильвании в Филадельфии (за что и была так названа), в 1973 г в работе Rowley [цит. по 2] было доказано, что она образуется именно путем транслокации. Так, у всех пациентов с ХМЛ в исследовании была обнаружена дополнительная последовательность на длинном плече 9 хромосомы. Это позволило предположить, что Ph-хромосома получается путем переноса части 22ой хромосомы на 9ую (а не простой делеции 22ой хромосомы, как думали изначально) [2].
Транслокация приводит к тому, что участок с онкогеном c-abl, кодирующим тирозинкиназу, переносится к специфическому участку разрыва на 22 хромосоме (breakpoint cluster region — bcr), вместе с тем индуцируя перенос 3′-части гена Абельсона (Abl) с 9ой хромосомы на 22ую вблизи 5′-конца такого же участка bcr [3]. Наиболее важная часть всего процесса — перестановка гена Abl на 22 хромосому рядом с геном bcr и образование химерного гена BCR-ABL [4].
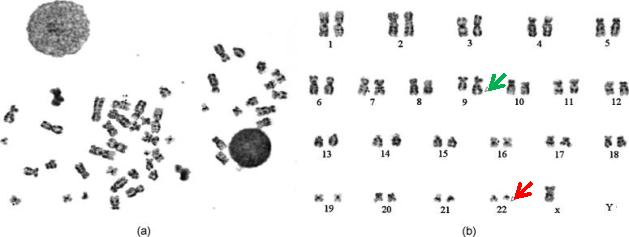
Что касается переноса именно между этими двумя хромосомами, здесь все не так однозначно. Одним из методов диагностики ХМЛ является автоматизированное кариотипирование клеток в стадии метафазы [6], на которой и выявляются атипичные хромосомы (см. Рис.1). Это дает основание полагать, что именно на стадии метафазы, когда хромосомы выстраиваются в экваториальной плоскости клетки, обеспечивается такое взаимное расположение 9ой и 22ой хромосомы, что возникает предпосылка к обмену их участками.
Рис. 1. а) Анализируемая клетка в метафазу и b) ее кариотип. Зеленая стрелка — удлиненная 9ая хромосома, красная стрелка — укороченная 22ая хромосома (Филадельфийская). Иллюстрация из [6] с изменениями.
Нормальный продукт гена BCR — цитозольный фосфопротеин массой 160кДа (р160 BCR ), функция которого не до конца определена. Известно, что первый экзон гена BCR кодирует серин/треонин-киназную активность этого белка, N-концевой домен которого отвечает за формирование димерной структуры, а С-конец обладает ГТФ-азной активностью. Также р160 BCR может быть вовлечен в каскад Ras путем фосфорилирования по тирозину в 177 положении, который таким образом становится способным связывать один из адаптерных белков этого пути [4].
Нормальный продукт гена ABL — тирозинкиназа массой 145 кДа (р145 ABL ), участвующая в процессах клеточного деления, дифференцировки, адгезии и ответа на стрессовые воздействия. С-конец отвечает за связывание с ДНК, а также имеет сайт связывания с актином. На N-конце белка находится три Src-домена: SH3, SH2, SH1. SH3- и SH2-домены регулирующие, а SH1-домен отвечает за наличие функции тирозинкиназы. Мутации в SH2-домене ослабляют связывание фосфотирозина, что приводит к снижению функции белка. SH3-домен имеет депрессорное значение, поэтому именно его удаление превращает белок в онкопротеин, т к его тирозинкиназная активность сильно возрастает [4].
Конечный продукт химерного гена представляет собой тетрамер, олигомеризация также стимулирует тирозинкиназную активность химерного белка [4].
Помимо этого классического варианта с транслокацией t(9;22), зарегистрированы больные ХМЛ с другим кариотипом. Так, в 1970 г коллективом авторов [цит. по 2] был описан случай 45-летней женщины с типичным ХМЛ. Ей было проведено генетическое исследование, в результате которого было установлено: во всех клетках костного мозга, взятых на исследование, обнаружены филадельфийские 22ые хромосомы, однако 9ые хромосомы во всех образцах интактны (см. Рис.). Это позволило предположить, что не всегда Ph-хромосома образуется одинаково: возможны как варианты с транслокацией t(9;22), так и транслокации между другими хромосомами, а также и простое выпадение фрагментов 22ой хромосомы. Вероятно, таким разнообразием цитогенетических механизмов объясняется гетерогенность течения ХМЛ [2].
Как уже было сказано, главный момент всех перестановок — сближение фрагментов ABL и BCR, поэтому в итоге не очень важно, как именно это сближение было достигнуто. Все вышеперечисленные варианты ведут к неконтролируемому функционированию мутантного продукта, что приводит к стимуляции многих путей клеточной прогрессии, но в особенности — гемопоэтического — поражаются стволовые клетки костного мозга. В результате наблюдается избыточная продукция незрелых клеток миелоидного ряда с неконденсированным хроматином — промиелоцитов, которые «давят» все остальные ростки в костном мозге, вытесняют жировую ткань, эритроциты, тромбоциты и т. д. (доля миелоидной ткани в межбалочных пространствах костного мозга может достигать 95–100 %).
Интересно, что несмотря на то, что у пациентов с ХМЛ также может наблюдаться миелофиброз (замещение гемопоэтической ткани костного мозга фиброзной), химерный ген обнаруживается только в клетках гемопоэтической ткани красного костного мозга, и не обнаруживается в фибробластах, что говорит о том, что фиброз является вторичным процессом, не связанным с мутацией напрямую [8].
В результате действия химерного белка нарушаются пути регуляции клеточного цикла, увеличивается пролиферация клеток, их чувствительность к факторам роста, а к проапоптотическим сигналам снижается, так же, как и снижается адгезивная способность к компонентам стромы костного мозга. Все это приводит к тому, что мутантные клетки имеют преимущество в делении (т. к. не чувствительны к апоптозу и быстрее делятся) и вытесняют здоровые клоны, а также выходят в кровь (из-за потери адгезивности) [9]
Почему же эти мутации затрагивают именно гемопоэтические клетки? Возможно, дело в том, что гемопоэтические и стромальные клетки происходят от разных предшественников. В эксперименте [10] было доказано, что стромальные клетки (адипоциты, фибробласты, эндотелиальные клетки и т. п.) и гемопоэтические — это две разные линии. Соответственно, и потенциал генетических изменений у них разный. И, конечно, имеет значение, что данные клетки относятся к быстро делящимся (все ростки включают регулярно обновляемые клетки). Чем быстрее клетки должны обновляться, тем раньше станут заметны их нарушения.
7. Wang X., Zheng B., Li S., Mulvihill J. J., Chen X., Liu H. Automated identification of abnormal metaphase chromosome cells for the detection of chronic myeloid leukemia using microscopic images. J Biomed Opt., 2010; 15(4)046026, doi: 10.1117/1.3476336
Лимфобластный лейкоз, осложненный филадельфийской хромосомой. Справка
Лейкоз (лейкемия) является злокачественным заболеванием белых кровяных телец. Заболевание возникает в костном мозге, а затем распространяется в кровь, лимфатические узлы, селезенку, печень, центральную нервную систему (ЦНС) и другие органы. Лейкоз может возникнуть как у детей, так и у взрослых.
Лейкоз является сложным заболеванием и имеет много различных типов и подтипов.
Лимфобластный лейкоз (острый лимфолейкоз) делится на два вида: В-линейный и Т-линейный, в зависимости от типа клеток – лимфоидных предшественников. По большей части, при остром лимфобластном лейкозе поражаются В-лимфоциты (примерно в 85% случаев), отвечающие за образование антител в организме.
Симптомы острого лимфобластного лейкоза
Синдром интоксикации – слабость, лихорадка, недомогание, потеря веса. Лихорадка может быть связана и с наличием бактериальной, вирусной, грибковой или протозойной (реже) инфекцией.
Анемический синдром – бледность, слабость, тахикардия, кровоточивость слизистых полости рта, геморрагический синдром на коже, бледность. Слабость возникает в результате анемии и интоксикации.
Дыхательные нарушения, связанные с увеличение лимфоузлов средостения, которые могут привести к дыхательной недостаточности. Этот признак характерен для Т-линейного ОЛЛ.
Могут появиться кровоизлияния в сетчатку глаза, отек зрительного нерва. При офтальмоскопии могут обнаруживаться лейкемические бляшки на глазном дне.
Из-за сильно сниженного иммунитета любое повреждение кожи является очагом инфекции.
Филадельфийская хромосома – это аномальная хромосома, редко встречающаяся у больных с острым лимфобластным лейкозом и образующаяся вследствие переноса части 9 хромосомы на 22. Такое слияние влечет за собой образование аномального протеина, играющего значительную роль в процессе превращения нормальной клетки в злокачественную. Данная хромосома встречается при нескольких типах лейкозов детей и взрослых.
Лечение острых лейкозов у взрослых
Острый лейкоз у взрослых – это не одно заболевание, а несколько, и больные с различными подтипами лейкоза неодинаково отвечают на лечение.
Выбор терапии основывается как на конкретном подтипе лейкоза, так и на определенных характеристиках болезни, которые называются прогностическими признаками. Эти признаки включают: возраст больного, количество лейкоцитов, ответ на химиотерапию и сведений о том, лечился ли ранее этот больной по поводу другой опухоли
Химиотерапия
Под химиотерапией подразумевается применение препаратов, уничтожающих опухолевые клетки. Обычно противоопухолевые препараты назначаются внутривенно или внутрь (через рот). Как только препарат поступает в кровоток, он разносится по всему организму.
Трансплантация стволовых клеток (ТСК)
Трансплантация стволовых клеток позволяет врачам использовать высокие дозы противоопухолевых препаратов с целью повышения эффективности лечения. И хотя противоопухолевые препараты разрушают костный мозг больного, пересаженные стволовые клетки помогают восстановить клетки костного мозга, продуцирующие клетки крови.
Лучевая терапия (использование рентгеновских лучей высоких энергий) играет ограниченную роль при лечении больных лейкозами.
Оперативное лечение больных лейкозом, в отличие от других видов злокачественных опухолей, как правило, не используется.
Материал подготовлен на основе информации открытых источников
Хронический миелоидный лейкоз – диагностика в Израиле
Злокачественная болезнь развивается очень медленно. Многие люди не нуждаются в лечении на протяжении нескольких месяцев и даже лет. Однако в некоторых случаях оно необходимо сразу же.
Доказано, что раннее выявление рака крови способствует составлению адекватного терапевтического протокола, который способен исцелить болезнь с наименьшим уроном для организма.
Компания Tlv.Hospital предлагает пройти полный диагностический контроль и получить экспертную оценку состояния здоровья в Израиле.
Мы максимально быстро подберем лучшего врача, оформим пребывание пациента в ведущем госпитале по коррекции раковых патологий, сформируем эффективный план лечения болезни по разумным ценам. Напрример, доктор Тавор Сигаль давно занимается лечением различных видов рака крови.
Оказавшись в сложной жизненной ситуации, позвоните нам, доверьте свои проблемы профессионалам.
У людей с хроническим миелолейкозом в крови присутствует избыточное количество белых клеток крови – гранулоцитов (зернистых лейкоцитов), поэтому эту болезнь иногда называют хронической гранулоцитарной лейкемией. При исследовании под микроскопом видно, что гранулоциты не полностью развиты (незрелые). С течением времени они накапливаются в селезенке, приводя к увеличению ее объема. Она расположена на левой стороне брюшной полости, под ребрами. Этот орган производит небольшое количество лимфоцитов, сохраняет клетки крови и разрушает старые, поврежденные.
Также гранулоциты заполняют костный мозг, снижая количество здоровых лейкоцитов, эритроцитов и тромбоцитов.
Чтобы лучше понять, что представляет собой хронический миелолейкоз и его лечение, будет полезно узнать несколько больше о крови человека.
Кровь в организме человека
Кровь состоит из клеток, которые находятся в плазме, жидкости.
Клетки крови производятся в костном мозге, губчатом веществе, которое заполняет внутреннюю, центральную часть костей, особенно в области таза и позвоночника. Обычно миллионы новых клеток крови синтезируются ежедневно, чтобы заменить старые и изношенные.
Все клетки крови образуются из стволовых. Различают два их типа:
Новые клетки крови являются незрелыми и называются бластными. Они не могут выполнять свою функцию. До созревания они пребывают в костном мозге. Здесь стволовые клетки делятся и растут, пока не образуют полностью развитые (зрелые) эритроциты, тромбоциты и лейкоциты.
Потом они высвобождаются в кровоток, чтобы выполнять различные функции:
Лейкоциты предупреждают развитие инфекций и борются с ними. Есть несколько видов белых клеток крови, два наиболее важных из них – это нейтрофилы и лимфоциты. Уровни этих клеток измеряются при общем анализе крови.
Как развивается хронический миелолейкоз?
У всех клеток есть определенный «набор инструкций», что делать и когда. Он хранится внутри них, в генах. Каждый ген контролирует тот или иной аспект поведения клеток. Например, некоторые определяют время отдыха, другие – роста, момент трансформации в зрелую клетку. Гены организованы в структуры или хромосомы.
Болезнь возникает, когда по ошибке ген переносится от одной хромосомы к другой во время деления клетки. Они объединяются. Это аномальное слияние останавливает процесс созревания бластов. Данные клетки являются лейкозными или бластными.
Филадельфийская хромосома
У большей части людей с данным заболеванием (95 из 100) в патологических клетках есть филадельфийская хромосома.
Основная часть клеток содержит 23 пары хромосом. Филадельфийская хромосома образуется, когда ген ABL на 9-й хромосоме ошибочно переносится к хромосоме 22 и прикрепляется к гену BCR. В результате образуется новый ген под названием BCR-ABL. Он синтезирует белок, который именуется тирозинкиназа. Избыток этого белка приводит к аномальному поведению клеток и изменениям в крови и костном мозге. Новые методы лечения хронического миелоидного лейкоза направлены на блокирование действий тирозинкиназы. Несмотря на то, что болезнь генетическая, она не является наследственной.
Причины хронического миелолейкоза
Существует ряд факторов, которые способны увеличить риск развития данного заболевания, хотя у большинства людей неизвестно, почему оно возникает.
В последние годы муссируется информация о том, что проживание вблизи атомных электростанций может оказывать определенное влияние. Исследования продолжаются до сих пор, но пока нет никаких доказательств.
Также не обнаружено связи между вероятностью ХМЛ и воздействием электромагнитных полей и бытового радона.
Симптомы хронического миелолейкоза
Признаки заболевания развиваются медленно, у многих людей нет никаких симптомов на ранних стадиях. Чаще всего миелоидную лейкемию выявляют случайно, когда анализ крови делают по другой причине, к примеру, перед операцией или во время регулярных медицинских осмотров.
Если признаки на ранних стадиях заболевания все же наблюдаются, то развиваются медленно и носят, как правило, мягкий характер. Они неспецифические, и их легко спутать с симптомами других распространенных болезней, таких как грипп.
Клинические проявления хронического миелолейкоза могут включать:
Если имеют место какие-либо из данных симптомов, стоит помнить, что они типичны для многих других заболеваний.
Диагностика хронического миелолейкоза в Израиле
В связи с незначительными симптомами болезнь обычно выявляется случайно. Анализ крови показывает высокое количество белых клеток крови – незрелых гранулоцитов.
Диагностикой и лечением заболевания занимается команда врачей в израильской клинике.
Первоначально гематолог собирает анамнез, обследует пациента, проверяет, не увеличены ли лимфатические узлы, селезенка или печень. Выполняется несколько анализов крови. Если их результаты показывают наличие лейкозных клеток, проводятся дополнительные тесты, которые помогают выявить тип лейкоза, степень развития заболевания. Это помогает спланировать лечение в Израиле.
Биопсия костного мозга
Иногда требуется проведение трепанобипсии, когда вместе с жидкостью извлекают костный фрагмент.
Дальнейшие тесты
В израильских клиниках могут быть задействованы и методы медицинской визуализации:
Цитогенетический тест исследует пробы крови и костного мозга с целью обнаружения филадельфийской хромосомы. Его результаты помогают врачам выбрать наилучший вариант лечения хронического миелолейкоза.
Стадии хронического миелолейкоза
Выделяют не стадии, а фазы ХМЛ: хроническую, ускоренную (фазу акселерации) и финальную (терминальную).
Хроническая фаза
Болезнь развивается очень медленно и часто стабильна в течение длительного времени. Могут отсутствовать какие-либо симптомы, и большинство людей ведет нормальный образ жизни.
В данный период больным редко необходимо посещать клинику. Лечение хронического миелолейкоза проводится амбулаторно и не вызывает множество побочных эффектов. Выполняются регулярно анализы крови, чтобы проверить, насколько хорошо организм отвечает на терапию.
У большинства пациентов, которые начинают лечить миелолейкоз в хронической фазе, болезнь хорошо контролируется, не вызывая симптомов. И если терапия постоянно продолжается, заболевание можно держать под контролем в течение многих лет и, возможно, десятилетий.
У некоторых людей ХМЛ плохо отвечает на лечение. И на протяжении приблизительно пяти лет после постановки диагноза болезнь может прогрессировать, перейдя из хронической фазы в более продвинутую.
Ускоренная фаза (акселерации)
У небольшого числа людей хронический миелоидный лейкоз может постепенно переходить на данный этап. Заболевание развивается быстрее, больше бластных клеток присутствует в крови и костном мозге. Иногда эти изменения можно увидеть с помощью анализов крови, применяя микроскоп. Если пациент плохо себя чувствует или обнаруживает новые симптомы, необходимо обязательно о них сообщить врачу.
Финальная фаза
Спустя некоторое время в ускоренной фазе (обычно месяц) болезнь переходит в терминальную, приобретая симптомы острого миелолейкоза. На этом этапе большое количество бластных клеток заполняют костный мозг, высокий их уровень присутствует в крови.
Иногда болезнь не отвечает на лечение. Тогда она минует ускоренную фазу и сразу переходит в финальную или фазу бластного криза.
Ремиссия
При ремиссии нормализуется состояние крови и костного мозга после проведенного лечения. Различают разные ее уровни.
Клиники Израиля могут обеспечить точную и быструю диагностику хронического миелолейкоза, подобрать наиболее подходящий вариант лечения, чтобы достичь наилучшего результата. Если вы нуждаетесь в помощи, обращайтесь к нам.
Хронический миелоидный лейкоз (ХМЛ)
Что такое хронический миелоидный лейкоз?
ХМЛ является хронической формой лейкоза. Это означает, что он медленно развивается в течение какого-то времени. Поэтому до появления симптомов могут пройти недели или месяцы. При острых формах лейкоза симптомы, напротив, развиваются стремительно, и ребенок быстро заболевает.
ХМЛ очень редко возникает у детей. Ежегодно в США и Канаде регистрируют только 110–120 случаев. Это составляет около 3% от случаев детского рака.
У каждого человека в норме имеется 23 пары хромосом. Они несут всю генетическую информацию (гены), составляющую человека. Мутация (ошибка) в генах может вызвать развитие заболевания, такого как рак.
Мутация, называемая филадельфийской хромосомой, образуется, когда часть хромосомы 9 и часть хромосомы 22 отрываются и меняются местами. Там, где к хромосоме 22 присоединяется фрагмент хромосомы 9,образуется ген bcr-abl.-ablgene is formed on chromosome 22 where the piece of chromosome 9 attaches. Он управляет синтезом фермента тирозинкиназы. Это приводит к тому, что слишком много кровеобразующих стволовых клеток превращаются в белые клетки крови ( гранулоциты или бласты ). Препараты, называемые ингибиторами тирозинкиназы (ИТК), предназначены для остановки действия фермента и являются первой линией терапии ХМЛ.
Филадельфийская хромосома не передается по наследству от родителя к ребенку. Мутация возникает случайно и спорадически.
Признаки и симптомы хронического миелоидного лейкоза
ХМЛ является хроническим заболеванием, т. е. развивается медленно, в отличие от острых лейкозов, при которых симптомы возникают быстро. Поначалу у детей с ХМЛ симптомы могут отсутствовать. Частые симптомы:
Диагностика хронического миелоидного лейкоза
Предположить диагноз ХМЛ позволяют результаты анализов крови и костного мозга. Дальнейшие анализы помогут подтвердить диагноз, определить генетическую основу заболевания и степень его распространения на другие части тела.
Исследования для диагностики ХМЛ:
Сначала врач проведет осмотр и изучит историю болезни пациента. В ходе медицинского осмотра врач проверяет общие показатели здоровья, в том числе наличие признаков заболевания — уплотнений или всего, что кажется необычным. Проводится тщательный осмотр глаз, ротовой полости, кожи и ушей. Может быть выполнено исследование состояния центральной нервной системы. При пальпации брюшной полости пациента врач проверяет, не увеличена ли в размере селезенка или печень.
Общий клинический анализ крови
Пациенту назначат анализ крови, называемый общим клиническим анализом крови. При этом берут образец крови и исследуют его характеристики:
При лейкозе в крови может содержаться слишком много лейкоцитов, большинство из которых будут бластами, ранними предшественниками клеток крови. У здоровых детей такие клетки обнаруживаются только в костном мозге.
Биохимический анализ крови
В образце крови измеряют количество определенных веществ, выделяемых в кровь органами и тканями организма. Отклонение от нормы (в большую или меньшую сторону) может быть признаком заболевания.
Подозрение на лейкоз может возникнуть после медицинского осмотра, изучения истории болезни и оценки результатов анализа крови.
Для подтверждения диагноза рака и точного определения типа рака проводят такие исследования, как пункция и биопсия костного мозга. Многим детям данную процедуру проводят во сне (под наркозом). Если пациент во время процедуры бодрствует, ему дают подходящий болеутоляющий препарат.
Пункция костного мозга: с помощью тонкой полой иглы врачи возьмут образец костного мозга из тазовой кости. Морфолог изучит костный мозг под микроскопом, чтобы обнаружить признаки рака.
Биопсия костного мозга: врачи извлекут небольшой фрагмент костной ткани для определения степени распространения рака в костном мозге. Обычно биопсия проводится непосредственно до или сразу после пункции.
Каким образом выполняют аспирацию/биопсию костного мозга?
Для диагностики лейкоза требуется проведение исследований костного мозга.
После подтверждения диагноза врачи проведут дополнительные анализы, чтобы точно определить вид лейкоза. Для этого применяются такие исследования:
Для диагностики определенных видов лейкоза используется иммунофенотипирование — сравнение опухолевых клеток с нормальными клетками иммунной системы.
Такими анализами являются иммуногистохимическое исследование и проточная цитометрия.
Цитогенетический анализ включает в себя лабораторные анализы, с помощью которых морфологи изучают определенные изменения в хромосомах.
Одним из таких исследований является FISH-анализ (флуоресцентная гибридизация in situ). В ходе этого анализа изучаются гены или хромосомы в клетках и тканях. Фрагменты ДНК, содержащие флуоресцентный краситель, изготавливают в лаборатории и добавляют в клетки или ткани на предметном стекле. Когда эти фрагменты ДНК прикрепляются к определенным генам или областям хромосом на предметном стекле, они становятся различимы.
Врач может порекомендовать провести лабораторные анализы, чтобы выявить специфические гены, белки и другие факторы, влияющие на развитиелейкоза.. Такое исследование важно, поскольку онкозаболевания вызваны ошибками (мутациями) в генах клетки. Выявление этих ошибок помогает точно определить подвид лейкоза. Уже исходя из этого врачи будут подбирать индивидуальный план лечения для каждого пациента. Если мутация связана с благоприятным прогнозом, ребенку назначают менее токсичное лечение. И наоборот, врачи могут назначать более интенсивное лечение пациентам слейкозомпри наличии мутаций, связанных с менее благоприятными исходами. Могут быть обнаружены мутации, для которых имеется таргетное лечение —воздействующееименно на эту мутацию.
Чтобы определить распространение опухоли, используют такие исследования:
Люмбальную пункцию выполняют для взятия образца спинномозговой жидкости из позвоночника с целью определитьстепень распространения ракана центральную нервную систему. Эта процедура также называется ЛП или поясничным проколом.
Иглу размещают между двумя позвонками, вводят в жидкость в области спинного мозга, и берут образец. При исследовании образца под микроскопом выявляют, есть ли признаки распространения злокачественных клеток в головной и спинной мозг. Организм постоянно вырабатывает спинномозговую жидкость и быстро восстановит небольшое количество, изъятое во время процедуры.
Рентгеновское излучение — это тип пучка энергии, который способен проходить сквозь тело и, попадая на пленку, создавать изображение областей внутри тела на экране компьютера или специальной пленке. Рентгенографию грудной клетки проводят для того, чтобы определить, есть ли новообразование в грудной клетке.
Лечение хронического миелоидного лейкоза
Лечение зависит от фазы заболевания. У ХМЛ бывает 3 фазы. Фаза зависит от количества лейкозных (бластных) клеток в крови и костном мозге.
Хроническая фаза: менее 10% бластных клеток.
Фаза акселерации: 10–19% бластных клеток.
Фаза бластного криза: 20% или более бластных клеток. Когда во время бластной фазы появляются усталость и жар, увеличивается в размере селезенка, это называется бластным кризом.
Таргетная терапия
Трансплантация гемопоэтических клеток
Другим вариантом лечения ХМЛ является аллогенная трансплантация гемопоэтических клеток (также называемая трансплантацией костного мозга или стволовых клеток). Трансплантация может привести к излечению ХМЛ, однако может вызывать серьезные побочные эффекты. При аллогенной трансплантации дети получают гемопоэтические клетки (клетки-предшественники клеток крови) от здорового донора. Для проведения трансплантации необходимо найти подходящего донора. До получения донорских клеток необходимо уничтожить собственные клетки крови в костном мозге пациента, для чего применяется химиотерапия и — в некоторых случаях — облучение. Во время трансплантации пациенту внутривенно вводятся здоровые донорские клетки. В случае успеха эти новые донорские клетки будут расти и замещать клетки пациента. В результате у пациента должны начать вырабатываться здоровые клетки крови.
Прогноз при лечении хронического миелоидного лейкоза
Цель современных исследований хронического миелоидного лейкоза
Ведутся исследования на тему: возможно ли вмешательство на ранних этапах курса лечения, уменьшающее эти осложнения?
Существующие методы лечения ХМЛ у детей основаны на опыте лечения взрослых. Тем не менее, в последние несколько лет, особенно с появлением ИТК, растет обеспокоенность тем, что детский хронический миелоидный лейкоз имеет много уникальных особенностей и их необходимо рассматривать и исследовать отдельно.
Эта концепция подтверждается наличием нескольких геномных различий между детьми и взрослыми пациентами, некоторые из которых связаны с ответом на терапию. Дальнейшее исследование этих открытий и оценка их влияния на течение заболевания имеют большое значение для ведения детей с ХМЛ. Например, обнаружение генетических изменений, на которые можно прицельно воздействовать таргетными препаратами параллельно с применением ИТК, что в настоящее время невозможно без трансплантации костного мозга.
Существующие прогностические шкалы, позволяющие предсказывать исход, не учитывают особенностей детей. Систематическое исследование большого числа детей с ХМЛ, получавших ИТК, может помочь получить информацию для улучшения лечения.
До сих пор неизвестно, почему у подгруппы детей с ХМЛ, получавших ИТК, развиваются побочные эффекты. Вероятно, эти ответы опосредуются генетическими факторами организма. Изучение возможных факторов организма, связанных с токсичностью ИТК, может способствовать выявлению подгруппы пациентов, которым может помочь альтернативное лечение, такое как трансплантация костного мозга.
Еще одной областью клинических испытаний является вмешательство, направленное на уменьшение длительных побочных эффектов, например применение гормона роста у детей с низким ростом, обусловленным приемом ИТК. Принимая во внимание ожидаемую долгую продолжительность жизни детей и относительно короткий период — около 15 лет, — в течение которого использовался ИТК, все еще существует неопределенность относительно потенциальных побочных эффектов у пациентов, подвергавшихся воздействию ИТК в течение длительного времени. Поэтому тщательное наблюдение этих детей представляет собой еще одну область исследований. Показания для трансплантации костного мозга являются областью исследований, в которых преимущества и токсичность трансплантата сравниваются с преимуществами контроля заболевания, а также острыми и отдаленными осложнениями, вызванными применением ИТК.
Наконец, приблизительно у 40% пациентов, которые оставались в молекулярной ремиссии в течение нескольких лет, прекращение приема ИТК было связано с безрецидивным состоянием. Областью исследования также являются попытки выявить пациентов, для которых можно безопасно прекратить применение ИТК.
—
Онлайн-ресурс Together не является рекламой каких-либо из фирменных продуктов, упомянутых в этой статье.