Ортофосфат магния
| Ортофосфат магния | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Фосфат магния |
| Традиционные названия | Фосфорнокислый магний |
| Химическая формула | Mg3(PO4)2 |
| Физические свойства | |
| Молярная масса | 262,855 г/моль |
| Термические свойства | |
| Температура плавления | 1357 °C |
| Классификация | |
| Рег. номер CAS | 7757-87-1 |
Ортофосфат магния — неорганическое соединение, соль магния и ортофосфорной кислоты с формулой Mg3(PO4)2. Бесцветные кристаллы. Образует несколько кристаллогидратов.
Содержание
Получение
Применение
Ссылки
Примечания
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Ортофосфат магния» в других словарях:
Ортофосфат аммония-магния — Общие Систематическое наименование Ортофосфат аммония магния Химическая формула NH4MgPO4 Физические свойства Состояние (ст. ус … Википедия
Ортофосфат стронция — Общие Химическая формула Sr3(PO4)2 Физические свойства Состояние (ст. усл.) бесцветные ромбоэдрические кристаллы Молярная масса 452.8 … Википедия
магния ортофосфат — magnio ortofosfatas statusas T sritis chemija formulė Mg₃(PO₄)₂ atitikmenys: angl. magnesium orthophosphate rus. магний ортофосфорнокислый; магния ортофосфат ryšiai: sinonimas – trimagnio bis(tetraoksofosfatas) … Chemijos terminų aiškinamasis žodynas
Гидроортофосфат магния — Гидроортофосфат магния … Википедия
Цитрат магния — Общие Системати … Википедия
Хлорид магния — Хлорид магния … Википедия
Карбонат магния — См. также: Магния карбонат (лекарственное средство) Карбонат магния … Википедия
Гидроксид магния — Гидроксид магния … Википедия
Сульфат магния — Общие Систематическое наименование Сульфат магния Традиционные названия Сернокислый магния, эпсомская соль Химическая формула MgSO4 Физические свойства Мол … Википедия
Бромид магния — Общие Систематическое наименование Бромид магния Традиционные названия Бромистый магний Химическая формула MgBr2 Физические свойства Состояние (ст. усл … Википедия
Структура, свойства и применение фосфата магния (Mg3 (PO4) 2)
фосфат магния это термин, используемый для обозначения семейства неорганических соединений, образованных магнием, щелочноземельным металлом и оксоанионфосфатом. Простейший фосфат магния имеет химическую формулу Mg3(РО4)2. Формула указывает, что для каждых двух анионов PO4 3- Есть три катиона Mg 2+ взаимодействуя с этими.
Также эти соединения могут быть описаны как соли магния, полученные из ортофосфорной кислоты (H3ПО4). Другими словами, магний «покрывает» фосфатные анионы независимо от их неорганического или органического представления (MgO, Mg (NO).3)2, MgCl2, Mg (OH)2, и т.д.).
В случае бобиерриты ее кристаллическая структура является моноклинной, с кристаллическими агрегатами с веерными формами и массивными розетками. Однако фосфаты магния характеризуются богатой структурной химией, что означает, что их ионы принимают множество кристаллических структур..
Формы фосфата магния и нейтральность его зарядов
В результате этих взаимодействий получается трехосновный фосфат магния: Mg3(РО4)2. Почему это трибаза? Потому что он способен принимать три эквивалента Н + чтобы сформировать H снова3ПО4:
Магний фосфаты с другими катионами
Компенсация отрицательных зарядов также может быть достигнута с участием других положительных видов.
Учитывая ситуацию, когда другой фосфат вмешивается и отрицательные заряды увеличиваются, другие дополнительные катионы могут быть добавлены к взаимодействиям, чтобы нейтрализовать их. Благодаря этому можно синтезировать многочисленные кристаллы фосфата магния (Na3RBMG7(РО4)6, например).
структура
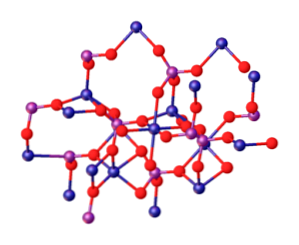
Верхнее изображение иллюстрирует взаимодействие между ионами Mg 2+ и ПО4 3- которые определяют кристаллическую структуру. Однако это только изображение, которое демонстрирует скорее тетраэдрическую геометрию фосфатов. Тогда кристаллическая структура включает тетраэдры фосфатов и сферы магния.
Для случая Mg3(РО4)2 Безводные ионы принимают ромбоэдрическую структуру, в которой Mg 2+ координируется с шестью атомами кислорода.
Выше показано на изображении ниже, с пометкой, что синие сферы являются кобальтом, достаточно заменить их на зеленые сферы магния:
Прямо в центре структуры может быть расположен октаэдр, образованный шестью красными сферами вокруг синеватой сферы..
Кроме того, эти кристаллические структуры способны принимать молекулы воды, образуя гидраты фосфата магния..
Это потому, что они образуют водородные связи с фосфат-ионами (HOH-O-PO3 3- ). Кроме того, каждый фосфат-ион способен принимать до четырех водородных связей; то есть четыре молекулы воды.
свойства
Это белое твердое вещество, образующее кристаллические ромбические пластины. Кроме того, он не имеет запаха и вкуса.
То есть, когда ионы поливалентны и их ионные радиусы не сильно различаются по размеру, твердое вещество проявляет устойчивость к его растворению.
приложений
Он был использован в качестве слабительного для запоров и желудочной кислотности. Однако его вредные побочные эффекты, проявляющиеся в виде диареи и рвоты, ограничивают его применение. Кроме того, это может привести к повреждению желудочно-кишечного тракта.
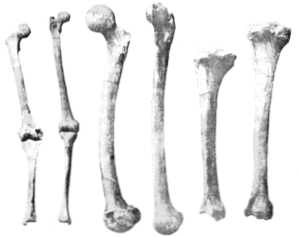
Использование фосфата магния для восстановления костной ткани в настоящее время изучается, изучая применение Mg (H)2ПО4)2 как цемент.
Эта форма фосфата магния отвечает следующим требованиям: она является биоразлагаемой и гистосовместимой. Кроме того, его использование в регенерации костной ткани рекомендуется для его силы и быстрого урегулирования.
Оценивается использование аморфного фосфата магния (AMP) в качестве биоразлагаемого и не экзотермического ортопедического цемента. Для получения этого цемента смешайте порошок AMP с поливиниловым спиртом, чтобы образовалась замазка..
Основная функция фосфата магния заключается в обеспечении вклада Mg в живые существа. Этот элемент вмешивается в многочисленные ферментативные реакции в качестве катализатора или посредника, являясь необходимым для жизни.
Дефицит Mg у людей связан со следующими эффектами: снижение уровня Ca, сердечная недостаточность, задержка Na, снижение уровней K, аритмия, длительные сокращения мышц, рвота, тошнота, низкий уровень циркулирующего вещества. Гормон паращитовидной железы и желудка и менструальные судороги, среди других.
Формула фосфата магния
Определение и формула фосфата магния
В обычных условиях представляет собой мелкие кристаллы белого цвета. Практически не растворяется в воде. Образует кристаллогидраты различного состава. Температура плавления 1357 o C.
Рис. 1. Фосфат магния. Внешний вид.
Химическая формула фосфата магния
Химическая формула фосфата магния Mg3(PO4)2. Она показывает, что в состав данной молекулы входят три атома магния (Ar = 24 а.е.м.), два атома фосфора (Ar = 31 а.е.м.) и восемь атомов кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу фосфата магния:
Mr(Mg3(PO4)2) = 3×24 + 2×31 + 8×16 = 72 + 62 + 128 = 262.
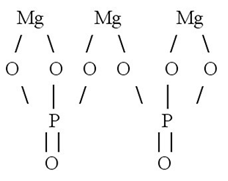
Графическая (структурная) формула фосфата магния
Структурная (графическая) формула фосфата магния является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
Ионная формула
Фосфат магния представляет собой электролит, который диссоциирует на ионы в водном растворе согласно следующему уравнению реакции:
Примеры решения задач
| Задание | В состав вещества входят 30,7% калия, 25,2% серы, 44% кислорода. Вывести формулу этого соединения. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим число атомов калия в молекуле через «х», число атомов серы через «у» и число атомов кислорода через «z».
Найдем соответствующие относительные атомные массы элементов калия, серы и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Ar(K) = 39; Ar(S) = 32; Ar(O) = 16.
Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения:
x:y:z = ω(K)/Ar(K) : ω(S)/Ar(S) : ω(O)/Ar(O);
x:y:z= 30,7/39 : 25,2/32 : 44/16;
x:y:z= 0,787 : 0,787 : 2,75.
Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 0,787):
0,787/0,787 : 0,787/0,787 : 2,75/0,787;
Следовательно, простейшая формула соединения калия, серы и кислорода имеет вид K2S2O7.
| Задание | Установите массовую формулу вещества, содержащего 40,0% кальция, 12,0% углерода и 48,0% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим количество моль элементов, входящих в состав соединения за «х» (кальций), «у» (углерод) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
x:y:z = ω(Ca)/Ar(Ca) : ω(C)/Ar(C) : ω(O)/Ar(O);
x:y:z= 40,0/40 : 12,0/12 : 48,0/16;
Значит формула соединения кальция, углерода и кислорода будет иметь вид CaCO3. Это карбонат кальция.
Конвертер величин
фосфат магния: состав и молярная масса
Молярная масса Mg3(PO4)2, фосфат магния 262.857724 г/моль
Массовые доли элементов в соединении
| Элемент | Символ | Атомная масса | Число атомов | Массовая доля |
|---|---|---|---|---|
| Magnesium | Mg | 24.305 | 3 | 27.740% |
| Phosphorus | P | 30.973762 | 2 | 23.567% |
| Oxygenium | O | 15.9994 | 8 | 48.694% |
Использование калькулятора молярной массы
Линейная плотность заряда
Калькулятор молярной массы
Все вещества состоят из атомов и молекул. В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль является единицей количества вещества в СИ. Один моль содержит точно 6,02214076×10²³ элементарных частиц. Это значение численно равно константе Авогадро NA, если выражено в единицах моль⁻¹ и называется числом Авогадро. Количество вещества (символ n) системы является мерой количества структурных элементов. Структурным элементом может быть атом, молекула, ион, электрон или любая частица или группа частиц.
Постоянная Авогадро NA = 6.02214076×10²³ моль⁻¹. Число Авогадро — 6.02214076×10²³.
Другими словами моль — это количество вещества, равное по массе сумме атомных масс атомов и молекул вещества, умноженное на число Авогадро. Единица количества вещества моль является одной из семи основных единиц системы СИ и обозначается моль. Поскольку название единицы и ее условное обозначение совпадают, следует отметить, что условное обозначение не склоняется, в отличие от названия единицы, которую можно склонять по обычным правилам русского языка. Один моль чистого углерода-12 равен точно 12 г.
Молярная масса
Молярная масса — физическое свойство вещества, определяемое как отношение массы этого вещества к количеству вещества в молях. Говоря иначе, это масса одного моля вещества. В системе СИ единицей молярной массы является килограмм/моль (кг/моль). Однако химики привыкли пользоваться более удобной единицей г/моль.
молярная масса = г/моль
Молярная масса элементов и соединений
Соединения — вещества, состоящие из различных атомов, которые химически связаны друг с другом. Например, приведенные ниже вещества, которые можно найти на кухне у любой хозяйки, являются химическими соединениями:
Молярная масса химических элементов в граммах на моль численно совпадает с массой атомов элемента, выраженных в атомных единицах массы (или дальтонах). Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении. Например, молярная масса воды (H₂O) приблизительно равна 1 × 2 + 16 = 18 г/моль.
Молекулярная масса
Молекулярная масса (старое название — молекулярный вес) — это масса молекулы, рассчитанная как сумма масс каждого атома, входящего в состав молекулы, умноженных на количество атомов в этой молекуле. Молекулярная масса представляет собой безразмерную физическую величину, численно равную молярной массе. То есть, молекулярная масса отличается от молярной массы размерностью. Несмотря на то, что молекулярная масса является безразмерной величиной, она все же имеет величину, называемую атомной единицей массы (а.е.м.) или дальтоном (Да), и приблизительно равную массе одного протона или нейтрона. Атомная единица массы также численно равна 1 г/моль.
Расчет молярной массы
Молярную массу рассчитывают так:
Например, рассчитаем молярную массу уксусной кислоты
Наш калькулятор выполняет именно такой расчет. Можно ввести в него формулу уксусной кислоты и проверить что получится.
Вас могут заинтересовать и другие конвертеры из группы «Другие конвертеры»:
Вы затрудняетесь в переводе единицы измерения с одного языка на другой? Коллеги готовы вам помочь. Опубликуйте вопрос в TCTerms и в течение нескольких минут вы получите ответ.
Другие конвертеры
Вычисление молярной массы
Молярная масса — физическое свойство вещества, определяемое как отношение массы этого вещества к количеству вещества в молях, то есть, это масса одного моля вещества.
Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении.
Использование конвертера «Вычисление молярной массы»
На этих страницах размещены конвертеры единиц измерения, позволяющие быстро и точно перевести значения из одних единиц в другие, а также из одной системы единиц в другую. Конвертеры пригодятся инженерам, переводчикам и всем, кто работает с разными единицами измерения.
Пользуйтесь конвертером для преобразования нескольких сотен единиц в 76 категориях или несколько тысяч пар единиц, включая метрические, британские и американские единицы. Вы сможете перевести единицы измерения длины, площади, объема, ускорения, силы, массы, потока, плотности, удельного объема, мощности, давления, напряжения, температуры, времени, момента, скорости, вязкости, электромагнитные и другие.
Примечание. В связи с ограниченной точностью преобразования возможны ошибки округления. В этом конвертере целые числа считаются точными до 15 знаков, а максимальное количество цифр после десятичной запятой или точки равно 10.
Мы работаем над обеспечением точности конвертеров и калькуляторов TranslatorsCafe.com, однако мы не можем гарантировать, что они не содержат ошибок и неточностей. Вся информация предоставляется «как есть», без каких-либо гарантий. Условия.
Если вы заметили неточность в расчётах или ошибку в тексте, или вам необходим другой конвертер для перевода из одной единицы измерения в другую, которого нет на нашем сайте — напишите нам!
Фосфат магния (Mg3 (PO4) 2): структура, свойства
Содержание:
В фосфат магния представляет собой термин, который используется для обозначения семейства неорганических соединений, образованных магнием, щелочноземельным металлом и оксоанионфосфатом. Простейший фосфат магния имеет химическую формулу Mg.3(PO4)2. Формула показывает, что на каждые два аниона PO4 3– есть три катиона Mg 2+ взаимодействуя с ними.
Точно так же эти соединения могут быть описаны как соли магния, полученные из ортофосфорной кислоты (H3PO4). Другими словами, магний «объединяется» между фосфатными анионами, независимо от их неорганического или органического происхождения (MgO, Mg (NO3)2, MgCl2, Mg (OH)2, так далее.).
В случае бобьеррита его кристаллическая структура моноклинная, с агрегатами кристаллов в форме вееров и массивных розеток. Однако фосфаты магния характеризуются богатой структурной химией, а это означает, что их ионы принимают множество кристаллических структур.
Формы фосфата магния и нейтральность его зарядов
В результате этих взаимодействий образуется трехосновный фосфат магния: Mg3(PO4)2. Почему трехосновный? Поскольку он способен принимать три эквивалента H + чтобы снова сформировать H3PO4:
Фосфаты магния с другими катионами
Компенсация отрицательных зарядов также может быть достигнута с участием других положительных видов.
Учитывая ситуацию, когда вмешивается другой фосфат и увеличиваются отрицательные заряды, другие дополнительные катионы могут присоединиться к взаимодействиям, чтобы нейтрализовать их. Благодаря этому можно синтезировать многочисленные кристаллы фосфата магния (Na3RbMg7(PO4)6, например).
Состав
Изображение выше иллюстрирует взаимодействие между ионами Mg. 2+ и ПО4 3– которые определяют кристаллическую структуру. Однако это только изображение, которое скорее демонстрирует тетраэдрическую геометрию фосфатов. Итак, в кристаллическую структуру входят фосфатные тетраэдры и магниевые сферы.
В случае Mg3(PO4)2 безводные ионы принимают ромбоэдрическую структуру, в которой Mg 2+ он координирован с шестью атомами O.
Сказанное выше проиллюстрировано на изображении ниже, с обозначением, что синие сферы являются кобальтовыми, достаточно заменить их зелеными магниевыми сферами:
Прямо в центре структуры может быть расположен октаэдр, образованный шестью красными сферами вокруг голубоватой сферы.
Точно так же эти кристаллические структуры способны принимать молекулы воды, образуя гидраты фосфата магния.
Это потому, что они образуют водородные связи с фосфат-ионами (HOH-O-PO3 3– ). Кроме того, каждый фосфатный ион способен принимать до четырех водородных связей; то есть четыре молекулы воды.
Свойства
Это белое твердое вещество, образующее кристаллические ромбические пластинки. Он также не имеет запаха и вкуса.
То есть, когда ионы поливалентны и их ионные радиусы не сильно различаются по размеру, твердое вещество проявляет сопротивление растворению.
Он плавится при 1184 ºC, что также свидетельствует о сильных электростатических взаимодействиях. Эти свойства варьируются в зависимости от того, сколько молекул воды он поглощает, и от того, находится ли фосфат в некоторых из своих протонированных форм (HPO4 2– или H2PO4 – ).
Приложения
Он использовался как слабительное при запорах и изжоге. Однако его вредные побочные эффекты, проявляющиеся в виде диареи и рвоты, ограничивают его применение. Кроме того, это может вызвать повреждение желудочно-кишечного тракта.
В настоящее время изучается использование фосфата магния для восстановления костной ткани, исследуется применение Mg (H2PO4)2 как цемент.
Эта форма фосфата магния отвечает требованиям: она биоразлагаема и гистосовместима. Кроме того, его рекомендуется использовать для регенерации костной ткани из-за его стойкости и быстрого схватывания.
Оценивается возможность использования аморфного фосфата магния (AMP) в качестве биоразлагаемого неэкзотермического ортопедического цемента. Для создания этого цемента порошок AMP смешивают с поливиниловым спиртом для образования замазки.
Основная функция фосфата магния состоит в том, чтобы служить источником Mg для живых существ. Этот элемент участвует в многочисленных ферментативных реакциях в качестве катализатора или промежуточного продукта, необходимого для жизни.
Дефицит Mg у людей связан со следующими эффектами: снижение уровня кальция, сердечная недостаточность, задержка натрия, снижение уровня калия, аритмии, устойчивые мышечные сокращения, рвота, тошнота, низкий уровень циркулирующего азота. гормон паращитовидной железы, желудочные и менструальные спазмы, среди прочего.
Ссылки
Наука и кино: есть ли в кино настоящая наука?