Мутация гена АВСВ1 (MDR1) у колли и родственных пород (MDR1 – ген множественной лекарственной резистентности)
Продукт гена MDR1 – Р – гликопротеин – компонент гемато – энцефалического барьера.
Главная функция ГЭБ — поддержание гомеостаза мозга. Он защищает нервную ткань от циркулирующих в крови микроорганизмов, токсинов, клеточных и гуморальных факторов иммунной системы, которые воспринимают ткань мозга как чужеродную. ГЭБ выполняет функцию высокоселективного фильтра.
При его повреждениях в мозг собаки могут проникать и не удаляться различные вещества.
В этом случае некоторые медикаментозные препараты могут представлять особую опасность.
Помимо влияния на проникновение препаратов в мозг, Р – гликопротеин функционирует в ЖКТ, печени и почках собаки. Эти органы, в норме, участвуют в распаде и выведении медикаментов. Поэтому у собак с MDR1 – недостаточностью изменяются фармакокинетические свойства ряда лекарственных препаратов, что приводит к повышению их биодоступности и/или снижению выведения веществ печенью, почками, кишечником.
Таким образом у собак с MDR1- недостаточностью увеличивается концентрации препаратов в плазме и может произойти неблагоприятная реакция на препарат.
Так как заболевание имеет генетическую природу, для определения собак с MDR1- недостаточностью, а также генетического носительства, был разработан ДНК тест. Он позволяет отличить здоровую собаку от собак являющихся носителями и от собак с повышенной чувствительностью в медикаментам.
Знание результатов теста позволит избежать высокой степени риска проявления побочных эффектов при использовании лекарственных препаратов.
Вещества, которые могут иметь пагубное воздействие на собак, имеющих мутацию MDR:
При применении указанных препаратов у собак с мутацией MDR1, возникают различные неврологические симптомы: тремор, атаксия, повышенное слюноотделение, слепота, кома, возможен летальный исход.
Чувствительность к медикаментам колли, шелти и некоторых других пород собак.
Для животных с мутантным геном MDR1 существует ряд опасных препаратов. При их введении в организм восприимчивой собаки могут появиться незапланированные реакции, связанные с проницаемостью гематоэнцефалического барьера. Это выражается неврологическими симптомами, такими как тремор, повышенное слюноотделение, судороги, слепота, кома. У таких животных биодоступность препаратов выше, чем у немутантных особей. То есть для этих собак стандартная доза оказывается токсической.
Данная мутация выделяется у многих пород собак, но наиболее часто (до 70% особей) встречается у длинношерстных и короткошерстных колли, длинношерстных уиппетов, австралийских овчарок, шелти, в меньшей степени – у бобтейлов, бордер-колли, бородатых колли, больших швейцарских овчарок, метисов этих пород. Ген MDR1 является рецессивным. На основании этого выделяют 3 группы животных.
Гомозиготные особи по нормальному гену +/+
Животные из этой группы не проявляют никакой реакции на медикаменты при правильном дозировании, не передают потомству мутацию по гену MDR1
Гетерозиготные особи по гену MDR1 +/-
Собаки из этой группы являются носителями мутации и могут передавать ее потомству. В большинстве случаев не проявляют нежелательной реакции на препараты при применении дозировок, не превышающих нормальные. Могут проявлять реакцию на введение таких препаратов как лоперамид, ацепромазин, эритромицин, ивермектин (в дозах >6мкг/кг).
Такие собаки дают нежелательную реакцию на медикаментозные препараты в нормальных дозах. Передают мутацию потомству
Препараты, опасные для собак с геном MDR1:
• Ацепромазин (препарат для премедикации, транквилизатор). Возможные названия: ветранквил. При введении препарата наступает более глубокая и длительная седация. Для гомозиготных по мутантному гену собак рекомендовано снизить дозу препарата на 30-50%, для гетерозиготных особей – на 25%.
• Буторфанол (анальгетик, препарат для премедикации). Подобно ацепромазину, буторфанол как правило, вызывают более глубокую и длительную седацию у собак с геном MDR1. Рекомендовано снизить дозу на 25% для собак гетерозиготных по мутации MDR1 и на 30-50% у собак, гомозиготных по мутации MDR1.
• Эритромицин. Может вызвать неврологические симптомы у собак с мутацией MDR1.
• Ивермектин (противопаразитарное средство). Нетоксичен в дозах, применяемых для профилактики дирофиляриоза. В дозах > 6 мкг/кг, используемых при лечении кожно-паразитарных заболеваний, приводит к неврологическим реакциям у гомозиготных по гену MDR1 гетерозиготных особей.
• Лоперамид (противодиарейный препарат). Возможные названия: имодиум, диара, диарол, лоперакал, суперилоп, энтеробене. Токсичен для животных гомозиготных по гену MDR1 и гетерозиготных особей.
• Мильбемицин (антигельминтик). Возможные названия: мильбемакс. Нетоксичен в профилактических дозах. Превышение дозы может привести к неврологическим нарушениям.
• Винкристин, винбластин, доксорубицин (химиотерапевтические препараты). Исследования показали, что собаки с мутацией MDR1 более чувствительны к этим препаратам.
Внешне носительство гена MDR1 никак не проявляется вплоть до введения указанных препаратов. Это не болезнь, собака, при соблюдении рекомендаций для своей генетической группы, проживет долгую и счастливую жизнь. Однако провести исследование на определение наличия мутантного гена все же стоит. Зная к какой группе относится ваша собака, вы сможете уберечь ее от неоправданных рисков по применению опасных для нее препаратов.
Mdr1 у собак что это
ГБУ РО «ОКБ им. Н.А. Семашко»
1 пульмонологическое отделение
Заведующая отделением, к.м.н. Алмазова Е.В.
Перхоть собаки – одна из наиболее распространенных причин респираторной аллергии. Она содержит несколько аллергенных компонентов1, которые обнаруживаются не только в домах владельцев животных, но и в общественных местах, школах и помещениях, где не содержатся собаки (вторичная экспозиция). Точно определить причинно-значимый аллерген может быть сложной задачей, так как и кожные аллергологические пробы, и тесты на определение аллерген-специфических иммуноглобулинов Е (sIgE) в сыворотке крови в ряде случаев дают ложноположительные результаты.
Наиболее известны такие аллергенные компоненты собаки, как липокалины Can f1 и Can f2и сывороточный альбумин Can f3, присутствующие в шерсти и перхоти животных. Кроме того, описан еще один мажорный аллерген – простатический калликреин Can f5, не имеющий перекрестной реактивности с Can f1, f2 и f32. Этот андроген-зависимый белок экспрессируется в ткани предстательной железы и присутствует только у кобелей3, преимущественно в моче, а также в шерсти и перхоти2. SIgE к Can f5 выявляются у 70% пациентов с аллергией на собак, причем примерно в трети случаев отмечается сенсибилизация только к этому аллергенному компоненту. Это позволяет предположить существование изолированных аллергических реакций на животных мужского пола. Стандартные экстракты аллергенов, используемые в диагностических целях, содержат смесь аллергенов, полученных от животных разного пола и породы, поэтому единственную возможность установить моносенсибилизацию к Can f5 предоставляет компонентная аллергодиагностика.
Датские пульмонологи впервые описали случай клинической аллергии на собак, возникающей исключительно после контакта с мужскими особями, при котором подтвердилась изолированная сенсибилизация к Can f5.
У 54-летней женщины в течение длительного времени после контакта с собаками возникали симптомы бронхиальной астмы (свистящее и затрудненное дыхание). Пациентка отмечала развитие симптоматики только при контакте с самцами этих животных, и хотела узнать, можно ли завести дома самку.
Помимо реакции на собак, у женщины развивались симптомы астмы и аллергического риноконъюнктивита при контакте с пыльцой березы и злаков. Она использовала ингаляционные бетта2-адреномиметики (тербуталин) по требованию и пероральные Н1-антигистаминные средства (фексофенадин) в сезон цветения растений и перед ожидаемым контактом с собаками. Пациентка недавно завершила курс подкожной аллерген-специфической иммунотерапии для лечения пыльцевой аллергии и отмечала положительный эффект.
Пациентке были выполнены стандартные диагностические исследования: кожный прик-тест, определение общего уровня IgE и уровня sIgE к аллергенам тимофеевки, пыльцы березы, клещей домашней пыли, перхоти собаки и кошки. При этом использовались стандартные образцы аллергенов собак, полученные от животных разного пола и породы. Также врачи по отдельности определили уровень sIgE к аллергенным компонентам Can f1, 2, 3 и 5. Данные исследования in vitro приведены в Табл.1.
Табл. 1. Уровни общего IgE и sIgE к отдельным аллергенам в сыворотке крови пациентки. Адаптировано из: Schoos A.M//J Allergy Clin Immunol Pract; 2017; May 9
Аллерген
Уровень, кЕ/л
Референсные значения, кЕ/л
Частые Вопросы о MDR1
 Частые Вопросы о MDR1
Частые Вопросы о MDR1

Австралийские овчарки, как и некоторые другие, в основном породы типа колли, могут быть носителями генетической мутации, которая делает их чувствительными к определенным лекарственным препаратам. Использование этих препаратов может стать причиной серьезной неврологической болезни или смерти.
К счастью, существует крайне точный тест ДНК, который поможет узнать, есть ли у вашей собаки эта мутация. Все, что вам надо сделать это сдать мазок с щеки. Для этого даже нет необходимости идти к ветеринару.
Какие лекарства вызывают реакции?
Ивермектин был первым известным лекарством, вызывающим реакцию, но он далеко не один. Ивермектин при малых дозировках, как обнаружено в препаратах от сердечного червя, не вызовет реакцию. Большие дозировки, необходимые для борьбы с червями, вызовут. Другие часто применяемые препараты включают ацепромазин и Имодиум. К счастью, существуют альтернативные доступные препараты, если вашей собаке требуется лечение.
На этом сайте предлагается жетон «медицинской тревоги» на ошейник для собак с MDR1, и еще там есть более обширный список, включающий альтернативные и родственные названия лекарств:
http://www.busteralert.com
Собаки, не носители мутации MDR1, могут смело принимать перечисленные лекарства.
Какие породы подвержены MDR1?
Австралийские овчарки
Коли (гладкие и д/ш)
Английские овчарки
McNabbs
Миниатюрные австралийские овчарки
Староанглийские овчарки
Немецкие овчарки
Длинношерстные Уиппеты
Шетландские овчарки
Silken Windhounds
Метисы, за которыми стоит любая из перечисленных пород.

 Re: Частые Вопросы о MDR1
Re: Частые Вопросы о MDR1

Насколько мутация MDR1 распространена у аусси?
32% аусси и 49% мини-аусси имеют хотя бы одну копию гена.
Как узнать, есть ли у моей собаки мутация MDR1?
Если ваша собака уже отреагировала на один из этих медикаментов, у нее есть мутация. Однако, реакции могут быть настолько опасными для вашей собаки, что лучше ей сдать анализ и узнать ее чувствительность до того, как она примет один из перечисленных медикаментов.
Что означают результаты тестов на MDR1?
Это тест на мутацию ДНК. Он определяет, имеет ли собака мутацию MDR1 или нет, и, если она имеет, то одну копию или две. Результат теста покажет вам генотип вашей собаки, обычно обозначаемый Нормальный/Нормальный, Нормальный/Мутант или Мутант/Мутант.
Собаки, у которых есть хотя бы одна копия гена мутанта должны рассматриваться как чувствительные к перечисленным лекарствам. Если ваша собака носитель мутации, предоставляйте копию результатов теста и список перечисленных лекарств каждому ветеринару, который лечит вашу собаку, и скажите ему, что к вашей собаке нельзя применять эти медикаменты.
Каких собак надо проверять и как часто?
Так как это тест ДНК, собаку надо проверить всего один раз. Из-за высокой частоты мутации в породе и разнообразия лекарств, на которые собака с мутацией может среагировать, все собаки, включая подобранных от неизвестных родителей и метисов аусси должны проходить обследование. Их жизни могут зависеть от этого.
Единственное исключение таково: если оба родителя собаки имеют результаты теста Нормальный/Нормальный, они не могут передать ген и их потомство не нужно проверять. Но, если собаку Нормальный/Нормальный повязать с собакой с неизвестным статусом или у которой есть хотя бы одна копия мутации, потомков надо проверить.
Как сделать тест?
(*опущу информацию для американцев и австралийцев)
В Англии тест доступен в Laboklin.
В Европе тест можно сделать в Genetic Counseling Services в Нидерландах:
www.gencouns.nl/engmdr1.html

 Re: Частые Вопросы о MDR1
Re: Частые Вопросы о MDR1

Что значит наличие MDR1 у собаки для моей программы разведения?
Вы можете вязать собак, несущих мутацию MDR1, даже если у них присутствуют две копии. Собаки с MDR1 реагируют на определенные лекарства. До того, как эти лекарства были введены в ветеринарную практику, никто не знал о существовании этой мутации, хотя она была по меньшей мере около полутора веков. Лекарства из списка MDR1, хоть они и ценные для ветеринарии, не являются природными и просто избежать их использования, если вы знаете статус MDR1 вашей собаки.
Заводчикам следует относиться к мутации, как к недостатку, но не как к дисквалифицирующему. Собак с мутацией лучше всего вязать с теми, у кого результат Нормальный/Нормальный. Если постоянно следовать такой практике, то частота мутации со временем снизится, и риск того, что не тестированная собака умрет из-за реакции, станет намного ниже.
Проверяйте своих племенных собак по рекомендациям, данным выше. Вы можете рассмотреть вариант проверки всех щенков, у которых хотя бы один родитель с мутацией. По крайней мере, приложите к документам щенка копии результатов родителей, когда его будут покупать, и рекомендуйте тем, чьи щенки могли унаследовать мутацию, проверить своих собак. Покупателей щенков необходимо проинструктировать, чтобы они предъявляли копии родительских результатов своим ветеринарам, чтобы их щенка лечили соответственно, учитывая медикаменты из списка. Если щенка приобрели для разведения, дайте новому владельцу знать, что проверка на MDR1 должна считаться необходимой наравне с проверкой бедер и глаз, и это необходимо сделать до того, как вязать собаку.
Со временем и увеличением числа проверенных собак вы сможете определять, надо ли проверять какую-либо конкретную собаку, проверив ее родословную и известные результаты тестов. Если по каждой линии вы найдете предков Нормальный/Нормальный, в тесте нет необходимости. Но если хотя бы по одной линии нет информации, или есть собака хотя бы с одной копией мутации, собаку стоит проверить.
Тест MDR1 недавно был добавлен как необязательное требование в Центре Информации Здоровья Собак (Canine Health Information Center (CHIC)) для аусси. На сайте OFA вы можете найти информацию о том, как подать ваши результаты теста. Собаки от двух родителей с результатами Нормальный/Нормальный, зарегистрированных в OFA, могут получить сертификат с отметкой СВР (чистый по происхождению) без самого тестирования этих собак.

 Re: Частые Вопросы о MDR1
Re: Частые Вопросы о MDR1

Вызывает ли мутация MDR1 эпилепсию?
Реакции на лекарства MDR1 не являются формой эпилепсии, и ни коим образом не связаны с эпилепсией, которая вызывается другими и еще не определенными генами. Мутация MDR1 – одна из многих вещей, которые вызывают не эпилептические припадки. Реакция на лекарство очень отличается от первичной эпилепсии. У собаки будет припадок, только если химические вещества накопятся в ее мозге. Лечение другое, прогноз другой, и сами припадки выглядят по-другому. Припадки, связанные с MDR1 возникают, только если восприимчивой собаке дали одно из перечисленных лекарств. Когда лекарства окончательно вымоются из организма собаки, припадки прекратятся. Если собака не принимала этих лекарств, у нее не будет припадков из-за гена MDR1.
Поскольку частота MDR1 настолько высока у аусси и мини аусси, возможно, что у собаки с эпилепсией тоже есть мутация MDR1. У такой собаки будет две болезни, а не одна. Может быть, что если собака с эпилепсией пережила припадок, вызванный MDR1, он может спровоцировать последующие эпилептические припадки. Припадки MDR1 всегда будут управляться одним из перечисленных лекарств. Припадки у собак с эпилепсией никак не связаны с тем, принимала или нет собака эти лекарства, только если у собаки одновременно и эпилепсия, и MDR1.
Библиотека
Опухолевые супрессоры и мутаторные гены
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
3.3.1. Типы опухолей, ассоциированные с аномалиями р53
Герминальные (произошедшие в половой клетке и передающиеся по наследству) мутации в одном из аллелей гена р53 вызывают синдром Ли-Фраумени, заключающийся во врожденном предрасположении к развитию различных новообразований, в первую очередь сарком, рака молочной железы, лимфолейкозов. Нередко синдром Ли-Фраумени характеризуется возникновением первично-множественных опухолей. Примечательно, что у трансгенных мышей, несущих инактивирующие мутации в гене р53, наблюдается картина, очень напоминающая синдром Ли-Фраумени. Примерно у трети животных, у которых инактивирован один из двух аллелей р53, в течение 6-9 месяцев после рождения возникают новообразования, причем их спектр очень сходен с наблюдаемым при синдроме Ли-Фраумени. При этом в части этих опухолей, как и новообразований у пациентов с синдромом Ли-Фраумени, сохраняется экспрессия неповрежденного аллеля гена р53. При врожденной инактивации во всех клетках организма обоих аллелей гена р53 опухоли развиваются практически у всех животных. Примерно такая же картина наблюдается у трансгенных мышей, несущих дополнительный экзогенный аллель р53, кодирующий белок с миссенс-мутацией.
3.3.2. Структурная организация и биохимические активности белка р53
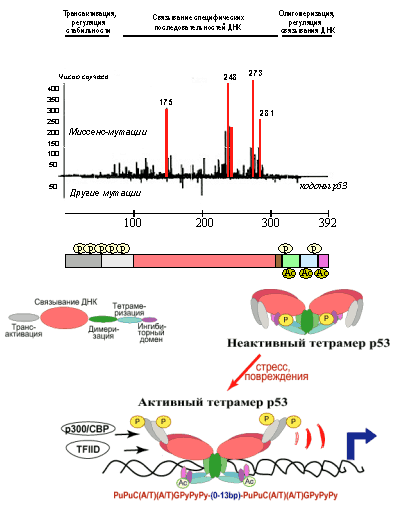
Продукт гена р53 имеет мол. массу 53кДа и состоит из 392 аминокислотных остатков. Он образует тетрамерный комплекс, способный регулировать транскрипцию ряда генов, имеющих в своем составе специфические последовательности ДНК, так называемые р53-респонсивные элементы. В молекуле р53 картировано несколько функционально-значимых доменов, играющих важную роль в осуществлении или регуляции его активности (Рис. 2).
N-концевой участок (аминокислоты 1-42) представляет собой домен, ответственный за транскрипционную активацию генов-мишеней. Он обладает способностью связываться с компонентами базальных факторов транскрипции, в частности с субъединицами hTAFII31, hTAF70 комплекса TFIID РНК-полимеразы II, а также с транскрипционным кофактором p300/CBP. Кроме того, этот домен участвует в белок-белковых взаимодействиях, регулирующих стабильность молекулы р53. И, наконец, в нем расположено несколько остатков серина и треонина, фосфорилирование которых регулирует активность р53.
Рис. 2. Схематическое изображение функциональных доменов р53, предполагаемой модели приобретения белком транскрипционно активной конформации и частоты встречаемости в новообразованиях человека мутаций в разных участках молекулы р53.
Далее идут участки ответственные за ядерную локализацию (аминокислоты 305-323) и димеризацию/тетрамеризацию молекул р53 (аминокислоты 323-356). С-концевой участок р53 (аминокислоты 363-392) представляет собой так называемый ингибиторный домен. В немодифицированном состоянии он препятствует посадке ДНК-связывающего домена на специфическую последовательность регулируемого гена. Фосфорилирование и ацетилирование его определенных сайтов вызывают изменения конформации белковой молекулы и переход тетрамеров р53 из неактивного (латентного) состояния в активное. В результате ДНК-связывающие домены освобождаются от блокирующего влияния ингибиторных доменов и приобретают способность садиться на р53-респонсивные элементы. Таким образом, к респонсивным генам привлекаются базовые факторы транскрипции, связывающиеся с N-концевым участком р53, и стимулируется синтез РНК генов-мишеней.
Помимо повышения транскрипции генов, содержащих специфические респонсивные элементы, белок р53 обладает также и рядом других активностей. В частности, он способен подавлять транскрипцию многих других генов, например протоонкогенов BCL2, JUN и FOS, гена фибронектина и т.д. В основе такой транс-репрессии лежит несколько механизмов: связывание и секвестрация активированным р53 ряда базовых факторов транскрипции (p300/CBP, TBP, CBF); способность связывать и рекрутировать к определенным генам гистоновые деацетилазы (HDAC), ремоделирующие хроматин; и т.д. Кроме того, р53 связывается с белками, вовлеченными в репликацию или репарацию ДНК и, как следствие, модулирует эти процессы. Так, взаимодействуя с белком RP-A, он ингибирует его способность активировать ДНК-полимеразы a и d, результатом чего является подавление репликации ДНК. Связывая компоненты комплекса TFIIH (ERCC2, ERCC3 и др.), р53 активирует его функцию и стимулирует тем самым эксцизионную репарацию ДНК. Связывание р53 с белком Rad51 ведет к стимуляции рекомбинаций ДНК и повышению эффективности репарацию двунитевых разрывов ДНК. На участие р53 в репарации ДНК указывает также и его способность проявлять активность 3′-5′-экзонуклеазы и узнавать участки одноцепочечной ДНК и/или неспаренные основания.
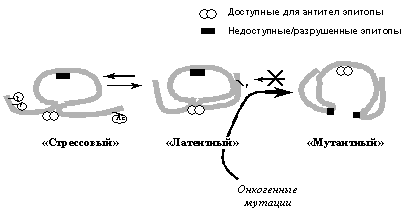
Рис. 3. Схематическое изображение различных конформационных состояний р53, распознаваемых специфическими антителами. Онкогенные мутации вызывают необратимый переход молекулы в денатурированное состояние, при котором открывается ранее недоступный эпитоп и, наоборот, исчезают некоторые ранее доступные эпитопы.
Характерные для опухолевых клеток миссенс-мутации приводят к резкому изменению конформации молекулы белка р53 (Рис. 3), что в значительной степени затрагивает все из вышеуказанных его активностей: происходит потеря или ослабление способности связывать и активировать гены с р53-респонсивными элементами, репрессировать другие специфические гены-мишени, ингибировать репликацию ДНК и стимулировать репарацию ДНК. Причем, так как р53 образует тетрамерные комплексы, мутации в одном аллеле гена р53 вызывают инактивацию и продукта второго, неповрежденного аллеля. Дело в том, что коэкспрессирующиеся нормальный и мутантный белок р53 образуют неактивные гетеромерные комплексы. Таким образом, мутантный белок ингибирует функции нормального белка р53 по доминантно-негативному механизму. По-видимому, именно эта особенность мутантных р53 в значительной мере ответственна за их онкогенный потенциал. В пользу этого свидетельствует тот факт, что введение в клетки короткого полипептида, соответствующего олигомеризационному домену р53, нарушает образование полноценных тетрамерных комплексов р53 и вызывает опухолевую трансформацию. Необходимо заметить, что помимо утраты нормальных функций р53, мутантные р53 с аминокислотными заменами в горячих точках (кодоны 175, 248 и др.) приобретают новые свойства, не свойственные белку р53 дикого типа (gain-of-function). Так, описано приобретение мутантными р53 способности активировать промоторы протоонкогенов MYC и ERB1, антиапоптотического гена BGL1 из семейства Bcl2, гена MDR1, детерминирующего множественную лекарственную устойчивость клеток и т.д. Предполагается, что это обусловлено способностью некоторых мутантных р53 связывать белки, в частности другие факторы транскрипции, с которыми нормальный р53 не взаимодействует, и модифицировать экспрессию генов, регулируемых этими транскрипционными факторами.
3.3.3. Физиологические функции р53 и их нарушения в неопластических клетках
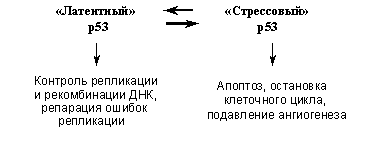
Молекулы белка р53 могут находиться в различных конформационных состояниях, в которых они обладают разными биохимическими активностями и выполняют разные физиологические функции. В обычных условиях р53 находится в так называемой латентной форме, в которой он обладает слабой транскрипционной активностью. Такой р53, однако, связывает белки репарационной машины (см. выше), проявляет активность 3′-5′-экзонуклеазы и стимулирует рекомбинацию и репарацию ДНК. При различных стрессах и внутриклеточных повреждениях происходят пост-трансляционные модификации, в частности фосфорилирование и ацетилирование определенных аминокислот молекулы р53, определяющие ее переход в так называемую стрессовую конформацию. Такой р53 значительно более стабилен (т.е. резко увеличивается его количество в клетке) и эффективно транс-активирует и/или транс-репрессирует специфические гены-мишени, следствием чего является индукция в аномальных клетках либо остановки клеточного цикла, либо апоптоза. Кроме того, активация р53 ведет к изменению экспрессии генов некоторых секретируемых факторов, в результате чего может изменяться размножение и миграция не только поврежденной, но и окружающих клеток. При этом, находясь в стрессовой конформации, р53 в значительной степени утрачивает активности, стимулирующие рекомбинацию и/или репарацию ДНК.
р53 дикого типа, в дополнение к латентной и стрессовой, может временно приобретать и так называемую мутантную конформацию, сходную с той, в которую молекула р53 необратимо переходит при онкогенных мутациях. Транзиторный переход р53 в мутантную конформацию происходит при воздействии определенных цитокинов и/или морфогенов (PDGF, тромбопоэтин, ретиноевая кислота и др.). Биологический смысл такого перехода пока неясен. Возможно, он заключается в полной инактивации рост-ингибирующих активностей р53 и/или изменении набора его генов-мишеней.
Таким образом, р53 играет важную охранную роль, являясь по образному выражению D.Lane, «стражем генома». Его повседневная функция заключается, по-видимому, в распознавании и исправлении ошибок, неизменно возникающих в ходе репликации ДНК. При массивных повреждениях ДНК, других внутриклеточных нарушениях или угрозе их возникновения происходит переключение функций р53 (Рис. 4): приобретая транскрипционные активности и изменяя экспрессию генов-мишеней, он вызывает либо остановку размножения аномальных клеток (временную, для устранения повреждений, или необратимую), либо их гибель (факторы, определяющие судьбу клетки при активации р53 будут рассмотрены ниже). В результате устраняется возможность накопления в организме генетически измененных клеток.
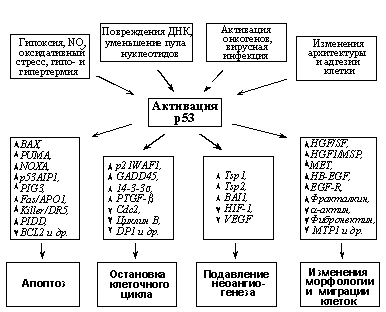
Механизмы активации р53 при стрессах и внутриклеточных повреждениях. Активация транскрипционных функций р53 наблюдается при самых разнообразных стрессах и внутриклеточных нарушениях: УФ- и g-облучении, присутствии в клетке разорванной ДНК, понижении внутриклеточного пула нуклеотидов, ингибировании ДНК- и РНК-полимераз, гиперэкспрессии онкогенов, вирусной инфекции, гипоксии, оксидативном стрессе, гипо- и гипертермии, различных нарушениях клеточной архитектуры (увеличении числа ядер, изменениях цитоскелета и адгезии) и т.д.
Ключевую роль в стабилизации белка р53 и повышении его транскрипционной активности играют изменения взаимодействия р53 с белком-ингибитором Mdm2, ген которого является потенциальным онкогеном. Белок Mdm2 связывается с N-концом молекулы р53 и, обладая активностями Е3 убиквитин-лигазы, стимулирует убиквитинизацию и, как результат, протеосомную деградацию белка р53. Поэтому, в норме уровень экспрессии р53 очень невелик, а время его жизни составляет всего около 30 минут. Кроме того, связываясь с N-концевым участком р53 в районе домена, взаимодействующего с базовыми факторами транскрипции, Mdm2 подавляет способность р53 транс-активировать гены-мишени.
Рис. 4. Охранные функции р53.
А). Функции «латентной» и «стрессовой» форм р53.
Б) Факторы, вызывающие транскрипционную активацию р53, гены-мишени активированного р53 и вызываемые изменениями их экспрессии биологические эффекты.
Важную роль в приобретении молекулами р53 конформации, способной транс-активировать гены-мишени, играют также модификации С-концевого участка, а именно ацетилирование его определенных аминокислотных остатков. При повреждениях ДНК и экспрессии активированного онкогена RAS эти события инициируются связыванием освобождающегося от Mdm2 N-концевого участка p53 с базальным фактором транскрипции р300/CBP, ацетилирующим сначала ингибиторный домен р53 по лизинам 373 и 382, а затем (после связывания р53 с респонсивными элементами) и белки хроматина в области генов-мишеней. Таким образом, последовательные пост-трансляционные модификации N-концевого и С-концевого участков р53 вызывают увеличение количества белка р53 в клетке, приобретение им способности связывать р53-респонсивные элементы и рекрутировать к генам мишеням базовые факторы транскрипции (компоненты комплекса TFIID РНК-полимеразы II и гистоновые ацетилазы p300/CBP, деконденсирующие хроматин), стимулируя тем самым транскрипцию их мРНК.
При некоторых стрессах, в частности при гипоксии, наблюдаются пост-трансляционные изменения р53, вызывающие его переход не к классической стрессовой конформации, а к ее варианту. Такой р53 не транс-активирует гены, содержащие р53-респонсивные элементы, но подавляет транскрипцию других генов-мишеней. Эта, так называемая репрессионная, форма также фосфорилирована по N-концу, но ее С-концевой участок не ацетилирован и связывает репрессионные комплексы Sin3/HDAC, вызывающие конденсацию хроматина генов-мишеней.
Гены-мишени р53 и их функции. В настоящее время, помимо Mdm2, обеспечивающего регуляцию самого р53 по принципу обратной связи (см. выше), идентифицировано более сотни генов, являющихся мишенями транскрипционных активностей р53. Они могут быть разделены на несколько групп, исходя из их физиологических функций (Рис. 4Б).
Идентифицирован также ряд генов-мишеней р53, продукты которых вызывают остановку в фазе G2 (задержка в ней наблюдается в случае, когда р53 активировался уже после того как клетка прошла G1-чекпойнт, или в клетках с инактивированным G1-чекпойнтом). Активированный р53 подавляет функцию комплекса циклин B/Cdc2, играющего ключевую роль в переходе из G2 в митоз, по нескольким механизмам. Во-первых, он транс-активирует ген 14-3-3-s, белковый продукт которого связывает и секвестрирует комплексы циклин B/Cdc2 в цитоплазме, не давая возможности им попасть в ядро, где они и должны проявлять свою активность. Во-вторых, он транс-активирует ген GADD45, белковый продукт которого обладает способностью связывать Сdc2, разрушая таким образом комплексы циклин B/Cdc2. В-третьих, р53 репрессирует транскрипцию генов циклина B и Cdc2, что уменьшает синтез их продуктов. Следует заметить, что, как и в случае остановки клеточного цикла в G1, задержка в G2 при повреждениях ДНК наблюдается и в клетках с инактивированным р53: она происходит в результате подавления функции фосфатаз Cdc25 (Cdc25A при остановке в G1 и Cdc25C при остановке в G2), активирующих соответствующие цикдинзависимые киназы. Однако в клетках с нарушенной функцией р53 происходит лишь кратковременная задержка в чекпойнтах, а активация р53 обеспечивает длительную остановку клеточного цикла, предотвращающую размножение вплоть до исправления дефекта.
Выявлено еще несколько десятков генов-мишеней р53. Среди них следует отметить ген каталитической субъединицы теломеразы (TERT), который репрессируется р53 (таким образом, р53 участвует, по-видимому, и в обеспечении репликативного старения клеток. По-видимому, р53 принимает участие и в процессах созревания клеток, так как некоторые из транс-активируемых им генов кодируют белки репертуара той или иной дифференцировки (мышечная креатинкиназа и др.).
3.3.4. Гомологи р53: р63 и р73