Стадии рака: классификация онкологических заболеваний
Стадия онкологического заболевания дает информацию о том, насколько велика опухоль и распространилась ли она по организму. Это помогает врачам определять прогноз пациента и план лечения.
С помощью врача-онколога, резидента Высшей школы онкологии Сергея Югая разбираемся, как врачи устанавливают стадии рака и что каждая из них означает.
На что влияет стадия онкологического заболевания?
Стадирование нужно, чтобы спрогнозировать, какие у пациента шансы на выздоровление, а также чтобы определить, какой метод лечения будет наиболее эффективен в конкретном случае, — поясняет Сергей Югай.
Все начинается с медицинского осмотра и обследований — УЗИ, КТ, МРТ, ПЭТ-КТ и других методов в зависимости от вида рака. Затем врач берет кусочек опухоли — биопсию или удаляет опухоль целиком во время операции, а после отправляет материал на гистологический анализ, чтобы поставить диагноз.
Стадии рака по TNM-классификации
Стадии онкологического процесса описывают разными способами — это зависит от вида опухоли. Один из самых распространенных способов — стадирование с помощью TNM-классификации.
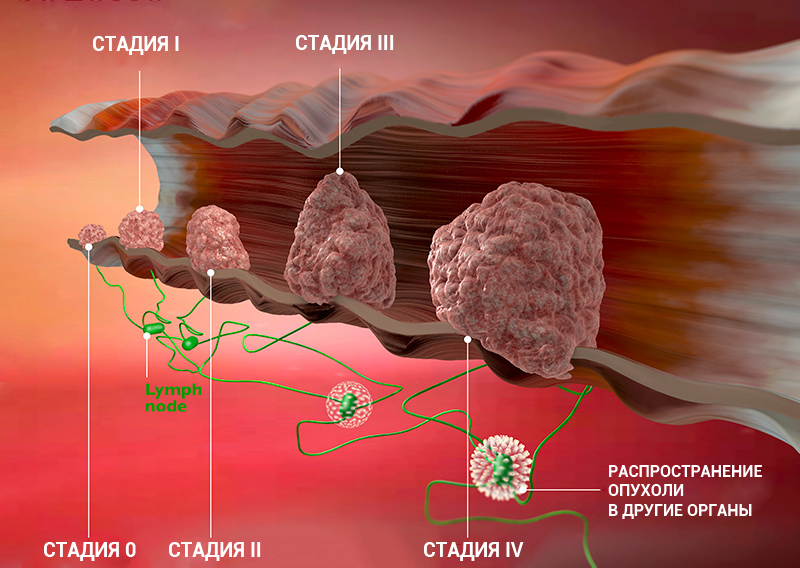
Т характеризует первичную опухоль, ее размеры и вовлечение окружающих структур в опухолевый рост, например, прорастание в стенку кишки или желудка. N говорит о наличии в лимфоузлах метастазов и количестве пораженных лимфоузлов, а М — о наличии отдаленных метастазов (во внутренних органах, костях, ЦНС или лимфоузлах, которые расположены далеко от первичной опухоли), — объясняет Сергей Югай.
Индекс Т принимает значения от 0 до 4. 0 означает, что первичная опухоль не обнаружена, 1 — опухоль маленькая, а 4 — опухоль проросла в прилегающие ткани. Таким образом, чем больше цифра рядом с Т, тем ситуация сложнее. При некоторых видах рака N принимает значение 0 или 1, при других — 0, 1 или 2, а иногда — 0, 1, 2 и 3. 0 означает, что опухоль не проникла в ближайшие лимфоузлы, а 3 — что поражено множество лимфоузлов. M0 показывает, что метастазов нет, а 1 — что метастазы есть.
Онкологи выставляют стадию по TNM клинически — до операции или когда операция не планируется и патоморфологически — при изучении удаленной во время операции опухоли, — объясняет Сергей.
Клиническая стадия обозначается буквой «c», например, cT2. Патоморфологическая — буквой «p», например, pN1.
От правильной стадии зависит тактика лечения. Например, пациент — мужчина с раком желудка и стадией cT1N0M0. Это значит, что опухоль прорастает в слизистую и подслизистый слой стенки желудка. В этом случае пациенту показана операция. Если же стадия выше (cT2N1M0, например), то есть опухоль пациента прорастает в мышечный слой, и есть метастазы в лимфоузлах, то может понадобиться химиотерапия перед операцией, которая позволит улучшить результаты лечения, — добавляет Сергей.
Стадию рака могут обозначать с помощью цифр — 0, I, II, III, IV. Что это значит?
Клинические стадии (0, I, II, III, IV) тесно связаны с системой TNM. Как правило, одна клиническая стадия включает в себя несколько вариантов стадирования по TNM. Эти варианты характеризуются схожими прогнозом и подходом к лечению. Например, стадии T1N3M0, T2N3M0, T3N2M0 рака легкого объединяются в IIIВ стадию, так как при любой из этих ситуаций пациент будет иметь примерно одинаковый прогноз и тактику лечения. В этом конкретном примере необходима химиолучевая терапия, а не операция, — комментирует Сергей Югай.
Меняется ли стадия после лечения, при прогрессировании заболевания?
Нет, стадия выставляется один раз. Но есть нюансы:
Например, мы хотим посмотреть, как опухоль ответила на лечение, чтобы понять, можно ли делать операцию. После лечения опухоль уменьшилась, и мы добавляем к стадии новые данные. При прогрессировании опухолевого процесса первоначальная стадия также остается прежней, но, к сожалению, прогноз будет менее благоприятный. Например, у человека II стадия рака желудка. Он прооперирован, и прогноз у него хороший. Через 2 года врачи обнаруживают у пациента метастазы в легких. Стадия остается II, но рак у пациента уже метастатический, что очень усложняет положение, — говорит Сергей.
Бывает, что люди сравнивают свою ситуацию с историями других пациентов. Если речь идет о разных онкологических заболеваниях, то такие сравнения некорректны — это заболевания с разными прогнозами и схемами лечения:
Например, с нейроэндокринным раком поджелудочной железы люди могут жить десятилетиями, а при метастатической стадии рака поджелудочной железы — полгода или год, — объясняет врач-онколог.
Что может повлиять на прогноз людей с одинаковой стадией и одним видом рака?
Сергей Югай выделяет три фактора:
Стадирование рака
Правильное и эффективное лечение рака напрямую зависит не только от определения его типа, но и от сведений о размере опухоли и степени ее распространения.
Для систематизации такой информации во всем мире принято использовать международную классификацию стадий злокачественных новообразований TNM.
Классификация TNM основана на трех факторах: размер первичной опухоли (T — tumor), вовлеченность регионарных лимфатических узлов (N — nodes) и наличие отдаленных метастазов (M — metastasis). Для каждого вида рака существует своя градация, это определяет подход к лечению, а также прогноз.
Например, для рака молочной железы показатель T определяет диаметр первичной опухоли и ее взаимодействие с окружающими тканями. Опухоль с показателями Т1-Т3, ограниченная молочной железой, определяется размером, а T4, независимо от размера, предполагает распространение опухоли на кожу или грудную стенку. В то же время, для меланомы показатель Т определяется только глубиной прорастания опухоли (инвазия до 1 мм — Т1, а более 4 мм — Т4).
Показатель N для разных опухолей тоже разный, включая количество лимфатических узлов, их размеры, выход за предел капсулы лимфатического узла и т. д. N описывает только регионарные лимфатические узлы, которые отличны для каждой конкретной опухоли. Например, для рака печени лимфатические узлы вдоль ворот печени являются регионарными — ближайшими лимфатическими узлами, собирающими лимфу от области опухоли. Но, в то же время, расположенные рядом мезентериальные или забрюшинные лимфатические узлы, уже не являются регионарными для данной опухоли, а значит, определяются как отдаленные метастазы (М).
Ранее для каждого типа рака стадия определялась взаимоотношением этих трех параметров, но со временем, по мере изучения биологии рака и механизмов развития опухолей, параметров становилось все больше. Сейчас во всем мире используют классификации 8-го пересмотра, которые каждые 5-7 лет выпускают две организации: The Union for International Cancer Control (UICC) и The American Joint Committee on Cancer (AJCC).
Сегодня стадия может быть клинической (с), когда перед операцией мы определяем ее по данным диагностических исследований. Например, при раннем раке молочной железы стадия может выглядеть так — cT2N0M0. А после операции, когда весь материал был подвергнут полноценному гистологическому исследованию, выставляется патоморфологический диагноз (р), и этот же случай может быть рестадирован в pT2pN2а (5/12) M0. Это означает, что клинически неопределяемые метастазы в подмышечных лимфатических узлах были выявлены в 5 из 12 удаленных и исследованных лимфатических узлах.
Существуют и другие нюансы, возьмем, к примеру, стадирование после проведенной неоадьювантной (предоперационной) химиотерапии (префикс yp), когда у женщины с местнораспространенным раком молочной железы сT3N1M0 лечение начали с химиотерапии, а после провели операцию и увидели, что все опухолевые клетки погибли от химиотерапевтического лечения. Это означает, что у данной женщины полный лечебный патоморфоз, а стадироваться эта ситуация будет так — ypT0ypN0, CR.
Помимо TNM, используются также следующие символы:
Стадия может зависеть даже от того, определяется ли в опухолевой ткани вирус папилломы человека (p16), как это происходит в случае с раком ротоглотки.
Не все параметры используются для каждой опухоли, но процесс стадирования становится все сложнее. Этим мы обязаны прогрессу в лечении и большим данным, диктующим необходимость все более разных подходов для разных стадий.
Стадия также определяет прогноз, хотя и здесь подходы сегодня пересматриваются. Благодаря иммунотерапии, многие (ранее «безнадежные») пациенты с самыми последними стадиями онкологического заболевания получают возможность полностью избавиться от него на долгие годы. В то время, как пациенты с третьей стадией других болезней или даже того же вида рака, не отвечающего на иммунотерапию, неуклонно прогрессируют и умирают.
Пример: 2 пациента с идентичным распространением одного и того же вида рака толстой кишки, но у одного из них есть высокий уровень микросателлитной нестабильности — фактора ответа на иммунотерапию, а у другого нет.
Онкология, как и многие другие разделы медицины, сегодня обращена в сторону персонализации. И недалек тот день, когда стадирование будет осуществляться по иному принципу — не по степени анатомического распространения, а исходя из биологических особенностей конкретного заболевания.
Система Grade: как упорядочить хаос
Генри Миллер писал: «Хаос — это порядок, который нам непонятен». Трансформация клеток с последующим безудержным ростом опухолевой массы представляет, на первый взгляд, участок анархии в организме, но изучение биологии канцерогенеза постепенно формирует понимание связей и законов опухолевой системы. В клинической практике переход от периода «смуты» выражается в совершенствовании классификаций опухолей. Одной из очевидных, но далеко не самых простых характеристик неоплазий является морфологическая картина. Она позволяет судить о «темпераменте» опухоли, определяющем степень ее злокачественности.
Градация (Grade) — категория степени гистологической злокачественности, основанная на том, как атипичные клетки и опухолевая ткань в целом выглядят при световой микроскопии.
Количество градаций варьирует от 3 до 4 в зависимости от типа опухоли. Если злокачественно трансформированные клетки и структурная организация опухолевой ткани близки к нормальным, опухоль является «хорошо дифференцированной» (Grade 1). Эти опухоли имеют тенденцию расти и метастазировать медленнее, чем «мало/плохо дифференцированные» (Grade 2 и/или Grade 3) или «недифференцированные» (Grade 3 или 4). Более высокий Grade сочетается с увеличением агрессивности опухоли и ухудшением прогноза.
Основываясь на этих и других различиях в микроскопической картине, патологоанатомы вычисляют числовую «оценку» большинства онкологических заболеваний. Факторы, используемые для определения степени злокачественности опухоли, различаются в зависимости от локализации.
Степень злокачественности опухоли не совпадает со стадией. Стадия определяется комбинацией значений T, N, M, описывающих размер первичной опухоли, поражение регионарных лимфатических узлов и наличие метастазов и их характеристику. Валидные гистологические системы классификации достаточно длительно используются при верификации рака молочной железы [1], предстательной железы [2], эндометрия [3], сарком мягких тканей [4] и опухолей почек [5].
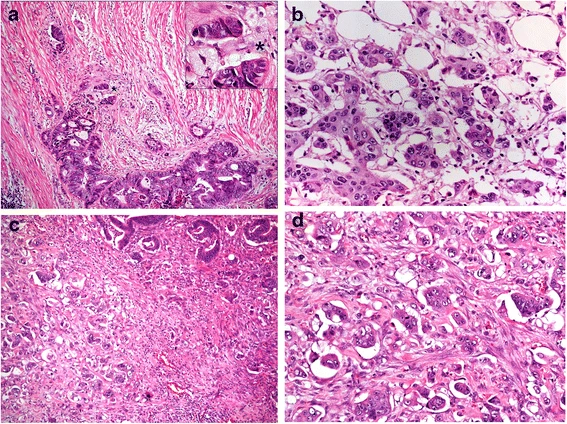
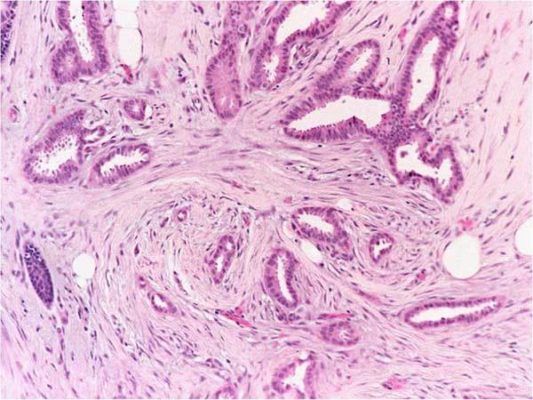
Для некоторых опухолей для определения градации используют уникальные по гистологическому строению участки. Например, низкодифференцированные кластеры (poorly differentiated clusters, PDCs) рассматриваются в качестве гистопатологического предиктора рака прямой кишки. PDCs состоит из пяти и более раковых клеток, которые формируют инвазивный компонент при отсутствии железистой паренхимы опухоли (рис.1) [6].
.
Рассмотрим для примера определение гистологической градации при раке молочной железы. Для объективизации процесса и унификации используется полуколичественная оценка морфологических характеристик опухоли. В настоящее время она представлена Ноттингемской модификацией системы Скарфа-Блума-Ричардсона или Ноттингемской градирующей системой, принятой во всем мире. Кратко ее пункты отражены в таблице 1 (и пусть вас не запутает мнемоника, основанная на аналогии с Tumor/Nodulus/Metastasis).
.
Разберем составляющие ингредиенты гистологической градации.
Оценка железистых структур проводится во всех участках доставленного материала. В зависимости от доли фрагментов с наличием таких элементов выставляется определенное число баллов:
Не всякая щель в препарате – железа, могут быть и артифициальные повреждения материала. Нам нужны только структуры с четко определяемым центральным просветом, окруженным поляризованными злокачественно трансформированными клетками.
Ядерный полиморфизм – морфологическое проявление опухолевой дифференцировки на цитологическом (клеточном) уровне. Это визуальный паттерн генетических поломок в опухолевой клетке: анеуплоидии, генетической нестабильности и изменения транскрипции.
Индивидуальность во взглядах делает нас особенными личностями, но, к сожалению, в морфологической оценке выражается в субъективизме, особенно при рассмотрении ядер клеток.
Ядерный полиморфизм оценивается по балльной системе:
Количество митозов указывает на уровень пролиферативной активности опухоли. Поэтому справедливо отдать лавры самого прогностически значимого компонента гистологической градации букве «М».
Митоз или не митоз — вот в чем вопрос… Для подсчета используют только достоверные фигуры митоза, отражающие различные его стадии. Этот показатель невероятно капризен и реагирует на качество фиксации материала. Поэтому в спектр компетенций патологоанатома включается также и взаимодействие с лабораторией, чтобы осознавать возможные «помехи» и при необходимости запрашивать повторную подготовку опухолевого материала.
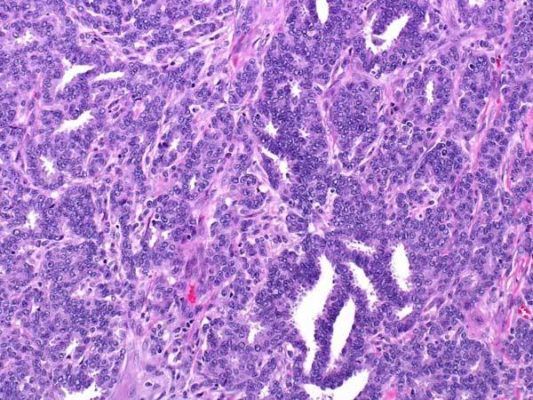
Рисунок 2. Grade 1: инвазивная протоковая карцинома состоит из небольших желез с достаточно однотипными ядрами. Карциномы G1 менее агрессивны и имеют лучший прогноз, чем менее дифференцированные. Они также чаще ER-положительные (иммуногистохимический показатель — экспрессия рецепторов эстрогена на опухолевых клетках), что является еще одной особенностью, связанной с более благоприятным прогно зом.
.
Рисунок 3. Grade 2: некоторые участки этой инвазивной протоковой карциномы образуют структуры наподобие трубчатых желез, но другие области представлены плохо сформированными железами с гнездными скоплениями клеток, содержащих умеренно атипичные ядра. Карциномы G2 имеют промежуточный прогноз.
.
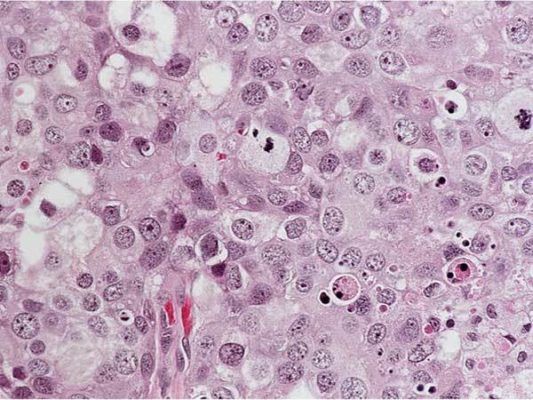
Рисунок 4. Grade 2: эта инвазивная протоковая карцинома состоит из отдельных и гнездно расположенных атипичных клеток с выраженным ядерным полиморфизмом и высокой митотической активностью. Карциномы G3 имеют максимально неблагоприятный прогноз. Молекулярный подтип таких опухолей чаще трижды негативный (отсутствует экспрессия рецепторов эстрогена, прогестерона, отрицательный HER2), что ассоциировано с агрессивным поведением опухоли и худшим прогнозом.
Опухолевая гетерогенность проявляется и в пролиферативной активности. Для максимально точной оценки подсчет проводят в 10 HPF (high-power field, поле зрения при большом увеличении микроскопа) по периферии опухолевого узла, где ожидается наибольшее число пролиферирующих клеток. Важным аспектом являются характеристики используемого микроскопа. Количество определяемых митозов зависит от площади поля зрения. Патологоанатом должен знать объем поля зрения на окуляре и показатели объектива своего верного «помощника».
.
А — объектив Nikon или Labophot с кратностью увеличения в 40 раз (40x) или сопоставимый с диаметром поля 0,44 мм;
В — объектив Leitz или Ortholux 25x или сопоставимый с диаметром поля 0,59 мм;
С — объектив Leitz или Diaplan 40x или сопоставимый с диаметром поля 0,63 мм.
Итоговая оценка Grade основана на подсчете суммы 3 вышеуказанных компонентов:
Введение в онкологическую практику оценки степени злокачественности опухоли подчеркивает важность биологических свойств атипичных клеток. Потенциал к неконтролируемому агрессивному росту, инвазии и метастазированию можно оценить по визуальным характеристикам отдельных клеток и особенностям сформированных ими структур. Для различных локализаций новообразований разрабатываются собственные системы оценки, которые непрерывно совершенствуются. Но даже самый точный, идеально сконструированный алгоритм не будет работать при отсутствии достаточной компетенции специалиста. Сохранить ясный взгляд, педантичность и скрупулезность в течение каждого, даже самого тяжелого рабочего дня крайне важно для онкоморфологов. Их кропотливый труд завершается распечаткой листа с надписью «результаты патологоанатомического исследования», на котором в нескольких строках в графе «заключение» расписаны ориентиры для клиницистов, определяющие судьбу пациента.
Лечение немышечно-инвазивного рака мочевого пузыря высокого риска
С.А. Иванов, И.Н. Заборский, В.С.
Чайков Медицинский радиологический научный центр им. А.Ф. Цыба ‒ филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» МЗ РФ; Обнинск, Россия
Автор для связи: Заборский Иван Николаевич Тел.: +7 (484) 399-32-56; e-mail: i.zaborskii@mail.ru
Введение
Рак мочевого пузыря (РМП) – одна из самых распространенных опухолей мочевыводящего тракта. В Российской Федерации на 2015 год частота встречаемости РМП на 100 000 тысяч населения составила 68,3. Прирост частоты встречаемости от 2005 года составил 22,3 [1].
Определение группы высокого риска
К немышечно-инвазивным формам рака мочевого пузыря (НМИ РМП) относятся следующие формы: Тis, Ta, T1. Распространенность опухоли от T2 до T4 относится к мышечно-инвазивным формам.
Для уротелиального рака согласно действующей системе ВОЗ /Международного общества уропатоморфологов (WHO/ISUP) рекомендуется следующее разделение по степеням дифференцировки:
Европейская организация по исследованию и лечению рака (EORTC) разработала систему распределения больных на 3 группы риска рецидива и прогрессии: низкого, высокого и промежуточного. В ее основе лежит мета-анализ результатов лечения 2596 больных РМП Та-Т1, включенных в 7 рандомизированных исследований EORTC. Каждому из перечисленных выше факторов риска присвоен балл соответственно степени его влияния на развитие рецидива или прогрессии. Суммой баллов определяется группа риска. Согласно рекомендациям Европейской урологической ассоциации, на 2017 год выделяют 3 группы риска, в которых значимо различаются частоты рецидивов и прогрессии в мышечно-инвазивный рак.
К группе низкого риска относятся: одиночная опухоль, 3см) T1G3/ HG и/или рецидивирующие опухоли T1G3/HG – T1G3/HG с карциномой in-situ простатического отдела уретры – атипичные формы уротелиальной карциномы – лимфососудистая инвазия
Неэффективность внутрипузырной БЦЖ-вакцины
Рекомендуется проведение радикальной цистэктомии.
Проведенный мета-анализ 7 рандомизированных исследований (1476 пациентов), изучивших однократное введение химиопрепаратов, в первые 24 часа после проведенной ТУР снижает риск рецидивирования у пациентов, получавших внутрипузырную химиотерапию на 11%. Эффект от ранней адъювантной химиотерапии отмечался как для одиночных, так и для множественных опухолей. Наиболее распространенным препаратом для внутрипузырной химиотерапии является Митомицин С, но значимых различий от применения различных препаратов (эпирубицина, доксорубицина и Митомицина С) получено не было [13].
По данным EAU, применение повторной внутрипузырной химиотерапии терапии для лечения рецидивных опухолей High Grade после проведенного оперативного лечения и ранее проведенной внутрипузырной химиотерапии не целесообразно. В данном случае препаратом выбора является вакцина БЦЖ.
Внутрипузырная иммунотерапия вакциной БЦЖ (Бацилла Calmette-Guerin) показала свою эффективность в профилактике рецидива РМП после выполненной ТУР. Мета-анализ 13 рандомизированных исследований, включающий в себя 2548 пациентов показал, что внутрипузырная имуннотерапия увеличивает время безрецидивной выживаемости на 38% (HR, 0.62. 95% Cl 0.50.77, р
Карцинома
Один из самых распространенный типов раковых опухолей у людей – карцинома. Этот тип неоплазии, злокачественного роста, который зарождается в тканях, которые покрывают как внешние поверхности тела, так и внутренние полости. Этот вид онкологии относится к опухолям эпителиального происхождения.
Акции
Запись на консультацию со скидкой 10%.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Содержание статьи:
Общие данные

Кроме того, будут характеризоваться как карцинома и те злокачественные опухоли, которые состоят из клеток, подвергшихся трансформации, которые имеют специфические характеристики на молекулярном, гистологическом и клеточном уровне, типичные для эпителиальной ткани.
По данным ВОЗ на долю карцином приходится ежегодно до 9,5 млн смертей. Лечение этих видов рака (карциномы) достаточно трудная задача, показатели выживаемости очень разнятся. Участки органов, часто поражаемые карциномами, включают:
Причины возникновения карцином
Пока точные причины, по которой развиваются разные типы рака, включая карциному, не определены. Но ученые выделили ряд факторов, предрасполагающих к развитию патологии:
Типы карциномы, классификация
Хотя карциномы могут возникать во многих частях тела, наиболее распространены следующие типы карциномы:
Основа классификации карцином – тип клеток и их локализация, а также стадии карциномы.
Карциномы могут распространяться на другие части тела или ограничиваться основным местом. Заболевание имеет различные формы, в том числе:
Важно знать также признаки опухоли в разных стадиях развития.

Стадия 2 – опухоль не более 5 см в диаметре, в лимфоузлах определяются единичные метастазы.
Стадия 3 – опухоль превышает 50 мм диаметром, есть массивные метастазы в области лимфоузлов.
Стадия 4 – определяются отдаленные метастазы по всему организму.
Карцинома: симптомы
Врачи дают описание того, как выглядит тот или иной тип карциномы.
Если выявлена базальноклеточная карцинома, вероятно, она возникла из-за слишком длительного пребывания на солнце. Возможно, было несколько серьезных солнечных ожогов или в течение жизни человек много времени проводил на солнце.
Когда плоскоклеточный рак развивается в коже, он часто обнаруживается на участках, подверженных воздействию солнца, таких как:
Плоскоклеточная карцинома, которая развивается на коже, имеет тенденцию к росту и распространению больше, чем рак базальных клеток. В редких случаях он может распространяться на лимфатические узлы.
На фоне карциномы возможен синдром интоксикации с лихорадкой, потерей аппетита и веса, слабостью, локальные изменения в области пораженной кожи, изменение цвета, уплотнение. Если поражен внутренний орган, страдают его функции.
Диагностика
Постановкой диагноза занимаются онкологи, они помимо оценки жалоб и осмотра, назначают целый ряд обследований. К ним относят:
Методы лечения

Карцинома: прогноз

Рекомендации
Для рака кожи основные рекомендации – это снизить облучение кожи УФ-лучами и оградить себя от влияния потенциальных канцерогенов. В целом, ведение здорового образа жизни с рациональным питанием, дозированными нагрузками помогает снизить риск онкологии.