Micrococcus (микрококки, род бактерий)
Микрококки (Micrococcus) — род грамположительных бактерий. Имеют форму сферы от 0,5 до 3 мкм в диаметре. Микрококки неподвижны. В природе распространены повсеместно: в почве, пыли, в воде. Особенностью микрококков является способность к развитию при низких температурах.
Micrococcus antarcticus приспособлены к существованию в антарктических условиях. Отличается тем, что оптимальная температура роста 16±8°С, а могут расти и при 0°С (для сравнения, оптимальная температура роста для Micrococcus luteus и Micrococcus lylae — 37°С).
Микрококки в организме человека
Большое количество микрококков обитает на коже человек, они также встречаются в дыхательных путях, в ротовой полости. Чаще всего микрококки не вызывают каких-либо заболеваний, однако они могут быть причиной оппортунистических инфекций, особенно у индивидуумов с ослабленным иммунитетом, например, у ВИЧ-инфицированных.
В исследовании, проведённом в Твери, Micrococcus spp. выделены из слизистой оболочки тела желудка у 22% здоровых детей (Апенченко Ю.С. и др.)
Микрококки в систематике бактерий
По современной классификации род Micrococcus входит в семейство Micrococcaceae, порядок Micrococcales, класс Actinobacteria, тип Actinobacteria, царство Бактерии.

В род микрококки включены виды: Micrococcus aerogenes, Micrococcus alkanovora, Micrococcus aloeverae, Micrococcus antarcticus, Micrococcus chenggongense, Micrococcus cohnii, Micrococcus endophyticus, Micrococcus flavus, Micrococcus indicus, Micrococcus leteus, Micrococcus luteus, Micrococcus lylae, Micrococcus terreus, Micrococcus thailandicus, Micrococcus xinjiangensis, Micrococcus yunnanensis.
Влияние препарата циклоферон на флору миндалин у часто болеющих детей
Опубликовано в журнале:
« Экспериментальная и клиническая фармакология » № 3, 2013 С.А. Ляликов, П.Г. Бедин, СЮ. Ермак, Р.В. Янович
УО «Гродненский государственный медицинский университет». Кафедра клинической лабораторной диагностики и иммунологии (заведующий кафедрой профессор С.А. Ляликов). Беларусь, г. Гродно.
Резюме. Для оценки способности препарата циклоферон влиять на микробиологический пейзаж поверхности миндалин у часто болеющих детей (ЧБД) была изучена микрофлора миндалин до и после стандартного курса этого препарата у 68 дошкольников, относящихся к категории ЧБД. Установлено, что микробный пейзаж поверхности миндалин детей после курса циклоферона характеризовался уменьшением разнообразия микрофлоры и снижением титра бактерий, в том числе и золотистого стафилококка, а также уменьшением количества штаммов, резистентных к бензилпенициллину, клиндамицину и ванкомицину. Таким образом, препарат циклоферон можно рекомендовать для реабилитации ЧБД.
Ключевые слова: часто болеющие дети, циклоферон, микрофлора миндалин.
Введение.
По современным литературным данным в группу часто болеющих детей (ЧБД) входят на том или ином возрастном этапе от 15 до 65% детской популяции [10], в связи с этим частые респираторные заболевания является актуальной проблемой педиатрии [4, 9]. В 1986 году В.Ю. Альбицким и А.А. Барановым была предложены критерии включения детей в группу часто болеющих. К (ЧБД) относят детей, страдающих острыми респираторными заболеваниями (ОРЗ) свыше 4-х раз в год в возрасте до 1 года, 6-и раз – в 1-3 года, 5-и раз – в 4-5 лет и 4-х раз – после 5 лет [1].
Система иммунитета в детском возрасте характеризуется относительно пониженным уровнем нейтрофилов – основных эффекторных клеток врожденного звена иммунного ответа, а также низкой продукцией иммуноглобулинов на фоне повышенного числа Т- и В-лимфоцитов, что свидетельствует о неполноценности адаптивного звена [8]. Это в совокупности с анатомо-физиологическими особенностями органов дыхания [6], недостаточными гигиеническими навыками и расширением контактов с окружающим миром делает детей дошкольного возраста особенно уязвимыми для инфекций.
Несмотря на то, что вирусы являются этиологическими агентами более чем в 80% случаев ОРЗ [2], по данным литературы в практической медицине для их лечения в большинстве случаев, даже при неосложнённом течении, используются антибактериальные (АБ) препараты [13, 14], что способствует развитию дисбиоза. Показано, что после перенесенного эпизода ОРЗ дисбиотические изменения микрофлоры зева сохраняются до 1,5 месяцев [11]. Гибель резидентной микрофлоры приводит к заселению биотопа условно-патогенными микроорганизмами. Существуют данные, что 35% детей, относящихся к группе ЧБД, имеют хроническую ЛОР патологию [10]. Не менее, чем в 30% случаев, ЧБД являются носителями β-гемолитического стрептококка группы А [3, 7]. Не менее 50% детей являются носителями золотистого стафилококка [7, 9].
Приведенное выше факты определили цель нашего исследования: оценить способность индуктора эндогенного интерферона – препарата циклоферон влиять на микробиологический пейзаж поверхности миндалин у часто болеющих детей.
Материалы и методы.
Было обследовано 68 детей (32 девочки и 36 мальчиков) в возрасте от 4 до 7 лет, медиана (Ме) – 5,1 лет, нижняя квартиль (Q25) – 4,5 года, верхняя квартиль (Q75) – 5,8 лет. Все дети посещали специализированные детские сады (№94 и №95) г. Гродно для ЧБД. Критериями включения в исследование были добровольное информированное согласие законных представителей детей, возраст 4-7 лет, отсутствие острых инфекционных заболеваний на момент обследования, наличие в анамнезе 6-и и более эпизодов ОРЗ за предшествующие 12 месяцев. Обследование включало клинический осмотр детей, анкетирование родителей и выкопировку данных из амбулаторной карты (форма №112-у).
Двукратно, до начала приема препарата циклоферон и через 2 недели после окончания приема детям выполнили посев микрофлоры с поверхности миндалин. Материал – слизь с поверхности миндалин – брали стерильными ватными тампонами натощак и помещали в универсальную гелевую транспортную среду Стюарта фирмы Copan (Италия). В течение 2 часов полученный материал доставлялся в лабораторию. Для идентификации микрофлоры и определения её чувствительности к антибактериальным препаратам была использована автоматизированная система VITEC-2 фирмы BioMerieux (Франция). Тестирование чувствительности к антибактериальным препаратам осуществлялось методом минимальных ингибирующих концентраций.
Препарат циклоферон (таблетки по 0,15) назначался двумя курсами (с перерывом в 1 месяц) по схеме, указанной в аннотации: на курс по 1 таблетке 1 раз в день за полчаса до еды в 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23 дни.
Статистический анализ проводился с использованием стандартного пакета прикладных программ Statistica версия 6.0. При сравнении двух независимых групп изучаемой переменной использовали тест Манна-Уитни (U), в случае зависимости групп – тест Вилкоксона (Z). При сравнении долей (процентов) использовался метод Фишера (Fisher exact test). Нулевая гипотеза об отсутствии различий между переменными отвергалась на уровне значимости α=0,05 (p ≤0,05) для каждого из использованных тестов. Для представления результатов статистической обработки использовали величины медианы (Me), верхней (Q75) и нижней квартилей (Q25) в формате Me (Q25-Q75).
Результаты и обсуждение.
Таблица 1.
Микрофлора с поверхности миндалин ЧБД, выделенная при первом обследовании
| Название | Количество культур | % носителей |
|---|---|---|
| Aerococcus viridans | 1 | 1,47 |
| Candida famata | 3 | 4,41 |
| Dermococcus nishinomiyaensis | 1 | 1,47 |
| Erisipelotrix rusiopathiae | 4 | 5,88 |
| Fackmalia hominis | 1 | 1,47 |
| Granulicatella adiacens | 3 | 4,41 |
| Granulicatella elegans | 1 | 1,47 |
| Kocuria kristinae | 1 | 1,47 |
| Kocuria rosea | 4 | 5,88 |
| Leuconostoc mesenterioides | 1 | 1,47 |
| Leuconostoc mesenteroides cremosis | 3 | 4,41 |
| Rothia mucilaginosa | 1 | 1,47 |
| S. aureus | 33 | 48,53 |
| S. epidermidis | 1 | 1,47 |
| S. haemolyticus | 1 | 1,47 |
| S. hominis | 7 | 10,29 |
| S. ludgunensis | 3 | 4,41 |
| S. vitulinus | 1 | 1,47 |
| Serratia marcescens | 1 | 1,47 |
| Sphingomonas thalpophilium | 1 | 1,47 |
| Str. oralis | 12 | 17,65 |
| Str. parasanguinis | 2 | 2,94 |
| Str. pneumoniae | 11 | 16,18 |
| Str. salivarius | 2 | 2,94 |
| Str. spp. | 4 | 5,88 |
| Всего | 103 |
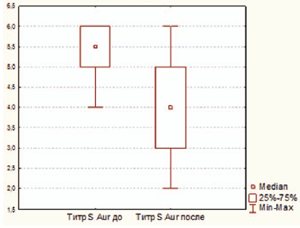
При повторном обследовании спектр микроорганизмов значительно сузился. В мазках с поверхности миндалин у детей были обнаружены представители только 16 семейств, родов и видов микроорганизмов (таблица 2). Как и при первом исследовании, золотистый стафилококк выявлялся практически у половины обследованных, но в более низких титрах (по сравнению с исходными р=0,04) (рисунок 1). У 11 детей (25,58%) рост бактерий отсутствовал, у 24 детей (55,81%) была идентифицирована 1 культура, у 6 (13,96%) – 2, у 2 (13,96%) – 3 культуры бактерий.
Таблица 2.
Микрофлора с поверхности миндалин ЧБД, выделенная при повторном обследовании
| Название | Количество культур | % носителей |
|---|---|---|
| Нет роста | 11 | 25,58 |
| Acinetobacter ursingii | 1 | 2,32 |
| Candida | 3 | 6,98 |
| E.coli | 1 | 2,32 |
| Enterobacter cloacae | 2 | 4,65 |
| Kocuria roseae | 1 | 2,32 |
| Micrococcus luteus | 1 | 2,32 |
| Pantoteae spp. | 1 | 2,32 |
| Ps.aeruginosa | 1 | 2,32 |
| S.aureus | 19 | 44,19 |
| S.epidermidis | 1 | 2,32 |
| S.warneri | 1 | 2,32 |
| Stenotrophomonas maltophyla | 1 | 2,32 |
| Str.oralis | 3 | 6,98 |
| Str.parasanguinis | 1 | 2,32 |
| Str.sanguinis | 2 | 4,65 |
| Str.spp. | 3 | 6,98 |
| Всего | 42 | 100,0 |
Рисунок 1. Динамика титра S. aureus у ЧБД, принимавших циклоферон
При анализе чувствительности к антибиотикам золотистого стафилококка, высеянного с поверхности миндалин ЧБД, при повторном исследовании было установлено несущественное уменьшение доли метициллин-, рифампицин-, эритромицин-, тетрациклин резистентных штаммов и достоверное снижение процента штаммов устойчивых к бензилпенициллину, ванкомицину и клиндамицину по сравнению с исходными показателями (таблица 3).
Таблица 3.
Доля (%) S. aureus, резистентных к антибиотикам до и после лечения
| Антибиотики | До приема циклоферона | После приема циклоферона | Р |
|---|---|---|---|
| MRSA | 10,00 | 5,26 | — |
| Бензилпенициллин | 84,09 | 63,64 | 0,05 |
| Ванкомицин | 26,67 | 4,55 | 0,03 |
| Клиндамицин | 20,93 | 0,0 | 0,02 |
| Линезолид | 0,0 | 0,0 | — |
| Моксифлоксацин | 0,0 | 0,0 | — |
| Оксациллин | 15,56 | 4,55 | — |
| Рифампицин | 4,44 | 0,0 | — |
| Эритромицин | 11,11 | 9,09 | — |
| Гентамицин | 0,0 | 0,0 | — |
| Ципрофлоксацин | 0,0 | 0,0 | — |
| Левофлоксацин | 0,0 | 0,0 | — |
| Тетрациклин | 6,67 | 0,0 | — |
| Нитрфурантоин | 0,0 | 0,0 | — |
| Бисептол | 0,0 | 0,0 | — |
| Дальфопристин | 0,0 | 0,0 | — |
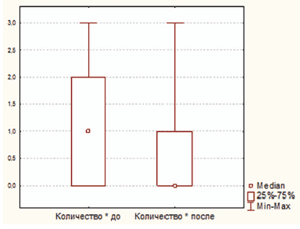
На фоне приема циклоферона изменилась не только обсемененность поверхности миндалин золотистым стафилококком, но и непатогенной микрофлорой. При повторном обследовании среднее количество обнаруженных непатогенных видов бактерий и их титры были достоверно ниже (в обоих случаях p
Рисунок 2. Количество непатогенных видов микроорганиз
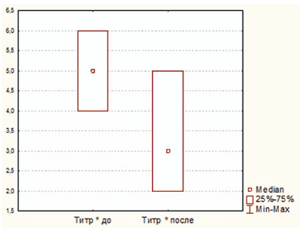
Рисунок 3. Динамика титра непатогенной микрофлоры у ЧБД, принимавших циклоферон
Поскольку циклоферон не обладает прямой антибактериальной активностью, можно предположить, что снижение обсемененности и видового разнообразия микроорганизмов поверхности миндалин обусловлено иммунокоррегирующими свойствами этого препарата.
Уменьшение количества устойчивых к антибиотикам штаммов на фоне приема циклоферона, несомненно, представляется весьма интересным и важным эффектом ввиду всеобщей тенденции к развитию резистентности к используемым в повседневной практике антибактериальным препаратам. Таким образом, препарат циклоферон можно рекомендовать к применению в составе комплексной терапии и для реабилитации ЧБД.
Выводы
Прием двух курсов препарата циклоферон (с перерывом в 1 месяц) по схеме, указанной в аннотации снижает у ЧБД видовое разнообразие микрофлоры поверхности миндалин, достоверно уменьшает обсеменённость поверхности миндалин микрофлорой, в том числе золотистым стафилококком.
Приём препарата циклоферон приводит к значимому снижению количества штаммов золотистого стафилококка устойчивых к бензилпенициллину, ванкомицину и клиндамицину.
Чем опасен грибок
Грибковое поражение кожи, лица, тела, микоз ногтя и любые иные присутствия грибка любой разновидности организма, крайне пагубно влияет на все тело в целом. Снижается иммунитет, ухудшается общее состояние пациента, осложняется течение многих хронических заболеваний.
Клиника Daily Medical и специалисты с большим опытом лечения грибка любой сложности, единогласны в мнении, что отсутствие своевременного лечения приводит к необратимым последствиям, поражению тканей и в целом снижении уровня жизни заболеваемого.
Элементарные знания как передается грибок, что делать в случае заражения, как обезопасить себя и близких, и как лечить грибковые заболевания, помогут избежать многолетнего мучения с этим недугом. Ниже в статье описаны способы профилактики, защиты и классификации разновидностей микозов.
Как выглядят грибковые заболевания кожи
Грибковые заболевания кожи, грибок на руках, ногах и ногтях это крайне распространенное заболевание. Грибок присутствует в организме каждого шестого жителя планеты. Разнообразие грибов в природе поражает своим количеством и отличиями поражения, для человека опасны не все виды. Поражают человеческий организм в основном такие грибки как:
Все грибковые заболевания выглядят по разному, зачастую отличить их разновидность не так-то просто, пораженные участки тела, как правило, подвергаются забору материала на анализ и уже после делается вывод о виде патогена и его характеристиках.
Как выглядят грибковые заболевания кожи, микозы и подкожные поражения можно судить только по характерным образованиям, которые обычно сопутствуют с зудом и болью. Это как мелкие бляшки небольшого размера, так и обширные поражения кожи в виде мицелия с основным очагом, которые быстро распространяются. В том передается ли грибок ногтей на руках, ногах, коже волосах и ногтях нет сомнений и при виде любых поражений у других людей рекомендуется избегать контакта с этим человеком.
Микоз ногтя
Микоз, дерматомикоз, а в случае с грибком ногтя онихомикоз, является также инфекционным заболеванием, передающимся бытовым путем. Чем опасен грибок ногтей и как влияет грибок ногтей на организм важно знать при случившемся заражении. Грибок ногтя, стоп, ногтей рук поражает не только поверхность нахождения, но и:
После всех вышеперечисленных минусах заболевания заразившийся задается вопросом можно ли умереть от грибка ногтей, однозначно нет, но невылеченный микоз ногтя приводит к куда более сложным последствиям, чем кажется на первый взгляд и негативно влияет на организм. Борьба с грибком на ногтях любой этиологии это необходимое и экстренное мероприятие, не всегда вылечить грибок на поздней стадии задача легкая.
К общим симптомам и проявлением грибка на ногтях относят:
Эти и многие другие симптомы любых изменений ногтей руки и ног свидетельствуют о наличии грибка ногтей. Для установления более точного диагноза необходимо обратиться к микологу. Но, как правило, каждый второй случай заболевания ногтей и стоп является грибковым.
Лечение и профилактика
Можно ли избавится от грибка в домашних условиях, вопрос который первым приходит на ум тем кому не посчастливилось стать обладателем этого неприятного заболевания. Ответ на этот вопрос однозначный, избавиться самостоятельно и диагностировать грибковое заболевание невозможно.
Необходима помощь специалиста, так как даже квалифицированный миколог и врач дерматолог не в состоянии на глаз определить характер и наличие именно грибкового поражения. Необходимо проведение лабораторного исследования и уже на основе этого применяется правильно подобранный метод лечения грибка.
Последствия запущенной формы грибкового заболевания непредсказуемы, так как грибок поражает не только отдельные участки, но и весь организм в целом. Особенно риску осложнений подвержена возрастная группа пациентов. Ниже рекомендации профилактики заболевания и советы как избежать заражения грибком:
Выводы
Как бороться с грибком и что делать если на ногтях грибок мы узнали из вышеописанного материала. В одном мнения сходятся при эффективной борьбе с любым грибковым заболеванием необходима помощь специалиста, заниматься самолечением и запускать течение болезни крайне не рекомендовано. А также важно не недооценивать элементарные методы профилактики и защиты от заражения.
Kocuria kristinae чем опасны

Поиск
Состояние краев век в зависимости от выявленной бактериальной флоры у пациентов с задними блефаритами, сочетанными с демодекозным поражением век
М.М. ШОКИРОВА, В.Г. КОПАЕВА, З.Г. МАЛЫШЕВА, Т.А. СИМОНОВА
МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова МЗ РФ, г. Москва, 127486, Бескудниковский бульвар, д. 59а
Копаева Валентина Григорьевна — доктор медицинских наук, профессор Научно-образовательного центра, тел. (499) 488-84-44, e-mail: [email protected]
Шокирова Мехринисо Махмадзокировна — аспирант, e-mail: [email protected]
Малышева Зоя Георгиевна — заведующая клинико-диагностической лабораторией, тел. (499) 488-85-59, e-mail: [email protected]
Симонова Татьяна Алексеевна — старший научный сотрудник клинико-диагностической лаборатории, тел. (499) 488-72-66, e-mail: [email protected]
Изучен состав микрофлоры конъюнктивальной полости (КП) и состояния краев век в зависимости от выявленного возбудителя у пациентов с задними блефаритами, сочетанными с демодекозным поражением век (ЗБДВ). Обследовано 210 пациентов с диагнозом ЗБДВ. Проводили микроскопию эпилированных ресниц, бактериологическое исследование мазка с конъюнктивы. Оценивали уровень гиперемии конъюнктивы и края век и выделительную функцию мейбомиевых желез (МЖ). При микроскопии ресниц в 100% случаев обнаруживали клещей рода Demodex. В конъюнктивальной полости в 6,4% случаев — нормальная микрофлора, в 76,5% — условно патогенная и в 17,1% случаев — отсутствие роста бактерий. Выявленная микрофлора КП в 85% случаев была чувствительна к фторхинолонам четвертого поколения. Уровень различий в гиперемии конъюнктивы и краев век при наличии бактерий, влияющих на состав липидов в секрете МЖ, и при наличии других видов бактерий в КП не был статистически достоверен. Полная облитерация устьев протоков МЖ была выявлена в 21,2% случаев у пациентов с наличием бактерий, влияющих на состав липидов в секрете МЖ, и в 7,2% — при наличии других видов бактерий. Степень выраженности гиперемии конъюнктивы и краев век у пациентов с ЗБДВ при наличии в КП бактерий, влияющих и не влияющих на состояние липидов в секрете МЖ, не имеет статистически достоверных различий. Однако постоянное нахождение в секрете МЖ бактерий, влияющих на состояние липидов, усугубляет застойные явления, способствует сужению и облитерации выводных протоков МЖ, несмотря на отсутствие в отдельных случаях ярких воспалительных явлений.
Ключевые слова: задний блефарит, микрофлора, чувствительность к антибиотикам, мейбомиевы железы, Demodex.
M.M. SHOKIROVA, V.G. KOPAEVA, Z.G. MALYSHEVA, T.A. SIMONOVA
Condition of the eyelids margins depending on the detected bacterial flora in patients with posterior blepharitis combined with demodectic lesion of the eyelids
The S. Fyodorov Eye Microsurgery Federal State Institution, 59а Beskudnikovskiy Blvd., Moscow, Russian Federation, 127486
Kopaeva V.G. — D. Med. Sc., Professor of the Scientific and Educational Center, tel. (499) 488-84-44, e-mail: [email protected]
Shokirova M.M. — post-graduate student, e-mail: [email protected]
Malysheva Z.G. — Head of the Clinical and Diagnostic Laboratory, tel. (499) 488-85-59, e-mail: [email protected]
Simonova T.A. — Senior Researcher of the Clinical Diagnostic Laboratory, tel. (499) 488-72-66, e-mail: [email protected]
The composition of microflora of the conjunctival cavity (CC) and the state of the eyelid edges depending on the revealed pathogen in patients with posterior blepharitis combined with demodicosis of eyelids (PBDEL) were studied. 210 patients with a diagnosis of PBDEL were examined. Microscopy of epilated eyelashes, bacteriological examination of the smear from the conjunctiva was performed. The level of hyperemia of the conjunctiva and the margin of the eyelids and the excretory function of the meibomian glands (MG) were assessed. At a microscopy of eyelashes in 100% of cases were found ticks of a sort Demodex. In the conjunctival cavity in 6.4% of cases — normal microflora, in 76.5% of cases — conditionally pathogenic and in 17.1% of cases — lack of bacterial growth. The revealed microflora of CC in 85% of cases was sensitive to fluoroquinolones of the fourth generation. The level of differences in conjunctival hyperemia and eyelid margins in the presence of bacteria that affect the lipid composition in meibum secretion, and in the presence of other bacterial species in the CC, was not statistically significant. Complete obliteration of the mouths of meibum ducts was detected in 21.2% of cases in patients with the presence of bacteria that affect lipid composition in meibum secretion and in 7.2% in the presence of other bacterial species. Manifestation rate of conjunctival hyperemia and eyelids in patients with PBDEL in the presence of bacteria in CC, which affect and do not affect the state of lipids in the secret of meibum, does not have statistically significant differences. However, the constant presence of bacteria in meibum, which affect the lipid state, exacerbates stagnant phenomena, contributes to narrowing and obliteration of the excretory ducts of the meibum, despite the absence of bright inflammatory phenomena in some cases.
Key words: posterior blepharitis, microflora, antibiotics sensitivity, meibomian glands, Demodex.
По мнению многих авторов, хронические блефариты могут являться следствием изменения липидов секрета мейбомиевых желез (МЖ) под действием липазы местной бактериальной флоры с последующей закупоркой отверстий выводных протоков МЖ и развитием обструктивной формы дисфункции мейбомиевых желез (ДМЖ) как наиболее частой формы функционального нарушения МЖ 1. По данным литературы, воспаление краев век расценивается как центральное патофизиологическое звено воспалительного процесса [5, 6].
Три основных вида бактерий — S.аureus, S.epidermidis и Corynеbacterium xerosis, паразитирующих в конъюнктивальной полости (КП) и на краях век, производят липазы, которые могут повлиять на состав липидов МЖ. Они запускают воспалительный процесс [7]. Закупоренные протоки являются благоприятной средой для роста и развития клещей демодекса и бактерий. Клещи и бактерии в свою очередь провоцируют дальнейшее развитие воспалительных процессов, которые могут способствовать развитию кист, ячменей, халязионов, язвы или флегмоны [8].
Постоянное нахождение клещей демодекса и бактерий в конъюнктивальной полости способствует развитию хронического процесса с последующим сужением и облитерацией выводных протоков МЖ. Однако известно, что S. epidermidis высевается с высокой частотой с кожи век и из конъюнктивальной полости как у здоровых лиц, так и у больных с блефаритами. Corynеbacterium xerosis считается нормальной микрофлорой конъюнктивальной полости [9]. Наличие этой флоры в конъюнктивальной полости при ЗБДВ не всегда вызывает воспалительную реакцию. Исходя из этого, изучение состава микрофлоры конъюнктивальной полости и состояния краев век в зависимости от выявленного возбудителя является актуальной задачей.
Цель исследования — изучение состава микрофлоры конъюнктивальной полости и состояния краев век в зависимости от выявленного возбудителя у пациентов с задними блефаритами, сочетанными с демодекозным поражением век.
Материал и методы
Исследования проведены у 210 пациентов с задними блефаритами, сочетанными с демодекозным поражением век. Изучен анализ данных, полученных при первичном обращении больных. Лабораторные исследования включали: бактериологическое исследование мазка с конъюнктивы, посев бактериологического материала для определения видовой принадлежности микроорганизмов и их чувствительности к антибиотикам, микроскопирование эпилированных ресниц с целью обнаружения клеща демодекса. Выделенные из конъюнктивальной полости культуры микроорганизмов исследовали на чувствительность к антибиотикам: хлорамфеникол, доксицилин, ципрофлоксацин, офлоксацин, левофлоксацин, гентамицин, эритромицин.
Спектр выбранных антибиотиков определялся прежде всего видовой принадлежностью бактерий, встречающихся в офтальмологической практике. Выделительную функцию протоков МЖ оценивали по методике (M.S. Norn, 1994) следующим образом: в норме на крае века видны отверстия выводных протоков МЖ. При стенозе выводные протоки не контурируются, но при надавливании выделяется капля секрета. При облитерации протоков секрет отсутствует.
Оценку степени выраженности закупорки протоков МЖ определяли по состоянию их устьев на межреберном пространстве век. Выделили три группы: до 10 закупоренных устьев 1/3 (1-я степень), до 20 — 2/3 (2-я степень) и выше 20 (3-я степень), что означает закрытие всех устьев протоков МЖ, с учетом того, что на каждом веке имеется до 30 отверстий протоков МЖ. Оценку наличия гиперемии краев век осуществляли по 4-балльной системе: 0 баллов — отсутствие гиперемии; 1 балл — наличие легких проявлений; 2 — умеренные проявления; 3 балла — выраженные проявления. Затем результаты суммировали и усредняли. Исследование проведено в отделе терапевтической офтальмологии (зав. проф. Д.Ю. Майчук) и в отделении санитарной и клинической микробиологии (зав. З.Г. Малышева).
Результаты и обсуждение
Изучение спектра микроорганизмов, находящихся в конъюнктивальной полости, показало: среди коагулазонегативных стафилококков превалировал S.epidermidis — 97 (46%); значительно в меньшей степени S.warneri — 7 (3,3%); в трех случаях (1,4%) обнаружен S.haemolyticus и в единичных случаях выявлены S.сaprae и S.hominis. Коагулазопозитивный стафилококк S.aurеus обнаружен у 26 (12,4%) пациентов.
Стрептококки выявлены у 18 больных (8,5%): S.mitis — у 7; S.mutans — у 4; S.salivarius –у 4; S.gallolyticus — у 1; S.constellatus — у 2. Бактерии группы кишечной палочки представлены Enterobacter cloаcea в четырех случаях (1,9%). Энтерококки выделены у двух пациентов (0,9%). Сorynеbacterium xerosis выявлен у 9 пациентов (5,1%), Кocuria kristinae — у 4 (2,2%) пациентов. В одном случае выявлена неферментирующая бактерия Pseudomonas putida.
Отсутствие бактерий отмечали у 36 (17,1%) пациентов. Сочетанное обсеменение двумя видами бактерий выявлено у 20 пациентов (9,5%). В основном наличие эпидермального стафилококка сочеталось со следующими видами бактерий: S.haemolyticus — 2; S.warneri — 3; S.aurеus — 6; Corynеbacterium xerosis — 1; Kocuria kristinae — 1; Enterobacter clocea — 2; S.salivarius — 2, S.mitis — 3.
Таким образом, общая картина микрофлоры конъюнктивальной полости у пациентов с ЗБДВ такова: Патогенные бактерии в КП отсутствовали; в 17,1% случаев наблюдалось отсутствие роста бактерий; в 6,4% — встречалась нормальная микрофлора (Сorynebacterium xerosis, Кocuria kristinae); в 76,5% случаев — условно-патогенная микрофлора (все остальные бактерии выявленные в конъюнктивальной полости), что подтверждает важную роль условно-патогенной микрофлоры в развитии данного заболевания.
Степень выраженности гиперемии конъюнктивы и краев век, оцениваемая по 4-балльной системе, при наличии бактерий, влияющих на состояние липидов секрета МЖ, и при наличии других видов бактерий в конъюнктивальной полости, не имела статистически выраженных отличий (1,8±0,7/1,7±0,6 по сравнению с 1,7±0,6/1,6±0,5). Примеры роста колоний бактерий, влияющих на состояние липидов в секрете мейбомиевых желез, показаны на рис. 1.
Рисунок 1.
Примеры роста колоний микроорганизмов, влияющих на состояние липидов в секрете МЖ
Результаты оценки выделительной функции протоков МЖ показали, что большее количество облитерированных протоков МЖ наблюдалось у пациентов с наличием бактерий, влияющих на состояние липидов в секрете мейбомиевых желез. При этом полная закупорка устьев протоков МЖ наблюдалась у 21,2% больных (табл. 1).
Таблица 1.
Степень закупорки устьев протоков мейбомиевых желез (n=210)
| Бактерии конъюнктивальной полости | Градации закупоренных устьев протоков МЖ | |||||||
| 1/3 (1-я степень) | 2/3 (2-я степень) | 3/3 (3-я степень) | ||||||
| n | % | n | % | n | % | |||
| Влияющие на липиды в секрете мейбомиевых желез (n=132) | 50 | 37,9 | 54 | 40,9 | 28 | 21,2 | ||
| Другие бактерии (n=42) | 30 | 71,4 | 9 | 21,4 | 3 | 7,2 | ||
| Отсутствие бактерий (n=36) | 21 | 58,3 | 10 | 27,8 | 5 | 13,9 | ||
Учитывая тот факт, что Сorynebacterium xerosis и Кocuria kristinae являются нормальной микрофлорой конъюнктивальной полости, посев этих бактерий на чувствительность к антибиотикам нами не проводился. Соответственно, исследование чувствительности к антибиотикам проведено у 161 пациента.
Результаты данного исследования у пациентов ЗБДВ выявили наиболее высокую чувствительность к антибиотикам группы фторхинолонов: левофлоксацину (85%) и офлоксацину (77,6%). Максимальная резистентность выделенной микрофлоры была отмечена к эритромицину (37,9%) и хлорамфениколу (40,4%) (табл. 2).
Таблица 2.
Чувствительность микрофлоры конъюнктивальной полости к антибиотикам (n=161)
| Препараты | Микрофлора конъюнктивальной полости | ||||||
| Чувствительная | Слабо чувствительная | Резистентная | |||||
| n | % | n | % | n | % | ||
| Левофлоксацин | 137 | 85 | 8 | 5,1 | 16 | 9,9 | |
| Офлоксацин | 125 | 77,6 | 22 | 13,8 | 14 | 8,6 | |
| Ципрофлоксацин | 113 | 70,2 | 38 | 23,6 | 10 | 6,2 | |
| Гентамицин | 123 | 76,4 | 12 | 7,5 | 26 | 16,1 | |
| Хлорамфеникол | 77 | 47,8 | 19 | 11,8 | 65 | 40,4 | |
| Эритромицин | 87 | 54 | 13 | 8,1 | 61 | 37,9 | |
Таким образом, в развитии задних блефаритов, сочетанных с демодекозным поражением век, выявлена важная роль бактерий (условно патогенной микрофлоры). Степень выраженности гиперемии конъюнктивы и краев век при наличии бактерий, выделяющих липазы, которые влияют на состояние липидов в секрете МЖ, и при наличии других видов бактерий в КП статистически не существенна. Однако у ряда пациентов (21,2%) с наличием бактерий, влияющих на состояние липидов в секрете мейбомиевых желез, выявлена полная облитерация устьев протоков МЖ.
Постоянное нахождение бактерий, влияющих на липиды в секрете мейбомиевых желез в конъюнктивальной полости у пациентов с ЗБДВ, статистически достоверно усугубляет застойные явления (p