Клюйверы (род Kluyvera)
Клюйверы — условно-патогенные бактерии, относящиеся к семейству Enterobacteriaceae, роду Kluyvera. Род состоит из 4 видов: К. ascorbata, К. cryocrescens, К. cochleae, К. georgiana. Типовой вид — К. ascorbata. Обитают в сточных водах, почве, воде, различных пищевых продуктах. Заболевания вызывают редко. Выделяются из патологического материала от человека, преимущественно из дыхательных, мочевыводящих путей, из фекалий, крови.

Рис. 3.46. Мазок из чистой культуры Е. cloacae. Окраска по Граму.
Энтеробактеры — прямые грамотрицательные палочки размером (0,5-1,0 х 1,0-3,0 мкм), располагающиеся поодиночно, парами, иногда — короткими цепочками. Подвижны (перитрихи). Факультативные анаэробы. Отличаются множественной устойчивостью к антибиотикам

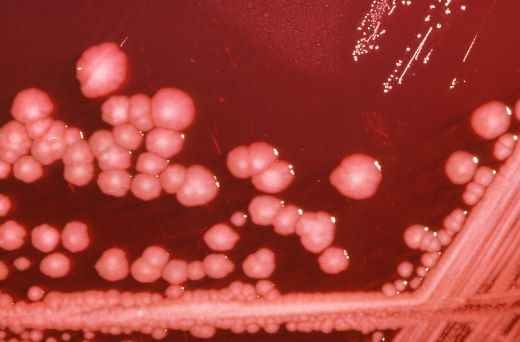
Рис. 3.47. Мазок из чистой культуры К. ascorbata. Окраска по Граму.
Бактерии рода Kluyvera представляют собой прямые грамотрицательные палочки с закругленными концами (0,5-0,7 х 2,0-3,0 мкм). Подвижны (перитрихи). Факультативные анаэробы
Болезнь Лайма: особенности клещевого боррелиоза
Никакое другое инфекционное заболевание не вызывает столько вопросов, как клещевой боррелиоз. Причинами этому являются многообразие клинической картины заболевания, различные мнения специалистов относительно диагностики и лечения данного заболевания и низкая информированность населения о данном заболевании. В данном обзоре мы постараемся предоставить наиболее объективную информацию о данном заболевании, насколько это возможно в настоящее время. Этот обзор основан, в основном, на данных Европейских экспертов (EUCALB).
Что такое боррелиоз (болезнь Лайма)
Возбудители
Эпидемиология
Риск заболеть боррелиозом после укуса клеща значительно выше, чем клещевым энцефалитом. Природные очаги клещевого боррелиоза совпадают с ареалом иксодовых клещей. Заболеваемость боррелиозом имеет сезонный характер и совпадает с активностью клещей. Первых пациентов с укусами клещей обычно регистрируют уже в марте-апреле. Последних, при наличии теплой погоды, регистрируют даже в октябре. Пик активности приходится на май-июнь. Процент инфицированных боррелиозом клещей отличается в разных регионах. Клещ одновременно может быть инфицирован боррелиями, вирусом клещевого энцефалита и другими возбудителями. Поэтому возможно развитие микст-инфекции.
Передача инфекции осуществляется трансмиссивным путем при укусе клеща (инокуляция), хотя не исключается возможность инфицирования и при попадании фекалий клеща на кожу, с последующим их втиранием при расчесах (контаминация). В случае разрыва клеща, при неправильном удалении? возбудитель может попасть в рану. Обсуждается алиментарный путь заражения при употреблении сырого козьего или коровьего молока.
Патогенез
На поздних сроках заболевания боррелии, играя роль пускового механизма, провоцируют развитие иммунопатологических процессов, имеющих большое значение для патогенеза нейроборрелиоза и хронических артритов. Среди подобного рода больных наиболее часто встречаются лица с генотипом HLA-DR2 и HLA-DR4. Уже на ранних сроках заболевания происходит выработка специфических антител, титр которых нарастает в динамике заболевания. Иммунный ответ наиболее выражен на поздних сроках, особенно при поражении суставов. При эффективной терапии и выздоровлении происходит нормализация уровня антител. Длительное их сохранение или появление в высоких титрах на поздних сроках свидетельствует о персистенции возбудителя даже при отсутствии клинических проявлений.
Боррелиозная инфекция
Стадия 1. Ранняя локальная инфекция
Характеризуется развитием на месте внедрения возбудителя первичного аффекта в виде хронической мигрирующей эритемы Афцелиуса-Липшютца, представляющей собой одиночное (иногда несколько) округлое красное пятно на месте укуса, которое в течение нескольких недель, постепенно центробежно разрастаясь, достигает 15-20 см и более в диаметре.
Стадия 2. Ранний диссеминированный боррелиоз
Для 2-й стадии заболевания, обусловленной лимфогенной и гематогенной диссеминацией возбудителя и развивающейся со 2-й по 21-ю неделю болезни (чаще на 4-5-й неделе), характерны поражения нервной системы (серозный менингит, неврит черепномозговых нервов, радикулоневрит), сердечно-сосудистой системы (миокардит, перикардит, нарушений проводимости (особенно атриовентрикулярной блокады). Нередко возникает гриппоподобный синдром (головная боль, лихорадка, слабость, миалгии). Поражения кожи на этой стадии могут носить характер вторичных кольцевидных элементов диаметром 1-5 см, эритематозной сыпи на ладонях по типу капилляритов, уртикарных высыпаний, а также доброкачественной лимфоцитомы кожи Шпиглера.
Стадия 3. Поздний хронический боррелиоз
3-я стадия заболевания характеризуется поражением суставов. Она начинается через 2 месяца и позже от начала болезни, иногда через 1-2 года. Обычно поражаются крупные суставы, особенно коленные, нередко с односторонней локализацией. В ряде случаев развивается симметричный полиартрит. Артриты, как правило, рецидивируют в течение нескольких лет и приобретают хроническое течение с деструкцией костей и хрящей. На поздней стадии заболевания персистирование возбудителя в организме больного приводит к хроническому течению болезни.
Диагностика
ПЦР-тестирование на наличие генетического материала возбудителя в данном случае малоэффективно. Антитела класса IgG могут выявляться на 1-3 неделях после инфицирования, максимальное количество IgG-антител синтезируется через 1,5-3 месяца после инфицирования. Антитела класса IgG часто не выявляются на ранней, локализованной стадии заболевания или при рано назначенной антимикробной терапии. Антитела класса IgG циркулируют в крови длительный срок (от нескольких месяцев до нескольких лет), даже после успешной антимикробной терапии и излечения инфекции. Иммунитет против боррелий не является стерильным. У переболевших людей возможно повторное заражение через несколько лет. Ложноположительные результаты определения антител класса IgG к боррелиям могут быть обусловлены присутствием в крови специфических антител при заболеваниях, вызываемых спирохетами (сифилис, возвратный тиф); низкий уровень антител IgG возможен при инфекционном мононуклеозе, гепатите В, ревматических болезнях (СКВ), заболеваниях периодонта, у 5-15 % здоровых лиц из эпидемической зоны.
Материал для исследования: сыворотка крови.
Забор материала на исследование: кровь берется в вакуумную пробирку без консервантов.
Подготовка к исследованию: специальной подготовки не требуется.
Исследование проводится иммуноферментным методом (ИФА)
Единицы измерения: качественный результат.
Положительный результат исследования свидетельствует о текущей или перенесенной в прошлом инфекции. Это может иногда приводить к неверной оценке результатов исследования, если клиническая картина заболевания нетипична.
Отрицательный результат исследования может быть при отсутствии инфицирования, при проведении исследования в ранние сроки заболевания или в отдалённые сроки после перенесенной инфекции. Нужно помнить, что отсутствие антител не исключает раннюю инфекцию, но действительно исключает хронический боррелиоз.
При получении сомнительного результата исследование необходимо повторить через 10-14 дней.
В принципе, на основании только серологических исследований нельзя определить необходимость назначения лечения и нельзя оценить эффективность терапии. Эти проблемы должны решаться индивидуально с учётом клинических данных.
Лечение
Больные со среднетяжелым течением болезни Лайма подлежат обязательной госпитализации в инфекционный стационар на всех стадиях заболевания. Пациенты с легким течением болезни (клещевая эритема, при отсутствии лихорадки и явлений интоксикации) могут лечиться дома. В качестве этиотропных препаратов используют антибиотики, выбор которых, доза и длительность применения зависят от стадии заболевания, преобладающего клинического синдрома и тяжести. Все укушенные клещами и переболевшие болезнью Лайма подлежат диспансерному наблюдению на протяжении 2 лет.
При возникновении поздних проявлений боррелиоза пациенты лечатся в специализированных стационарах (ревматологическом, неврологическом, кардиологическом) по клиническим показаниям. Реконвалесценты боррелиоза с остаточными явлениями наблюдаются узкими специалистами в зависимости от поражения той или иной систем (невропатологом, кардиологом, ревматологом).
Профилактика
Вопрос о пользе профилактики боррелиоза после укуса клеща с помощью антибиотиков спорный. Назначение антибиотиков в первые дни после укуса может снизить риск заболевания. Но назначаться они должны только врачом. Если укус произошел, то необходимо срочно обратится за медицинской помощью.
В связи с отсутствием мер специфической профилактики особое значение имеют выявление больных по ранним клиническим признакам и обязательная антибиотикотерапия по рациональной схеме, позволяющая избегать тяжелых поздних осложнений.
Семейство Enterobacteriaceae. Часть 1
Автор: врач – клинический фармаколог Трубачева Е.С.
.jpg)
Автор: врач – клинический фармаколог Трубачева Е.С.
Morganella spp. и Proteus spp.
Особо выдающихся представителей семейства Enterobacteriaceae мы уже разбирали в отдельных статьях, а именно представительницу рода Esherichia — кишечную палочку E.coli, а также одну из представительниц клебсиелл — Klebsiella pneumonia. В ближайших статьях мы постараемся осветить все оставшееся семейство, как, во-первых, одно из самых проблемных в плане развития резистентности к антимикробным препаратам, а во-вторых — как возбудителей, наиболее часто являющихся причиной внутрибольничных инфекций.
Микробиологические аспекты
Основными клинически значимыми представителями родов семейства Enterobacteriaceae, вызывающими заболевания у человека, являются:
Естественно совсем уж экзотику мы рассматривать не станем, но по наиболее часто встречающимся представителям обязательно пробежимся.
Клинические аспекты
Почему данное семейство так актуально? Наверное, потому, что почти ни одна нозология не обходится без его представителей. В самом широком смысле семейство Enterobacteriaceae является причиной следующих заболеваний:
Как мы видим, наши знакомые отметились практически везде. Но надо обязательно помнить, что выявление вышеуказанных представителей у здоровых людей из респираторного тракта, урогенитального и уж тем более желудочно-кишечного ни в коем случае не говорит о том, что человек чем-то болен, так как в большинстве своем эти микробы являются представителями нормальной микрофлоры, а не все люди умеют мыть руки, особенно летом.
Когда можно думать о наличии бактериальной патологии? Во-первых, когда имеется четкая клиника, во-вторых, когда микробы выделены из стерильных в норме сред, таких как кровь и ликвор, брюшная или плевральная полость, точнее, экссудат оттуда и, в-третьих, когда микроорганизмы выделены в клинически значимых концентрациях (тут в помощь будет ваша бак. лаборатория).
Стоит отметить еще один немаловажный момент — не все представители семейства Enterobacteriaceae умеют жить вне организма человека, и поэтому не размножаются во внешней среде, а потому обнаружение оных на пищевых продуктах и всевозможных поверхностях в лечебных учреждениях говорит о фекальном загрязнении, проще говоря, о неумении обрабатывать руки после посещения туалетной комнаты. Одним из таких микробов-детекторов является кишечная палочка, и стоит ее поймать даже не на руках персонала, а, например, на компьютерной мышке, как дальше можно уже ничего не искать, а начинать очередной этап избиения младенцев, пардон, обучения правилам асептики и антисептики, в частности, обработки рук.
Но давайте перейдем к частностям — и первым микроорганизмом, который будем сегодня рассматривать, станет:
Morganella spp.
Зверюшка названа так в честь своего первооткрывателя Гарри Р. Моргана.
Начнем традиционно с микробиологических аспектов
Семейство морганелл включает единственный вид M. morganii, включающий два подвида M. morganii и M. sibonii, которые различаются только ферментацией трегалозы.
Морганеллы являются представителями нормальной микрофлоры как человека, так и животных, а потому могут присутствовать в качестве сапрофитов в окружающей (внебольничной!) среде.
Морганеллы имеют довольно сложные отношения с антибактериальными препаратами и обладают природной резистентностью к:
Проявляют высокую чувствительность к:
Клинические аспекты
Как говорилось выше, морганеллы являются частью нормальной микрофлоры человека, крайне редко вызывая инфекционные заболевания. Чаще всего они являются возбудителями осложненных инфекций мочевыводящих путей.
Факторами риска развития инфекции являются:
В качестве механизмов резистентности морганеллы способны продуцировать бета-лактамазы, чем и объясняется их природная устойчивость к пенициллинам и цефалоспоринам 1-2 поколений. При нерациональном использовании антибиотиков они начинают вырабатывать бета-лактамазы расширенного спектра и факторы устойчивости к фторхинолонам, которыми довольно бодро делятся с соседями по семейству Enterobacteriaceae. Отдельно стоит отметить способность отдельных штаммов морганелл к резистентности к имипенему.
Какие заболевания вызывают чаще всего:
Терапевтические аспекты
Антибактериальная терапия будет полностью зависеть от результата из микробиологической лаборатории. Повторимся еще раз, микроб изначально умеет вырабатывать бета-лактамазы, а потому в случае развития осложненных инфекции мочевыводящих путей, которые чаще всего уже не связанны с кишечной палочкой, препаратами выбора становятся карбопенемы (имипенем, если штамм к нему чувствителен, или меропенем), дозирование которых проводится с учетом клиренса креатинина. Длительность лечения должна быть не менее 7 дней. В качестве альтернативы можно использовать цефалоспорин 4-го поколения Цефипим каждые 8 часов или фторхинолоны.
Аминогликозиды, несмотря на чувствительность к оным, при лечении заболеваний мочевыводящих путей лучше не применять в виду их нефро- и отоксичности, и по этой же причине их невозможно будет использовать около трех месяцев после проведенной терапии, например, в лечении синегнойной инфекции. Цефалоспорины третьего поколения тоже применять не стоит, так как морганеллы довольно быстро обзаводятся бета-лактамазами расширенного спектра, которые, как мы помним, эту генерацию препаратов быстро инактивируют.
Proteus spp.
Микробиологические аспекты
Протей долгое время был практически родным отцом морганеллы, так как последняя рассматривалась как один из видов рода протей. Этот род примечателен тем, что занимает почетное второе место по выявляемости после кишечной палочки в семействе Enterobacteriaceae.
В данный момент представителями рода протей являются P. mirabilis, вызывающий порядка 90% инфекционных заболеваний, а также P. vulgaris и P. penneri.
Клинические аспекты
Протеи выступают возбудителями порядка 10% неосложненных инфекций мочевыводящих путей, с чем могут быть связаны неудачи в лечении последних с использованием аминопенициллинов.
Как и все клинически значимые возбудители семейства Enterobacteriaceae, протей является возбудителем нозокомиальных инфекций, таких как пневмония, вплоть до сепсиса. Кроме того выступает возбудителем интраабдоминальных, а также хирургических инфекций кожи и мягких тканей, сепсиса, связанного с медицинскими вмешательствами как последствий нозокомиальной пневмонии в результате недостаточной дезинфекции, например, бронхоскопов.
Таким образом, мы видим, что, как и в предыдущем случае, проще правильно помыть руки и обработать инструменты, чем лечить это все с учетом природной и приобретенной резистентности.
Терапевтические аспекты
Как и в случае с морганеллой, нам просто необходим результат микробиологического исследования с определением чувствительности по МПК возбудителя либо результаты микробиологического мониторинга, которые помогут предположить зверей в случае неудачи ранее проводимого лечения.
В случае ампициллин-чувствительного P.mirabilis именно ампициллин может выступать препаратом первой линии. Кроме того, возможно использование цефуроксима и фторхинолонов. Обязательным аспектом лечения является его длительность. В случае неосложненных инфекций мочевыводящих путей (цистита) — не менее 3 дней, пиелонефрита — 10–14 дней, осложненных инфекций — 10–21 день. Сепсис является состоянием, требующим индивидуального подхода, но лечим не менее 14 дней.
На этом на сегодня мы закончим, но повторим одну базовую и, чего уж, наиважнейшую истину: в лечении инфекций, связанных с любым представителем семейства Enterobacteriaceae, самым главным будет являться профилактика. А именно правильное и тщательное мытье рук. Обеспечим мытье рук, не будет большинства проблем с инфекциями, вызванными указанным семейством.
Синдром «рука-нога-рот» или энтеровирусный везикулярный стоматит с экзантемой
Эти вирусы имеют достаточно широкое распространение среди населения, однако чаще поражают детей до 5 лет. Заболевание чаще встречается в весеннее-осенний период, иногда отмечается сезонный подъем заболеваемости по возвращении детей после отдыха с южных курортов. Инфекция передается воздушно-капельным путем, а также имеет фекально-оральный механизм передачи, т.е. факторами передачи помимо чихания и кашля могут быть игрушки, посуда и предметы обихода.
Вирусы этого семейства достаточно устойчивы во внешней среде — способны сохранять жизнеспособность в условиях комнатной температуры до 2-х недель.
Это острое инфекционное заболевание, вызываемое РНК-содержащими вирусами семейства пикорнавирусов : вирусами Коксаки А16, А5, А10, А9, В1, В3 и энтеровирусом 71.
По характерной клинической картине заболевание получило название синдрома «рука-нога-рот» (или энтеровирусный везикулярный стоматит с экзантемой) произошедшего от английского Hand-Foot-and-Mouth Disease (HFMD) и представляет собой симптомокомплекс, состоящий из поражения слизистой ротовой полости – энантемы и появления сыпи на верхних и нижних конечностях – экзантемы.
Инкубационный период длится от нескольких дней до 1 недели. Первыми проявлениями заболевания являются повышение температуры до 37,5-38,5 градусов, чувство недомогания, слабость, головная боль, саднение в горле. Такая симптоматика сохраняется несколько дней и очень напоминает симптомы любого ОРВИ. Но в отличие от ОРВИ, через 1-2 дня на коже кистей в области ладоней, на подошвах; несколько реже на бедрах и предплечьях появляется сыпь в виде везикул с прозрачным содержимым на фоне красно-розового цвета. Везикулы имеют в основном размеры до спичечной головки. Подобные высыпания появляются в области рта и в самой ротовой полости – носящие характер микроязвочек (афт), болезненных и чувствительных к контрастной пище. Все высыпные элементы имеют тенденцию к обратному развитию в течение нескольких дней.

Разрешающиеся высыпания в области ладоней и подошв могут оставлять достаточно выраженное шелушение в течение некоторого времени и, что характерно – у части заболевших спустя небольшое количество времени наблюдается расслаивание и растрескивание ногтевых пластин (ониходистрофия), что особенно пугает родителей и нередко служит поводом для поиска грибкового поражения. Эти проявления также полностью обратимы.
Прогноз заболевания чаще всего благоприятный. Наступает самопроизвольное выздоровление. Необходимо изолировать ребенка от остальных детей, т.к. он является крайне заразным для детского коллектива. Вся терапия сводится к симптоматическим средствам (жаропонижающие, антигистаминные), местно – растворы анилиновых красителей на везикулы (Фукорцин), полоскание полости рта слабыми растворами антисептиков (мирамистин, отвар ромашки), рекомендуется обильное питье, щадящая диета. Однако, редко, возможны осложнения в виде развития менингита, энцефалита. Тревожные симптомы при болезни «рука-нога-рот», которые позволят заподозрить неблагоприятное течение заболевания и требуют срочного вызова врача: повышение температуры выше 39º, стойкая высокая температура, появление рвоты (иногда многократной), усиление головной боли, боли в глазных яблоках, постоянный плач и капризность ребенка на фоне лихорадки, постоянная сонливость или наоборот психомоторное возбуждение пациента. При появлении таких симптомов необходимо немедленно вызвать скорую медицинскую помощь.
При подозрении на синдром «рука-нога-рот» Вы всегда можете проконсультироваться у педиатров, инфекционистов и дерматологов в клинике по телефонам: +7 495 735-88-99/ +7 495 735-88-77
или записаться на прием через форму обратной связи
Чем опасна вакцинация от коронавируса
Что известно о COVID-19?
Это РНК-содержащий вирус животного происхождения, относящийся к группе коронавирусов. Согласно данным ВОЗ, он передается от заболевшего человека через мелкие капли, которые выделяются при чихании и кашле из носа и рта. С момента заражения до появления первых симптомов проходит от 1 до 14 дней (в среднем – 7). Носитель вируса еще не знает о своей болезни, но в плане заражения уже представляет опасность для окружающих. По информации коронавирусной эпидемиологии, COVID-19 в 2-3 раза заразнее гриппа, но в 2-3 раза менее заразен, чем корь.
При легком течении болезни ее симптомы сходны с ОРВИ и заканчиваются выздоровлением через 14 дней без каких-либо дальнейших последствий. В тяжелых случаях COVID продолжается до 8 недель. Даже при отсутствии выраженных признаков заболевания у переболевших формируется иммунитет. Но учитывая, пусть и нечастые случаи повторного заражения, сохраняется он не слишком долго. Гораздо большим эффектом обладает вакцина.
Как действует вакцина?
Сегодня в мире используется несколько иммунопрепаратов, разработанных специалистами разных стран и прошедших необходимые клинические испытания. Все они предназначены для формирования иммунитета к возбудителю. После их введения иммунная система:
У человека, прошедшего вакцинацию, формируется стойкий иммунитет к COVID.
Опасна ли вакцинация?
Каждый человек реагирует на иммунопрепарат индивидуально. Поэтому даже самая качественная вакцина может вызвать побочные эффекты. Их появление на непродолжительное время – единственная опасность.
Чем опасна вакцинация от коронавируса:
Эти неприятные симптомы исчезают в течение нескольких дней.
Тяжелые состояния после введения иммунопрепарата могут развиваться у людей, имеющих противопоказания. Нельзя проводить вакцинацию, если наблюдаются:
При этих патологиях прививка может спровоцировать обострение.
Также противопоказанием является возраст (младше 18 и старше 65 лет), беременность, недавно перенесенная тяжелая форма коронавирусной инфекции. У переболевших людей в первое время после выздоровления отмечается высокий уровень антител, а вакцина повысит его еще больше. Последствия могут проявиться бурной иммунной реакцией в форме цитокинового шторма.
Как уменьшить негативные проявления?
Снизить развитие побочных явлений поможет соблюдение всех рекомендаций врача. Чтобы уменьшить риск развития негативных симптомов после вакцинации, нужно:
При отсутствии противопоказаний и соблюдении всех требований, риск побочных эффектов сводится к минимуму.
После прививки от коронавируса врачи советуют соблюдать щадящий режим и выпивать не менее 1,5 литров жидкости в день. При повышении температуры рекомендуется принять жаропонижающее средство. Если слабость не проходит в течение нескольких дней, появились аллергические реакции, нужно немедленно обратиться к доктору.
Когда будет массовая вакцинация?
Массовая вакцинация в США, Канаде и европейских странах началась еще в декабре прошлого года. В это же время стартовала она и в России. Но на начальном этапе мероприятие проводилось только для определенной категории лиц – молодых людей и тех, кто по роду своей профессиональной деятельности не может ограничить число контактов. Сегодня привиться от ковида можно в любом регионе страны.