Формула оксидов.
Классификация оксидов.
По классификации оксидов, солеобразующими оксидами являются те оксиды, которые могут взаимодействовать с кислотами либо основаниями с возможностью появления соответствующей соли и воды. Солеобразующими оксидами называют:
Основные оксиды, зачастую образующиеся из металлов со степенью окисления +1, +2. Могут реагировать с кислотами, с кислотными оксидами, с амфотерными оксидами, с водой (только оксиды щелочных и щелочно-земельных металлов). Элемент основного оксида становится катионом в образующейся соли. Na2O, CaO, MgO, CuO.
Примечание: металл менее активный, чем алюминий.
Амфотерные оксиды, образуют металлы со степенью окисления от +3 до +5 (к амфотерным оксидам относятся также BeO, ZnO, PbO, SnO). Реагируют с кислотами, щелочами, кислотными и основными оксидами.
При взаимодействии с сильной кислотой или кислотным оксидом проявляют основные свойства: ZnO + 2HCl → ZnCl2 + H2O
При взаимодействии с сильным основанием или основным оксидом проявляют кислотные свойства:
Несолеобразующие оксиды не вступают в реакцию ни с кислотами, ни с основаниями, а значит, солей не образуют. N2O, NO, CO, SiO.
В соответствии с номенклатурой ИЮПАК, названия оксидов складываются из слова оксид и названия второго химического элемента (с меньшей электроотрицательностью) в родительном падеже:
Если элемент может образовывать несколько оксидов, то в их названиях следует указать степень окисления элемента:
Можно использовать латинские приставки для обозначения числа атомов элементов, которые входят в молекулу оксида:
Часто используются также тривиальные названия некоторых оксидов:
Химия, Биология, подготовка к ГИА и ЕГЭ

Хлор — самый богатый на кислоты элемент!
5 кислот — таким рекордом может похвастаться не каждый!
Хлор — элемент 7-й группы главной подгруппы и к тому же 3-го периода.
Это означает много степеней окисления! 🙂
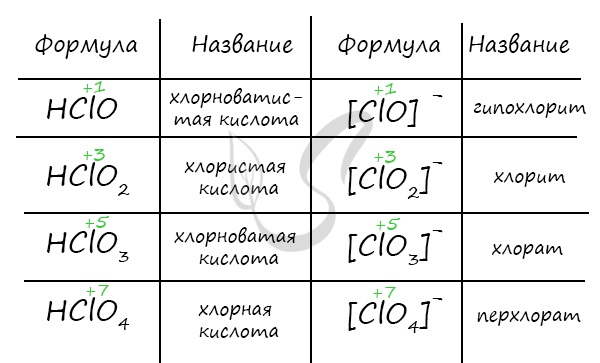
Кислоты хлора
Ей присущи все свойства кислот: взаимодействие с металлами до водорода, взаимодействие с основными оксидами, с основаниями, с солями.
При взаимодействии с окислителями окисляется до Cl2:
2HCl + H2SO4 = SO2 + Cl2↑ + 2H2O
2. HClO — хлорноватистая кислота.
Степень окисления хлора = +1.
Бесцветный раствор. Это очень слабая кислота. Неустойчивая. Небольшая степень диссоциации. Ей соответствует кислотный оксид Cl2O.
Получение:
Сl2 + H2O = HCl + HClO
НО: это сильная кислота-окислитель: 2HClO + H2S = S + Cl2 + H2O
3. HClO2 — хлористая кислота.
Степень окисления хлора = +3.
Бесцветная. Кислота средней силы. Неустойчивая. Ей соответствует кислотный оксид Cl2O3.
Проявляет окислительные свойства.
4. HClO3 — хлорноватая кислота.
Степень окисления хлора = +5
В свободном виде она не получена, «живет» только в растворах. Сильное вещество как просто кислота, и как кислота-окислитель. Кислотный оксид — Cl2O5.
Сильная кислота — окислитель: HClO3 + S + H2O= H2SO4 + HCl
5. HClO4 — хлорная кислота.
Степень окисления хлора= +7
Одна из самых сильных кислот, одна из самых сильных окислителей.
Взрывоопасна. Бесцветная, летучая, парит на воздухе.
Кислотный оксид — Cl2O7.
Обратите внимание на изменение свойств кислот с изменением степени окисления:
Соединения хлора
Хлороводород, соляная кислота (HCl)
Способы получения хлороводорода
Промышленный способ:
Лабораторный способ:
В лаборатории HCl получают действием концентрированной H2SO4 на хлориды:
Физические свойства хлороводорода
HCl хорошо растворяется в воде: при обычной температуре в 1 л воды растворяется
450 л газа (реакция экзотермическая). Насыщенный раствор содержит 36-37 % HCl по массе, имеет резкий, удушающий запах.
Химические свойства хлороводорода
Газообразный HCl
Безводный НСl химически инертен по отношению к металлам, оксидам и гидроксидам металлов, а также ко многим другим веществам. Что означает, что в отсутствие воды хлороводород не проявляет кислотных свойств.
И только при очень сильном нагревании газообразный HCl реагирует с металлами, даже такими малоактивными, как Сu и Аg.
Восстановительные свойства HCl проявляются также в малой степени:
Раствор HCl
Водный раствор HCl является сильной кислотой, т.к. молекулы HCl практически полностью распадаются на ионы:
Общие свойства кислот
Он проявляет все свойства кислот:
Вступает в реакции с органическими соединениями:
с аминами:
с аминокислотами:
Кислородсодержащие кислоты галогенов
Хлорноватистая кислота (HClO) и ее соли
Хлорноватистая кислота очень слабая кислота и существует только в разбавленных водных растворах.
Получение хлорноватистой кислоты:
Химические свойства хлорноватистой кислоты:
HClO + KI → KIO3 + HCl
2HBr + HClO → HCl + Br2 + H2O
4HClO + MnS → 4HCl + MnSO4
HClO + KOH → KClO + H2O
3HClO → 2HCl + НСlO3
Химические свойства солей хлорноватистой кислоты (гипохлоритов):
NaClO + 2HCl → NaCl + Cl2 + H2O
Хлористая кислота (HClO2) и ее соли
Хлористая кислота HClO2– слабая кислота, существует только в водных растворах, очень неустойчива
Способы получения хлористой кислоты:
Химические свойства хлористой кислоты:
Соли хлористой кислоты – хлориты
Хлорноватая кислота (HClO3) и ее соли
Хлорноватая кислота HClO3– существует только в водных растворах, в свободном виде не выделена. Является сильной кислотой
Получение хлорноватой кислоты:
Действием кислот на хлораты:
Химические свойства хлорноватой кислоты:
Соли хлорноватой кислоты – хлораты:
Получают хлораты при пропускании хлора через подогретый раствор щелочи:
Хлорная кислота (HClO4) и ее соли
Хлорная кислота HClO4– летучая, хорошо растворимая в воде жидкость, не имеющая цвета. Является сильной кислотой и сильным окислителем. Взрывоопасна. Кислотный оксид — Cl2O7, соли хлорной кислоты — перхлораты.
Получение хлорной кислоты
Перегонкой при пониженном давлении смеси перхлората калия с серной кислотой:
Химические свойства хлорной кислоты
Химические свойства солей хлорной кислоты – перхлоратов:
Оксиды хлора
Оксид хлора (I), оксид дихлора ( Cl2O)
В газообразном состоянии имеет темно-желтый цвет, в жидком состоянии – красно-бурый. Неустойчив на свету при повышении температуры.
Получение оксид хлора (I)
Химические свойства оксида хлора (I)
Оксид хлора (IV), диоксид хлора, двуокись хлора ( ClO2)
ClO2 – ядовитый газ желто-зеленого цвета с резким запахом. Взрывается при механическом воздействии, при нагревании до 100 ºС и при контакте с восстановителем
Получение двуокиси хлора
В промышленности ClO2 получают, пропуская оксид серы (IV) через подкисленный раствор хлората натрия NaClO3:
В лаборатории ClO2получают при взаимодействии хлората калия с щавелевой кислотой в присутствии концентрированной серной кислоты:
Химические свойства оксида хлора (IV)
6ClO2 + 3H2O = HCl + 5HClO3 (горячая вода)
Оксид хлора (VI), триоксид хлора (ClO3 (Cl2O6))
ClO3 (Cl2O6) – вязкая жидкость красного цвета. Соприкосновение с органическими веществами приводит к взрыву.
Получение оксида хлора (VI)
Получают окислением озоном ClO2
Химические свойства оксида хлора (VI)
Оксид хлора (VII) (Cl2О7)
Cl2О7 – тяжелая, маслянистая жидкость, не имеющая цвета. Наиболее устойчивый из всех оксидов хлора. Очень взрывоопасен.
Получение оксида хлора (VII)
Получают при взаимодействии оксида фосфора (V) с концентрированной хлорной кислотой:
Химические свойства Cl2O7
Проявляет кислотные свойства.
Кислородсодержащие соединения галогенов
Получение кислот
Хлорноватистую кислоту можно получить в реакции хлора с водой, соли хлорноватистой кислоты (гипохлорита) с более слабой кислотой.
В реакции хлорной извести с диоксидом углерода и водой также выделяется хлорноватистая кислота.
Хлорноватую кислоту получают взаимодействием разбавленной серной кислоты и хлората бария.
Химические свойства
HClO + LiOH → LiClO + H2O
И кислоты, и их соли разлагаются схожим образом.
KI + HClO → KIO3 + HCl
Соли этих кислот образуются в результате реакции диспропорционирования, происходящей между щелочью и галогеном.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Кислородсодержащие соединения галогенов
Кислородсодержащие соединения галогенов
Если сопоставить свойства кислот со структурой молекул, то можно отметить следующее: с ростом степени окисления хлора уменьшается число несвязывающих электронных пар и происходит постепенное достраивание кислородного окружения хлора до тетраэдрического.
Увеличение силы кислот HClO – HСlO4 обусловлено тем, что с ростом числа кислородных атомов электронные облака всё больше стянуты к центральному атому и связь Н – О становится всё более полярной.
Кислородсодержащие кислоты хлора
Возрастание силы кислот связано с увеличением количества кислорода, который оттягивает на себя электронную плотность и прочность связи Н – О ослабевает.
Возрастание устойчивости связано с увеличением степени окисления хлора и большим количеством электронов, принимающих участие в образовании связи. Во всех соединениях Cl – находится в состоянии sp 3 гибридизации.
Самая высокая окислительная способность у хлорноватистой кислоты, за счет атомарного кислорода, который достаточно быстро выделяется в результате разложения хлорноватистой кислоты.
HСlO = HCl + O
Растворяясь в воде, оксиды дают соответствующие кислоты. Будучи кислотными оксидами, реагируют с основаниями и основными оксидами с образованием соответствующих солей
Схемы разложения HСlO (зависят от условий протекания процесса)
1. HClO → HСl + O
3. 2HClO → Cl2O + H2O
Сама кислота, а также ее соли могут образоваться в результате реакции обменного взаимодействия, а также окислительно-восстановительных. Соли обладают отбеливающим эффектом в результате образования атомарного кислорода при разложении гипохлоритов
Cl2 + H2O → HCl + HClO
ClF + H2O → HClO + HF
Cl2 +2KOHхол → KCl + KClO + H2O
Гипохлорит калия термически разлагается по различным схемам:
2KClO → 2KCl + O2
KClO → KCl + KClO2 или KClO3, (KClO4)
Получение белильной извести
Белильная известь – смешанная соль (хлорид-гипохлорит кальция). Хлор имеет различную степень окисления, получают реакцией взаимодействия хлора с гидроксидом кальция
— 
под действием углекислого газа
4KClO3 → KCl + 3KClO4 –реакция диспропорционирования
Окислительные свойства почти не проявляет.
Хлорная кислота HClO4 –самая сильная кислота в ряду кислородсодержащих кислот хлора, окислительные свойства практически не проявляет, сама кислота и ее соли – перхлораты – достаточно устойчивые. Кислоту можно получить реакцией обменного взаимодействия с концентрированной серной кислотой. При нагревании перхлораты могут разлагаться по типу реакции внутримолекулярного окисления-восстановления.
2KClO4 → 2KCl + 4O2разложение
Самая высокая окислительная способность у хлорноватистой кислоты.