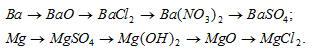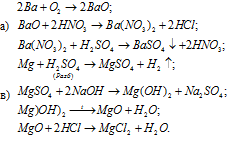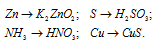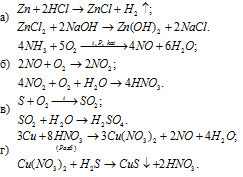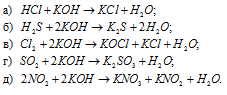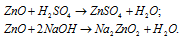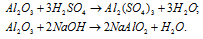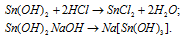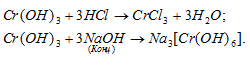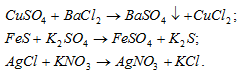Какой оксид соответствует h2so4
§8.2 Оксиды и их классификация.
Как мы уже знаем, оксиды бывают кислотные и основные. Это деление положено в основу их классификации.
Большинство кислотных оксидов хорошо реагирует с водой, давая кислоту. Например, кислый вкус простой газированной воды объясняется образованием угольной кислоты Н 2 СО 3 из кислотного оксида СО 2 :
СО 2 + Н 2 О = Н 2 СО 3 (угольная кислота)
В простейших случаях формулу образующейся кислоты легко получить из формулы кислотного оксида простым сложением. Например:
кислотный оксид (не растворим в воде)
соль кремниевой кислоты H 2 SiO 3
Полученную соль кремниевой кислоты можно превратить в саму кремниевую кислоту добавлением другой кислоты:
Na 2 SiO 3 + 2 HCl = H 2 SiO 3 + 2 NaCl
Таким образом, кислотному оксиду всегда соответствует определенная кислота :
CO 2 (оксид углерода) – H 2 CO 3 (угольная кислота) ;
SO 3 (оксид серы VI) – H 2 SO 4 ( серная кислота) ;
SiO 2 (оксид кремния) – H 2 SiO 3 ( кремниевая кислота).
Поскольку реакция с основаниями является общей для всех кислотных оксидов, им можно дать такое определение:
Оксиды, которые взаимодействуют с основаниями с образованием соли и воды, называются КИСЛОТНЫМИ ОКСИДАМИ.
** Кислотные оксиды, как мы видим, образованы в основном неметаллами. Вам следует запомнить только два оксида металлов, которые также являются кислотными. Это оксиды хрома и марганца, в которых металлы имеют НАИБОЛЬШУЮ из всех возможных степень окисления:
CrO 3 (оксид хрома VI) – H 2 CrO 4 (хромовая кислота) ;
Mn 2 O 7 (оксид марганца VII) – HMnO 4 (марганцовая кислота).
Осн о вные оксиды образуются только металлами. Некоторые из них легко реагируют с водой, давая соответствующее основание:
Li 2 O + H 2 O = 2 LiOH (основание – гидроксид лития).
Еще один пример – хорошо известная нам реакция получения гашеной извести из оксида кальция и воды.
CaO + H 2 O = Ca(OH) 2 (основание – гидроксид кальция).
Существует, однако большое количество нерастворимых основных оксидов. Их относят именно к основным оксидам благодаря реакциям с кислотами :
ZnO + H 2 O = реакция не идет (ZnO не растворим в воде);
ZnO + 2 HCl = ZnCl 2 (соль) + H 2 O
[ZnO + H 2 O] = Zn(OH) 2
Zn(OH) 2 + 2 HCl = ZnCl 2 (соль) + H 2 O
Каждому основному оксиду соответствует определенное основание:
MgO (оксид магния) – Mg(OH) 2 (гидроксид магния);
Fe 2 O 3 (оксид железа III) – Fe(OH) 3 (гидроксид железа III);
Na 2 O (оксид натрия) – NaOH (гидроксид натрия).
Таким образом, общее свойство основных оксидов заключается в способности реагировать с кислотами с образованием соли и воды.
Оксиды, которые взаимодействуют с КИСЛОТАМИ с образованием соли и воды, называются ОСНОВНЫМИ ОКСИДАМИ.
** Оксиды хрома и марганца, в которых металл имеет низшую степень окисления, являются обыкновенными основными оксидами (как и оксиды всех остальных металлов). Вот какие гидроксиды им соответствуют:
CrO (оксид хрома II) – Cr(OH) 2 (гидроксид хрома II);
MnO (оксид марганца II) – Mn(OH) 2 ( гидроксид марганца II).
Соединения хрома (II) крайне неустойчивы и быстро переходят в соединения хрома (III). С применением многих интересных оксидов мы уже познакомились в главе 6 «кислород».
8.6. Исходя из Периодической таблицы, напишите формулы оксидов следующих элементов: калия, бария, железа (II), хрома (III), хлора (VII), кремния (IV). Подчеркните формулы кислотных оксидов.
** 8.7. Исходя из Периодической таблицы, напишите формулы оксидов следующих элементов: германия Ge (одну формулу), селена Se (две формулы), фосфора P (две формулы), бора B (одну формулу), бериллия Be (одну формулу).
8.8. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ca → CaO → Ca(OH) 2 → CaSO 4
S → SO 2 → SO 3 → H 2 SO 4 → CaSO 4
8.9. Какой объем газообразного оксида серы (VI) при н.у. потребуется для нейтрализации раствора, получившегося при растворении 56 г CaO в воде?
§ 20. Кислородсодержащие соединения серы (VI)
К кислородсодержащим соединениям серы (VI) относятся их высшие формы — оксид серы (VI) SO3 и соответствующая ему серная кислота H2SO4.

Что вам известно о серной кислоте?
Оксид серы (VI) SO3
Состав и строение. Оксид серы(VI) называют также серным ангидридом или триоксидом серы. Отдельные молекулы его (в газообразном состоянии) имеют форму равностороннего треугольника, в центре которого — предельно окисленный атом серы, а в вершинах — атомы кислорода. Все четыре атома, составляющие молекулу SO3, расположены в одной плоскости, а валентные углы между ними равны 120°. Молекулы оксида серы (VI) склонны к полимеризации, т. е. к последовательному соединению друг с другом в более крупные молекулы.
Физические свойства. Оксид серы (VI) — бесцветная маслянистая жидкость, кипящая при 44,7 °С и кристаллизующаяся при 17 °С. При хранении, особенно в присутствии влаги, он полимеризуется и превращается в твердое прозрачное вещество (полимер), напоминающее лед и состоящее из длинных шелковистых кристаллов. Оксид серы (VI) малорастворим в воде, но хорошо растворяется в серной кислоте.
Химические свойства. SO3 — кислотный оксид. Растворяясь, он реагирует с водой, образуя серную кислоту. Это реакция экзотермическая и сопровождается выделением большого количества теплоты:

Получение. Оксид серы (VI) можно получить каталитическим окислением оксида серы (IV):

Реакция окисления оксида серы (IV) является обратимой. Она имеет огромное значение для промышленного получения серной кислоты.
При изучении химии вы познакомились с реакциями, идущими до конца, на примере реакций ионного обмена электролитов узнали, в каких случаях это происходит, т. е. познакомились с условиями необратимости реакций.
Серная кислота H2SO4
Серная кислота — молекулярное вещество, относящееся к сильным двухосновным кислотам. Структуру молекулы серной кислоты изображает ее модель, приведенная на рисунке 21.
Физические свойства. Безводная серная кислота — тяжелая бесцветная маслянистая жидкость, растворяющаяся в воде в любых соотношениях. Она гигроскопична, нелетуча, без запаха, не проводит электрический ток. При 10,3 °С она затвердевает, образуя кристаллы, похожие на лед. Серная кислота кипит при 296 °С с разложением. Серная кислота, поступающая в продажу, имеет плотность 1,84 г/см 3 (массовая доля серной кислоты около 96 %).
Серная кислота очень хорошо растворима в воде: она растворяется в ней в любых пропорциях.
Растворение концентрированной серной кислоты в воде — физикохимический экзотермический процесс.
При растворении серной кислоты в воде образуются гидраты и выделяется большое количество теплоты. Поэтому смешивать концентрированную серную кислоту с водой надо крайне осторожно, соблюдая следующее правило безопасности:
Кислоту осторожно тонкой струйкой вливают в воду, а не наоборот. Не вливать воду в кислоту, иначе произойдет сильное разбрызгивание разогретого и опасного раствора серной кислоты (рис. 22)!

Если, наоборот, вливать воду в кислоту, вода не будет опускаться вниз, а будет проникать лишь на небольшую глубину. Разогревание раствора вследствие идущей там реакции гидратации сосредоточится на поверхности. Раствор здесь может нагреться до кипения. Образующийся пар будет разбрызгивать кислоту (учитывая, что кислота имеет в 3 раза меньшую теплоемкость, чем вода).
Серная кислота — химически активное вещество. Однако следует иметь в виду, что свойства разбавленной и концентрированной серной кислоты весьма различны.

Охарактеризуйте серную кислоту как электролит.
Химические свойства разбавленной серной кислоты. В растворе серная кислота, будучи сильным электролитом, изменяет окраску индикаторов: лакмус становится красным, а метиловый оранжевый розовеет. Она ступенчато диссоциирует на ионы:

Проблема. Почему степень диссоциации по первой ступени намного выше, чем по второй?
Как двухосновная кислота серная кислота образует соли двух видов: средние — сульфаты (Na2SO4, CaSO4) и кислые — гидросульфаты (NaHSO4, Ca(HSO4)2 и др.)?

Серная кислота в растворе обладает общими для класса кислот химическими свойствами, которые обусловлены ионом Н + (Н3O + ). Они проявляются в реакциях ионного обмена и окислительно-восстановительных.
1. Окислительно-восстановительные реакции характерны для взаимодействия растворов серной кислоты с металлами.
Металлы, стоящие в ряду активности (в ряду напряжения) до водорода (за исключением свинца), окисляются ионом водорода кислоты, а сам он восстанавливается до молекулярного водорода.
Металлы, стоящие в ряду активности после водорода, с разбавленной серной кислотой не взаимодействуют (Сu, Ag, Pt, Аu).
2. Реакции обмена происходят при взаимодействии серной кислоты с основными и амфотерными оксидами, основаниями и солями.
Задание. Запишите молекулярные, полные и сокращенные ионные уравнения таких реакций.
Качественная реакция на серную кислоту и ее соли, с помощью которой можно распознать их среди других веществ, — реакция с растворимыми солями бария:
Суть процесса: выпадает белый осадок сульфата бария, нерастворимый ни в воде, ни в кислотах:

Катион бария Ва 2+ является реагентом на сульфат-ион

Опыт 1. Качественная реакция на сульфат-ион. Налейте в одну пробирку 1 мл раствора разбавленной серной кислоты, а в другую 1 мл раствора сульфата натрия. Прилейте в обе пробирки такой же объем раствора хлорида бария. Что наблюдаете? Во вторую пробирку добавьте немного раствора азотной кислоты. Что изменилось? Запишите уравнения реакций в полной и сокращенной ионной форме.
Опыт 2. Экспериментальная задача. В трех пробирках без этикеток находятся растворы серной кислоты, сульфата натрия и сульфита натрия. С помощью каких реактивов и в какой последовательности следует распознавать эти вещества? Составьте план исследования. Проделайте эти реакции. Запишите уравнения химических реакций.
Классификация неорганических веществ
Среди простых веществ выделяют металлы и неметаллы. Среди сложных: оксиды, основания, кислоты и соли. Классификация неорганических веществ построена следующим образом:
Большинство химических свойств мы изучим по мере продвижения по периодической таблице Д.И. Менделеева. В этой статье мне хотелось бы подчеркнуть ряд принципиальных деталей, которые помогут в дальнейшем при изучении химии.
Оксиды
Все оксиды подразделяются на солеобразующие и несолеобразующие. Солеобразующие имеют соответствующие им основания и кислоты (в той же степени окисления (СО)!) и охотно вступают в реакции солеобразования. К ним относятся, например:
Солеобразующие оксиды, в свою очередь, делятся на основные, амфотерные и кислотные.
Основным оксидам соответствуют основания в той же СО. В химических реакциях основные оксиды проявляют основные свойства, образуются исключительно металлами. Примеры: Li2O, Na2O, K2O, Rb2O CaO, FeO, CrO, MnO.
Основные оксиды взаимодействуют с водой с образованием соответствующего основания (реакцию идет, если основание растворимо) и с кислотными оксидами и кислотами с образованием солей. Между собой основные оксиды не взаимодействуют.
Li2O + H2O → LiOH (основный оксид + вода → основание)
Здесь не происходит окисления/восстановления, поэтому сохраняйте исходные степени окисления атомов.
Эти оксиды действительно имеют двойственный характер: они проявляют как кислотные, так и основные свойства. Примеры: BeO, ZnO, Al2O3, Fe2O3, Cr2O3, MnO2, PbO, PbO2, Ga2O3.
С водой они не взаимодействуют, так как продукт реакции, основание, получается нерастворимым. Амфотерные оксиды реагируют как с кислотами и кислотными оксидами, так и с основаниями и основными оксидами.
ZnO + KOH + H2O → K2[Zn(OH)4] (амф. оксид + основание = комплексная соль)
ZnO + N2O5 → Zn(NO3)2 (амф. оксид + кисл. оксид = соль; СО азота сохраняется в ходе реакции)
Fe2O3 + HCl → FeCl3 + H2O (амф. оксид + кислота = соль + вода; обратите внимание на то, что СО Fe = +3 не меняется в ходе реакции)
Проявляют в ходе химических реакций кислотные свойства. Образованы металлами и неметаллами, чаще всего в высокой СО. Примеры: SO2, SO3, P2O5, N2O3, NO2, N2O5, SiO2, MnO3, Mn2O7.
Кислотные оксиды вступают в реакцию с основными и амфотерными, реагируют с основаниями. Реакции между кислотными оксидами не характерны.
SO2 + Na2O → Na2SO3 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +4)
SO3 + Li2O → Li2SO4 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +6)
P2O5 + NaOH → Na3PO4 + H2O (кисл. оксид + основание = соль + вода)
Реакции несолеобразующих оксидов с основаниями, кислотами и солеобразующими оксидов редки и не приводят к образованию солей. Некоторые из несолеобразующих оксидов используют в качестве восстановителей:
FeO + CO → Fe + CO2 (восстановление железа из его оксида)
Основания
Основания классифицируются по количеству гидроксид-ионов в молекуле на одно-, двух- и трехкислотные.
Так же, как и оксиды, основания различаются по свойствам. Все основания хорошо реагируют с кислотами, даже нерастворимые основания способны растворяться в кислотах. Также нерастворимые основания при нагревании легко разлагаются на воду и соответствующий оксид.
Mg(OH)2 → (t) MgO + H2O (при нагревании нерастворимые основания легко разлагаются)
Если в ходе реакции основания с солью выделяется газ, выпадает осадок или образуется слабый электролит (вода), то такая реакция идет. Нерастворимые основания с солями почти не реагируют.
Ba(OH)2 + NH4Cl → BaCl2 + NH3 + H2O (в ходе реакции образуется нестойкое основание NH4OH, которое распадается на NH3 и H2O)
KOH + BaCl2 ↛ реакция не идет, так как в продуктах нет газа/осадка/слабого электролита (воды)
В растворах щелочей pH > 7, поэтому лакмус окрашивает их в синий цвет.
Al(OH)3 + HCl → AlCl3 + H2O (амф. гидроксид + кислота = соль + вода)
Al(OH)3 + KOH → K[Al(OH)4] (амф. гидроксид + основание = комплексная соль)
При нагревании до высоких температур комплексные соли не образуются.
Кислоты
Кислоты отлично реагируют с основными оксидами, основаниями, растворяя даже те, которые выпали в осадок (реакция нейтрализации). Также кислоты способны вступать в реакцию с теми металлами, которые стоят в ряду напряжений до водорода (то есть способны вытеснить его из кислоты).
Zn + HCl → ZnCl2 + H2↑ (реакция идет, так как цинк стоил в ряду активности левее водорода и способен вытеснить его из кислоты)
Cu + HCl ↛ (реакция не идет, так как медь расположена в ряду активности правее водорода, менее активна и не способна вытеснить его из кислоты)
Все кислоты подразделяются на сильные и слабые. Напомню, что мы составили подробную таблицу сильных и слабых кислот (и оснований!) в теме гидролиз. В реакции из сильной кислоты (соляной) можно получить более слабую, например, сероводородную или угольную кислоту.
В завершении подтемы кислот предлагаю вам вспомнить названия основных кислот и их кислотных остатков.
Блиц-опрос по теме Классификация неорганических веществ
Как решать задачи с участием кислот и оснований
Задача 140.
Написать формулы ангидридов указанных кислот: H2SO4; H3BO3; Н4P2O7; НОСI; HMnO4.
Решение:
Ангидридами кислот называют оксиды, которые при взаимодействии с водой образуют кислоту.
H2SO4 – серная кислота, которой соответствует ангидрид SO3;
H3BO3 – ортоборная кислота, которой соответствует ангидрид B2O3;
H4P2O7 – тетраметафосфорная кислота, которой соответствует ангидрид P2O5;
HOCl – хлорноватистая кислота, которой отвечает ангидрид Cl2O;
HMnO4 – марганцевая кислота, которой отвечает ангидрид Mn2O7.
Задача 141.
Написать формулы оксидов, соответствующих указанным гидроксидам: H2SiО3; Сu(ОН)2; Н3АsО4; Н2WO4; Fе(ОН)3.
Решение:
Задача 142.
Составить уравнения реакций, с помощью которых можно осуществить указанные превращения:
Решение:
Задача 143.
Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
Решение:
Задача 145.
Какие соли можно получить, имея в своем распоряжении CuSO4, AgNO3, К3PO4, ВаСI2? Написать уравнения реакций и назвать полученные соли.
Решение:
Имея в своём распоряжении CuSO4, AgNO3, К3PO4, ВаСI2 можно получить следующие соли:
а) При взаимодействии CuSO и К3PO4 образуется нерастворимая соль ортофосфат меди:
б) Реакция CuSO4 с ВаСI2 протекает с выпадением в осадок нерастворимого сульфата меди:
в) при взаимодействии AgNO3 и К3PO4 образуется нерастворимая соль фосфата серебра:
г) При сливании растворов AgNO3 и ВаСI2 выпадает осадок нерастворимого хлорида серебра:
д) При сливании растворов К3PO4 и ВаСI2 выпадает осадок нерастворимого ортофосфата бария:
Таким образом, можно получить следующие нерастворимые соли: Cu3(PO4)2 – ортофосфат меди (II); BaSO4 – сульфат бария; Ag3PO4 – ортофосфат серебра; AgCl – хлорид серебра; Ba3(PO4)2 – ортофосфат бария.
Задача 146.
Назвать следующие соединения: К2О2, МnO2, ВаО2, МnО, СrO3, V2O5.
Решение:
Задача 147.
Как доказать амфотерный характер ZnO, А12O3, Sn(ОН)2, Cr(ОН)3?
Решение:
а) ZnO – оксид цинка – амфотерный оксид, который реагирует с кислотами, образуя соль и воду, с основаниями – цинкаты.
б) А12O3 – оксид алюминия – амфотерный оксид, который реагирует с кислотами с образованием соли и воды, с основаниями – алюминаты.
в) Sn(ОН)2 – гидроксид олова (II) – амфотерный гидроксид, который реагирует с кислотами, образуя соль и воду, с основаниями – тригидроксостаннаты (II).
г) Cr(ОН)3 – гидроксид хрома (III) амфотерный гидроксид, который реагирует с кислотами, образуя соль и воду, с концентрированным раствором NaOH – гексагидроксохроматы (III).
Задача 148.
Можно ли осуществить в растворах указанные ниже реакции:
Решение:
а) Хлорид бария и другие его растворимые соли являются качественными реактивами на обнаружение ионов SO4 2– В результате реакции выпадает осадок нерастворимого сульфата бария: