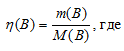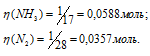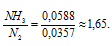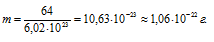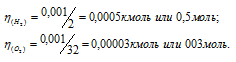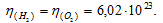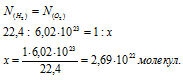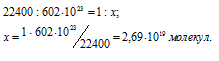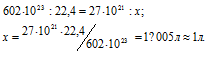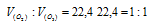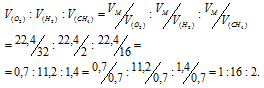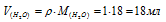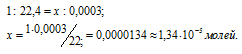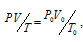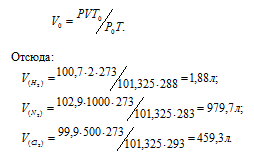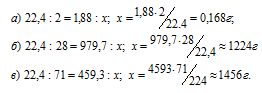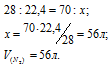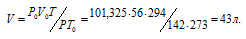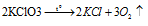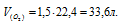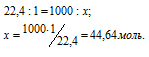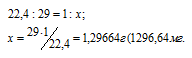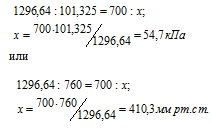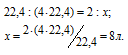ЧАСТЬ 1
1. 1 моль любого газа при н. у. занимает одинаковый объём, равный 22,4 л. Этот объём называется молярный и обозначается Vm.
2. Количество вещества (n) — отношение объёма газа при н. у. к молярному объёму: n = V/Vm=> Vm измеряется в л/моль.
3. Следовательно, количество вещества.
4. Дополните таблицу «Количественные характеристики веществ», делая необходимые вычисления.
ЧАСТЬ 2
1. Установите соотношение между названием и размерностью величины.
2. Укажите формулы, которые являются производными от основной формулы n = V/Vm.
2) V=n•Vm
3) Vm=V/n
3. Сколько молекул содержат 44,8 л (н. у.) углекислого газа? Решите задачу двумя способами.

4. Придумайте условие задачи, в которой нужно найти число молекул N, если известен объём V.
Найти число частиц оксида азота(II), если его объём равен 67,2 л.
Решите задачу любым способом.
5. Вычислите массу 78,4 л (н. у.) хлора.
6. Найдите объём 297 г фосгена (COCl2).
Как можно защитить себя во время химической тревоги? Приготовьте сообщение об устройстве противогаза.
Чем объясняется применение нашатырного спирта в медицине?
8. Придумайте задачу с использованием изученных понятий. С помощью компьютера создайте рисунок, иллюстрирующий данную задачу. Предложите способ её решения. Верно ли, что 22,4 л азота или 22,4 л водорода одинаковы по массе? Ответ подтвердите вычислениями.
Какой объем при нормальных условиях занимают 2 моль любого газа?
Кл. БИОЛОГИЯ, ХИМИЯ
На 28 апреля (биология)
Выполнить на отдельном двойном листике контрольную работу, дату указать 24 апреля. Условия заданий переписывать обязательно, указать правильный вариант ответа (все варианты ответов не переписывать) (Ф.И. укажите на полях)
Контрольная работа № 4
по теме: «Млекопитающие»
Часть 1. Выберите один правильный ответ.
1. Какой признак характерен только для представителей класса Млекопитающие?
А) проявляют заботу о потомстве;
Б) размножаются половым путем;
В) активно передвигаются;
Г) имеют млечные железы в коже.
В организме млекопитающего животного грудная и брюшная полости разделены
А) брюшной мышцей; В) грудной клеткой;
Б) диафрагмой; Г) поверхностью желудка.
В какой камере сердца начинается большой круг кровообращения?
А) левом желудочке; В) правом желудочке;
Б) левом предсердии; Г) правом предсердии.
4. Какая кость не входит в состав нижних конечностей?
А) бедренная; В) кисть;
Обмен газами при дыхании происходит в:
А) альвеолах легких; В) гортани;
Б) трахеи; Г) бронхах.
Из каких отделов состоит пищеварительный тракт млекопитающих?
А) рот, глотка, пищевод;
Б) рот, пищевод, желудок, тонкая, толстая кишки, прямая кишка;
В) рот, желудок, печень, поджелудочная железа, прямая кишка;
Г) рот, пищевод, желудок, печень, поджелудочная железа, тонкая и толстая кишки, прямая кишка с анальным отверстием.
Откуда и каким путем в тело зародыша млекопитающих поступают питательные вещества и кислород?
А) зародыш развивается за счет питательного желтка и дышит через жабры;
Б) из крови матери через кровеносные сосуды плаценты питательные вещества и кислород поступают в кровеносное русло зародыша;
В) кровь матери поступает в организм зародыша;
Г) питание и дыхание зародыша не зависит от тела матери.
8. К отряду Насекомоядных относится:
Б) кенгуру; Г) ехидна.
9. Поставьте цифры, обозначающие камеры желудка в той последовательности, как пища претерпевает пищеварительную обработку в желудке коровы:
1. Книжка; 2. Ротовая полость; 3. Сычуг; 4. Сетка; 5. Рубец
Часть 2.
1. Вы берите три правильных ответа из шести.
Для первозверей характерно:
Б) насиживание яиц или донашивание их в сумке;
В) отсутствие клоаки;
Г) вскармливание детенышей молоком;
Д) наличие высокой температуры;
2. Установите соответствие.
(Напишите «Отряд» и из 1го столбика выпишите его представителей)
Часть 3. Дайте полный развернутый ответ.
1. В чем состоит сходство и отличие в размножении и развитии однопроходных (первозверей), сумчатых и плацентарных?
Кл. ХИМИЯ
На отдельном двойном листике без указания даты, выполнить контрольную работу №2. Условия задания переписывать (кроме первого задания) (Ф.И. напишите на полях)
КОНТРОЛЬНАЯ РАБОТА №2 (Химия 7 кл)
по теме: «Простые вещества. Кислород. Водород»
1. Выбрать признаки, характерные для:
а) водорода; б) кислорода; в) озона
Признаки: без цвета, без вкуса, без запаха, хорошо растворяется в воде, плохо растворяется в воде, лёгкий газ, тяжёлый газ, поддерживает горение, горит синем пламенем, имеет запах свежести, в химических реакциях является окислителем, в химических реакциях является восстановителем, при низких температурах образует голубую жидкость, образуется в процессе фотосинтеза, является составной частью Солнца.
а) Признаки водорода:
б) признаки кислорода:
Выбрать правильный вариант ответа:
2. В промышленности кислород получают из: а) хлората калия; б) воды;
в) воздуха; г) перманганата калия
3. Ученый, получивший кислород и первый описавший его, это:
а) Дж. Дальтон; б) Г.Кавендиш; в) Дж. Пристли; г) А.Лавуазье
4. На заполненный сосуд кислородом указывает то, что внесенная в этот сосуд: а) горящая лучинка гаснет; б) горящая лучинка вызывает взрыв; в) тлеющая лучинка вызывает взрыв; г) тлеющая лучинка ярко вспыхивает
5. Катализатором разложения хлората калия при получении кислорода является: а) оксид кальция; б) оксид серы(IV); в) оксид магния; г) оксид марганца (IV)
6. Формула оксида азота(IV):
а) N2O; б) NO2; в) N2O5; г) NO (для подтверждения вашего ответа укажите валентность азота во всех формулах)
Вполните задания
7. Закончите уравнения реакций горения, расставьте коэффициенты:
8. Напишите формулы оксидов:
1) оксид кальция; 2) оксид серы(IV); 3) оксид магния; 4) оксид марганца(IV)
9. Определите массовую долю кислорода: в оксиде углерода (IV)
Какой объем при нормальных условиях занимают 2 моль любого газа?
11. Определить массу 0, 25 моль серной кислоты H 2 SO4
Дата добавления: 2021-07-19 ; просмотров: 16 ; Мы поможем в написании вашей работы!
Задачи на молярный объём газов
Теоретический материал смотри на странице «Молярный объём газа».
Основные формулы и понятния:
| Закон Авогадро При одинаковой температуре и давлении одинаковые объемы любых газов содержат одинаковое кол-во молекул Если V1=V2; T1=T2; P1=P2, то N1=N2 |
Из закона Авогадро, например, следует, что при одинаковых условиях в 1 литре водорода и в 1 литре кислорода содержится одинаковое кол-во молекул, хотя их размеры сильно разнятся.
Первое следствие из закона Авогадро:
| При одинаковых условиях 1 моль любого газа занимает один и тот же объём Если N1=N2; T1=T2; P1=P2, то V1=V2 |
Объём, который занимает 1 моль любого газа при нормальных условиях (н.у.), равен 22,4 литра и называется молярным объёмом газа (Vm).
Что называют нормальными условиями (н.у.):
Из первого следствия закона Авогадро вытекает, что, например, 1 моль водорода (2 г) и 1 моль кислорода (32 г) занимают один и тот же объем, равный 22,4 литра при н.у.
Зная Vm, можно найти объем любого кол-ва (ν) и любой массы (m) газа:
Типовая задача 1 : Какой объём при н.у. занимает 10 моль газа?
Типовая задача 2 : Какой объём при н.у. занимает 16 г кислорода?
Второе следствие из закона Авогадро:
| Относительная плотность одного газа по другому газу равна отношению их молярных или относительных молекулярных масс DY(X) = M(X)/M(Y) = Mr(X)/MrY |
Зная пллотность газа (ρ=m/V) при н.у., можно вычислить молярную массу этого газа: M=22,4·ρ
Плотностью (D) одного газа по другому называют отношение массы определённого объёма первого газа к массе аналогичного объёма второго газа, взятого при одинаковых условиях.
Типовая задача 3 : Определить относительную плотность углекислого газа по водороду и воздуху.
| Закон объёмных отношений при одинаковых условиях отношение объёмов газов (а также объёмы газообразных продуктов), которые вступают в реакцию, соотносятся, как небольшие целые числа, коэффициенты в уравнениях реакций показывают числа объёмов реагировавших и образовавшихся газов |
Из уравнения реакции видно, что кол-ва реагирующих веществ не соответствуют отношению стехиометрических коэффициентов в уравнении. В таких случаях вычисления проводят по веществу, которого меньше, т.е., это вещество закончится первым в ходе реакции. Чтобы определить какой из компонентов находится в недостатке, надо обратить внимание на коэффициенте в уравнении реакции.
Однако, торопиться не надо. В нашем случае для реакции с 1,5 моль кислорода необходимо 3 моль водорода (1,5·2), а у нас его только 2 моль, т.е., не хватает 1 моль водорода, чтобы прореагировали все полтора моля кислорода. Поэтому, расчёт кол-ва воды будем вести по водороду:
Из уравнения Клапейрона:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Расчет числа молекул и объемов газообразных веществ
Решениие задач по химии на закон Авогадро
m(B)- масса вещества (В);
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 10 23 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
Один моль любого вещества содержит 6,02 . 1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:
Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 10 23 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 10 23 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
Ответ: 2,69 . 10 19 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 . 10 21 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 10 23 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 . 10 21 молекул газа, составив пропорцию:
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
Учитывая, что в одном моле вещества содержится 6,02 . 10 23 молекул, находим число молекул в 0,0003л газа:
Ответ: 8,07 . 10 18 молекул.
Расчет числа молекул, объемов и давления газообразных веществ
Задача 62.
Вычислить массу: а) 2л Н2 при 15 °С и давлении 100,7кПа (755мм рт. ст.); 6) 1м3 N2 при 10 °С и давлении 102,9 кПа (772мм рт. ст.); в) 0,5 м 3 Cl2 при 20 °С и давлении 99,9 кПа (749,3мм рт. ст.).
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
Рассчитаем массу каждого газа, учитывая, что мольный объём газа равен 22,4л и, зная молекулярную массу газов, получим:
Ответ: а) 0,168г; б) 1.23кг; в) 1,456кг.
Задача 63.
Определить объем, занимаемый 0,07кг N2 при 21°С и давлении 142 кПа (106 мм рт. ст.).
Решение:
Зная мольный объём и мольную массу азота (28г/моль), находим объём, который будет занимать 0,07кг (70г) азота при нормальных условиях:
Затем приведём полученный объём к температуре Т = 21 о С (294К) и Р = 142кПа, используя выражение, объединяющее законы Гей-Люссака и Бойля-Мариотта:
Ответ: 43л.
Задача 64.
Бертолетова соль при нагревании разлагается с образованием КСI и О2. Сколько литров кислорода при 0 °С и давлении 101,3 кПа можно получить из 1 моля КСIО3?
Решение:
Уравнение реакции термического разложения бертолетовой соли имеет вид:
Из уравнения реакции следует, что из двух молей бертолетовой соли образуется три моля кислорода, т.е. из одного моля соли образуется полтора моля кислорода (2:3 = 1:х; x = 1.3/2 = 1,5моль).
Объём кислорода при нормальных условиях (T0 =0 °С и P0 =101.325кПа) можно рассчитать по формуле:
Ответ: 33,6л.
Задача 65.
Сколько молей содержится в 1м 3 любого газа при нормальных условиях?
Решение:
Зная, что один моль любого газа при нормальных условиях (Т0 =0 °С и Р0 =101.325 кПа) занимает 22,4л, рассчитаем количество молей газа в 1м 3 (1000 л) из пропорции:
Ответ: 44,64моль.
Задача 66.
Чему равно атмосферное давление на вершине Казбека, если при 0 °С масса 1л взятого там воздуха равна 700 мг?
Решение:
Мольная масса воздуха равна 29 г/моль. Нормальными условиями для газов являются температура 0 °С и давление 101,325 кПа (760 мм рт ст.). Масса одного литра воздуха при нормальных условиях равна 1296,64 мг:
Теперь рассчитаем атмосферное давление на вершине Казбека из пропорции:
Ответ: 54,7к Па (410,3 мм рт. ст.).
Задача 67.
При взаимодействии одного объема СО и одного объема Сl2 образуется один объем фосгена. Установить формулу фосгена.
Решение:
По условию задачи выходит, что из молекулы угарного газа и одной молекулы хлора образуется одна молекула фосгена. Так как молекула угарного газа СО состоит из одного атома углерода и одного атома кислорода, а молекула хлора Cl2 состоит из двух атомов хлора, то, следовательно, молекула фосгена будет состоять из одного атома углерода, одного атома кислорода и двух атомов хлора. Тогда формула фосгена будет иметь вид: CCl2O.
Уравнение реакции будет иметь вид:
Ответ: ССl2O.
Задача 68.
Какой объем СО2 получается при сгорании 2л бутана? Объемы обоих газов измерены при одинаковых условиях.
Решение:
Уравнение реакции горения бутана имеет вид:
Из уравнения реакции следует, что при сгорании одного моля бутана образуется четыре моля углекислого газа. Известно, что при одинаковых условиях одинаковое количество газов занимают одинаковый объём. Один моль любого газа при нормальных условиях занимает объём в 22,4 л.
Исходя, из этих утверждений рассчитаем объём выделившегося углекислого газа при сгорании 2 л бутана, составив пропорцию:
Ответ: 8л.
Из уравнения реакции следует, что из одной молекулы метана и двух молекул кислорода образуются одна молекула углекислого газа и две молекулы воды, т. е. реакция протекает без изменения объёма. Начальный объём системы состоял из одного объёма метана и трёх объёмов кислорода, после реакции в системе остался один объём не прореагировавшего кислорода и три объёма продуктов реакции (один объём метана и два объёма паров воды). Поскольку реакция протекает без изменения объёма, а по окончании реакции содержимое сосуда приводится к первоначальной температуре, а общее число молекул газов не изменилось, то давление в системе останется прежним, т. е. 600 кПа.
Ответ: не изменится.
Задача 70. После взрыва 0,020 л смеси водорода с кислородом осталось 0,0032 л кислорода. Выразить в процентах по объему первоначальный состав смеси.
Решение:
Находим объём газов, вступивших в реакцию:
0,020 – 0,0032 = 0,0168 л.
Уравнение реакции горения водорода имеет вид:
При взаимодействии водорода с кислородом из двух молекул водорода и одной молекулы кислорода получаются две молекулы воды, следовательно, из трёх молекул образовавшихся газов одна молекула будет принадлежать кислороду. Таким образом, объём кислорода, вступившего в реакцию, будет составлять одну треть объёма смеси газов – продуктов реакции. Отсюда количество кислорода, вступившего в реакцию, составляет 0,00565 л (0 0168/3 = 0,0056).
Следовательно, общее количество кислорода до реакции составляло 0,0088л (0,0056 + 0,0032 = 0,0088).
Тогда содержимое водорода до реакции составляло 0,0112л (0,02 – 0,0088 = 0.0112).
Рассчитаем в процентах первоначальный состав газовой смеси: