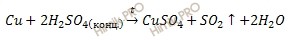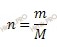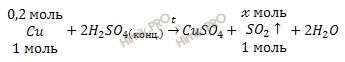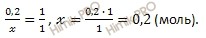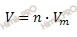При взаимодействии с концентрированной серной кислотой 128 г меди выделяется газ обьемом ___л(н?
При взаимодействии с концентрированной серной кислотой 128 г меди выделяется газ обьемом ___л(н.
(запишите число с точностью до целых).
n = 1 моль n = 1 моль
М = 64 г / моль Vm = 22, 4 л / моль
V(SO2) = 128 * 22, 4 / 64 = 45 л.
Составьте уравнение реакции взаимодействия меди с концентрированной серной кислотой, расставьте коэффициенты методом электронного баланса?
Составьте уравнение реакции взаимодействия меди с концентрированной серной кислотой, расставьте коэффициенты методом электронного баланса.
Помогите пожалуйста?
При взаимодействии цинка с концентрированной серной кислотой может выделиться газ :
а)сероводород, б)кислород ; в)диоксид серы ; в)водород.
При взаимодействии меди с концентрированной серной кислоты выделяется оксид серы 4 сколько меди должно вступить в реакцию чтобы получить 3, 2 г SO2?
При взаимодействии меди с концентрированной серной кислоты выделяется оксид серы 4 сколько меди должно вступить в реакцию чтобы получить 3, 2 г SO2.
При взаимодействии 16г меди с концентрированной азотной кислотой выделяется газ объемом :а)2?
При взаимодействии 16г меди с концентрированной азотной кислотой выделяется газ объемом :
При взаимодействии 0?
При взаимодействии 0.
2 моль сульфида железа(2) с соляной кислотой выделяется газ объемом_____л (запишите число с точностью до сотохых).
Верны ли следующие суждения о концентрированной серной кислоте?
Верны ли следующие суждения о концентрированной серной кислоте?
А. Концентрированная серная кислота — сильный окислитель.
Б. При взаимодействии меди с концентрированной серной кислотой выделяется оксид серы(IV).
3) верны оба суждения
4) оба суждения неверны.
Объём водорода (н?
У. ), выделившийся при взаимодействии 3, 75 моль цинка с избытком разбавленного раствора серной кислоты, равен _______ л.
(Запишите число с точностью до целых.
Какой газ выделяется при взаимодействии разбавленной азотной кислоты и меди а так же концентрированной азотной кислоты и меди?
Какой газ выделяется при взаимодействии разбавленной азотной кислоты и меди а так же концентрированной азотной кислоты и меди.
Какой объем газа (н?
Какой объем газа (н.
У) выделится при взаимодействии концентрированной азотной кислоты с медью, если в реакцию вступает 0, 68 моль кислоты?
Какой объем газа (н?
Какой объем газа (н.
У) выделится при взаимодействии концентрированной азотной кислоты с медью, если в реакцию вступает 0, 68 моль кислоты?
Количество моль надо умножить на молярную массу. M = M * n = 32г / моль * 3моль = 96г.
M(FeSO4 * 7H2O) = (152 + 126) = 278 m(FeSO4) = 50 * 4 / 100 = 2 В 278г кристаллогидрата содержится 152г железа(2) сульфата а в Хг кристаллогидрата 2г железа сульфата Х = 2 * 278 / 152 = 3, 66г Оттветнужно взять 3, 66 г кристаллогидрата и долить водой..
BaO + H2SO4 = BaSO4 + H2O SO3 + MgO = MgSO4 Ni(OH)2 = NiO + H2O.
Если нужны пояснения, готова предоставить по первому требованию : ).
Химик.ПРО – решение задач по химии бесплатно
Рассчитайте объем сернистого газа (SO2), который выделяется при взаимодействии меди (Cu) массой 12,8 грамм с избытком концентрированной серной кислоты (H2SO4).
Решение задачи
Составим уравнения реакции взаимодействия меди с концентрированной серной кислоты (H2SO4):
Найдем химическое количество меди по формуле, устанавливающей связь между химическим количеством вещества и массой:
Учитывая, что молярная масса меди (Cu) равна 63,5 г/моль получаем:
n (Cu) = 12,8/63,5 = 0,2 (моль).
По уравнению реакции рассчитаем, сколько моль сернистого газа (SO2) образуется в ходе реакции:
при участии 0,2 моль Cu образуется 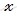
при участии 1 моль Cu образуется 1 моль SO2
Найдем сколько литров сернистого газа (SO2) образуется при взаимодействии меди (Cu) с избытком концентрированной серной кислоты (H2SO4) по формуле, устанавливающей связь между объемом и химическим количеством вещества:
V (SO2) = 0,2 ∙ 22,4 = 4,48 (л).
Ответ:
объем сернистого газа равен 4,48 литра.