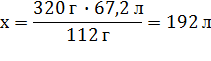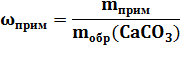Какой объём хлора прореагирует с железом массой 400г, если массовая доля примесей в нём 20%?
Билет №6 (3)
Осуществить превращения:
Медь → хлорид меди (II) → гидроксид меди (II) → оксид меди (II) → медь
Cu 



3. Cu(OH)2 
4. CuO + H2 
Билет №7 (3)
При прокаливании 300 г известняка, содержащего 10% примесей, получено 75 г негашеной извести. Найти массовую долю выхода продукта реакции от теоретически возможного.
Na NaOh Na2co3 NaCl NaNo3
Какой объём хлора прореагирует с натрием массой 34,5г. Определить массу хлорида натрия.
2 моль 1 моль 2 моль
m(Na) = 23 г/моль ∙ 2 моль = 46 г
m(NaCl) = 58,5 г/моль ∙ 2 моль = 117 г
V(Cl2) = 22,4 л/моль ∙ 1 моль = 22,4 л
Ответ: V(Cl2) = 16,8 л; m(NaCl) = 87,8 г
Магний → хлорид магния → гидроксид магния → оксид магния → сульфат магния
Mg MgCl2 Mg(oh)2 MgO MgSo4
Mg + 2HCl 
Mg(OH)2 
MgO + 2H + → Mg 2+ + H2O
Какой объём хлора прореагирует с железом массой 400г, если массовая доля примесей в нём 20%?
mприм = 0,2 ∙ 400 г = 80 г
m(Fe) = mобр – mприм = 400 г – 80 г = 320 г
m(Fe) = 56 г/моль ∙ 2 моль = 112 г
V(Cl2) = Vm ∙ ν = 22,4 л/моль ∙ 3 моль = 67,2 л
Медь → хлорид меди (II) → гидроксид меди (II) → оксид меди (II) → медь
Cu CuCl2 Cu(oh)2 CuO Cu
Cu(OH)2 
CuO + H2 
При прокаливании 300 г известняка, содержащего 10% примесей, получено 75 г негашеной извести. Найти массовую долю выхода продукта реакции от теоретически возможного.
CaCO3 
mприм = 300 г ∙ 0,1 = 30 г
m(CaCO3) = 300 г – 30 г = 270 г


Какова масса соли, получившейся в результате взаимодействия 100 г соляной кислоты с 14 г оксида кальция?
1 моль 2 моль 1 моль
M(CaCl2) = 40 + 71 = 111 г/моль
m(CaCl2) = 111 г/моль ∙ 0,25 моль = 27,75 г ≈ 27,8 г
Ответ: m(CaCl2) = 27,8 г
Какой объём ацетилена необходимо сжечь для получения 24 л оксида углерода (IV)?
ТП 111 25.06.20. Выполнить задание в экзаменационном билете.
Афонина Дарья Владимировна О
Быкова Мария Александровна
Вашурина Татьяна Александровна
Галузина Валерия Александровна
Горячева Екатерина Вадимовна
Грачева Анита Витальевна О
Жилко Елизавета Витальевна
Ижбулдин Юрий Арсеньевич
Калашникова Виктория Евгеньевна
Карасев Кирилл Алексеевич
Киселева Анна Сергеевна
Кобызева Юлия Валерьевна
Кривоносова Виктория Сергеевна
Ларин Даниил Дмитриевич
Логинов Александр Дмитриевич
Мосолов Никита Александрович
Рулев Кирилл Вячеславович
Рыбакова Анастасия Дмитриевна
Сказченко Андрей Сергеевич
Сметанин Никита Сергеевич
Краснослободцев Евгений Романович
ЭКЗАМЕНАЦИОННЫЕ БИЛЕТЫ ПО ХИМИИ
НАПИСАТЬ ОТВЕТ В ТЕТРАДИ до 13.00 ОТПРАВИТЬ НА ЭЛ.ПОЧТУ
Периодический закон и периодическая система химических элементов Д.И. Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
Предельные углеводороды, общая формула гомологов данного ряда, строение. Химические свойства метана. Практическое применение алканов.
Задача. Выведите молекулярную формулу вещества, если массовая доля углерода в нём составляет 82,75%, водорода 17,25%. Относительная плотность паров по воздуху равна 2.
Строение атомов химических элементов. Закономерности в изменении свойств химических элементов и их соединений в зависимости от строения их атомов.
Непредельные углеводороды ряда этилена, общая формула состава, электронное и пространственное строение, химические свойства этилена.
Натрий → гидроксид натрия → карбонат натрия → хлорид натрия → нитрат натрия
Оксиды, их классификация, свойства.
Аминокислоты, их строение и химические свойства. Биологическая роль аминокислот и их применение.
Задача. Какой объём хлора прореагирует с натрием массой 34,5г. Определить массу хлорида натрия.
Классификация химических реакций.
Крахмал, строение молекул, физические и химические свойства, возможное применение в вашей профессии.
Магний → хлорид магния → гидроксид магния → оксид магния → сульфат магния
Обратимость химических реакций. Химическое равновесие и условия его смещения, практическое применение.
Ацетилен – представитель углеводородов с тройной связью в молекуле. Химические свойства, получение и применение ацетилена в органическом синтезе.
3.Задача. Какой объём хлора прореагирует с железом массой 400г, если массовая доля примесей в нём 20%?
Скорость химических реакций. Зависимость скорости от природы, концентрации веществ, площади поверхности соприкосновения реагирующих веществ, температуры, катализатора.
Ароматические углеводороды. Бензол, структурная формула, свойства и получение. Применение бензола и его гомологов.
Медь → хлорид меди (II) → гидроксид меди (II) → оксид меди (II) → медь
Основные положения теории химического строения органических веществ А.М. Бутлерова. Основные направления развития этой теории.
Электролиз как окислительно-восстановительный процесс. Электролиз расплавов и растворов на примере хлорида натрия.
Задача.При прокаливании 300 г известняка, содержащего 10% примесей, получено 75 г негашеной извести. Найти массовую долю выхода продукта реакции от теоретически возможного.
Изомерия органических соединений и её виды.
Оксиды, их классификация, характеристика химических свойств. Возможное применение оксидов в вашей профессии
3.Задача. Какова масса соли, получившейся в результате взаимодействия 100 г соляной кислоты с 14 г оксида кальция?
Основания, их классификация и свойства на основе представлений об электролитической диссоциации, практическое применение.
Фенол, его строение, свойства, получение и применение.
3.Задача. Какой объём ацетилена необходимо сжечь для получения 24 л оксида углерода (IV)?
Карбоновые кислоты. Строение, свойства, получение и применение
Предельные одноатомные спирты, их строение, физические и химические свойства. Получение и применение этилового спирта.
3.Ряд превращений. Гидроксид меди (II) → сульфат меди (II) → медь →
→ оксид меди (II) → нитрат меди (II)
Электрохимический ряд металлов. Вытеснение металлов из растворов солей другими металлами. Коррозия металлов. Способы защиты металлов от коррозии.
Альдегиды, их строение и свойства. Применение муравьиного и уксусного альдегидов.
Какой объём ацетилена можно получить из образца карбида кальция массой 100 г, если массовая доля примесей в нём 15%?
Мыло. Понятие о синтетических моющих средствах.
Предельные одноосновные карбоновые кислоты, их строение и свойства на примере уксусной кислоты, практической применение.
Железо → хлорид железа (II) → гидроксид железа (II) → сульфат железа (II) → хлорид железа (II)
Дисперсные системы.Примеры.Практическое применение в вашей профессии.
Жиры, их состав, свойства
Вычислите массу соли, образованной при взаимодействии уксусной кислоты массой 120 г и гидроксида натрия массой 60 г?
Кислоты, их классификация и свойства на основе представлений об электролитической диссоциации, практическое применение. Применение в вашей профессии.
Общая характеристика высокомолекулярных соединений, состав, строение, реакции, лежащие в основе их получения.
Какой объём ацетилена можно получить из карбида кальция массой 38,4 г
Гидрооксиды, их классификация и свойства на основе представлений об электролитической диссоциации, практическое применение. Применение в вашей профессии.
Глюкоза – представитель моносахаридов, строение, физические и химические свойства, применение.
Какая масса раствора с массовой долей гидроксида натрия 4% расходуется на нейтрализацию соляной кислоты массой 73 г?
Соли, их классификация, состав, свойства на основе представлений теории электролитической диссоциации, возможное применение в вашей профессии..
Алкины, общая формула гомологов данного ряда, строение. Химические свойства. Практическое применение алкинов.
Катализ, катализаторы, практическое применение.
Анилин – представитель аминов, строения и свойства; получение и значение в развитии органического синтеза.
Магний → хлорид магния → гидроксид магния → оксид магния → сульфат магния
Циклоалканы. общая формула гомологов данного ряда, строение. Химические свойства.
2. Скорость химической реакции. Правило Вант-Гоффа.Влияние температуры,давления,катализатора на скорость реакции.
Железо → хлорид железа (II) → гидроксид железа (II) → сульфат железа (II) → хлорид железа (II)
1.Алюминий. Положение в периодической системе, строение атома, физические и химические свойства. Роль алюминия в современной технике и в вашей профессии.
2. Многоатомные спирты. Строение, свойства, применение на примере глицерина.
Оксид кальция, полученный при прокаливании 20г карбоната кальция, обработали водой. Вычислите массу полученного продукта.
1.Углеводы.Классификация.Строение, физические и химические свойства, применение.
2.Вода. Ее потребление в быту и на производстве. Роль воды в химических реакциях. Гидролиз.
1.Растворы.Способы выражения концентраций растворов.Растворение.
2.Сложные эфиры. Строение, свойства, получение и применение.
Натрий → гидроксид натрия → карбонат натрия → хлорид натрия → нитрат натрия