О видах исследований на новую коронавирусную инфекцию COVID-19
Сегодня наиболее актуальной задачей общественного здравоохранения является обеспечение безопасности населения Российской Федерации. С этой целью проводится массовое тестирование населения на коронавирусную инфекцию. Оно позволяет выявить как заболевших на ранней стадии, так и бессимптомных носителей. В настоящее время существует несколько видов исследований, у каждого из которых свои цели и назначения. Все исследования можно разделить на две большие группы: прямые – обнаружение возбудителя и непрямые – обнаружение иммунного ответа человека на контакт с возбудителем.
1. Анализ на антитела (IgM и IgG)
Тест на антитела класса IgG позволяет оценить коллективный иммунитет населения нашей страны к COVID-19. Пройти его может любой, кто хочет как можно скорее узнать свой иммунный статус по отношению к новой коронавирусной инфекции и при этом не имеет симптомов заболевания и контактов с инфекцией. Полученные результаты могут служить не только для определения антительного иммунного ответа у конкретного человека, но и для оценки количества переболевших в разных группах населения. Некоторые тесты на антитела методом иммуноферментного анализа крови (ИФА) еще и определяет титр – количество выявленных антител.
Для определения антител также могут использоваться экспресс-тесты – они выявляют наличие или отсутствие антител. Экспресс-тест на антитела прост в исполнении, может использоваться на приеме у врача, результат может быть получен через несколько минут, но обладает меньшей чувствительностью, чем тесты, выполненные методом ИФА.
Какой метод специфической лабораторной диагностики наиболее информативен при коронавирусной инфекции
Заведующая клинико-диагностической лабораторией Городской клинической инфекционной больницы Минска, главный внештатный специалист по лабораторной диагностике комитета по здравоохранению Мингорисполкома, кандидат мед. наук Людмила Анисько отвечает на вопросы о лабораторных исследованиях коронавирусной инфекции.
Людмила Анисько, главный внештатный специалист по лабораторной диагностике комитета по здравоохранению Мингорисполкома, кандидат мед. наук Какими направлениями представлена лабораторная диагностика при работе с COVID-пациентами?
Для лабораторной диагностики COVID-19 в клинической практике применяются специфические и неспецифические методы. К специфическим относят ПЦР, которая выявляет генетический материал (РНК) вируса в биологическом материале пациента (назофарингеальные мазки, бронхоальвеолярный лаваж и др.), и иммунохимические исследования, определяющие антитела в крови пациента, вырабатывающиеся после встречи с возбудителем инфекции. К неспецифическим — общий и биохимический анализ крови, исследование показателей гемостаза, в том числе D-димеров, кислотно-основного состояния, определение уровня провоспалительных маркеров: СРБ, ИЛ-6, прокальцитонина.
Какой вид материала для лабораторного исследования является основным?
Наиболее информативным материалом для ПЦР-исследования на Covid-19, по ряду публикаций, является бронхоальвеолярный лаваж (93 %). Для ПЦР как прямого метода исследования важно правильно взять материал. Так как в большинстве случаев заболевание протекает с пневмонией, то и наиболее информативным будет материал из нижних отделов дыхательных путей. Однако получить его не всегда удается. Кроме того, значительная часть инфицированных переносит COVID-19 в легкой и бессимптомной формах, в связи с чем широкое применение получили назофарингеальные мазки. Их информативность составляет чуть менее 70 %. На сегодняшний день именно такой материал является основным.
Что может стать дополнительным материалом и в каких случаях он необходим?
Кровь, которая нужна для определения антител к COVID-19. В большинстве публикаций обращает на себя внимание высокая результативность комбинированного применения ПЦР-исследования с тестами на антитела.
Есть мнение, что мазок из ротоглотки неинформативен, поскольку новый коронавирус не остается там надолго, а продвигается вглубь организма. По данным иностранных источников, доля ложноотрицательных тестов при взятии такого мазка составляет от 40 % до 60 %. Хотелось бы услышать ваше мнение на этот счет.
В Беларуси для повышения информативности забирается комбинированный мазок, то есть в одну пробирку помещается аппликатор с мазком из носоглотки и ротоглотки. Следует отметить, что информативность материала напрямую зависит от качества его взятия.
Какой мазок можно считать качественным?
При взятии мазка из носоглотки перед процедурой необходимо очистить ее от слизи. Далее легким движением по наружной стенке носа вводят сухой аппликатор на глубину 7–10 см (по наружной стенке полости носа на глубину 2–3 см до нижней носовой раковины, слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину на 5–6 см у взрослых и удаляют вдоль наружной стенки полости носа, производя вращательные движения). Таким образом, общая глубина погружения аппликатора должна составлять не менее половины расстояния от ноздри до ушного отверстия. При взятии мазка из ротоглотки также сухим стерильным аппликатором вращательными движениями берут мазок с поверхности миндалин, небных дужек и задней стенки ротоглотки, аккуратно прижимая язык пациента шпателем. Забранный биоматериал транспортируется при температуре 4 °С ± 2 °С в лабораторию и при такой температуре может храниться до 5 дней. Если необходимо более длительное хранение, прибегают к замораживанию.
Влияет ли на результаты исследований качество тест-систем?
Безусловно. Любая диагностическая тест-система имеет аналитические характеристики, где отражаются ее чувствительность и специфичность. Чем лучше будет чувствительность тест-системы, тем меньше будет ложноотрицательных результатов. Высокая специфичность тест-системы снижает число ложноположительных результатов.
Какие показатели в анализах крови при COVID-19 имеют наиболее важное значение?
В общем анализе — количество лейкоцитов, лимфоцитов, тромбоцитов. Дело в том, что при данной инфекции в большинстве случаев наблюдается лимфопения, что является неблагоприятным прогностическим показателем.
В биохимическом анализе — активность КФК, ЛДГ коррелирует со степенью поражения легочной ткани; СРБ, ферритин — основные острофазные белки, являющиеся маркерами воспаления, они коррелируют с тяжестью заболевания и распространенностью воспалительной инфильтрации в легких.
Креатинфосфокиназа (КФК) катализирует реакцию фосфорилирования креатина и содержится в клетках сердечной мышцы, скелетной мускулатуры, головного мозга, щитовидной железы, легких. Фермент креатинфосфокиназы относится к разряду клеточных ферментов, то есть в норме активность его в крови невысокая, но при разрушении клеток органа, где его содержание высоко, фермент поступает в кровь, и в биохимическом анализе можно наблюдать возрастание его активности. Следует отметить, что креатинфосфокиназа существует в виде трех изоферментов (ВВ, МВ, ММ), что определяет органоспецифичность. Так, КФК-ММ оказывается повышен в большей степени в результате повреждений мышц и редко при повреждениях сердца; КФК-МВ увеличивается более чем в 1,5 раза при инфаркте миокарда; КФК-ВВ повышается при некоторых формах рака, травме сердечной мышцы, заболеваниях соединительной ткани, у новорожденных при родовой травме мозга, при родах (источником являются матка и плацента). Отмечено повышение общей КФК при гипоксических состояниях, что можно наблюдать у пациентов с полисегментарной пневмонией.
Лактатдегидрогеназа (ЛДГ) — клеточный фермент, существующий в пяти формах изоферментов (1, 2, 3, 4, 5), катализирует обратимое восстановление пирувата до лактата. Данный фермент присутствует во всех клетках организма. Повышение активности ЛДГ в сыворотке отмечено при остром повреждении сердца, почек, печени, скелетных мышц, легких, кожи или гемолизе.
С-реактивный белок (СРБ) — мультифункциональный белок острой фазы воспаления, играющий важную роль в защите от чужеродных агентов и в аутоиммунных процессах. Данный белок имеет много свойств, характерных для иммуноглобулинов (антител): он связывается с бактериальными полисахаридами и гликолипидами, с поврежденными клеточными мембранами. Повышение его концентрации в крови свидетельствует о протекающей воспалительной реакции. Ферритин — сложный железосодержащий белковый комплекс. является одним из белков острой фазы воспаления. его уровень в крови закономерно повышается при легочных инфекциях, хронических инфекциях мочевыводящих путей, остеомиелите, ожогах и др.
Коагулограмма
У пациентов с COVID-19 довольно часто наблюдается повышение уровня D-димеров, прямо пропорциональное степени тяжести заболевания. Этот показатель является объективным маркером венозной тромбоэмболии. Значительный рост данного показателя ассоциируется с высоким риском смертности и указывает на активацию системы свертывания вследствие инфекции/сепсиса, цитокинового шторма или надвигающейся полиорганной недостаточности (Ning Tang et al.).
Кроме того, наиболее часто коагулопатия у пациентов с COVID-19 характеризуется ростом уровня фибриногена, который коррелирует с повышением концентрации маркеров воспаления (например, СРБ). В журнале Nature Machine Intelligence было опубликовано исследование. В анализах крови, которые были собраны в январе и феврале 2020 года у 485 пациентов с COVID-19 из Уханя, искусственный интеллект обнаружил три биомаркера, предсказывающие высокий риск смерти при COVID-19 (за 10 дней c вероятностью 90 %). Это ЛДГ, лимфоциты и С-реактивный белок. Что вы думаете по поводу этого исследования?
ЛДГ — цитозольный фермент, при COVID-19 отражает массивность и глубину поражения легочной ткани. Лимфоциты участвуют в клеточном и гуморальном иммунном ответе. При COVID-19 имеет место дисрегуляторный иммунный ответ, что проявляется лимфопенией, снижением кластеров CD4 и CD8 лимфоцитов. Повышение уровня СРБ наблюдается у 2/3 пациентов с COVID-19, причем существует прямая корреляция между уровнем повышения и тяжестью процесса. На значения данных маркеров может оказывать влияние ряд других состояний, не связанных с COVID-19, а значит их необходимо учитывать только в совокупности с клинической картиной.
Важно контролировать уровень прокальцитонина, чтобы избежать необоснованного назначения антибиотиков.
Методы специфического лабораторного тестирования новой коронавирусной инфекции
Полный текст:
Аннотация
В обзоре представлено описание специфического лабораторного тестирования SARS-CoV-2. Показана эффективность определенных типов тестов в зависимости от поставленных медицинских и эпидемиологических задач. Также отмечена важность применения определённых методов диагностики для массового и оперативного тестирования пациентов на новую коронавирусную инфекцию, что позволит ускорить их выявление. Показана эффективность применения тест-систем, с которыми можно будет работать в амбулаторных условиях без наличия в медицинском учреждении стационарной лаборатории, что позволит упростить и увеличить пропускную способность медицинских учреждений, которые проводят диагностику SARS-CoV-2. Данный обзор будет полезен как медицинским работникам лабораторных специальностей, так и всем врачам клинического профиля, которые сейчас работают с новой коронавирусной инфекцией.
Ключевые слова
Для цитирования:
Перевезенцев О.А., Холодная Т.О., Самсонов А.Е., Бурцев Д.В. Методы специфического лабораторного тестирования новой коронавирусной инфекции. Медицинский вестник Юга России. 2020;11(3):27-33. https://doi.org/10.21886/2219-8075-2020-11-3-27-33
For citation:
Perevesentsev O.A., Cholodnaya T.O., Samsonov A.E., Burtsev D.V. Methods of specific laboratory testing of new coronavirus infection. Medical Herald of the South of Russia. 2020;11(3):27-33. (In Russ.) https://doi.org/10.21886/2219-8075-2020-11-3-27-33
Изучение факторов патогенности коронавируса SARS-CoV-2 показало, что в клетки человека он проникает через рецепторы к ангиотензин-превращающему ферменту 2 типа (ACE2), который достаточно широко представлен в различных тканях: он экспрессируется в легких на уровне альвеол, кишечнике, гонадах, почках и т.д. [4]. Поэтому потенциально при новой коронавирусной инфекции могут поражаться не только дыхательные пути, но и друие ткани и органы [1][4][5]. С диагностической точки зрения, это означает, что вирусная ДНК может детектироваться не только в биоматериале из дыхательных путей (назофарингеальные соскобы, БАЛ, мокрота), но и в других биологических жидкостях (фекалии, моча, кровь) [1][4][6][7]. Также, теоретически, он может обнаруживаться в моче и в семенной жидкости у мужчин [1].
В настоящее время референсным методом диагностики новой коронавирусной инфекции SARS-CoV-2 является метод полимеразной цепной реакции в реальном времени с обратной транскрипцией вирусной РНК [8]. Из-за достаточно стремительного распространения нового коронавируса по миру особое значение приобретает максимально широкий охват данным молекулярно-генетическим тестированием населения различных стран для эффективного проведения противоэпидемических мероприятий [8]. Например, показано, что до начала глобального ограничения сообщения с Китаем как первичного источника пандемии число недиагностированных случаев инфицирования SaRS-CoV-2 примерно 79 % от общего числа, что сыграло ключевую роль в перерастании локальной вспышки коронавирусной инфекции в глобальную пандемию [9]. Показателен опыт стран, где именно за счёт широкого охвата тестами максимального количества человек удалось снизить скорость эпидемического распространения SARS-CoV-2. Например, в Южной Корее за 9 недели после первого обнаруженного случая инфицирования SARS-CoV-2 было проведено более 300 тыс. тестов (5828,6 тестов на миллион человека населения) [10][11]. Схожие подходы к тестированию были использованы в Сингапуре, Гонконге и на Тайване [12][13]. Кроме широкого охвата тестирования населения также важным является быстрое получение результата молекулярно-генетического тестирования, особенно у пациентов клиническими проявлениями COVID19, которые находятся в начале развивающегося патологического процесса, и у индивидов с бессимптомным носительством SARS-CoV-2 [8]. Быстрая молекулярно-генетическая дифференциальная диагностика COVID19 с другими респираторными патологиями, в том числе, с сезонными ОРВИ и гриппом, позволяет нивелировать внутрибольничное распространение инфекции, что является важным фактором сдерживания эпидемического процесса и снижает нагрузку на медицинскую систему в целом [14][15].
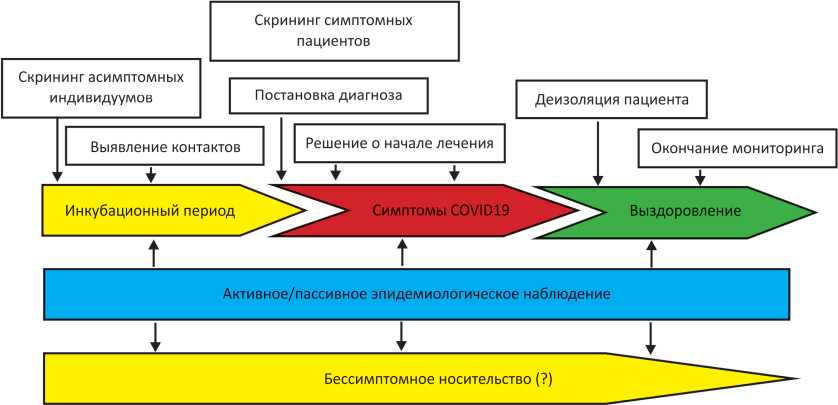
Правильная оценка результатов молекулярно-генетического тестирования должна учитывать стадийность развития патологического процесса при инфицировании SARS-CoV-2 2 [8]. На рис. 1 показана схема постановки диагностических задач на различных стадиях развития инфекционного патологического процесса новой коронавирусной инфекции.
Таким образом, для каждой из стадий развития инфекции SARS-CoV-2 максимально подходит только определённый тип лабораторного тестирования [8]. Дизайн теста должен соответствовать определённым параметрам: напрямую ли он детектирует вирусную ДНК (ПЦР в реальном времени с обратной транскрипцией) или же косвенно (исследование специфических антител), время выполнения исследования, его пропускная способность, его дозирование (возможность использования перед тестированием минимального количества образцов), а также возможность использования тестов в амбулатории или пункте оказания первичной медицинской помощи в случае отсутствия хорошо оснащенной молекулярно-генетической или иммунологической лаборатории. Также важным является специфичность и особенно чувствительность тест-системы. Если принять за базис стадийность степени репликации SARS-C.V-2 в зависимости от стадии заболевания и тяжести его протекания, ПЦР тесты с низкой чувствительностью подойдут для тестирования симптоматических пациентов, но у асимптомных индивидуумов могут дать ложноотрицательный результат. Разберём теперь, каким образом лучше проводить тестирование на SARS-CoV-2 c точки зрения развития заболевания и наблюдения с развитием эпидемического процесса. В задачи данного обзора не входит рассмотрение тест-систем конкретных производителей, но базисные параметры используемых лабораторных тестов рассмотреть необходимо.
В настоящее время, как уже было отмечено выше, базисным референсным методом диагностики инфекции SARS-CoV-2 является метод real-time PCR с обратной транскрипцией вирусной РНК. Но появляются новые методы диагностики рассматриваемой инфекции, в частности, иммунологические, которые для ряда задач подходят больше, чем молекулярно-генетическое исследование 3 [8]. В табл. 1 представлен перечень типов специфического лабораторного тестирования нового коронавируса согласно стадийности развития заболевания и задач наблюдения за эпидемическим процессом по схеме, показанной на рис. 1.
Рисунок 1. Диагностическая схема специфического лабораторного тестирования пациентов с подозрением на инфицирование SARS-CoV-2.
Figure 1. Diagnostic scheme for specific laboratory testing of patients with suspected SARS-CoV-2 infection.
В вышеприведённой таблице зелёным выделены ячейки, тесты в которых хорошо адаптированы для поставленных диагностических и прогностических задач с точки зрения точности тестирования, его формата и времени получения результата. Желтым выделены ячейки, тесты в которых доступны или разработаны для их использования в короткие сроки, но имеют существенные ограничения для своего применения (например, многие из существующих тест-систем для ПЦР в реальном времени с обратной транскрипцией могут давать ложно-отрицательные результаты у индивидуумов в инкубационном периоде с низкой вирусной нагрузкой или же у пациентов с вирусоносительством, где тоже может предполагаться низкая вирусная нагрузка). Красным выделены ячейки, которые не применяются для соответствующих поставленных задач. NAAT — тест амплификации нуклеиновых кислот (nucleic acid amplification test), который является альтернативой RT-PCR и для SARS-CoV-2 представлен методом изотермальной амплификации (TMA, LAMP).
Рассмотрим некоторые особенности забора материала для молекулярно-генетического анализа на SARS-CoV-2. CDC рекомендует брать материал из респираторного тракта [5]. В основном, анализируются назофарингеальные соскобы, но могут проводить анализ и орофарингеальных соскобов из средней носовой раковины и передней носовой полости 4 [16]. Для забора образцов предпочтительней использовать алюминиевые или пластиковые зонды с ватными тампонами, причем для увеличения концентрации вирусных частиц в образце желательно материал, полученный из разных отделов респираторного тракта, помещать в одну пробирку с универсальной транспортной средой. Для анализа также может использоваться мокрота, БАЛ и эндотрахеальный аспират, молекулярно-генетическии анализ которых может дать, в ряде случаев. Более надежный результат, чем пробы, взятые из верхних дыхательных путей, так как вирус SARS-CoV-2 более тропен к клеткам нижних отделов респираторного тракта [5].
В США для молекулярно-генетического тестирования новой коронавирусной инфекции применяется одобренный CDC тестовый набор, который содержит праймеры к двум локусам вирусного нуклеокапсида (N1 и N2) и для гена человеческой РКАазы P [8]. Данный набор отличается от рекомендованного ВОЗ, в котором используются праймеры к генам SARS-CoV РНК-зависимой РНК-полимеразы (RdRP) и капсидного белка (E) [17]. Оба тестовых набора обладают достаточно высокой аналитической чувствительностью и специфичностью и минимальной перекрёстной реакцией с другими циркулирующими видами коронавирусов, причем порог положительного результата в обоих тестах находится до 40-го цикла амплификации [8]. Данные тесты могут использоваться как в качестве скрининговых, так и в качестве подтверждающих и в референсных лабораториях, и в лабораториях, выполняющих массовое тестирование. Также FDA одобрено около 20 коммерческих тестов, которые могут быть использованы молекулярно-генетическими лабораториями для расширения тестирования на новый коронавирус. Что касается компонентов диагностического набора, рекомендованного ВОЗ, то показано, что диагностические ПЦР тест системы, основанные на выявлении специфической последовательности E гена SARS-CoV-2, являются более чувствительными, чем основанные на выявлении RdRp, но в первых из них может быть затруднена интерпретация результата из-за высокой зависимости качества ПЦР от сторонних факторов [18].
Релевантность методов специфического лабораторного тестирования на новую коронавирусную инфекцию для выполнения определенных медицинских задач
Relevance of methods of specific laboratory testing for a new coronavirus infection for performing certain medical tasks
Для быстрого молекулярно-генетического анализа в режиме «полевых условий» амбулаторных учреждений здравоохранения первичного медицинского звена новой коронавирусной инфекции FDA был одобрен ряд тестсистем, с которыми может медицинский персонал вне стационарных лабораторий. Данные тесты позволяют получить результат максимум за 1 час, работа с ними не требует особой лабораторной квалификации. Это тест-системы в виде готовых картриджей, работающих на платформах Abbott ID NOW (Abbott Laboratories), BioFire FilmArray (bioMer rieux), cobas Liat (Roche Diagnostics), и GeneXpert (Cepheid) [19]. Использование таких тестсистем, которые быстро дают результат вне лаборатории, может иметь решающее значение для быстрого выявления инфицированных новым коронавирусом. Например, такие тесты на базе платформы GeneXpert хорошо себя зарекомендовали для массового быстрого тестирования таких социально значимых инфекций, как туберкулез или ВИЧ [8]. Поэтому благодаря их пропускной способности можно будет проводить массовое тестирование на SARS-CoV-2 в странах и регионах со слабо развитой стационарной лабораторной службой, хотя у таких аналитических систем могут быть определённые ограничения касательно их чувствительности и специфичности.
Рассмотрим теперь кратко перспективы использования иммунологических тестов на новую коронавирусную инфекцию. Касательно тестов ни вирусный антиген, как показывает практика иммунологического тестирования антигенов вирусов гриппа респираторно-синтициальной инфекции, данные тест-системы могут давать результаты в амбулаторных условиях первичного медицинского звена за время порядка минут [20]. Но такой тип тест-систем для выше указанных сезонных ОРВИ показывает неоптимальную чувствительность для подтверждения случая заболевания. Для нового коронавируса такие иммунологические тесты сейчас активно разрабатываются, причем их основой служат моноклональные антитела к нуклеокапсидному белку 5 [21]. Касательно же серологических тестов на специфические антитела класса IgA, IgM, и IgG, то для возможности их использования ситуация двоякая. С одной стороны, метод ИФА на поиск антител в периферической крови или слюне может быть проще по исполнению, чем все молекулярно-генетические методы, поэтому его можно использовать в определённых ситуациях [9][22]. Однако данный метод имеет ряд ограничений, таких как зависимость от времени начала симптомов, когда, как уже отмечалось выше, пациент наиболее активно выделяет вирусные частицы в окружающуо среду, инерционность активной выработки антител на инфекционный агент (антитела образуются через несколько дней до недели в количестве, достаточном для их обнаружения), перекрёстная реакция с другими видами коронавирусов человека [21][22]. Данные серологические тесты могут быть полезны у пациентов сна поздних стадиях заболевания, когда снижается репликация и активное вирусовыделение SAES-CoV-2, в этом случае молекулярно-генетические тесты дадут ложноотрицательный результат. Ряд исследований, например, показывает почти 100 % корреляции между положительным анализом методом RT-PCR и уровнем выработанных специфических антител класса IgM, и IgG методом ИФА у пациентов, госпитализированных с симптомами COVID19 [23]. Также, как показано на выше приведенной схеме, такие тесты незаменимы для эпидемиологического наблюдения и эпидемиологических исследований, могут также применяться для разработки вакцинных препаратов и вакцин против нового коронавируса и. потенциально, полезны для медицинских работников, причем. Необязательно напрямую контактирующих с больными COVID19.
Финансирование. За счёт ГАУ РО Областной консультативно-диагностический центр.
Financing: at the cost Regional consulting and diagnostic center, Rostov-on-Don.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interest. Authors declares no conflict of interest.
1. Center for Systems Science and Engineering (2020) CoronavirusCOVID-19 global cases. Johns Hopkins University. Accessed 3 Apr 2020. https://coronavirus.jhu.edu/map.html
2. FIND. COVID-19 Diagnostics Resource Centre. http://www.finddx.org/covid-19/
3. FIND. COVID-19 Diagnostics Resource Centre. http://www.finddx.org/covid-19/
4. Centers for Disease Control and Pevention. Interim Guidelines for Collecting, Handling, and Testing Clinical Specimens from Persons for Coronavirus Disease 2019 (COVID-19).
https://www.cdc.gov/coronavirus/2019-nCoV/lab/guidelines-clinical-specimens%20html
5. FIND. SARS-CoV-2 Diagnostic Pipeline. https://www.finddx.org/covid-19/pipeline/
Список литературы
1. Paoli D, Pallotti F, Colangelo S, Basilico F, Mazzuti L, Turriziani O, et al. Study of SARS-CoV-2 in semen and urine samples of a volunteer with positive naso-pharyngeal swab. // J Endocrinol Invest. – 2020. – V.23. – P.1–4. https://doi.org/10.1007/s40618-020-01261-1
2. Ashour HM, Elkhatib WF, Rahman MM, Elshabrawy HA. Insights into the Recent 2019 Novel Coronavirus (SARSCoV-2) in Light of Past Human Coronavirus Outbreaks. // Pathogens. – 2020. – V.9(3). – P.186. https://doi.org/10.3390/pathogens9030186
3. Cascella M, Rajnik M, Cuomo A, Dulebohn SC, Di Napoli R. Features, Evaluation, and Treatment of Coronavirus (COVID-19) [Updated 2020 Aug 10]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2020 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK554776/
4. Chen Y, Guo Y, Pan Y, Zhao ZJ. Structure analysis of the receptor binding of 2019-nCoV. // Biochemical and Biophysical Research Communications. – 2020. – V.525, Is.1. – P. 135-140. https://doi.org/10.1016/j.bbrc.2020.02.071.
6. Xie C, Jiang L, Huang G, Pu H, Gong B, Lin H, et al. Comparison of different samples for 2019 novel coronavirus detection by nucleic acid amplification tests. // Int J Infect Dis. – 2020. – V.93. – P.264-267. https://doi.org/10.1016/j.ijid.2020.02.050.
7. Peng X, Xu X, Li Y, Cheng L, Zhou X, Ren B. Transmission routes of 2019-nCoV and controls in dental practice. // International Journal of Oral Science. – 2020. – V.12(1). https://doi.org/10.1038/s41368-020-0075-9
8. Cheng MP, Papenburg J, Desjardins M, Kanjilal S, Quach C, Libman M, et al. Diagnostic Testing for Severe Acute Respiratory Syndrome–Related Coronavirus-2. A Narrative Review. // Ann Intern Med. – 2020. – V. 172(11). – P. 726-734. https://doi.org/10.7326/M20-1301.
9. Li R, Pei S, Chen B, Song Y, Zhang T, et al. Substantial undocumented infection facilitates the rapid dissemination of novel coronavirus (SARS-CoV-2). // Science. – 2020. – V. 368(6490). – P. 489-493. https://doi.org/10.1126/science.abb3221
10. Sheridan C. Fast, portable tests come online to curb coronavirus pandemic. // Nat Biotechnol. – 2020. – V. 38(5). – P. 515-518. https://doi.org/10.1038/d41587-020-00010-2
13. Wang CJ, Ng CY, Brook RH. Response to COVID-19 in Taiwan. // JAMA. – 2020. – V. 323(14). – P.1341. https://doi.org/10.1001/jama.2020.3151
14. Webb GF, Blaser MJ, Zhu H, Ardal S, Wu J. Critical role of nosocomial transmission in the toronto sars outbreak. // Math Biosci Eng. – 2004. – V. 1(1). – P.1-13. https://doi.org/10.3934/mbe.2004.1.1.
15. Wong T, Wallington T, McDonald LC, Abbas Z, Christian M, et al. Late recognition of SARS in nosocomial outbreak, Toronto. // Emerg Infect Dis. – 2005. – V.11(2). – P.322-5. https://doi.org/10.3201/eid1102.040607.
16. Zou L, Ruan F, Huang M, Liang L, Huang H, et al. SARSCoV-2 Viral Load in Upper Respiratory Specimens of Infected Patients. N // Engl J Med. – 2020. – V. 382(12). – P.1177-1179. https://doi.org/10.1056/NEJMc2001737.
17. Wang W, Xu Y, Gao R, Lu R, Han K, et al. Detection of SARSCoV-2 in Different Types of Clinical Specimens. // JAMA. – 2020. – V. 323(18). – P.1843–4. https://doi.org/10.1001/jama.2020.3786.
19. A Hogan C, Caya C, Papenburg J. Rapid and simple molecular tests for the detection of respiratory syncytial virus: a review. // Expert Rev Mol Diagn. – 2018. – V.18(7). – P.617-629. https://doi.org/10.1080/14737159.2018.1487293.
20. Prendergast C, Papenburg J. Rapid antigen-based testing for respiratory syncytial virus: moving diagnostics from bench to bedside? // Future Microbiol. – 2013. – V.8(4). – P. 435-44. https://doi.org/10.2217/fmb.13.9.
21. Guo L, Ren L, Yang S, Xiao M, Chang D, et al. Profiling Early Humoral Response to Diagnose Novel Coronavirus Disease (COVID-19). // Clin Infect Dis. – 2020. – V. 71(15). – P. 778- 785. https://doi.org/10.1093/cid/ciaa310.
22. Patrick DM, Petric M, Skowronski DM, Guasparini R, Booth TF, et al. An Outbreak of Human Coronavirus OC43 Infection and Serological Cross-reactivity with SARS Coronavirus. // Can J Infect Dis Med Microbiol. – 2006. – V.17(6). – P.330-6. https://doi.org/10.1155/2006/152612.
23. Infantino M, Grossi V, Lari B, Bambi R, Perri A, Manneschi M, et al. Diagnostic accuracy of an automated chemiluminescent immunoassay for anti‐SARS‐CoV‐2 IgM and IgG antibodies: an Italian experience. // Journal of Medical Virology. – 2020. – V.92(9). – P. 1671-1675. https://doi.org/10.1002/jmv.25932
Об авторах
Перевезенцев Олег Александрович, кандидат медицинских наук, ассистент кафедры персонализированной и трансляционной медицины
Холодная Татьяна Олеговна, кандидат медицинских наук, ассистент кафедры персонализированной и трансляционной медицины
Самсонов Андрей Евгеньевич, заведующий учебной частью персонализированной и трансляционной медицины
Бурцев Дмитрий Владимирович, доктор медицинских наук, доцент, заведующий кафедрой персонализированной и трансляционной медицины
Для цитирования:
Перевезенцев О.А., Холодная Т.О., Самсонов А.Е., Бурцев Д.В. Методы специфического лабораторного тестирования новой коронавирусной инфекции. Медицинский вестник Юга России. 2020;11(3):27-33. https://doi.org/10.21886/2219-8075-2020-11-3-27-33
For citation:
Perevesentsev O.A., Cholodnaya T.O., Samsonov A.E., Burtsev D.V. Methods of specific laboratory testing of new coronavirus infection. Medical Herald of the South of Russia. 2020;11(3):27-33. (In Russ.) https://doi.org/10.21886/2219-8075-2020-11-3-27-33