Как определить анод и катод
Классические термины из физики и химии часто встречаются в инструкциях к использованию современных приборов. Необходимо точно знать, что такое определение под собой подразумевает и как его применять к тем или иным конструкциям и явлениям.
Что такое анод и катод
Потребитель сталкивается с понятиями анод и катод при зарядке и разрядке аккумулятора, зарядке и обслуживании батареи.
Понять разницу между катодом, анодом, положительным и отрицательным зарядом проще всего, вспомнив некоторые положения из электрохимии.
В обоих случаях один из электродов несет более высокий потенциал. Этот электрод считается положительным. Электрод с более низким потенциалом и необязательно отрицательным, будет носить название отрицательный. Ток, соответственно, течет от носителя более высокого потенциала к носителю более низкого потенциала.
По определению анодом выступает электрод, на котором протекает окислительная реакция. Это означает, что электрод служит источником электронов. В химии его же нередко именуют восстановителем.
Катод
Под катодом подразумевают электрод, на котором протекает реакция восстановления. Здесь электрод забирает электроны и называется окислителем.
Принимая, что ток является движением положительно заряженных частиц, а не отрицательных, получается, что ток в растворе идет от катода к аноду. В цепи, соединяющей элементы гальванической пары, электроны идут от минуса к плюсу и с этой точки зрения катод является плюсом, а анод – минусом.
Противоречие кажущееся, ведь направление тока определяется движением положительных частиц, хотя фактически в металлической цепи его обеспечивает движение электронов.
Как определить анод и катод
Если с батарейкой все довольно просто (полюс и минус не меняются местами), то с зарядкой аккумулятора дело обстоит сложнее.
Во время зарядки разность между большим и меньшим потенциалом увеличивается, то есть потенциал положительного электрода становится выше, чем его же потенциал в покое – накапливается заряд, а потенциал отрицательного электрода становится меньше, чем он же в состоянии покоя. Отсюда вытекает, что положительный электрод выступает анодом, а отрицательный – катодом.
При использовании устройства потенциал положительного электрода (анода) всегда остается больше, чем потенциал отрицательного (катода). Но во время цикла разрядки/зарядки роль электрода меняется: при разрядке положительным становится катод, отрицательным – анод. Во время зарядки положительным выступает анод, отрицательным – катод.
Если речь идет о растворах и электрофизических реакциях в них, проще запомнить, что катионы – всегда частицы с положительным зарядом, а значит двигаются к минусу. Анионы – частицы всегда с отрицательным зарядом и двигаются к плюсу.
Что такое анод и катод: объясняю простыми словами
Для корректной работы полупроводниковых приборов, работающих в цепях с постоянным током, электроды радиоэлементов необходимо подключать с учетом их полярности. Неправильное подключение может привести к выходу из строя радиоэлемента либо к отказу в работе электронного прибора. С целью избегания ошибок электроды таких деталей получили специальное название – анод и катод.
Часто эти электроды обозначаются на схемах соответствующими символами «+» или «–», либо определяются по схематическому изображению радиоэлемента. На корпусах деталей иногда проставляется точка или другая метка, позволяющая определить направление тока на конкретном электроде. Иногда полярность выводов приходится определять по специальным таблицам или с помощью измерительного прибора.
Понятие анода и катода
Для лучшего понимания терминов дадим определения этих понятий.
Под данным термином будем подразумевать электрод, по которому электрический ток втекает в разглядываемый прибор. При этом подразумевается, что электрический ток образуется потоком положительных зарядов. В действительности, по металлическим проводникам перемещаются электроны (носители отрицательных зарядов), которые движутся в сторону положительного полюса источника электрического тока.
Проще говоря, положительным электродом будем считать анод, а отрицательным электродом – катод. При подключении радиоэлементов следует соблюдать их полярность, руководствуясь обозначениями на схемах.
Катод
Это электрод, по которому электрический ток вытекает с прибора (подразумевается конвенциальное понимание тока, в виде потока положительных зарядов). Таким образом, если к аноду подключается провод с положительным потенциалом, то к катоду – клеммы с отрицательными потенциалами.
Вышеуказанные термины применяются по отношению к гальваническим элементам. В гальванике анод – это электрод, на поверхности которого проходит реакция окисления металла. Названия электродов встречаются:
При монтаже радиодеталей очень важно не перепутать электроды. Для этого необходимо знать, как определить их назначение.
Как определить, где анод, а где катод?
При определении катода и анода необходимо в первую очередь ориентироваться на направление тока, а не на полярность источника питания. Несмотря на то, что эти понятия тесно связаны с полярностью тока, они больше обусловлены направлениями векторов электричества.
Например, в аккумуляторах, при перезарядке, происходит изменение ролей катода и анода. Это связано с тем, что во время зарядки изменяется направление электрического тока. Электрод, выполнявший роль электрода при работе аккумулятора в режиме источника питания во время зарядки выполняет функции катода и наоборот – катод превращается в анод.
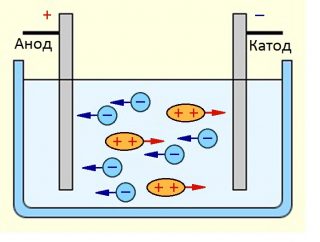
На рис. 1, изображено процесс электролиза, при котором происходит перемещение анионов (отрицательных ионов) и катионов (положительных ионов). Анионы устремляются к аноду, а положительные катионы – в сторону катода.
При электролизе перемещаются носители зарядов разных знаков, однако, по определению, анодом является тот электрод, в который втекает ток. На рисунке анод подсоединён к положительному полюсу источника тока, а значит, ток условно втекает в этот электрод.
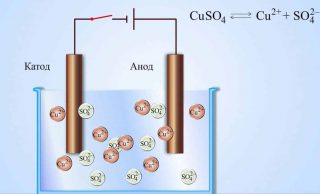
Обратите внимание на рисунок 2, где изображена схема гальванического элемента.

Плюсовой вывод источника тока является катодом, а не анодом, как можно было бы ожидать. При внимательном изучении принципа работы гальванического элемента можно понять, почему анод является отрицательным полюсом.
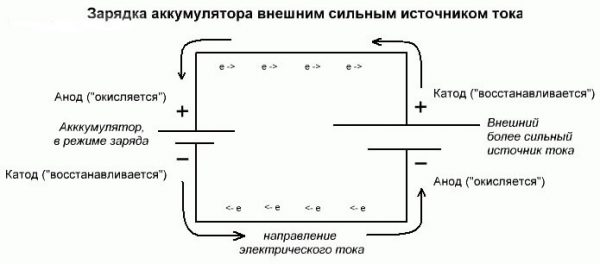
Обратите внимание на рисунок строения гальванического источника тока. Стрелки (вверху) указывают направление движения электронов, однако направлением тока условно принято считать перемещение от плюса к минусу. То есть, при замыкании цепи, ток входит именно в отрицательный полюс, который и является анодом, на котором происходит реакция окисления. Иначе говоря, ток от положительного электрода через нагрузку попадает на анод, являющийся отрицательным полюсом гальванического элемента. При вдумчивом подходе все стает на свои места.
При определении позиций анода и катода в радиоэлектронных элементах пользуются справочными материалами.
На назначение электродов указывает:
Определение назначений выводов у полупроводниковых диодов можно определить с помощью измерительных приборов. Например, все типы диодов (кроме стабилитронов) проводят ток только в одном направлении. Если вы подключили тестер или омметр к диоду, и он показал незначительное сопротивление, то к положительному щупу прибора подключен анод, а к отрицательному – катод.
Если известен тип проводимости транзистора, то с помощью того же тестера можно определить выводы эмиттера и коллектора. Между ними сопротивление бесконечно велико (тока нет), а между базой и каждым из них проводимость будет (только в одну сторону, как у диода). Зная тип проводимости, по аналогии с диодом, можно определить: где анод, а где катод, а значит определить выводы коллектора или эмиттера (см. рис. 5).

Что касается вакуумных диодов, то их невозможно проверить путем измерения обычными приборами. Поэтому их выводы расположены таким образом, чтобы исключить ошибки при подключении. В электронных лампах выводы точно совпадают с расположением контактов гнезда, предназначенного для этого радиоэлемента.
Анод и катод: где плюс, а где минус?
Из сказанного выше следует, что ток всегда течет в направлении от анода к катоду. Вывод один – на анод поступает плюс, а катод подсоединяется к минусу. Придерживаясь этого правила можно безошибочно определить, где плюс, а где минус.

В гальванотехнике на катоде происходит реакция восстановления. То есть положительные ионы из раствора оседают на катоде. По этому признаку определяем знак минус.
Как определить катод и анод радиодеталей мы рассмотрели выше. Если есть схема устройства то по ней довольно легко можно указать направление тока, и, соответственно, назначение электродов. При отсутствии схемы пользуйтесь признаками и метками на корпусах деталей.
Примечание: по отношению к стабилитрону некорректно применять термин катод и анод, так как он проводит ток в разных направлениях.
Отдельно заострю ваше внимание на элементах питания. Обычно «+» указывается на гальванических устройствах, а на аккумуляторах часто маркируются обе клеммы. В аккумуляторах автомобильного типа плюсовую клемму делают толще. По этому признаку также можно определить полярность полюсов.
В качестве выводов см. рисунок 6.
Цифрами обозначено:
Применение
Электроды в качестве анода и катода наиболее часто применяются:
Рассмотрим в общих чертах сферы применения анодов и катодов.
В электрохимии
В данной сфере анод и катод являются ключевыми понятиями, в процессе прохождения электрохимических реакций, используемых в основном для восстановления металлов. Такие реакции называют электролизом. Использование процессов электролиза позволяет получать чистые металлы, так как на катоде образуются атомы только того металла, положительные ионы которого содержатся в растворе электролита.
Методом электролиза наносят очень тонкое цинковое покрытие стальных листов и деталей любой конфигурации. Гальваническое покрытие эффективно защищает металл от коррозии.
В вакуумных электронных приборах
Примером вакуумных приборов служат радиоэлектронные лампы, электронно-лучевые трубки, кинескопы телевизоров. Они работают по одному и тому же принципу: Разогретый катод испускает электроны, которые устремляются к аноду с высоким положительным электрическим потенциалом.
Образование электронов на раскаленном электроде называется термоэмиссией, а электрический ток, возникающий между катодом и анодом, называется термоэмиссионным. Ценность таких приборов в том, что они проводят ток только в одном направлении – от катода к аноду.
Добавление сетки между электродами позволяет регулировать параметры тока в широких пределах, путем изменения напряжения на сетке. Такие вакуумные лампы используются в качестве усилителей сигналов. В данное время вакуумные приборы используются довольно редко, так как их с успехом заменяют миниатюрные полупроводниковые диоды и транзисторы, часто выполненные на монокристалле в виде микросхемы.
В полупроводниковых приборах
Электронные детали на основе полупроводников ценятся малым потреблением тока и небольшими размерами. Они почти вытеснили вакуумные лампы из употребления. Выводы полупроводниковых приборов традиционно называют анодами и катодами.
При всех плюсах полупроводников, у этих приборов есть недостаток – они «шумят». В усилителях большой мощности эти шумы становятся заметными. В качественной усилительной аппаратуре по-прежнему применяются вакуумные лампы.
Электронно-лучевые кинескопы в современных телевизорах вытесняются экранами с LED подсветкой. Они более экономичны, отлично передают цветовую палитру, позволяют сделать приемник почти плоским.
как определить какой металл будет служить анодом при работе гальванического элемента?
В гальваническом элементе анодом становится металл, обладающий меньшим значением электродного потенциала, а катодом – металл с большим значением электродного потенциала. К примеру, гальванический элемент состоит из цинкового и никелевого электродов, опущенных в раствор своей соли. Как определить, какой из двух электродов в гальваническом элементе будет являться анодом, а какой катодом?
Отвечаю. Почти в каждом задачнике по химии в конце задачника есть таблица стандартных электродных потенциалов. Открываешь его и ищешь стандартные электродные потенциалы цинка и никеля по полуреакциям восстановления.
Zn(2+) + 2e = Zn | Еº(Zn(2+)/Zn) = − 0,76 B
Ni(2+) + 2e = Ni | E°(Ni(2+)/Ni) = – 0,234 B
E°(Ni(2+)/Ni) > Еº(Zn(2+)/Zn)
Стандартный электродный потенциал никеля больше, чем стандартный электродный потенциал цинка, значит, в данном гальваническом элементе цинковый электрод будет анодом, а никелевый – катодом.
Кроме того, для того чтобы определиться, какой из двух металлов в гальваническом элементе является анодом, а какой – катодом, можно воспользоваться электрохимическим рядом напряжений. Чем левее стоит металл в электрохимическим ряду напряжений, тем более сильным восстановителем он является, значит, тем меньшее имеет значение стандартного электродного потенциала восстановления. Металл, стоящий в электрохимическом ряду напряжений левее является анодом, а металл, стоящий в электрохимическом ряду напряжений правее – катодом.
Электрохимический ряд напряжений металлов (сокращенный вариант)
Li, K, Ca, Na, Mg, Al, Zn, Cr, Fe, Ni, Pb, H2, Cu, Ag, Hg, Au
Как видишь, цинк в электрохимическом ряду напряжений стоит левее, а никель – правее. Значит, в гальваническом элементе цинковый электрод будет являться анодом, а никелевый – катодом.
Какой металл называется анодом при контакте двух металлов
Ано́д (др.-греч. ἄνοδος — движение вверх) — электрод некоторого прибора, присоединённый к положительному полюсу источника питания. Электрический потенциал анода положителен по отношению к потенциалу катода.
Содержание
Анод в электрохимии
При процессах электролиза (получение элементов из солевых растворов и расплавов под действием постоянного электрического тока), анод — электрически положительный полюс, на нём происходят окислительно-восстановительные реакции (окисление), результатом которых, в определённых условиях, может быть разрушение (растворение) анода, что используется, к примеру, при электрорафинировании металлов.
Аноды — множественное число слова «анод»; эта форма применяется преимущественно в металлургии, где применяются аноды для гальваники, используемые для нанесения на поверхность изделия слоя металла электрохимическим способом, либо для электрорафинирования, где металл с примесями растворяется на аноде и осаждается в очищенном виде на катоде. Основное распространение получили аноды из цинка (бывают сферические, литые и катаные, чаще используются последние), никеля, меди (среди которых отдельно выделяют медно-фосфористые, марки АМФ), кадмия (применение которых сокращается из-за экологической вредности), бронзы, олова (применяются при производстве печатных плат в радиоэлектронной промышленности), сплава свинца и сурьмы, серебра, золота и платины. Аноды из недрагоценных металлов применяются для повышения коррозионной стойкости, повышения эстетических свойств предметов и др. целей. Аноды из драгоценных металлов применяются гальваническим производством для повышения электропроводности изделий и др.
Анод в вакуумных электронных приборах
В вакуумных электронных приборах анод — электрод, который притягивает к себе летящие электроны, испущенные катодом. В электронных лампах и рентгеновских трубках конструкция анода такова, что он полностью поглощает электроны. А в электронно-лучевых приборах анод является элементом электронной пушки. Он поглощает лишь часть летящих электронов, формируя после себя электронный луч.
Анод у полупроводниковых приборов
Электрод полупроводникового прибора (диода, тиристора), подключённый к положительному полюсу источника тока, когда прибор открыт (то есть имеет маленькое сопротивление), называют анодом, подключённый к отрицательному полюсу — катодом.
Знак анода и катода
В литературе встречается различное обозначение знака анода — «+» или «-», что определяется, в частности, особенностями рассматриваемых процессов.
В то же время при работе гальванического элемента (к примеру, медно-цинкового), избыток электронов (и отрицательный заряд) на одном из электродов обеспечивается не внешним источником тока, а собственно реакцией окисления металла (растворения цинка), то есть здесь отрицательным, если следовать приведённому определению, будет уже анод. Электроны, проходя через внешнюю цепь, расходуются на протекание реакции восстановления (меди), то есть катодом будет являться положительный электрод.
В электротехнике анод — положительный электрод, ток течет от анода к катоду, электроны, соответственно, наоборот.
См. также
Литература
Ссылки
Полезное
Смотреть что такое «Анод» в других словарях:
АНОД — (греч. anodos восходящая дорога). В гальваническом элементе, одна из двух пластинок или проволок, по которой вступает или выходит из жидкости электрический ток. Противоположность катоду. Словарь иностранных слов, вошедших в состав русского языка … Словарь иностранных слов русского языка
анод — отрицательный электрод Словарь русских синонимов. анод сущ., кол во синонимов: 1 • электрод (10) Словарь синонимов ASIS. В.Н. Тришин … Словарь синонимов
анод — электровакуумного прибора; анод; отрасл. коллектор Электрод, основным назначением которого обычно является прием основного потока электронов при электрическом разряде … Политехнический терминологический толковый словарь
анод — (устройства) электрод, через который электрический ток входит в среду, имеющую удельную проводимость, отличную от удельной проводимости анода [СТ МЭК50(151) 78] анод [IEV number 151 13 02] EN anode electrode capable of emitting positive charge… … Справочник технического переводчика
АНОД — (от греческого anodos движение вверх, восхождение), электрод электронного или электротехнического прибора (например, электронной лампы, гальванического элемента, электролитической ванны), характеризующийся тем, что движение электронов во внешней… … Современная энциклопедия
АНОД — (от греч. anodos движение вверх восхождение), электрод радио или электротехнического прибора или устройства (напр., гальванического элемента, электронной лампы, электролитической ванны), характеризующийся тем, что движение электронов (во внешней… … Большой Энциклопедический словарь
АНОД — АНОД, положительный ЭЛЕКТРОД электролитической батареи, к которому притягиваются АНИОНЫ в процессе ЭЛЕКТРОЛИЗА … Научно-технический энциклопедический словарь
АНОД — АНОД, анода, муж. (греч. anodos восхождение) (физ.). Положительный электрод, ант. катод. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
АНОД — АНОД, а, муж. (спец.). Положительный электрод; противоп. катод. | прил. анодный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
АНОД — (от греч. anodos движение вверх), 1) электрод электронного или ионного прибора, соединяемый с положит. полюсом источника. 2) Положит. электрод источника электрич. тока (гальванич. элемента, аккумулятора). 3) Положит. электрод электрич. дуги.… … Физическая энциклопедия
Что такое анод и катод?
Часто возникает проблема определения, какой из электродов является катодом, а какой — анодом. Для начала нужно разобраться с терминами.
Понятие катода и анода — простое объяснение
В сложных веществах электроны между атомами в соединениях распределены неодинаково. В результате взаимодействия частицы перемещаются от атома одного вещества к атому другого. Реакция именуется окислительно-восстановительной. Потеря электронов называется окислением, элемент, отдающий электроны — восстановителем.
Присоединение электронов носит название восстановление, принимающий элемент в этом процессе — окислитель. Переход электронов от восстановителя к окислителю может протекать по внешней цепи, и тогда его можно использовать в качестве источника электрической энергии. Устройства, в которых энергия химической реакции превращается в электрическую энергию, называются гальваническими элементами.
Простейший классический пример гальванического элемента — две пластины, изготовленные из различного металла и погруженные в раствор электролита. В такой системе окисление происходит на одном металле, а восстановление — на другом.
ВАЖНО! Электрод, на котором протекает окисление, называется анодом. Электрод, на котором протекает восстановление — катодом.
Из школьных учебников химии известен пример медно-цинкового гальванического элемента, работающего за счет энергии реакции между цинком и сульфатом меди. В устройстве Якоби — Даниэля пластина из меди помещена в раствор сульфата меди (медный электрод), цинковая пластина погружена в раствор сульфата цинка (цинковый электрод). Цинковый электрод отдает катионы в раствор, создавая в нем избыточный положительный заряд, а у медного электрода раствор обедняется катионами, здесь раствор заряжен отрицательно.
Замыкание внешней цепи заставляет электроны перетекать от цинкового электрода к медному. Равновесные отношения на границах фаз прерываются. Идёт окислительно-восстановительная реакция.
Энергия самопроизвольно протекающей химической реакции превращается в электрическую.
Если химическую реакцию провоцирует внешняя энергия электрического тока, идёт процесс, называемый электролизом. Процессы, протекающие при электролизе, обратны процессам, протекающим при работе гальванического элемента.
ВНИМАНИЕ! Электрод, на котором происходит восстановление, также называется катодом, но при электролизе он заряжен отрицательно, а анод — положительно.
Применение в электрохимии
Аноды и катоды принимают участие во многих химических реакциях:
Электролизом расплавленных соединений и водных растворов получают металлы, производят очистку металлов от примесей и извлечение ценных компонентов (электролитическое рафинирование). Из металла, подлежащего очистке, отливают пластины. Они помещаются в качестве анодов в электролизер. Под воздействием электрического тока металл подвергается растворению. Его катионы переходят в раствор и разряжаются на катоде, образуя осадок чистого металла. Примеси, содержащиеся в первоначальной неочищенной металлической пластине, либо остаются нерастворимыми в виде анодного шлама, либо переходят в электролите, откуда удаляются. Электролитическому рафинированию подвергают медь, никель, свинец, золото, серебро, олово.
Электроэкстракция — процесс выделения металла из раствора в ходе электролиза. Для того чтобы металл перешёл в раствор, его обрабатывают специальными реагентами. В ходе процесса на катоде происходит выделение металла, характеризующегося высокой чистотой. Так получают цинк, медь, кадмий.
Чтобы избежать коррозии, придать прочность, украсить изделие поверхность одного металла покрывают слоем другого. Этот процесс называется гальваностегией.
Гальванопластика — процесс получения металлических копий с объёмных предметов электроосаждением металла.
Применение в вакуумных электронных приборах
Принцип действия катода и анода в вакуумном приборе может продемонстрировать электронная лампа. Она выглядит как герметически запаянный сосуд с металлическими деталями внутри. Прибор используется для выпрямления, генерирования и преобразования электрических сигналов. По числу электродов выделяют:
Диод — вакуумный прибор с двумя электродами, катодом и анодом. Катод подключен к отрицательному полюсу источника питания, анод — к положительному. Предназначение катода — испускать электроны под действием нагрева электрическим током до определенной температуры. Посредством испущенных электронов создается пространственный заряд между катодом и анодом. Самые быстрые электроны устремляются к аноду, преодолевая отрицательный потенциальный барьер объемного заряда. Анод принимает эти частицы. Создается анодный ток во внешней цепи. Электронным потоком управляют с помощью дополнительных электродов, подавая на них электрический потенциал. Посредством диодов переменный ток преобразуется в постоянный.
Применение в электронике
Сегодня используется полупроводниковые типы диодов.
В электронике широко используется свойство диодов пропускать ток в прямом направлении и не пропускать в обратном.
Работа светодиода основана на свойстве кристаллов полупроводников светиться при пропускании через p-n переход тока в прямом направлении.
Гальванические источники постоянного тока — аккумуляторы
Химические источники электрического тока, в которых протекают обратимые реакции, называются аккумуляторами: их перезаряжают и используют многократно.
При работе свинцового аккумулятора происходит окислительно-восстановительная реакция. Металлический свинец окисляется, отдает свои электроны, восстанавливая диоксид свинца, принимающего электроны. Металлический свинец в аккумуляторе — анод, он заряжен отрицательно. Диоксид свинца — катод и заряжен положительно.
По мере разряда аккумулятора расходуются вещества катода и анода и их электролита, серной кислоты. Чтобы зарядить аккумулятор, его подключают к источнику тока (плюсом к плюсу, минусом к минусу). Направление тока теперь обратное тому, какое было при разряде аккумулятора. Электрохимические процессы на электродах «обращаются». Теперь свинцовый электрод становится катодом, на нем проходит процесс восстановления, а диоксид свинца — анодом, с протекающей процедурой окисления. В аккумуляторе вновь создаются вещества, необходимые для его работы.