Жидкие металлы
Полезное
Смотреть что такое «Жидкие металлы» в других словарях:
ЖИДКИЕ МЕТАЛЛЫ — непрозрачные жидкости, обладающие большими теплопроводностью и электропроводностью, а также др. св вами, характерными для тв. металлов. Ж. м. явл. все расплавл. металлы и сплавы металлов с рядом металлидов. Нек рые полуметаллы и полупроводники… … Физическая энциклопедия
ЖИДКИЕ МЕТАЛЛЫ — расплавы всех металлов и ряда полупроводников (Si, Ge, InSb и др.), обладающие высокими электро и теплопроводностью, отрицательными коэффициентами электропроводности и другими свойствами твердых металлов. Многие жидкие полупроводники (расплавы Te … Большой Энциклопедический словарь
жидкие металлы — расплавы всех металлов и ряда полупроводников (Si, Ge, InSb и др.), обладающие высокими электро и теплопроводностью, отрицательным коэффициентом электропроводности и другими свойствами твёрдых металлов. Многие жидкие полупроводники (расплавы Te … … Энциклопедический словарь
Жидкие металлы — непрозрачные жидкости с характерным блеском, обладающие большой теплопроводностью, электропроводностью и другими особенными свойствами твердых металлов. Жидкими металлами являются все расплавленные металлы и сплавы металлов. Некоторые… … Энциклопедический словарь по металлургии
ЖИДКИЕ МЕТАЛЛЫ — непрозрачные жидкости с характерным блеском, обладающие большой теплопроводностью, электропроводностью и другими особенностями, свойственным твердым металлам. Жидкими металлами являются все расплавленные металлы и сплавы металлов. Некоторые… … Металлургический словарь
МЕТАЛЛЫ — (от греч. metallon, первоначально шахта, руда, копи), простые в ва, обладающие в обычных условиях характерными св вами: высокими электропроводностью и теплопроводностью, отрицательным температурным коэфф. электропроводности, способностью хорошо… … Физическая энциклопедия
Жидкие полупроводники — вещества, обладающие в жидком состоянии свойствами полупроводников (См. Полупроводники). Плавление многих твёрдых полупроводников (Si, Ge и др.) сопровождается резким увеличением электропроводности до значений, типичных для металлов (См.… … Большая советская энциклопедия
ЖИДКОСТЬ — агрегатное состояние в ва, промежуточное между твёрдым и газообразным. Ж. присущи нек рые черты твёрдого тела (сохраняет свой объём, образует поверхность, обладает определ. прочностью на разрыв) и газа (принимает форму сосуда, в к ром находится,… … Физическая энциклопедия
КОРРОЗИЯ МЕТАЛЛОВ — самопроизвольное физико химическое разрушение и превращение полезного металла в бесполезные химические соединения. Большинство компонентов окружающей среды, будь то жидкости или газы, способствуют коррозии металлов; постоянные природные… … Энциклопедия Кольера
Строение и свойства жидких металлов | 09.05.2012
Агрегатные состояния жидких металлов
Существует четыре основных состояния вещества: жидкое, твердое, газообразное и плазма, из которых к литейным процессам следует отнести два первых.
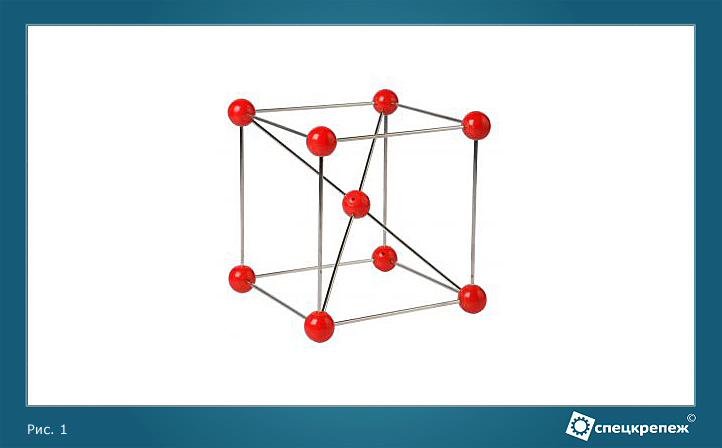
В обычных условиях структура металла представляет собой кристаллическую решетку. Кристалл рассматривают как правильную совокупность атомов, которые не обязательно имеют одинаковую природу. Всякий атом занимает свое место, определяемое характером его геометрической взаимосвязи с кристаллической решеткой и характеризующее собой среднее положение центра этого атома (рисунок 1).
Рисунок 1 – Кристаллическая решетка железа
В действительности атом совершает тепловые колебания в пространстве между соседними атомами. При нагревании в определенный момент тепловые колебания становятся настолько сильными, что дальний порядок между атомами нарушается и металл переходит в жидкое состояние.
Жидкие металлы, как и другие жидкости, незначительно перегретые над точкой начала кристаллизации, гораздо ближе по структуре и свойствам к твердому телу, нежели к газам. На это указывает ряд факторов:
Строение жидких металлов
Рисунок 2 – Кластер
В соответствии с теорией флуктуации в жидкости спонтанно возникают локальные отклонения от ее средней концентрации, энергии и плотности, число и вероятность которых диктуются законами статистической механики.
Для объяснения определенных свойств жидких расплавов используется теория Стюарта и Бенца, согласно которой в жидкостях непрерывно разрушаются и создаются группировки элементарных частиц, называемых роями или сиботаксисами. Эти группировки являются нестойкими образованиями и не имеют четких границ раздела.
Согласно кластерной модели Архарова и Новохатского расплав представляет собой сочетание кластеров и разупорядоченной зоны. Кластеры характеризуются определенной упорядоченностью строения центральной части и нестабильностью периферийных частей. При повышении температуры кластеры распадаются на более мелкие, при охлаждении металла укрупняются.
Основной смысл общепринятой в настоящее время теории Я.И. Френкеля состоит в том, что переход из твердого в жидкое состояние обусловлен скачкообразным увеличением количества вакансий. Это вызывает большую подвижность частиц и жидкости в целом, а также объясняет скачек растворимости многих веществ, при расплавлении растворителя. Необходимый избыток энергии обеспечивается флуктуациями. Вакансии (дырки) имеют размер порядка 10 –10 м. По Томпсону работа образования сферической полости в жидкости радиусом r равна:
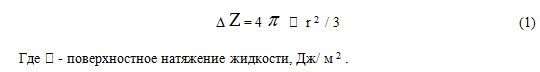
Работа ΔZ соизмерима с теплотой испарения. Важен тот факт, что для превращения жидкости в кристаллическое состояние необходимо при температуре превращения отвести тепло, соответствующее скрытой теплоте плавления. При этом атомы переводятся в позиции с меньшей потенциальной энергией, чем в жидкости. Однако в обоих случаях каждый атом имеет минимальную свободную энергию, но в жидкости эти минимумы выше, чем в кристалле.
В большинстве случаев плотность расплава меньше, чем у кристалла. Кристаллы же германия, кремния, галлия и висмута менее плотные своих расплавов и упругие свойства обеспечиваются исключительно упорядочением атомов.
Есть и другие теории жидкого состояния, но ни одна из них не позволяет по параметрам элементарных частиц жидкости высчитать ее микроскопические свойства. Не дают они объяснения многим явлениям, которые наблюдаются в жидкости, например, возможности значительного переохлаждения.
Свойства жидких металлов
Сходство жидкого и кристаллического состояния заключается, главным образом, в характере межчастичного взаимодействия и в термодинамических свойствах, но существует принципиальное различие в строении жидких и твердых тел. Известная хаотичность в расположении частиц в жидкости и большая их подвижность, роднящие жидкость с газами, сочетаются с сильным межчастичным взаимодействием, как и в твердом теле. Этим сочетанием обусловлен комплекс свойств, характерный только для жидкого состояния вещества.
Плотность
Подбором состава сплавов обеспечивают заданную его плотность и коэффициент линейного расширения. Это важно, например, для армированных (выполненных из разнородных материалов) изделий, служащих при изменяющихся в широких пределах температурах
Практическое значение изменения плотности металла до начала и в процессе кристаллизации состоит в том, что оно предопределяет объемную усадку (или рост), с которой связаны усадочные раковины, рыхлость, напряжения в наружных и внутренних участках слитков, заготовок и отливок (рисунок 3).
Температура плавления
Сталь 1420-1520 0 С
Чугун 1150-1250 0 С
Бронзы 1000-1150 0 С
Латуни 900- 950 0 С
Алюминиевые сплавы 580- 630 0 С
Магниевые сплавы 600- 650 0 С
Цинковые сплавы 390- 420 0 С
Так как фазовые превращения сопровождаются тепловыми эффектами, объемными изменениям и фазовыми напряжениями, то их учитывают, задавая оптимальные режимы охлаждения слитков, заготовок и отливок, а также при рассмотрении процессов структурообразования и ликвации.
Вязкость
Вода (25 0 С) – 0,00089;
Сталь (1600 0 С) – 0,0050 – 0,0085;
Железо (1600 0 С) – 0,0045 – 0,0050.
Поверхностное натяжение
Литейные свойства
Свойства, непосредственно влияющие на получение слитков и отливок требуемого качества, называются литейными. Они зависят от комплекса физико-химических свойств, проявляющихся в образующихся фазах при охлаждении расплава, но полностью ими не определяются. К литейным свойствам относят жидкотекучесть и заполняемость литейных форм, усадку и связанные с ней процессы образования различных дефектов, склонность к образованию дефектов на базе неметаллических и газовых включений, активность взаимодействия с окружающей средой и контактирующими материалами, первичную и вторичную кристаллизацию, литейные напряжения и трещиноустойчивость, химическую и структурную неоднородность. Лучшим сочетанием литейных свойств обладают сплавы с большим количеством эвтектики. Литейные свойства чугуна значительно выше литейных свойств стали.
|
| «Спецкрепеж» |
|