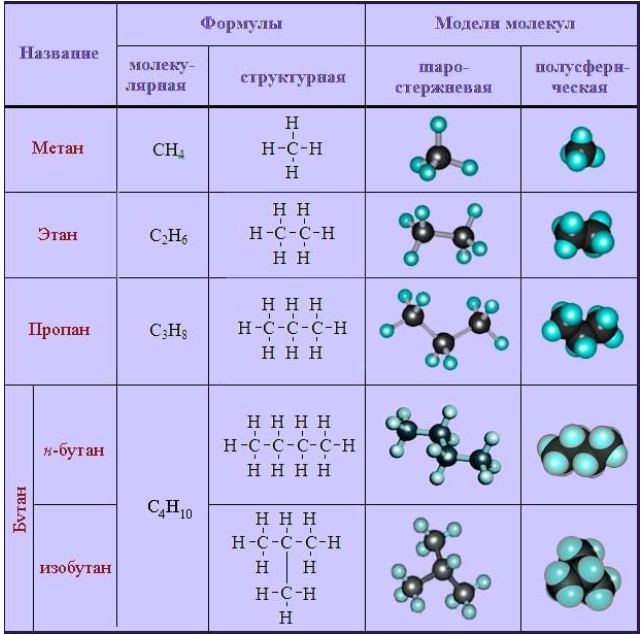
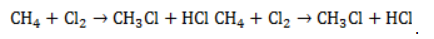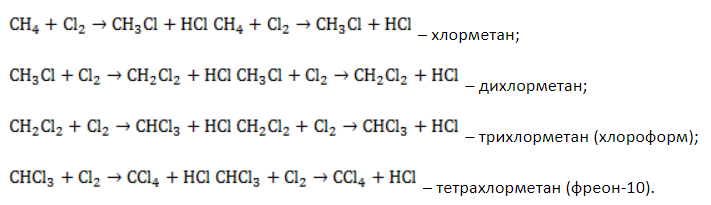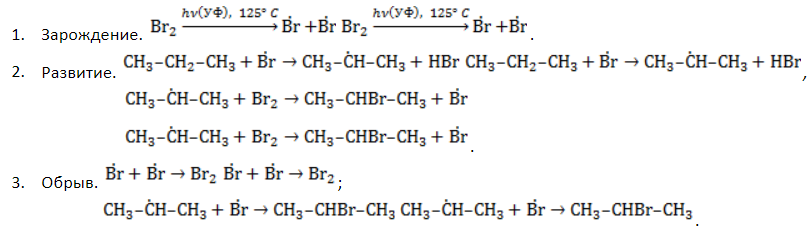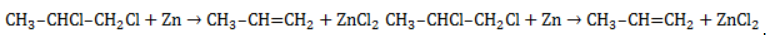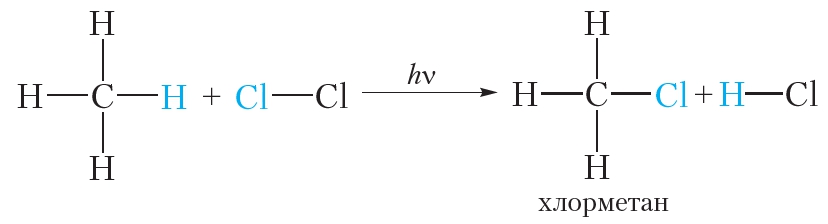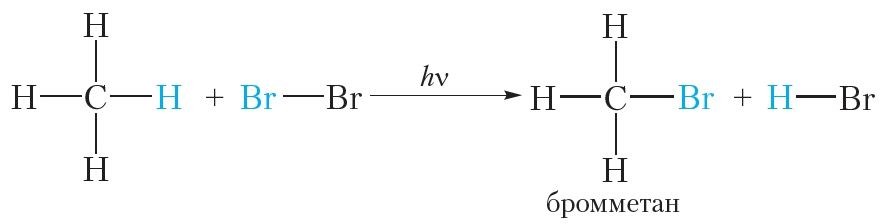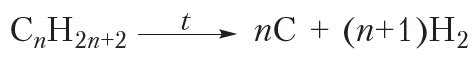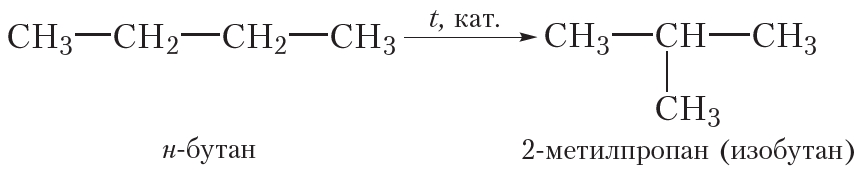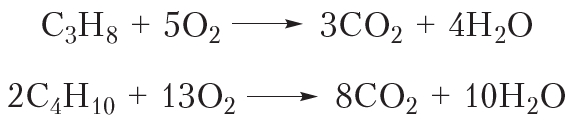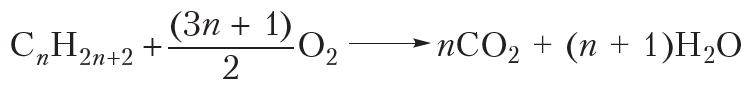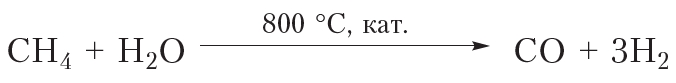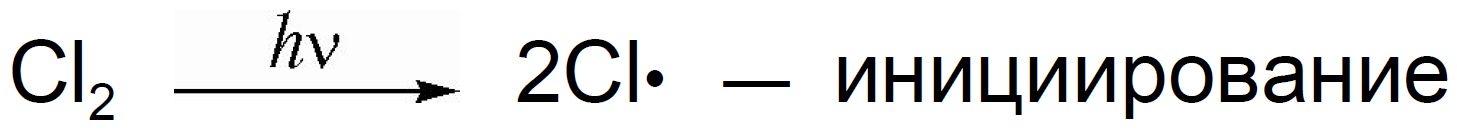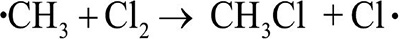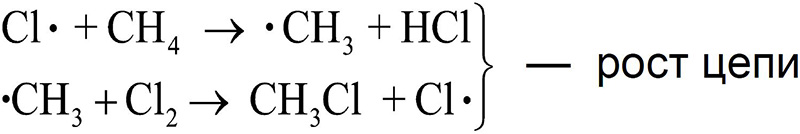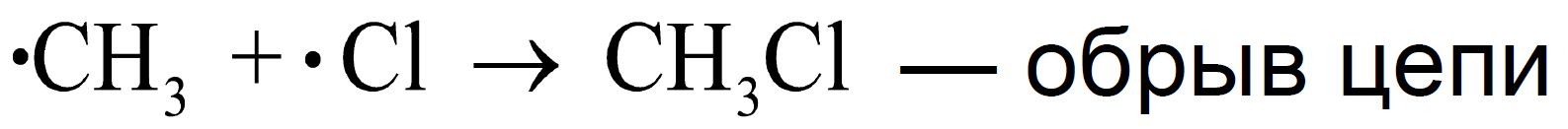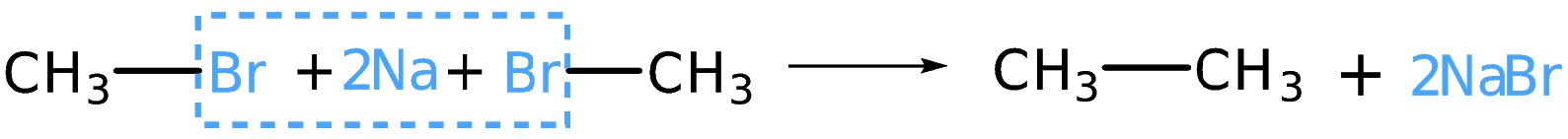Галогенирование алканов на примере пропана
Галогенирование – процесс присоединения к молекуле органического соединения атома галогена – это одно из химических взаимодействий, в которых участвуют углеводороды ряда алканов. Благодаря общности структуры молекул у всех членов гомологического ряда реакции с галогеном обладают единым характером. При этом галогенирование пропана и следующих за ним в гомологическом ряду соединений имеет особенности, связанные с наличием в молекулах вторичных, третичных и четвертичных атомов углерода.
Краткая характеристика алканов
К простейшим органическим соединениям относятся ациклические насыщенные, или предельные углеводороды (алканы). Их отличают следующие структурные особенности:
Общая формула имеет вид 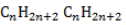
Механизм замещения у алканов носит радикальный характер, так как разрыв слабополярной связи C-H протекает с образованием пары свободных радикалов – нейтральных частиц, имеющих по одному неспаренному электрону. Атом водорода может замещаться галогеном, нитрогруппой или сульфогруппой.
Галогенирование алканов
Реакция свободно-радикального замещения (обозначается символом SR – от англ. substitution radical reaction) водородного атома в молекуле алкана атомом галогена называется галогенированием. Ее инициирование требует воздействия ультрафиолетового облучения или повышенной температуры. Реакция носит цепной характер, так как в каждом ее акте образуются свободные радикалы, генерирующие следующий акт.
Замещение фтором – фторирование – чрезвычайно экзотермический процесс, сопровождающийся взрывом и разрушением молекулы алкана. Реакция с участием йода, наоборот, является эндотермической и обратимой – в ходе ее происходит восстановление продукта реакции йодоводородом, поэтому прямое йодирование неэффективно. Практический интерес представляют реакции алканов с хлором и бромом.
Стадии галогенирования
Удобнее всего рассмотреть, какой механизм имеет реакция хлорирования алканов, на примере метана. При облучении или нагреве реакционной смеси реакция инициируется, и далее цепная реакция протекает в несколько стадий.
В общем виде уравнение галогенирования метана хлором записывается в форме:
Процесс замещения не ограничивается образованием хлорметана, на молекулы которого также воздействуют радикалы 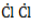
Выход продуктов зависит от мольного соотношения реагентов и условий реакции. Так, при эквимолярном количестве метана и хлора и температуре 440° C соотношение молярных долей продуктов в процентах составляет около 39:41:19:1.
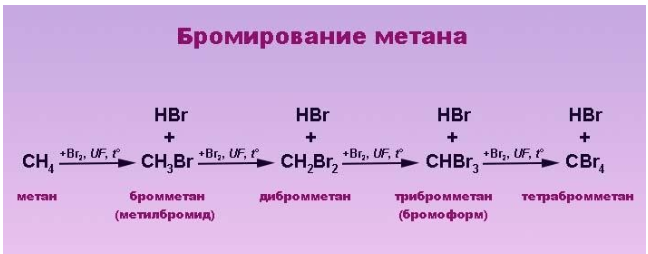
Реакция бромирования отличается меньшим выделением энергии и протекает медленнее, так как его реакционная способность ниже, чем у хлора.
Региоселективность
Начиная с пропана 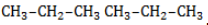
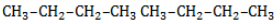
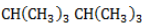
Селективность зависит от следующих факторов:
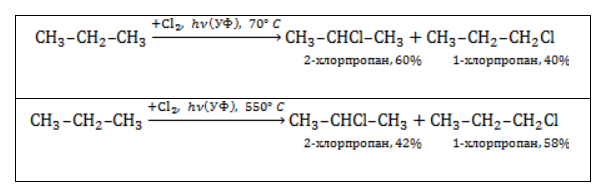
Хлорирование и бромирование пропана
В реакции пропана с хлором при низкой температуре селективная направленность выражена слабо. Несмотря на то, что образующиеся в ходе реакции радикалы 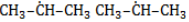
При нагревании радикалы хлора атакуют первичные атомы даже более активно, так как на разрыв их связи с водородом затрачивается меньше энергии.
При бромировании пропана региоселективность вследствие меньшей активности брома достигает высоких значений:
Бромирование протекает аналогично реакции с участием простейших алканов с преимущественным замещением водорода у вторичных атомов:
Продуктом этой реакции является 2-бромпропан.
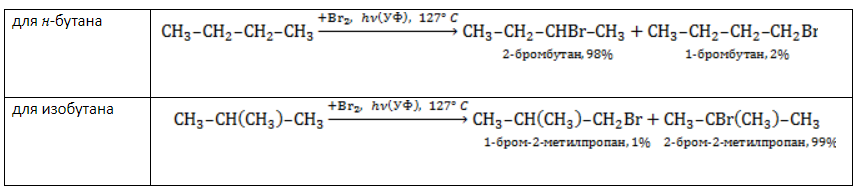
Галогенирование бутана
В реакциях бутана с хлором селективность не играет заметной роли. Даже при низкой температуре соотношение продуктов хлорирования может быть различным:
Бромирование бутана демонстрирует большую селективность:
Реакция отщепления
Активные двухвалентные металлы (как правило, магний или цинк) отщепляют от молекул дигалогеналканов атомы хлора или брома, если они замещают водород у двух соседних атомов углерода. Между последними образуется двойная связь. Продуктом такой реакции является алкен.
Пример реакции дегалогенирования алканов – отщепление цинком атомов хлора от 1,2-дихлорпропана с образованием пропилена (пропена) и хлорида цинка:
Применение галогеналканов
Хлорированные и бромированные алканы применяются в качестве промежуточных соединений в различных отраслях, таких как синтез высокомолекулярных соединений, производство лаков, красок и растворителей. Хлоралканы служат сырьем для фторалканов, которые нельзя получить прямым фторированием.
Токсичность галогеналканов тем меньше, чем активнее входящий в их состав галоген. Поэтому фторалканы наиболее безопасны. Фторсодержащие фреоны широко используются в качестве вспенивателей, хладагентов и пропеллентов.
Химия. 10 класс
§ 10. Химические свойства, получение и применение алканов
Химические свойства, получение и применение алканов
Существует огромное число различных алканов. Их многообразие объясняется как возможностью образования углеродных цепей различной длины, так и изомерией. В связи с этим изучать химические свойства каждого алкана отдельно не представляется возможным. В то же время молекулы различных алканов имеют сходное строение: атомы углерода соединены между собой и атомами водорода одинарными ковалентными связями. Учитывая это, можно ожидать, что химические свойства различных алканов будут во многом сходными.
Все алканы характеризуются низкой химической активностью. Они не взаимодействуют с растворами кислот, оснований, солей. На них не действует такой сильный окислитель, как KMnO4, и такие сильные восстановители, как щелочные металлы. Вы знаете, что щелочные металлы очень активны и реагируют практически со всеми веществами, с которыми соприкасаются, в том числе легко окисляются кислородом воздуха. Чтобы уберечь щелочные металлы от окисления, их хранят под слоем керосина — смеси, состоящей в основном из насыщенных углеводородов. При этом алканы, входящие в состав керосина, не реагируют со щелочными металлами.
Из-за низкой химической активности алканов реакции с их участием протекают в жёстких условиях (при нагревании или облучении ультрафиолетовым излучением).
Мы изучим реакции алканов с галогенами (Cl2 и Br2) и кислородом (O2), а также превращения, которые они претерпевают при нагревании.
1. Галогенирование. Взаимодействие с галогенами
Взаимодействие алканов с галогенами — хлором и бромом — протекает при нагревании или облучении ультрафиолетовым излучением.
Если смесью газообразных метана и хлора заполнить стеклянный сосуд и поместить его в тёмное место, реакция протекать не будет. Однако при нагревании смеси или облучении её ультрафиолетовым излучением протекает химическая реакция замещения атомов водорода в молекуле метана на атомы хлора:
В уравнениях реакций, протекающих при облучении, над стрелкой записывают буквы hv. Данная реакция называется реакцией галогенирования и относится к реакциям замещения.
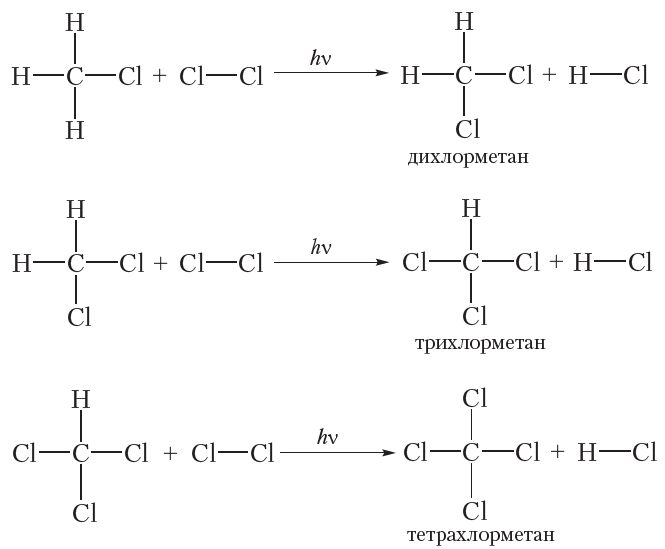
Если только один атом водорода в молекуле замещается на атом галогена, то реакцию называют моногалогенированием. Приведённая выше реакция является реакцией монохлорирования метана. В избытке хлора оставшиеся три атома водорода молекулы метана могут последовательно замещаться на галоген:
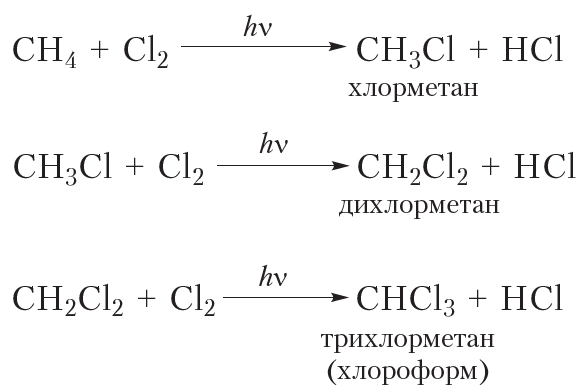
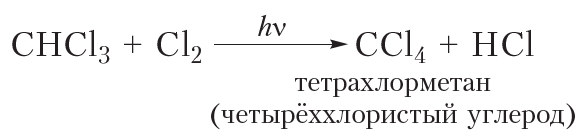
Приведём уравнения реакций всех четырёх стадий хлорирования метана с использованием молекулярных формул:
Рассмотрим реакции монохлорирования гомологов метана.
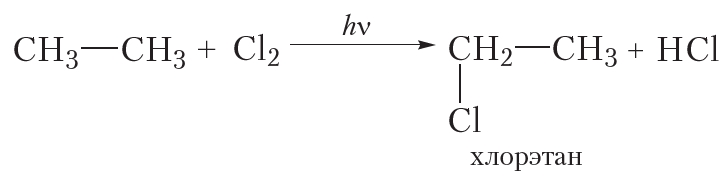
Для этана уравнение реакции следующее:
Отметим, что в названии «хлорэтан» нет необходимости указывать цифрой положение атома хлора. Это связано с тем, что при замещении любого атома водорода в молекуле этана на атом хлора образуется одно и то же вещество:
Таким образом, при монохлорировании этана так же, как и в случае метана, получается только одно органическое вещество — хлорэтан.
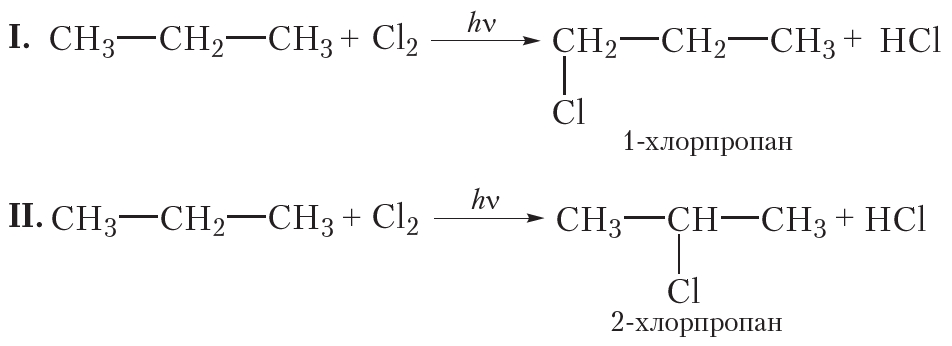
При монохлорировании пропана образуется смесь двух органических веществ:
В случае I происходит замещение на галоген атома водорода при первом атоме углерода, продукт реакции 1-хлорпропан. В случае II замещается атом водорода при втором атоме углерода, продуктом реакции является 2-хлорпропан. Обратите внимание на то, что при построении названий нумерацию атомов углерода начинают с того конца углеродной цепи, к которому ближе расположен атом хлора.
В результате реакции монохлорирования пропана образуются два продукта: 1-хлорпропан и 2-хлорпропан, имеющие одинаковые молекулярные формулы C3H7Cl. Это неудивительно, ведь 1-хлорпропан и 2-хлорпропан — изомеры.
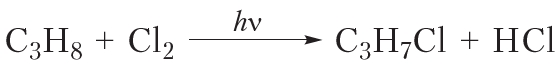
Если мы запишем уравнение реакции монохлорирования пропана с использованием молекулярных формул, оно будет выглядеть следующим образом:
Уравнение реакции, записанное в таком виде, не только не позволяет определить, какой именно продукт (1-хлорпропан или 2-хлорпропан) имеется в виду, но и приводит к распространённому заблуждению, что при монохлорировании пропана образуется только один органический продукт — C3H7Cl, хотя на самом деле их два. Поэтому в органической химии при записи уравнений реакций обычно используют структурные, а не молекулярные формулы веществ.
В результате хлорирования алканов происходит замещение одного или нескольких атомов водорода в молекуле алкана на атомы галогена. Поэтому получающиеся органические вещества называют галогенпроизводными алканов.
Пример. Замещение двух атомов водорода хлором в молекуле этана.
Реакция протекает в два этапа.
а) Первая стадия хлорирования этана. На первой стадии происходит замещение одного атома водорода. При этом образуется только одно органическое вещество — хлорэтан:
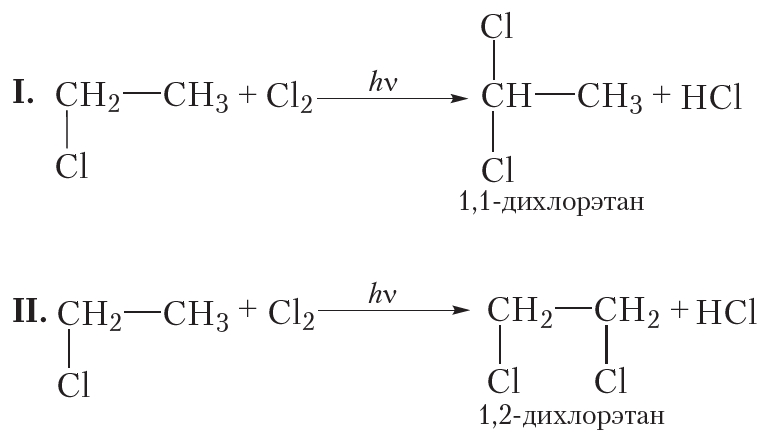
б) Вторая стадия хлорирования этана. На данной стадии происходит взаимодействие молекулы хлора с молекулой хлорэтана, образовавшегося на первой стадии. Очевидно, что при этом могут образоваться два органических вещества:
Действительно, в результате хлорирования этана можно получить смесь двух дихлорпроизводных.
Алканы вступают в реакции замещения также с бромом. Например:

С механизмом реакции галогенирования алканов вы можете познакомиться, перейдя по ссылке в QR-коде.
В реакциях галогенирования атомы водорода в молекуле алкана замещаются на атомы галогена, при этом углеродная цепь молекулы сохраняется. В других реакциях алканов их углеродный скелет изменяется или полностью разрушается. Рассмотрим такие реакции.
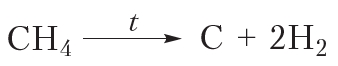
2. Пиролиз
При сильном нагревании алканов в их молекулах происходит разрыв связей 

Общая схема реакции пиролиза алканов (n — число атомов углерода в молекуле алкана):
Эту реакцию используют в промышленности для получения сажи и водорода.
3. Изомеризация
4. Горение. Взаимодействие с кислородом
Важнейшее свойство алканов — горение. Алканы воспламеняются при поджигании. Уравнение реакции горения метана:
Последующие члены гомологического ряда алканов также горят при поджигании. Можно записать общее уравнение реакции горения:
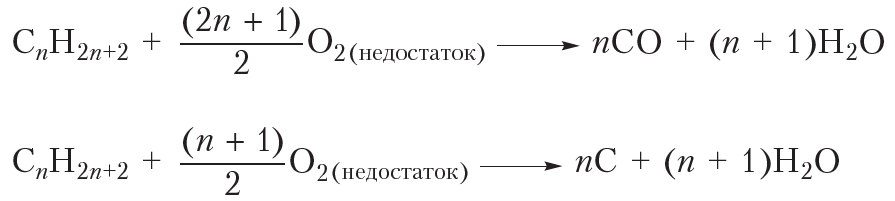
Видно, что при горении атомы водорода из молекулы алкана переходят в молекулы воды, а атомы углерода — в молекулы углекислого газа. Если горение алкана происходит в условиях недостатка кислорода, то, наряду с углекислым газом (СО2), может образоваться угарный газ (СО) или углерод (С) в виде сажи:
Отметим, что свойство гореть в кислороде присуще почти всем органическим соединениям. Поскольку все органические вещества содержат углерод, то при их горении могут образовываться оксиды углерода и сажа.
Образование угарного газа (CO) при неполном сгорании органического вещества смертельно опасно из-за высокой токсичности СО. Отравление угарным газом может произойти при неправильной эксплуатации печей и каминов.
Как видно, химические свойства алканов не отличаются большим разнообразием. Для них характерны в основном реакции окисления (в частности, горения), разложения и изомеризации при высокой температуре, а также реакции замещения, в результате которых получают галогенпроизводные алканов.
§ 10. Химические свойства, получение и применение алканов
| Сайт: | Профильное обучение |
| Курс: | Химия. 10 класс |
| Книга: | § 10. Химические свойства, получение и применение алканов |
| Напечатано:: | Гость |
| Дата: | Воскресенье, 14 Ноябрь 2021, 20:01 |
Оглавление
Химические свойства, получение и применение алканов
Существует огромное число различных алканов. Их многообразие объясняется как возможностью образования углеродных цепей различной длины, так и изомерией. В связи с этим изучать химические свойства каждого алкана отдельно не представляется возможным. В то же время молекулы различных алканов имеют сходное строение: атомы углерода соединены между собой и атомами водорода одинарными ковалентными связями. Учитывая это, можно ожидать, что химические свойства различных алканов будут во многом сходными.
Все алканы характеризуются низкой химической активностью. Они не взаимодействуют с растворами кислот, оснований, солей. На них не действует такой сильный окислитель, как KMnO4, и такие сильные восстановители, как щелочные металлы. Вы знаете, что щелочные металлы очень активны и реагируют практически со всеми веществами, с которыми соприкасаются, в том числе легко окисляются кислородом воздуха. Чтобы уберечь щелочные металлы от окисления, их хранят под слоем керосина — смеси, состоящей в основном из насыщенных углеводородов. При этом алканы, входящие в состав керосина, не реагируют со щелочными металлами.
Из-за низкой химической активности алканов реакции с их участием протекают в жёстких условиях (при нагревании или облучении ультрафиолетовым излучением).
Мы изучим реакции алканов с галогенами (Cl2 и Br2) и кислородом (O2), а также превращения, которые они претерпевают при нагревании.
1. Галогенирование. Взаимодействие с галогенами
Взаимодействие алканов с галогенами — хлором и бромом — протекает при нагревании или облучении ультрафиолетовым излучением.
Если смесью газообразных метана и хлора заполнить стеклянный сосуд и поместить его в тёмное место, реакция протекать не будет. Однако при нагревании смеси или облучении её ультрафиолетовым излучением протекает химическая реакция замещения атомов водорода в молекуле метана на атомы хлора:
В уравнениях реакций, протекающих при облучении, над стрелкой записывают буквы hv. Данная реакция называется реакцией галогенирования и относится к реакциям замещения.
Если только один атом водорода в молекуле замещается на атом галогена, то реакцию называют моногалогенированием. Приведённая выше реакция является реакцией монохлорирования метана. В избытке хлора оставшиеся три атома водорода молекулы метана могут последовательно замещаться на галоген:
Приведём уравнения реакций всех четырёх стадий хлорирования метана с использованием молекулярных формул:
Рассмотрим реакции монохлорирования гомологов метана.
Для этана уравнение реакции следующее:
Отметим, что в названии «хлорэтан» нет необходимости указывать цифрой положение атома хлора. Это связано с тем, что при замещении любого атома водорода в молекуле этана на атом хлора образуется одно и то же вещество:
Таким образом, при монохлорировании этана так же, как и в случае метана, получается только одно органическое вещество — хлорэтан.
При монохлорировании пропана образуется смесь двух органических веществ:
В случае I происходит замещение на галоген атома водорода при первом атоме углерода, продукт реакции 1-хлорпропан. В случае II замещается атом водорода при втором атоме углерода, продуктом реакции является 2-хлорпропан. Обратите внимание на то, что при построении названий нумерацию атомов углерода начинают с того конца углеродной цепи, к которому ближе расположен атом хлора.
В результате реакции монохлорирования пропана образуются два продукта: 1-хлорпропан и 2-хлорпропан, имеющие одинаковые молекулярные формулы C3H7Cl. Это неудивительно, ведь 1-хлорпропан и 2-хлорпропан — изомеры.
Если мы запишем уравнение реакции монохлорирования пропана с использованием молекулярных формул, оно будет выглядеть следующим образом:
Уравнение реакции, записанное в таком виде, не только не позволяет определить, какой именно продукт (1-хлорпропан или 2-хлорпропан) имеется в виду, но и приводит к распространённому заблуждению, что при монохлорировании пропана образуется только один органический продукт — C3H7Cl, хотя на самом деле их два. Поэтому в органической химии при записи уравнений реакций обычно используют структурные, а не молекулярные формулы веществ.
В результате хлорирования алканов происходит замещение одного или нескольких атомов водорода в молекуле алкана на атомы галогена. Поэтому получающиеся органические вещества называют галогенпроизводными алканов.
Пример. Замещение двух атомов водорода хлором в молекуле этана.
Реакция протекает в два этапа.
а) Первая стадия хлорирования этана. На первой стадии происходит замещение одного атома водорода. При этом образуется только одно органическое вещество — хлорэтан:
б) Вторая стадия хлорирования этана. На данной стадии происходит взаимодействие молекулы хлора с молекулой хлорэтана, образовавшегося на первой стадии. Очевидно, что при этом могут образоваться два органических вещества:
Действительно, в результате хлорирования этана можно получить смесь двух дихлорпроизводных.
Алканы вступают в реакции замещения также с бромом. Например:

С механизмом реакции галогенирования алканов вы можете познакомиться, перейдя по ссылке в QR-коде.
В реакциях галогенирования атомы водорода в молекуле алкана замещаются на атомы галогена, при этом углеродная цепь молекулы сохраняется. В других реакциях алканов их углеродный скелет изменяется или полностью разрушается. Рассмотрим такие реакции.
2. Пиролиз
При сильном нагревании алканов в их молекулах происходит разрыв связей 

Общая схема реакции пиролиза алканов (n — число атомов углерода в молекуле алкана):
Эту реакцию используют в промышленности для получения сажи и водорода.
3. Изомеризация
4. Горение. Взаимодействие с кислородом
Важнейшее свойство алканов — горение. Алканы воспламеняются при поджигании. Уравнение реакции горения метана:
Последующие члены гомологического ряда алканов также горят при поджигании. Можно записать общее уравнение реакции горения:
Видно, что при горении атомы водорода из молекулы алкана переходят в молекулы воды, а атомы углерода — в молекулы углекислого газа. Если горение алкана происходит в условиях недостатка кислорода, то, наряду с углекислым газом (СО2), может образоваться угарный газ (СО) или углерод (С) в виде сажи:
Отметим, что свойство гореть в кислороде присуще почти всем органическим соединениям. Поскольку все органические вещества содержат углерод, то при их горении могут образовываться оксиды углерода и сажа.
Образование угарного газа (CO) при неполном сгорании органического вещества смертельно опасно из-за высокой токсичности СО. Отравление угарным газом может произойти при неправильной эксплуатации печей и каминов.
Как видно, химические свойства алканов не отличаются большим разнообразием. Для них характерны в основном реакции окисления (в частности, горения), разложения и изомеризации при высокой температуре, а также реакции замещения, в результате которых получают галогенпроизводные алканов.
Получение и применение алканов
Алканы входят в состав природного газа и нефти, поэтому основной метод их получения — выделение из природных источников (природного газа и нефти).
Вместе с тем, алканы могут быть получены из других органических веществ. Эти реакции мы будем рассматривать по мере дальнейшего изучения органической химии.
Другим направлением использования алканов является получение из них различных веществ. То есть алканы применяются в качестве сырья в химической промышленности. Взаимодействием метана с водяным паром получают водород:
Этот процесс называют конверсией метана. Образующаяся смесь водорода и оксида углерода(II) называется синтез-газом. Из водорода, выделенного из синтез-газа, и азота воздуха получают аммиак. Эти процессы осуществляют в больших масштабах на предприятии ОАО «Гродно Азот».
Из алканов получают углеводороды с двойными и тройными связями (ненасыщенные углеводороды). Эти углеводороды являются химически более активными, и из них синтезируют множество полезных органических веществ. Способы получения и свойства ненасыщенных углеводородов рассмотрим в следующих параграфах.
Молекулы различных алканов имеют сходное строение, поэтому алканы обладают сходными химическими свойствами.
Алканы при повышенной температуре или облучении вступают в реакции замещения с галогенами (хлором и бромом), в результате которых углеродный скелет молекулы алкана сохраняется, а атомы водорода замещаются атомами галогенов.
При сильном нагревании алканов в их молекулах происходит разрыв связей 

Нагревая алканы неразветвлённого строения в присутствии катализатора, можно получить разветвлённые алканы (изомеризация).
Алканы сгорают в кислороде. В результате реакции могут образовываться СО2, СО, С и Н2О.
Алканы содержатся в природном газе и нефти.
Алканы в основном используются в качестве топлива, а также для получения других веществ (водород, ненасыщенные углеводороды).
*Механизм реакции галогенирования алканов
Какое же воздействие оказывает ультрафиолетовое излучение на смесь метана с хлором? Сначала под действием излучения молекула хлора распадается на два атома хлора, каждый из которых имеет неспаренный электрон. Эта реакция называется инициированием:
Частицы, имеющие неспаренный электрон, называются радикалами. Радикалы при обычных условиях чрезвычайно неустойчивы и сразу же вступают во взаимодействие с другими молекулами.
Так, образовавшийся в результате распада молекулы хлора радикал Cl• взаимодействует с молекулой метана. При этом образуется молекула хлороводорода и радикал метил •CH3:
Радикал •CH3, в свою очередь, взаимодействует со следующей молекулой хлора, образуя хлорметан и новый радикал хлор:
Далее снова повторяются превращения (1) и (2). Цепочка этих превращений может повторяться сотни раз, поэтому подобные реакции называют цепными. Реакции (1) и (2) называются ростом цепи:
Цепь может оборваться в результате взаимодействия двух радикалов. Такая реакция называется обрывом цепи :
Следует отметить, что облучение смеси ультрафиолетовым светом необходимо лишь для распада молекулы хлора на атомы — стадии инициирования. Так как на стадии роста цепи в реакциях участвуют активные частицы (радикалы), то на этой стадии подвод энергии уже не требуется. Поэтому реакция хлорирования метана продолжает протекать даже после прекращения облучения.
По цепному радикальному механизму протекает реакция между водородом и кислородом, известная вам из курса неорганической химии. Такие реакции идут с очень большими скоростями и могут сопровождаться взрывом.
*Получение алканов
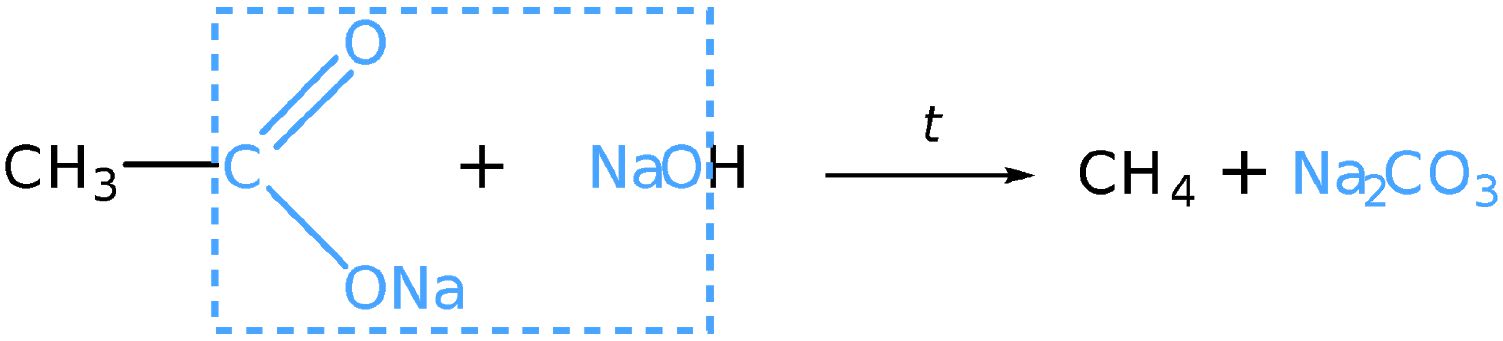
Нагревание солей карбоновых кислот со щёлочью
Реакция Вюрца
Одним из методов получения алканов является реакция Вюрца, которая заключается во взаимодействии галогенпроизводных алканов с металлическим натрием. В качестве примера приведём реакцию получения этана:
Очевидно, что данную реакцию следует использовать для получения алканов симметричного строения, т. е. состоящих из двух одинаковых частей.
Реакция названа в честь её первооткрывателя — французского химика Шарля Адольфа Вюрца (1817–1884).
Вопросы и задания
1. Напишите уравнение реакции монобромирования этана.
2. Напишите уравнения реакций, которые протекают при взаимодействии н-бутана с хлором. Считайте, что только один атом водорода в молекуле н-бутана замещается на хлор. Подпишите названия образующихся органических веществ.
3. Сколько хлорпроизводных можно получить в результате хлорирования этана? Напишите уравнения реакций получения всех возможных хлорпроизводных этана, назовите хлорпроизводные. Можно ли при записи уравнений реакций в данном случае использовать молекулярные формулы?
4. Напишите уравнение реакции горения бутана в избытке кислорода. Какой объём (н. у.) углекислого газа образуется при сжигании 1 моль бутана?
5. Напишите уравнение реакции пиролиза метана с образованием водорода и углерода. Найдите массу углерода, который может быть получен при полном разложении 44,8 дм 3 (н. у.) метана.
6. Назовите основные области применения алканов.
9*. Напишите структурную формулу вещества состава С3Н6О2, если известно, что его водный раствор имеет кислую реакцию, а при прокаливании его натриевой соли с NaOH образуется этан. Напишите уравнения протекающих реакций. (Ответ: пропановая кислота.)
10*. Предложите две возможные структурные формулы вещества состава С4Н8О2, если известно, что его раствор имеет кислую реакцию. При прокаливании натриевой соли вещества с гидроксидом натрия образуется пропан. (Ответ: бутановая кислота и 2-метилпроановая кислота.)
11*. Установите строение углеводорода С6Н14, при монобромировании которого образуется третичное бромпроизводное. Этот углеводород может быть получен по методу Вюрца без побочных продуктов. Напишите схемы протекающих реакций. (Ответ: 2,3-диметилбутан. )
12*. Получите пропан из уксусной кислоты.
13*. В газообразной смеси метана и хлора на три молекулы метана приходится одна молекула хлора.
а) Рассчитайте массовые доли метана и хлора в этой смеси.
б) Исходную смесь объёмом 45 л (н. у.) поместили в замкнутый сосуд и облучили светом. Считая, что только один атом водорода в молекуле метана замещается на хлор, рассчитайте массы всех веществ в смеси, образовавшейся после окончания реакции.
(Ответ:
а) Массовые доли: метана — 40,3 %; хлора — 59,7 %.
б) m(CH4) = 16 г; m(CH3Cl) = 25,25 г; m(HCl) = 18,25 г.)